Азеотропная смесь хлороформ вода
1. Азеотропная перегонка
Азеотропные смеси. В главе I мы уже рассмотрели некоторые свойства растворов, близких к идеальным. В настоящей главе нам необходимо будет познакомиться с растворами, по своим свойствам далеко отстоящими от идеальных, и в первую очередь с так называемыми нераздельнокипящими, или азеотропными, смесями (азеотропами).
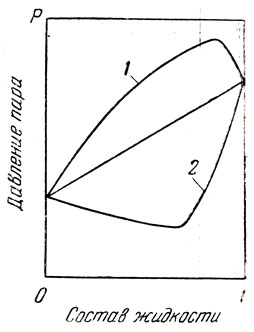
Растворы двух смешивающихся жидкостей могут, в зависимости от природы последних, по своим свойствам в той или иной степени отличаться от идеального раствора. При этом, как было показано на рис. 5, кривая зависимости давления пара от состава содержания в паре нижекипящего компонента) отклоняется от аддитивной прямой. Отклонение свойств двойной смеси от идеального раствора может быть настолько большим, что кривая давления пара будет проходить через максимум (положительное отклонение) или через минимум (отрицательное отклонение) (рис. 70).
Смесь двух жидкостей такого состава, при котором давление пара имеет максимальное значение, обладает самой низкой температурой кипения из всех возможных смесей этих жидкостей. Наоборот, смесь с минимальным давлением пара обладает самой высокой температурой кипения. Согласно второму закону Коновалова — Гиббса «в экстреммах * давлений пара или точек кипения смесей состав жидкой и парообразной фаз совпадают». Следовательно, смеси жидкостей этого состава при перегонке дают дестиллат того же состава, почему они и названы нераздельнокипящими, или азеотропными, смесями. При перегонке смеси двух веществ, способных образовать азеотропную смесь с минимумом температуры кипения, вначале отгоняется азеотропная смесь, а затем тот из компонентов смеси, который имелся в избытке по сравнению с составом азеотропной смеси. Если вещества образуют азеотропную смесь с максимумом температуры кипения, то при перегонке вначале отгоняется один из компонентов, который имеется в избытке по отношению к составу азеотропа, и лишь затем последний.
* ( Точках максимума и минимума на кривой зависимости свойств смеси от ее состава.)
Рис. 70. Зависимость давления пара от состава смеси двух веществ, образующих азеотроп: 1 — положительное отклонение от закона Рауля; 2 — отрицательное отклонение от закона Рауля
Азеотропная смесь с минимальной температурой кипения в дальнейшем для краткости иногда будет называться «минимальный азеотроп», а азеотропная смесь с максимальной температурой кипения — «максимальный азеотроп».
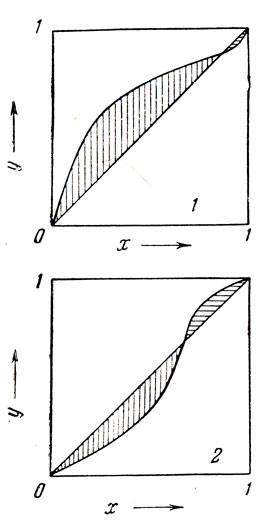
Процесс перегонки азеотропов удобно рассматривать с помощью диаграммы равновесия (рис. 71). Кривая равновесия двойных азеотропных смесей пересекает диагональ в точке, отвечающей составу азеотропной смеси. В этой точке, как гласит второй закон Коновалова-Гиббса у=х (свойство диагонали диаграммы равновесия). При перегонке азеотроп ведет себя как один из компонентов смеси. Поэтому из всей диаграммы равновесия можно вырезать одну из заштрихованных частей, как это показано на рис. 71, и рассматривать эту часть как диаграмму равновесия смеси одного из компонентов и азеотропа.
В растворе двух компонентов, которые могут образовать минимальный азеотроп, «нижекипящим компонентом» всегда является именно азеотроп, независимо от того, какую из заштрихованных частей рассматривать. Максимальный же азеотроп всегда является «вышекипящим компонентом».
В настоящее время известно свыше 3000 минимальных азеотропов и около 300 максимальных. Составы некоторых двойных азеотропных смесей приведены в приложении II. О составе и температуре кипения азеотропов см. также 12, 14, 23, 24, 25 .
Причиной отклонения свойств реальных растворов от свойств идеального раствора является взаимодействие молекул, которое может быть вызвано как физическими силами, так и химическими, например водородной связью. Чем дальше отстоят температуры кипения жидкостей друг от друга, тем большие силы необходимы для того, чтобы образовалась азеотропная смесь, и, наоборот, чем меньше разница температур кипения, тем скорее при прочих равных условиях можно ожидать появления азеотропной смеси. Так, например, этиловый спирт с водой (Δt=22°) образуют азеотропную смесь, между тем как метиловый спирт с водой (Δt=35°) уже не дают азеотропной смеси, хотя природа сил в обоих приведенных примерах одинакова.
Рис. 71. Диаграмма равновесия смеси двух веществ, образующих азеотроп: 1 — минимальный азеотроп; 2 — максимальный азеотроп
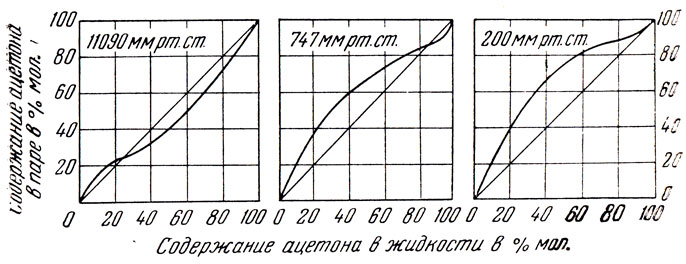
Большое влияние на температуру кипения и состав азеотропной смеси оказывает давление. Это видно, в частности, на примере смеси ацетон — метиловый спирт 76 . На рис. 72 приведены кривые равновесия этой смеси при трех различных давлениях. Как известно, при атмосферном давлении ацетон и метиловый спирт образуют азеотропную смесь, содержащую 12% вес. метилового спирта, с темп. кип. 56,7°. Однако при 200 мм рт. ст. раствор этих двух веществ не образует азеотропной смеси. Как и в обычных условиях, нижекипящим компонентом является ацетон; при 11090 мм рт. ст. азеотропная смесь содержит 75% метилового спирта, но нижекипящим компонентом является при этом уже метиловый спирт; при 15000 мм рт. ст. ацетон и метиловый спирт вновь утрачивают способность давать азеотропную смесь и нижекипящим компонентом является метиловый спирт. Бущмакин и Воейкова 77 показали, что смесь бензол — четыреххлористый углерод, применяемая для определения числа теоретических тарелок колонок, при давлениях ниже 280 мм может превращаться в азеотроп.
Рис. 72. Кривые равновесия смеси ацетона с метиловым спиртом при разных давлениях
Таким образом, смеси, которые обычно считают азеотропными, например смесь ацетона и метилового спирта, при давлении, отличающемся от атмосферного, могут разделяться перегонкой; в то же время смеси, которые обычно относят к неспособным давать азеотроп, как, например, упомянутая выше смесь бензола и четыреххлористого углерода, при давлении, отличающемся от атмосферного, приобретают эту способность.
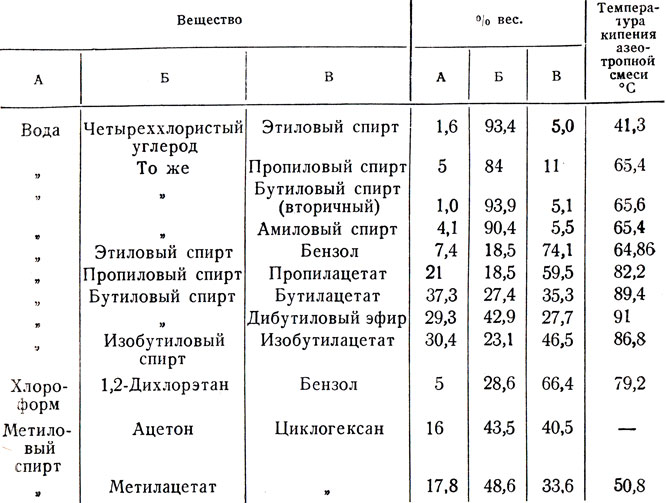
Число компонентов азеотропной смеси может быть и больше двух. В табл. 10 приведены некоторые азеотропные смеси, состоящие из трех компонентов.
Процесс азеотропной перегонки. Если раньше считалось, что образование азеотропной смеси служит только помехой при разделении ее компонентов, то в настоящее время это явление часто используется для выделения чистых веществ. Основным залогом успеха в последнем случае является правильный подбор добавляемого вещества («добавки»). Добавка для азеотропной перегонки может образовывать с компонентами смеси минимальный или максимальный азеотроп. В первом случае желательно подобрать такое вещество, которое давало бы азеотроп с компонентом или компонентами, находящимися в смеси в меньшем количестве; при этом отделение минимального азеотропа потребует меньше времени. Напротив, если добавка приводит к образованию максимального азеотропа, то желательно, чтобы в состав последнего входил компонент смеси, содержащийся в избытке.
Желательно, чтобы добавка при азеотропной перегонке, приводящая к образованию минимального азеотропа, давала азеотроп с одним компонентом смеси, если же все компоненты смеси образуют азеотроп с добавкой, то один из них должен кипеть значительно ниже других. При разделении азеотропной смеси добавка должна давать с одним из компонентов азеотроп, кипящий значительно ниже исходной азеотропной смеси. Иногда целесообразно в качестве добавки взять вещество (или даже два вещества), образующие тройную азеотропную смесь, кипящую намного ниже двойных минимальных азеотропов, если они присутствуют в смеси или образуются при введении добавки.
Общеизвестно, например, что уксусную кислоту, которая не дает азеотропной смеси с водой, очень трудно отделить от последней ректификацией. Добавка этил- или бутилацетата, образующих с водой азеотропную смесь, позволяет полностью удалить из смеси воду и получить чистую кислоту. Ацетон дает, как уже указывалось раньше, азеотропную смесь с метиловым спиртом. Ректификация ацетона с добавкой дихлорэтилена или другого галоидоалкила, дающего азеотроп с метиловым спиртом, который кипит ниже азеотропа ацетона с тем же метиловым спиртом, позволяет получить чистый ацетон. Азеотропная перегонка ацетона, не содержащего метилового спирта, с сероуглеродом позволяет очистить его от примеси ацетальдегида.
Таблица 10. Тройные азеотропные смеси с минимальной температурой кипения
Как указывается в литературе 7 , очистка ацетона азеотропной перегонкой более удобна, чем очистка по бисульфитному методу или с помощью иодистого натрия. Добавление метилового спирта, уксусной кислоты или метилэтилкетона к узким гептан-толуольным фракциям нашло применение в заводских способах выделения толуола из его смеси с парафиновыми и нафтеновыми углеводородами. При этом толуол остается в остатке. Абсолютирование спирта ректификацией с добавкой бензола также нашло промышленное применение. При этом отгоняется тройная азеотропная смесь, кипящая при 64,8°, т. е. ниже двойных азеотропных смесей спирт — бензол (темп. кип. 68,2°) и спирт — вода (темп. кип. 78°). Азеотропной перегонкой пользуются также для высушивания разнообразных веществ, удаления воды из реакционной смеси и очистки разнообразных соединений вплоть до элементоорганических, например хлорсиланов.
Необходимым требованием к добавке, образующей азеотропную смесь с выделяемым веществом, является легкость последующего отделения от него. Для этой цели весьма удобно подбирать добавки, отличающиеся по растворимости от выделяемого вещества. Так, например, при перегонке смеси углеводородов с добавкой спирта последний легко отделить от углеводородов растворением в воде. Если добавка рассчитана на образование азеотропных смесей с минимальной температурой кипения (минимальных азеотропов), то желательно, чтобы температура кипения добавки была ниже температуры вещества, выделяемого азеотропной перегонкой; если же, напротив, добавка дает максимальный азеотроп, то температура кипения ее должна быть выше температуры кипения выделяемого вещества. В этих случаях разность между температурами кипения азеотропной смеси и вещества, не входящего в ее состав, будет значительно больше. Наконец, следует еще раз отметить, что изменение давления при перегонке может иногда привести к азеотропной перегонке в более благоприятных условиях или даже к азеотропной перегонке веществ, не образующих азеотропной смеси при атмосферном давлении.
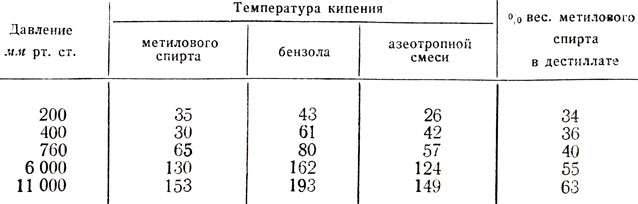
Таблица 11. влияние давления на температуру кипения азеотропной смеси метиловый спирт — бензол и на состав дестиллата
Перегонка смеси бензола и метилового спирта при давлении, меньшем, чем атмосферное, как это видно из табл. 11, увеличивает содержание бензола в дестиллате. Если же задачей азеотропной перегонки этой смеси является выделение метилового спирта, то может оказаться целесообразней перегонку проводить при повышенном давлении.
Источник
Азеотропная смесь хлороформ вода
СВОЙСТВА, ОЧИСТКА И ПРИМЕНЕНИЕ ВАЖНЕЙШИХ РЕАГЕНТОВ, РАСТВОРИТЕЛЕЙ И ВСПОМОГАТЕЛЬНЫХ ВЕЩЕСТВ
Из: ОРГАНИКУМ (Практикум по органической химии) Т.2, М.: Мир, 1979, стр.353.
Очистка. Для удаления следов кислорода пропускают через промывную склянку, наполненную раствором 2г пирогаллола и 6г KOH в 50мл воды. Затем газ высушивают, пропуская через колонку с натронной известью.
Примеси.Хлорид цинка, соединения серы. Очистка.Мелко раздробленный порошок активированного угля нагревают 2-3ч на водяной бане с 4-кратным количеством 20% азотной кислоты, отмывают водой до нейтральной реакции, сушат при 100-110°C.
Т. кип.20.8°C Получение из паральдегида. К паральдегиду, помещенному в перегонный прибор с колонкой, прибавляют каплю концентрированной серной кислоты и осторожно подогревают: ниже 35°C перегоняется ацетальдегид. Его собирают в охлаждаемый льдом приемник либо непосредственно вводят в реакционную смесь.Осторожно! Образует взрывоопасные смеси с воздухом (4-57vol% ацетальдегида)! Пары ацетальдегида раздражают слизистые оболочки дыхательных путей, могут вызывать сердцебиение и расстройство желудка.
100г ацетона при 13атм и 15°C растворяет
30л ацетилена.
Чистый ацетилен взрывается уже под давлением 2атм, поэтому его хранят в стальных баллонах в ацетоновом растворе. Раствором пропитана пористая масса (например, кизельгур). Для того чтобы предотвратить захват ацетона, баллоны при пользовании должны стоять вертикально. Сушка и очистка. Ацетилен можно сушить, пропуская над пятиокисью фосфора, следы ацетона устраняют активированным углем. Осторожно!Пределы взрывчатости смесей с воздухом: 1.5-80vol% ацетилена. Ацетилен нельзя приводить в соприкосновение с серебром или медью, так как при этом образуются взрывчатые ацетилениды. Содержащийся в баллонах ацетилен ядовит из-за примеси фосфина.
Т. кип. 56.2°C; n20=1.3591 Смешивается со спиртом, эфиром и водой в любых соотношениях. Не образует азеотропной смеси с водой.
T. кип. 81.5°C; n20=1.3441Смешивается с водой, спиртом и эфиром в любых отношениях. Азеотропная смесь с водой кипит при 76.7°C и содержит 84.1% ацетонитрила. Очистка и сушка. Кипятят с обратным холодильником с пятиокисью фосфора несколько раз до тех пор, пока ацетонитрил перестанет окрашиваться. Затем отгоняют, перегоняют еще раз над поташом и, наконец, фракционируют на колонке. Осторожно! Пожароопасная жидкость класса BI. Ацетонитрил ядовит, особую опасность представляет имеющаяся в нем примесь свободной синильной кислоты (см. «Синильная кислота»).
T. кип. 80.1°C; т. пл. 5.5°C; n20При 20°C бензол растворяет 0.06% воды; при той же температуре вода растворяет 0.07% бензола. Азеотропная смесь с водой кипит при 69.25°C и содержит 91.17% бензола. О тройной азеотропной смеси с водой и этанолом см. «Этанол»
Примеси. Сырой бензол содержит
0.15% тиофена.
Сушка. Бензол можно осушить азеотропной перегонкой; при этом отбрасывают первые 10% дистиллята. Для более тщательного обезвоживания удаляют воду натрием: свежие кусочки натрия добавляют до прекращения выделения водорода.
Удаление тиофена. К 1л бензола прибавляют 80мл концентрированной серной кислоты, энергично перемешивают 30мин при комнатной температуре, темный слой кислоты отделяют. Эту операцию повторяют до тех пор, пока кислота станет окрашиваться лишь слабо. Бензол тщательно отделяют и перегоняют.
Внимание! ЛВЖ, относится к классу AI. Взрывоопасны смеси с воздухом, содержащие 0.8-8.6vol% бензола. По пожарной опасности относится к первой категории. Бензол является сильным кровяным ядом . Он может всасываться и через кожу. Хронические отравления ведут к поражению печени и нервной системы.
Первая помощь при отравлении ароматическими углеводородами. Снять пропитанную одежду, кожу тщательно промыть водой с мылом. При попадании в глаза промывать их 10-15мин проточной водой. Если ароматический углеводород попал в желудок, вызвать рвоту либо принять в качестве слабительного Paraffinium liquidum из расчета 3мл на 1 кг веса тела или раствор 1 столовой ложки сульфата натрия в 250мл воды. Ни в коем случае не давать касторовое масло, молоко или спирт! В тяжелых случаях — дыхание кислородом.
T. кип. 118.5°C
Гидразингидрат легко растворим в воде и спирте, нерастворим в эфире. Гигроскопичен.
Получение 85% гидразингидрата. 100г 30% гидразингидрата смешивают с 200г ксилола и перегоняют на колонке. Начиная с 99°C отгоняется азеотропная смесь ксилола и воды, при 118-119°C перегоняется 85% гидразингидрат.
Определение содержания гидразина: при титровании кислотой в присутствии метилоранжа образуется монохлоргидрат.
Осторожно! Гидразин разъедает кожу. Он является также кровяным ядом, вызывает судороги и поражает сердце.
Первая помощь. Пораженные места кожи промыть разбавленной уксусной кислотой. Противоядием является глюкоза, принимаемая внутрь.
Т. кип. 72°C при 12mmHg; t. пл. 18.5°C; n 20 D =1.4783
Примеси. Вода, диметилсульфид, диметилсульфон.
Сушка. Оставить стоять на 1сутки над подходящим молекулярным ситом или 2ч кипятить с обратным холодильником над гидридом кальция. Затем перегоняют в вакууме водоструйного насоса в токе сухого, чистого азота
Т. кип. 153.0°C; п 25 d =1.4269
Диметилформамид смешивается с водой (в любых соотношениях) и с большинством органических растворителей. Кроме того, он растворяет многие соли.
Примеси. Диметилформамид часто содержит амины, аммиак, формальдегид,
Очистка и сушка. Перегоняют смесь 250мл диметилформамида, 30 бензола и 12г воды. Сначала отгоняется бензол, вода, амины, аммиак; затем в вакууме — очень чистый диметилформамид; он имеет нейтральную реакцию, без запаха. Диметилформамид следует защищать от света, так как на свету он разлагается на диметиламин и формальдегид.
Внимание! Диметилформамид не безопасен для здоровья.>
Т. кип. 101°C; т. пл. 12°C; n 20 D =1.4224
Диоксан смешивается с водой в любых соотношениях.
Примеси. Диоксан может содержать уксусную кислоту, воду, этиленацеталь уксусного альдегида. Относительно образования перекисей см. «Диэтиловый эфир» .
Очистка. Кипятят 3ч с обратным холодильником с концентрированной соляной кислотой, взятой в количестве 10% от массы диоксана. Во время кипячения через жидкость пропускают слабый ток азота. Затем водный слой отделяют, диоксан встряхивают с твердым едким кали, фильтруют, вводят натрий и кипятят 1ч с обратным холодильником. После перегонки в диоксан кладут несколько кусочков натриевой проволоки.
Осторожно! Пожароопасная жидкость класса BI. Взрывоопасны смеси с воздухом, содержащие 1.97 -25 vol % диоксана. По пожарной опасности относится к первой группе.
Т. кип. 83.7°C; n 20 D =1.4444; d 4 =1.253
Азеотропная смесь с водой кипит при 72°C и содержит 81.5% дихлорэтана.
Очистка и сушка. Промывают концентрированной серной кислотой, затем водой и перегоняют над пятиокисью фосфора.
Внимание! Взрывоопасны смеси с воздухом, содержащие 6.2-15.9vol% дихлорэтана. По пожарной опасности относится к первой группе.
Дихлорэтан вызывает расстройства зрения. Дополнительные сведения см. разд. «Четыреххлористый углерод» . Из-за опасности взрыва дихлорэтан нельзя приводить в соприкосновение с натрием.
Т. кип. 244.3°C; 130°C при 8mmHg; n 20 D =1.4475.
Дигликоль смешивается с водой.
Примеси. Этиленгликоль, триэтиленгликоль. Очистка. Перегонка в вакууме.
Диэтиленгликоль используют для заполнения нагревательных бань. Целесообразно поверх налить слой парафинового масла.
Внимание! Относительно ядовитости см. «Этиленгликоль» .
Диэтиловый эфир (эфир)
Т. кип. 34.6°C; n 20 D =1.3527; d 15 4 =0.7193
При 15°C эфир растворяет 1.2% воды, а вода при 20°C — 6.5% эфира. Азеотропная смесь с водой содержит 1.26% воды и кипит при 34.15°C. Продажный продукт всегда содержит некоторые количества спирта и воды.
Сушка. Абсолютный эфир получают при многодневном стоянии над хлоридом кальция. Затем хлорид кальция отфильтровывают, а эфир сушат над натриевой проволокой. Натрий добавляют до тех пор, пока его поверхность не станет оставаться блестящей.
Внимание! На свету эфир образует взрывчатые перекиси. Поэтому рекомендуется хранить эфир над едким кали, который переводит образующиеся гидроперекиси в нерастворимые соли, а кроме того, служит и очень подходящим осушителем.
Осторожно! ЛВЖ, относится к классу AI. Взрывоопасны смеси с воздухом, содержащие 1.2-51vol% эфира.
Т. кип. 136-144°C (продажный ксилол представляет собой смесь трех изомерных ксилолов).
Азеотропная смесь с водой кипит при 92°C и содержит 64.2% ксилола. О симптомах отравления см. «Бензол»
Смесь углеводородов: см. «Бензин».
Очистка. См. «Гексан».
Внимание! ЛВЖ, относится к классу AI. Смеси лигроина с воздухом взрывоопасны.
Т. кип. 64.7°C; n 20 D =1.3286
Сушка. На 1л метанола прибавляют 5г стружек магния, после окончания самопроизвольной реакции кипятят 2-3ч с обратным холодильником и перегоняют. Если в метаноле содержится >1% воды, то магний не реагирует. В этом случае немного магния обрабатывают чистым метанолом и после начала реакции прибавляют эту затравку к основной массе. При этом общее количество магния несколько увеличивают по сравнению с указанным выше.
Осторожно! ЛВЖ, относится к классу BI. Взрывоопасны смеси с воздухом, содержащие 5.5-36.5vol% метанола. По пожарной опасности относится к первой группе.
Метанол вызывает приступы тошноты, нарушает деятельность сердца и нервной системы, вызывает слепоту.
Нитрозными газами называют смеси окислов азота, которые часто образуются при работе с азотной кислотой.
Осторожно! Нитрозные газы даже в малых количествах опасны для здоровья. Они вызывают раздражение дыхательных путей и глаз, а также тошноту и головную боль. Раздражение проходит через 15-60мин, однако через несколько часов неожиданно начинается кашель с пенистыми, ржаво-красными выделениями, затрудняется дыхание (такое состояние может появиться даже через двое суток). Это свидетельствует о появлении отека легких, который вместе с развивающимся метгемоглобинозом крови создает серьезную угрозу жизни. При вдыхании нитрозных газов обязательно надо поставить в известность врача.
Для защиты использовать дыхательный фильтр В.
Первая помощь. См. разд. «Фосген»
Т. кип. 10.7°C
Окись этилена поступает в стальных баллонах.
Осторожно! Взрывоопасны смеси с воздухом, содержащие 3-80% окиси этилена.
Под действием щелочи взрывоподобная полимеризация.
При попадании на кожу возникают (часто лишь через несколько часов) нарывы, затем наступает некроз. Заживание очень медленное. При вдыхания даже малых количеств появляются выделения изо рта и носа, длительная рвота, понос, чувство тяжести в животе, возбужденное состояние. Высокие концентрации вызывают наркотическое состояние, угрожают кровеобмену. В результате возможны поражения сердца, печени и почек.
Первая помощь. Немедленно снять смоченную одежду. Основательно промыть кожу. Вдыхать свежий воздух (лучше кислород), предохранять от охлаждения. Транспортировать только лежа.
Т. пл. 107°C
Для очистки перекись бензоила растворяют в небольшом количестве холодного хлороформа и осаждают метанолом. Сырой продажный продукт сушат в вакуум-эксикаторе над пятиокисью фосфора.
Осторожно! Опасность взрыва! Перекись бензоила нельзя перекристаллизовывать из горячих растворов. Температуру плавления определять лишь в исключительных случаях!
T. кип. 115.6°C; n 20 d =1.5100
Пиридин гигроскопичен; он смешивается с водой, спиртом и эфиром в любых отношениях.
Азеотропная смесь с водой кипит при 94°C и содержит 57% пиридина.
Очистка и сушка. Сушат над едким кали, перегоняют на хорошей колонке, собирая фракцию от 114 до 116°C.
Очистка для гидрирования. 500г технически чистого пиридина оставляют на 24ч над едким кали, сливают с осушителя и перегоняют. Дистиллят смешивают с 15г свежеперегнанного анилина и постепенно прибавляют при хорошем перемешивании 5г чистого амида натрия в порошке. Эту операцию проводят в трехгорлой колбе с мешалкой и обратным холодильником с хлоркальциевой трубкой. После прибавления всего амида натрия продолжают перемешивание и нагревают на водяной бане до прекращения выделения аммиака. Пиридин отгоняют; остаток в колбе разлагают, добавляя спирт. Дистиллят кипятят с обратным холодильником 1 ч с 10мл безводной фосфорной кислоты и перегоняют на колонке.
Осторожно! Пожароопасная жидкость класса BI. Взрывоопасны смеси с воздухом, содержащие 1.8-12.5vol% пиридина.
Пиридин вызывает на коже экзему. Вдыхание паров пиридина вызывает тошноту, боли в желудке, повреждение нервной системы.
Приготовление. Растворяют 1г нитрата серебра в 10мл воды, раствор хранят в темноте. Перед употреблением небольшое количество этого раствора смешивают с равным объемом раствора 1г едкого натра в 10мл воды, выпавший осадок окиси серебра растворяют, осторожно добавляя концентрированный раствор аммиака.
Осторожно! Остатки реактива следует немедленно выливать. При стоянии образуется сильно взрывчатое гремучее серебро.
Получение. Готовят 0.025%-ный водный раствор фуксина и пропускают через него сернистый газ до обесцвечивания.
Эта смазка не содержит жира, устойчива к эфиру.
Получение. В нагретый до 160°C глицерин вносят растворимый крахмал до достижения желаемой консистенции (которую определяют, охлаждая каплю смеси).
Сушка: ср. «Метанол»и «Этанол». Для сушки высших спиртов используют раствор метилата магния; его готовят из магния при 2-3-часовом кипячении (обратный холодильник) с 10-кратным количеством метанола (содержание воды
Т. кип. 110.8°C; n 20 D =1.4969
Азеотропная смесь с водой кипит при 84.1°C и содержит 81.4% толуола.
Сушка: см. «Бензол»
Осторожно! ЛВЖ, относится к классу AI. Взрывоопасны смеси с воздухом, содержащие 1.27-7vol% толуола. По пожарной опасности относится ко второй группе.
Симптомы отравления: см. «Бензол»
Т. кип. 287°C, 165°C при 14mmHg
См. разд. «Диэтиленгликоль»
T. кип. 7.6°C
Фосген легко растворим в бензоле и толуоле, мало растворим в холодной воде. Фосген имеет удушающий, своеобразный запах (напоминает запах гниющего сена).
Осторожно! Фосген один из наиболее ядовитых газов. Признаки отравления (насморк, затруднение дыхания, кровавый кашель) появляются нередко лишь через много часов. После того как исчезнут явления раздражения, может наступить кажущееся облегчение, во время которого, однако, в течение нескольких часов развивается отек легких, который часто приводит к смерти в результате нарушения сердечной деятельности и обмена веществ.
Хлорированные углеводороды могут в результате пиролиза образовывать. фосген: необходимо соблюдать осторожность при использовании огнетушителей с четыреххлористым углеродом. Даже при легких отравлениях фосгеном необходимо обратиться к врачу.
Для защиты следует использовать дыхательный фильтр В.
Первая помощь. Пострадавшего уложить и транспортировать только лежа. Даже при легком отравлении необходим полный покой. Полезен свежий воздух, лучше кислород, однако искусственного дыхания делать нельзя. Завернуть в. одеяло, чтобы предотвратить переохлаждение.
Избыток фосгена поглощают 20% раствором едкого натра.
Т. кип. 78.33°C; n 20 D =1.3616; d 20 4 =0.789
Этанол смешивается с водой, эфиром, хлороформом, бензолом в любых отношениях. Азеотропная смесь с водой кипит при 78.17°C и содержит 96% этанола. Тройная азеотропная смесь с водой (7.4%) и бензолом (74.1%) кипит при 64.85°C.
Примеси. Синтетический спирт загрязнен уксусным альдегидом и ацетоном, этиловый спирт, полученный при брожении,— высшими спиртами (сивушными маслами). Для денатурации добавляют пиридин, метанол и бензин.
Сушка. В 1л продажного «абсолютного» спирта растворяют 7г натрия,. прибавляют 27.5г диэтилового эфира фталевой кислоты, кипятят 1ч с обратным холодильником, затем перегоняют с небольшой колонкой. Переходящий спирт содержит менее 0.05% воды. Из продажного «абсолютного» спирта следы воды можно удалить и другим способом, 5г магния 2-3ч кипятят с 50мл «абсолютного» спирта, к которому добавлен 1мл четыреххлористого углерода,. затем прибавляют 950мл «абсолютного» спирта, кипятят еще 5ч с обратным. холодильником. В заключение перегоняют.
Обнаружение воды. Спирт, содержащий более 0.05% воды, осаждает объемистый белый осадок из бензольного раствора триэтилата алюминия.
Внимание! Горючая жидкость класса BI. Взрывоопасны смеси с воздухом,. содержащие 2.6-18.9vol% этанола.
Т. кип. 92°C при 10mmHg; n 20 D =1.3406
Примеси. Дигликоль, тригликоль, пропиленгликоль, вода.
Очистка и сушка. Перегонка в вакууме; основную фракцию длительное время сушат сульфатом натрия и перегоняют в вакууме на хорошей колонке.
Внимание! Ядовитость гликолей обычно недооценивают: они вызывают тошноту и рвоту.
Свойства и очистка органических растворителей
Bunge W., in: Houben-Weyl, Bd. I /2, 1959, S.765-868.
Органические растворители. Ред. А. Вайсбергер. Пер. с англ.-М.: ИЛ 1958, с.519.
Несчастные случаи при работах в химических лабораториях.
Первая помощь.
Справочник химика. Ред. Б. П. Никольский. Т.3.-Л.: Химия, 1968, с.507.
Источник