- Что получается при взаимодействии аммиака с водой
- § 24. Аммиачная вода
- Аммиак: получение и свойства
- Аммиак
- Строение молекулы и физические свойства
- Способы получения аммиака
- Химические свойства аммиака
- Аммиачная вода: формула, получение, применение
- Описание
- Получение
- Физические свойства
- Химические свойства
- Техника безопасности при работе с веществом
- Где используется водный раствор аммиака?
- Применение аммиачной воды в сельском хозяйстве
Что получается при взаимодействии аммиака с водой
§ 24. Аммиачная вода
Водородные соединения уже изученных нами неметаллов растворяясь в воде, реагируют с нею с образованием ионов гидроксония. Реагирует с водой при растворении в ней и аммиак, но иначе.
Опустим в кристаллизатор с водой сосуд, наполненный аммиаком, отверстием вниз. Вода быстро заполнит сосуд доверху, то показывает, что аммиак очень хорошо растворяется в воде. В 1 объеме воды ПРИ обычной температуре растворяется до 700 объемов аммиака. Водный раствор аммиака называется аммиачной водой.
Водородные соединения изученных вами неметаллов диссоциируют в растворе, как кислоты. Исследуем и аммиачную воду при помощи прибора для обнаружения электропроводности растворов (рис. 1). При погружении в нее электродов лампочка засветится. Следовательно, в растворе содержатся ионы
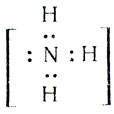
Какие же ионы образуются при растворении аммиака в воде. Прильем к раствору несколько капель раствора фиолетового лакмуса или фенолфталеина: в аммиачной воде лакмус окрашивается не в красный цвет (как в растворах галогеноводородов, сероводорода), а в синий, фенолфталеин — в малиновый цвет. Мы обнаружили присутствие в аммиачной воде ионов гидроксила ОН — . Откуда они появились? Молекулу аммиака можно рассматривать, как ион азота 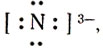
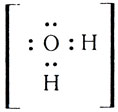
Одна электронная пара при атоме азота остается свободной, не участвующей в образовании химической связи. Молекулу же воды мы уже рассматривали как ион кислорода 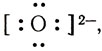
Не участвуют в образовании связей у атома кислорода две электронные пары. Атомы неметаллов в таких водородных соединениях могут за счет свободных электронных пар связывать дополнительные ионы Н + (вспомните ион гидроксония).
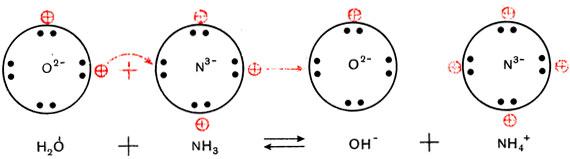
Трехзарядный ион азота в молекуле аммиака сильнее удерживает связанные с ним протоны и сильнее притягивает добавочный протон, чем двухзарядный ион кислорода в молекуле воды. Поэтому при взаимодействии аммиака с водой происходит перемещение протонов из молекул воды в молекулы аммиака:
(Кружки с крестиками изображают ионы водорода Н + , или протоны.)
Образуются ионы гидроксила ОН
и положительно заряженные ионы NH4 + , которые получили название «аммоний».
Упрощенно реакция между аммиаком и водой изображается так:
Эта реакция обратимая. Лишь малая доля растворенного аммиака присутствует в растворе в виде ионов аммония, большая часть его содержится в виде молекул NH3. Потому аммиачная вода пахнет аммиаком и при стоянии на открытом воздухе или при нагревании выделяет весь растворенный в ней аммиак.
В молекуле аммиака атом азота образует три ковалентные связи, а в ионе аммония — четыре. Но из этих четырех связей по-прежнему лишь три образованы за счет спаривания электронов атома азота с электронами присоединенных атомов. А мы определили валентность именно как число электронов, затраченных рассматриваемым атомом на спаривание с электронами присоединенных атомов. Поэтому валентность азота в зоне аммония, как и в аммиаке, остается равной 3.
Независимо от различного происхождения все 4 связи в зоне аммония совершенно равноценны, и этот ион имеет форму правильной трехгранной пирамиды — тетраэдра.
В медицине и в быту разбавленный раствор аммиака называется аммиачной водой или нашатырным спиртом. Его дают нюхать при обмороке для приведения в сознание. В домашнем хозяйстве он применяется в качестве слабой щелочи при стирке белья и выведении пятен.
В сельском хозяйстве концентрированную аммиачную воду используют в качестве жидкого удобрения.
- Что представляет собой водный раствор аммиака? Какие молекулы и ионы в нем присутствуют? Как эти ионы образуются?
- * Во что превратилась бы молекула метана СН4, если бы в ядро углеродного атома внедрился протон?
- Перед нами стакан, наполненный аммиаком и закрытый пластинкой, и второй открытый стакан. Как «перелить» аммиак из первого стакана во второй, чтобы аммиак по возможности не смешался с воздухом? Как обнаружить результаты опыта, если в нашем распоряжении имеется бумага, пропитанная раствором фенолфталеина?
Источник
Аммиак: получение и свойства
Аммиак
Строение молекулы и физические свойства
В молекуле аммиака NH3 атом азота соединен тремя одинарными ковалентными полярными связями с атомами водорода:
Геометрическая форма молекулы аммиака — правильная треугольная пирамида. Валентный угол H-N-H составляет 107,3 о :
У атома азота в аммиаке на внешнем энергетическом уровне остается одна неподеленная электронная пара. Эта электронная пара оказывает значительное влиение на свойства аммиака, а также на его структуру. Электронная структура аммиака — тетраэдр , с атомом азота в центре:
Аммиак – бесцветный газ с резким характерным запахом. Ядовит. Весит меньше воздуха. Связь N-H — сильно полярная, поэтому между молекулами аммиака в жидкой фазе возникают водородные связи. При этом аммиак очень хорошо растворим в воде, т.к. молекулы аммиака образуют водородные связи с молекулами воды.
Способы получения аммиака
В лаборатории аммиак получают при взаимодействии солей аммония с щелочами. Поск ольку аммиак очень хорошо растворим в воде, для получения чистого аммиака используют твердые вещества.
Например , аммиак можно получить нагреванием смеси хлорида аммония и гидроксида кальция. При нагревании смеси происходит образование соли, аммиака и воды:
Тщательно растирают ступкой смесь соли и основания и нагревают смесь. Выделяющийся газ собирают в пробирку (аммиак — легкий газ и пробирку нужно перевернуть вверх дном). Влажная лакмусовая бумажка синеет в присутствии аммиака.
Видеоопыт получения аммиака из хлорида аммония и гидроксида кальция можно посмотреть здесь.
Еще один лабораторный способ получения аммиака – гидролиз нитридов.
Например , гидролиз нитрида кальция:
В промышленности аммиак получают с помощью процесса Габера: прямым синтезом из водорода и азота.
Процесс проводят при температуре 500-550 о С и в присутствии катализатора. Для синтеза аммиака применяют давления 15-30 МПа. В качестве катализатора используют губчатое железо с добавками оксидов алюминия, калия, кальция, кремния. Для полного использования исходных веществ применяют метод циркуляции непровзаимодействовавших реагентов: не вступившие в реакцию азот и водород вновь возвращают в реактор.
Более подробно про технологию производства аммиака можно прочитать здесь.
Химические свойства аммиака
1. В водном растворе аммиак проявляет основные свойства (за счет неподеленной электронной пары). Принимая протон (ион H + ), он превращается в ион аммония. Реакция может протекать и в водном растворе, и в газовой фазе:
Таким образом, среда водного раствора аммиака – щелочная. Однако аммиак – слабое основание . При 20 градусах один объем воды поглощает до 700 объемов аммиака.
Видеоопыт растворения аммиака в воде можно посмотреть здесь.
2. Как основание, аммиак взаимодействует с кислотами в растворе и в газовой фазе с образованием солей аммония.
Например , аммиак реагирует с серной кислотой с образованием либо кислой соли – гидросульфата аммония (при избытке кислоты), либо средней соли – сульфата аммония (при избытке аммиака):
Еще один пример : аммиак взаимодействует с водным раствором углекислого газа с образованием карбонатов или гидрокарбонатов аммония:
Видеоопыт взаимодействия аммиака с концентрированными кислотами – азотной, серной и и соляной можно посмотреть здесь.
В газовой фазе аммиак реагирует с летучим хлороводородом. При этом образуется густой белый дым – это выделяется хлорид аммония.
NH3 + HCl → NH4Cl
Видеоопыт взаимодействия аммиака с хлороводородом в газовой фазе (дым без огня) можно посмотреть здесь.
3. В качестве основания, водный раствор аммиака реагирует с растворами солей тяжелых металлов , образуя нерастворимые гидроксиды.
Например , водный раствор аммиака реагирует с сульфатом железа (II) с образованием сульфата аммония и гидроксида железа (II):
4. Соли и гидроксиды меди, никеля, серебра растворяются в избытке аммиака, образуя комплексные соединения – аминокомплексы.
Например , хлорид меди (II) реагирует с избытком аммиака с образованием хлорида тетрамминомеди (II):
Гидроксид меди (II) растворяется в избытке аммиака:
5. Аммиак горит на воздухе , образуя азот и воду:
Если реакцию проводить в присутствии катализатора (Pt), то азот окисляется до NO:
6. За счет атомов водорода в степени окисления +1 аммиак может выступать в роли окислителя , например в реакциях с щелочными, щелочноземельными металлами, магнием и алюминием . С металлами реагирует только жидкий аммиак.
Например , жидкий аммиак реагирует с натрием с образованием амида натрия:
Также возможно образование Na2NH, Na3N.
При взаимодействии аммиака с алюминием образуется нитрид алюминия:
2NH3 + 2Al → 2AlN + 3H2
7. За счет азота в степени окисления -3 аммиак проявляет восстановительные свойства. Может взаимодействовать с сильными окислителями — хлором, бромом, пероксидом водорода, пероксидами и оксидами некоторых металлов. При этом азот окисляется, как правило, до простого вещества.
Например , аммиак окисляется хлором до молекулярного азота:
Пероксид водорода также окисляет аммиак до азота:
Оксиды металлов , которые в электрохимическом ряду напряжений металлов расположены справа — сильные окислители. Поэтому они также окисляют аммиак до азота.
Например , оксид меди (II) окисляет аммиак:
2NH3 + 3CuO → 3Cu + N2 + 3H2O
Источник
Аммиачная вода: формула, получение, применение
Аммиачная вода находит широкое применение в качестве реагента в синтезе различных веществ, а также как удобрение в сельском хозяйстве. Наибольший эффект достигается при одновременном ее внесении в почву с органикой. Основной промышленный способ получения вещества — насыщение воды парами аммиака.
Описание
Аммиачная вода (синонимы: гидрат аммиака, гидроокись аммония) представляет собой водный раствор аммиака, в котором он присутствует в основном в виде гидроксида аммония. Концентрация аммиака обычно составляет 22 или 25 %.
Химическая формула аммиачной воды такая: NH3H2O.
По внешнему виду вещество представляет собой бесцветную или светло-желтую жидкость с резким запахом нашатырного спирта. Раствор хранят герметично укупоренным в помещениях, защищенных от воздействия атмосферы. Следует избегать контакта тары с источниками тепла и прямыми солнечными лучами.
В зависимости от целей использования это вещество выпускают двух марок:
- А — для применения в различных отраслях. Изготовление раствора производится с помощью парового конденсата или химически очищенной воды.
- Б — для нужд сельского хозяйства (более низкой степени чистоты).
Требования к техническому аммиаку марки А изложены в ГОСТ 9-92. Существует также государственный стандарт, регламентирующий характеристики этого вещества, применяемого в химии в качестве реактивов (ГОСТ 3760-79). Согласно этому документу выделяют 3 степени чистоты раствора: х. ч. (химически чистый), ч. д. а. (чистый для анализов), ч. (чистый).
Получение
Получение аммиачной воды производится несколькими способами:
- Испарением жидкого аммиака и поглощением его паров в абсорбере с жидкостным рециклом. Перед подачей в хранилище готовый продукт охлаждается низкотемпературным хладоносителем.
- Смешиванием сжиженного аммиака с водой (без его испарения) под давлением. Оба вещества подаются в смеситель при помощи насосов.
- Впрыскиванием концентрированного жидкого аммиака в реактор со скоростью до 12,5 м/с и подачей воды со скоростью до 6 м/с. Такая технология позволяет непрерывно получать гидроксид аммония.
Первый способ является наиболее распространенным. Применяемый при этом аммиак может быть получен синтетическим путем или при коксовании каменного угля в печах. Реакция синтеза обратима. В ходе образования продукта выделяется тепло, для устранения которого используют холодильники, охлаждаемые оборотной водой. В растворах гидроксид аммония находится в равновесии с аммиаком. По этой причине жидкость имеет характерный аммиачный запах.
Физические свойства
Основными физическими характеристиками этого вещества являются следующие:
- плотность аммиачной воды (25 % раствор, температура +15 ˚С) — 910-930 кг/м 3 ;
- молярная масса — 35,046 г/моль;
- давление паров аммиака (при температуре +40 ˚С) — 1 атм.;
- плотность паров — 0,59 г/см 3 ;
- температура, при которой происходит выпадение твердой фазы — -31…-53,9 ˚С;
- температура самовоспламенения — 651 ˚С.
При транспортировке и хранении аммиак способен улетучиваться, в результате наблюдается потеря азота в составе соединения.
Чугун и черные металлы, резина и алюминий устойчивы к воздействию гидроксида аммония. Цветные металлы и их сплавы при контакте с ним корродируют.
Химические свойства
К основным химическим параметрам вещества относятся:
- слабые основные свойства вследствие диссоциации в воде на катионы аммония и анионы гидроксида (-ОН);
- окраска индикаторов: лакмусовая бумага — синий, фенолфталеин — малиновый;
- раствор бурно реагирует при контакте с концентрированными кислотами, сильными окислителями, альдегидом акриловой кислоты, галогенами, диметилсульфатом (со взрывом), азотнокислым серебром, ртутью.
В нормальных условиях продукт химически стабилен. При взаимодействии с кислотами аммиачная вода образует соответствующие соли аммония.
Техника безопасности при работе с веществом
Сам по себе водный раствор аммиака является негорючей и невзрывоопасной жидкостью, но при выделении паров аммиака в помещениях могут скапливаться взрывоопасные концентрации. Даже в малых концентрациях они вызывают следующие негативные реакции со стороны организма человека:
- обильное слезотечение;
- сильный кашель;
- удушье;
- ринит;
- головокружение;
- разъедание желудочно-кишечного тракта при проглатывании;
- ожог слизистых оболочек;
- отек легких при накоплении в них паров (в результате длительного вдыхания в течение 48 часов), что в конечном итоге может привести к смерти.
Поэтому при работе с этим веществом соблюдают следующие меры предосторожности:
- использование вытяжного шкафа;
- герметизация технологического оборудования и тары;
- использование средств индивидуальной защиты: резиновых перчаток, спецодежды, противогазов и защитных очков.
Это соединение является также токсичным для флоры и фауны водоемов.
Где используется водный раствор аммиака?
10 % аммиачный раствор в воде — это всем известная «нашатырка», или нашатырный спирт. В медицине его традиционно использовали при обмороках. В быту это соединение применяют в следующих целях:
- чистка ювелирных изделий из серебра;
- мойка окон и других глянцевых, зеркальных поверхностей (для устранения разводов);
- удаление пятен на тканях;
- устранение неприятных запахов в холодильнике.
Существуют также другие области использования этого соединения:
- химическая промышленность — производство соды, марганца, азотной кислоты, ферросплавов, полимерных материалов и красителей;
- военная промышленность — изготовление взрывчатых веществ;
- пищевая промышленность — добавка Е527 (эмульгатор);
- текстильная промышленность — крашение тканей;
- производство холодильной техники — хладагент;
- строительство — противоморозная и антикоррозионная добавка в железобетонных конструкциях;
- другие отрасли — серебрение зеркал, изготовление светокопировальных материалов.
Применение аммиачной воды в сельском хозяйстве
Гидрат аммиака — дешевый и эффективный источник азота для сельскохозяйственных культур, особенно необходимый в период их вегетативного роста. Растения лучше всего усваивают этот элемент в виде солей азотной кислоты и солей аммония. При поглощении аммиака частицами почвы он диссоциирует на катионы аммония и ионы нитратов. Аммиачный азот имеет высокую степень подвижности в грунте и легко мигрирует с его жидкой фазой.
Существуют следующие особенности использования аммиачной воды в качестве удобрения:
- Период внесения в почву — осенью под перепашку земли (сентябрь), весной — под предпосевное рыхление (апрель), подкормка культур с большими площадями питания в течение всего лета (кукуруза, свекла и другие).
- Применение возможно на всех видах почв. Особенно эффективно использование удобрения на грунтах с тяжелым механическим составом, так из легкой почвы аммиак быстро улетучивается.
- Не рекомендуется применять гидрат аммония на одном и том же месте подряд в течение нескольких лет, поскольку он повышает минерализацию почвы. Это способствует уменьшению содержания органики в ней.
- На легких почвах удобрение лучше вносить весной. Земля должна прогреться до температуры не менее +10 ˚С.
- Водный аммиак необходимо заделывать глубоко в почву (на 10 и 15 см в тяжелую и легкую соответственно). Поверхностное внесение недопустимо, чтобы предотвратить испарение аммиака. Для этого в сельском хозяйстве используют специальные машины. Можно эту процедуру проводить также одновременно с поливом в прохладную погоду.
Такое удобрение позволяет получить высокий урожай и сохранить плодородие земли. Его влияние на характеристики почвы также заключается в следующем:
- Аммиачная вода подкисляет почву, поэтому для ее нейтрализации необходимо вносить карбонат кальция CaCO3 (в расчете 0,3 ц на 1 ц гидрата аммония).
- После подкормки в зоне распространения удобрения наблюдается снижение количества микроорганизмов. Через 6-8 недель после того, как аммиак превратится в нитраты, их число увеличивается в результате роста растительных остатков. То же наблюдается с дождевыми червями.
Кроме этого, аммиачную воду в сельском хозяйстве применяют для аммонизации кормов и антисептической обработки помещений.
Источник