- Деминерализация воды
- Какие ионы жесткости бывают?
- Как работает деминерализация?
- Деминерализованная вода – что это такое
- Особенности деминерализованной воды
- Вода глубокой очистки
- Выпаривание
- Электролиз
- Обратный осмос
- Области применения
- Вред от потребления обессоленной воды
- Дистиллированная и деминерализованная вода
- Дистиллированная вода
- Металлические дистилляторы
- Получение бидистиллята
- Определение качественных показателей дистиллированной воды
- Деминерализация пресной воды ионообменным методом
Деминерализация воды

Да, именно так вода — это всегда раствор минералов (минеральных солей различной концентрации). Отсюда и термин — » деминерализация » — удаление минералов.
Почему минералы , растворенные в воде так опасны? Помимо вредного воздействия на организм (ведь минералы могут быть как полезными для здоровья человека, так и являться вредными), растворенные минералы несут угрозу всем поверхностям, по которым течет такая вода, в особенной степени это относится к тем устройствам, где происходит нагрев воды (чайник, бойлер, водопроводные трубы, утюг, стиральная машина и др.) Вот что будет с Вашей стиральной машиной, если вода жесткая и не подвергается процессу умягчения.
Решено! От минералов (солей жесткости) нужно избавляться! На помощь приходит ионный обмен. Ионы — электрические заряженные атомы или молекулы инородных примесей в воде. Хорошо, что соли жесткости имеют электрические заряды, притягивая эти заряженные ионы жесткости к определенному материалу при водоподготовке можно добиться того, что вода избавиться от них. Снижение концентрации ионов жесткости в водном растворе и будет являться процессом умягчения воды. Убрали жесткость — получили мягкость. Удаление ионов жесткости из воды решает специальная деионизирующая смола.
Какие ионы жесткости бывают?

Положительно заряженные ионы солей жесткости:
- Кальций | Calcium | Ca++
- Магний | Magnesium | Mg++
- Железо | Iron | Fe+++
- Марганец | Manganese | Mn++
- Натрий | Sodium | Na+
- Водород | Hydrogen | H+
От данных солей будем избавляться с помощью ионообменных смол, которые тоже в свою очередь делятся на 2 вида катиониты и аниониты .
Катиониты борются с вышеперечисленными положительно-заряженными ионами (особую проблему вызывают первые два: кальций и магний).
Аниониты призваны удалять из водного раствора отрицательно-заряженные ионы солей жесткости. К которым относятся:
- Хлориды | Chlorides | Cl —
- Сульфаты | Sulfates | SO 4 —
- Нитраты | Nitrates | NO 3 —
- Силикаты | Silica | SiO 2 —
- Гидроокислы | Hydroxyl | OH —
В случае с положительными ионами самыми проблемными принято считать Железо, Магний и Кальций.
Отрицательные проблемные ионы солей жесткости: Нитраты, Сульфаты и Хлориды.
Как работает деминерализация?

По форме — это шарики от половины до полутора мм в диаметре. Допустим они как бусинки, но без отверстий. Вода, проходя в фильтре, через смолу отдает катиониту или аниониту ионы жесткости с зарядом.
Катионит забирает на себя (не в себя) железо, магний, кальций, железо.
Анионит получает на свою поверхность нитрат, сульфат, хлорид и силикаты.
До определенного момента они могут накапливать на себе данные ионы. Далее ионообменные смолы необходимо реактивировать ( регенерировать ) для того чтобы процесс деминерализации начать сначала.
Для этого в фильтр с ионообменной смолой подают регенерационный раствор, который смывает с поверхности ионитов соли жесткости в канализацию, перезаряжает и готовит к повторному использованию.
*** Вы всегда можете купить ионообменные смолы для умягчения воды. Для оформления заказа перейдите на эту страницу.
Источник
Деминерализованная вода – что это такое
Особенности деминерализованной воды
Вода – это жизнь. Все мы с детства знаем, что наш организм практически целиком состоит из воды. Мы пьем много воды, чтобы быть здоровыми, и всегда стараемся пить только чистую, безопасную воду. Но почему же тогда вода глубокой очистки вредна для организма? Что такое деминерализованная вода и зачем она нужна?
Вода глубокой очистки
Деминерализованная или деионизированая вода – это вода глубокой очистки, в которой понижено содержание солей. От дистиллированной ее отличает, то, что неэлектролиты в ней присутствуют.
На сегодняшний день существует множество способов получения деионизированной воды. Для разных нужд необходима вода более или менее глубокой очистки, поэтому разные методы применяются для разных целей.
Выпаривание
Суть метода заключается в том, что загрязнённая вода выпаривается. При этом примеси остаются, а чистая вода конденсируется. Этот метод очень энергетически затратен, но позволяет удалить и неэлектролитические примеси.
Электролиз
Способ отчистки воды под действием электрического поля. Поле действует на свободные ионы, растворенные в воде, и притягивает их, а вода становится чище.
Обратный осмос
Принцип очистки заключается в том, что воду под большим давлением пропускают через полупроницаемую мембрану, мельчайшие поры которой, пропускают молекулы воды, но задерживают примеси. Этот метод в сочетании с остальными позволяет получить бидистиллированную воду, которая считается самой чистой на сегодняшний день.
Области применения
В любой воде содержатся минеральные соли, мы даже часто покупаем специальную минеральную воду с повышенным содержанием некоторых солей.
Но мы также знаем, что жесткая вода или вода с повышенным содержанием солей калия и кальция, малопригодна для бытовых нужд. При стирке она образует осадок, который выводит из строя стиральные машины, а на чайнике появляется в виде накипи.
Но если для быта нам необходимо лишь слегка уменьшить содержание солей, то для фармакологической и пищевой промышленности. Такая вода необходима на нефтехимических предприятиях и производствах, занимающихся обработкой металлов.
Еще одна группа, использующая деминерализованную воду – автомобилисты. Они доливают воду глубокой отчистки в антифриз. В охлаждающей жидкости содержится вода, но при смене погоды она может испаряться. Так же такая вода необходима для работы омывателя стекол
Лишь обессоленная вода может являться диэлектриком, так как ионы солей в растворе способны проводить электричество. Это открывает еще одно поле использования: в научно-исследовательских целях. Деминерализованная вода нашла свое применения в области энергетики.
Последнее время деионизированная вода более популярна, чем дистиллированная. Устройства для дистилляции быстрее изнашиваются из-за наличия солей в жидкости, в то время как деминерализация менее затратна.
Вред от потребления обессоленной воды
Если деминерализованная вода полезна для приборов и машин, то влияние на человека не так однозначно. Вода глубокой отчистки способна вымывать из организма соли, порой это бывает необходимо. Например, доказано положительное влияние умеренного потребления обессоленной воды при:
- обнаружении отложений в печени;
- нарушении работы почек;
- диабете;
- аллергии;
- интоксикации и отравлениях.
Но принимать воду глубокой отчистки рекомендуется только посоветовавшись с врачом и малыми порциями.
Помимо вредных примесей в воде присутствуют также и полезные, но вода глубокой очистки лишена любых примесей, как часто выражаются врачи: это «мертвая» вода.
Некоторые примеси необходимы для нормальной работы организма, но деионизированная вода не содержит этих примесей и не поддерживает реакции. К тому же такая вода невкусная, она абсолютно пресная и не устраняет чувство жажды.
Регулярное употребление воды глубокой отчистки в пищу может привести к разрушению слизистой оболочки желудочно-кишечного тракта. Это показывают эксперименты на крысах.
Однозначно доказано пагубное влияние на процесс обмена минеральными веществами при употреблении обессоленной воды. Эта вода вымывает минеральные вещества из биологических жидкостей. Что влияет на гормональный фон и производство красных кровяных телец. В то же время, увеличивается выделение воды из организма.
При частом употреблении слабо минеральной воды уменьшается концентрация кальция и магния в организме. Кальций является строительным веществом многих костей и тканей организма, а магний необходим для протекания более чем трехсот биологических процессов.
Также было доказано, что при регулярном потреблении деминерализованной воды возрастает поступление токсичных металлов. «Мертвая» вода обладает слабыми защитными свойствами.
Источник
Дистиллированная и деминерализованная вода
Природная вода всегда содержит различные примеси, от характера и концентрации которых зависит ее пригодность для тех или иных целей.
Питьевая вода, подаваемая централизованными хозяйственно-питьевыми системами водоснабжения и водопроводами, по ГОСТ 2874-73, может иметь общую жесткость до 10,0 мг-экв/л, а сухой остаток до 1500 мг/л.
Естественно, что подобная вода непригодна для приготовления титрованных растворов, для выполнения различных исследований в водной среде, для многих препаративных работ, связанных с применением водных растворов, для ополаскивания лабораторной посуды после мытья и т. п.
Дистиллированная вода
Метод деминерализации воды дистилляцией (перегонкой) основан на разности давлений паров воды и растворенных в ней солей. При не очень высокой температуре можно принять, что соли практически нелетучи и деминерализованная вода может быть получена испарением воды и последующей конденсацией ее паров. Этот конденсат принято называть дистиллированной водой.
Вода, очищенная методом дистилляции в перегонных аппаратах, используется в химических лабораториях в количествах больших, чем другие вещества.
По ГОСТ 6709-72, вода дистиллированная — прозрачная, бесцветная жидкость, не имеющая запаха, с pH = 5,44-6,6 и содержанием сухого остатка не более 5 мг/л.
По Государственной фармакопее, сухой остаток в дистиллированной воде не должен превышать 1,0 мг/л, а pH = 5,0 4-6,8. Вообще требования к чистоте дистиллированной воды по Государственной фармакопее выше, чем по ГОСТ 6709-72. Так, фармакопея допускает содержание растворенного аммиака не более 0,00002%, ГОСТ не более 0,00005%.
Дистиллированная вода не должна содержать восстанавливающих веществ (органические вещества и восстановители неорганической природы).
Наиболее четкий показатель чистоты воды — ее электропроводимость. По литературным данным, удельная электрическая проводимость идеально чистой воды при 18°С равна 4,4*10 в минус 10 См*м-1,
При небольшой потребности в дистиллированной воде перегонку воды молено осуществить при атмосферном давлении в обычных установках из стекла.
Однократно перегнанная вода обычно загрязнена СO2, NH3 и органическими веществами. Если требуется вода с очень низкой проводимостью, то необходимо полностью удалить СO2. Для этого через воду при 80-90 °С в течение 20-30 ч пропускают сильную струю очищенного от СO2 воздуха и затем воду перегоняют при очень медленном токе воздуха.
Для этой цели рекомендуется применять сжатый воздух из баллона или засасывать его извне, поскольку в химической лаборатории он весьма загрязнен. Воздух до подачи в воду пропускают сначала через промывную склянку с конц. H2SO4, затем через две промывные склянки с конц. КОН и, наконец, через склянку с дистиллированной водой. При этом следует избегать применения длинных резиновых трубок.
Большую часть СO2 и органических веществ можно удалить, если к 1 л перегоняемой воды добавлять около 3 г NaOH и 0,5 г KMnO4 и отбрасывать некоторое количество конденсата в начале перегонки. Кубовый остаток должен составлять не менее 10-15% загрузки. Если конденсат подвергнуть вторичной перегонке с добавлением 3 г KHSO4, 5 мл 20% Н3РО4 и 0,1-0,2 г KMnO4 на литр, то это гарантирует полное удаление NH3 и органических загрязнений.
Продолжительное хранение дистиллированной воды в стеклянной посуде всегда приводит к ее загрязнению продуктами выщелачивания стекла. Поэтому дистиллированную воду долго хранить нельзя.
Металлические дистилляторы
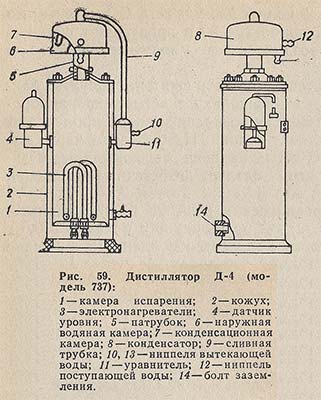
Дистилляторы с электронагревом. На рис. 59 изображен дистиллятор Д-4 (модель 737). Производительность 4 ±0,3 л/ч, потребляемая мощность 3,6 кВт, расход охлаждающей воды до 160 л/ч. Масса аппарата без воды 13,5 кг.
В камере испарения 1 вода нагревается электронагревателями 3 до кипения. Образующийся пар через патрубок 5 поступает в конденсационную камеру 7, вмонтированную в камеру 6, через которую непрерывно протекает водопроводная вода. Из конденсатора 8 дистиллят вытекает через ниппель 13.
В начале работы водопроводная вода, непрерывно поступающая через ниппель 12, заполняет водяную камеру 6 и по сливной трубке 9 через уравнитель 11 заполняет камеру испарения до установленного уровня.
В дальнейшем, по мере выкипания, вода будет поступать в камеру испарения только частично; основная же часть, проходя через конденсатор, точнее через его водяную камеру 6, будет сливаться по сливной трубке в уравнитель и далее через ниппель 10 в канализацию. Вытекающая горячая вода может быть использована для хозяйственных нужд.
Аппарат снабжен датчиком уровня 4, предохраняющим электронагреватели от перегорания в случае понижения уровня воды ниже допустимого.
Избыток пара из камеры испарения выходит через трубку, вмонтированную в стенку конденсатора.
Аппарат устанавливают на ровной горизонтальной поверхности и посредством болта заземления 14 присоединяют к общему контуру заземления, к которому также присоединяют электрощит.
При первоначальном пуске аппарата пользоваться дистиллированной водой по прямому назначению можно только после 48-часовой работы аппарата.
Периодически необходимо механически очищать от накипи электронагреватели и поплавок датчика уровня.
Аналогично устроен дистиллятор Д-25 (модель 784), производительность которого 25 ±1,5 л/ч, потребляемая мощность 18 кВт.
В этом аппарате девять электронагревателей — три группы по три нагревателя. Для нормальной и длительной работы аппарата достаточно, чтобы одновременно включались шесть нагревателей. Но для этого требуется периодически, в зависимости от жесткости питающей воды, производить механическую очистку от накипи трубки, по которой вода поступает в камеру испарения.
При первоначальном пуске дистиллятора Д-25 пользоваться дистиллированной водой по прямому назначению рекомендуется после 8-10 ч работы аппарата.
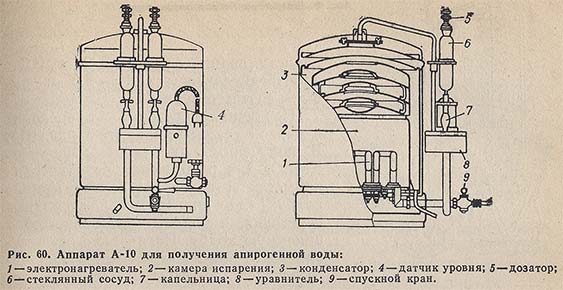
Значительный интерес представляет аппарат для получения апирогенной воды для инъекций А-10 (рис. 60). Производительность 10 ±0,5 л/ч, потребляемая мощность 7,8 кВт, расход охлаждающей воды 100-180 л/ч.
В этом аппарате в камеру испарения вместе с перегоняемой водой поступают реагенты для ее умягчения (алюмокалиевые квасцы Al2(SO4)3-K2SO4-24H2O) и для удаления NH3 и органических загрязнений (KMnO4 и Na2HPO4).
Раствор квасцов заливают в один стеклянный сосуд дозирующего устройства, а растворы KMnO4 и Na2HPO4 — в другой — из расчета на 1 л апирогенной воды квасцов 0,228 г, KMnO4 0,152 г, Na2НРO4 0,228 г.
При первоначальном пуске или при пуске аппарата после длительной консервации использовать получаемую апирогенную воду для лабораторных нужд можно только через 48 ч работы аппарата.
Перед эксплуатацией металлических дистилляторов с электронагревом следует проверить правильность включения всех проводов и наличие заземления. Категорически запрещается включать эти аппараты в электросеть, не заземлив. При любой неисправности дистилляторы должны быть отключены от сети.
Качество дистиллированной воды в известной степени зависит от длительности работы аппарата. Так, при пользовании старыми дистилляторами в воде могут содержаться хлорид-ионы.
Приемники должны быть из нейтрального стекла и, во избежание попадания СO2, соединены с атмосферой через хлоркальциевые трубки, наполненные гранулами натронной извести (смесь NaOH и Са(ОН)2).
Огневой дистиллятор. Дистиллятор ДТ-10 со встроенной топкой рассчитан на эксплуатацию в условиях отсутствия водопровода и электроэнергии и позволяет за 1 ч получать до 10 л дистиллированной воды. Представляет собой цилиндрической формы конструкцию из нержавеющей стали высотой около 1200 мм, смонтированную на основании длиной 670 мм и шириной 540 мм.
Дистиллятор состоит из встроенной топки с топочной фурнитурой, камеры испарения на 7,5 л, камеры охлаждения на 50 л и сборника дистиллированной воды на 40 л.
Вода в камеры испарения и охлаждения заливается вручную. По мере расхода воды в камере испарения она автоматически пополняется из камеры охлаждения.
Получение бидистиллята
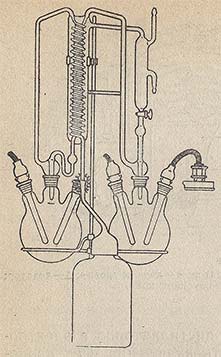
Однократно перегнанная вода в металлических дистилляторах всегда содержит небольшие количества посторонних веществ. Для особо точных работ пользуются повторно перегнанной водой — бидистиллятом. Промышленность серийно выпускает аппараты для бидистилляции воды БД-2 и БД-4 производительностью 1,5-2,0 и 4-5 л/ч соответственно.
Первичная перегонка происходит в первой секции аппарата (рис. 61). В полученный дистиллят добавляют KMnO4 для разрушения органических примесей и переводят его во вторую колбу, где происходит вторичная перегонка, и бидистиллят собирают в приемную колбу. Нагревание осуществляется с помощью электрических нагревателей; стеклянные водяные холодильники охлаждаются водопроводной водой. Все стеклянные детали изготовляются из стекла пирекс.
Определение качественных показателей дистиллированной воды
Определение pH. Это испытание производят потенциометрическим методом со стеклянным электродом или — при отсутствии рН-метра — колориметрическим методом.
Пользуясь штативом для колориметрирования (штатив для пробирок, снабженный экраном), в четыре занумерованные одинаковые пробирки диаметром около 20 мм и вместимостью 25-30 мл, чистые, сухие, из бесцветного стекла помещают: в пробирки № 1 и 2 — по 10 мл испытуемой воды, в пробирку № 3 — 10 мл буферной смеси, отвечающей pH = 5,4, а в № 4 — 10 мл буферной смеси, отвечающей pH = 6,6. Затем в пробирки № 1 и 3 прибавляют по 0,1 мл 0,04% водноспиртового раствора метилового красного и перемешивают. В пробирки № 2 и 4 прибавляют по 0,1 мл 0,04% водноспиртового раствора бромтимолового синего и перемешивают. Воду считают соответствующей стандарту, если содержимое пробирки № 1 не краснее содержимого пробирки № 3 (pH = 5,4), а содержимое пробирки № 2 не синее содержимого пробирки № 4 (pH = 6,6).
Определение сухого остатка. В предварительно прокаленной и взвешенной платиновой чашке выпаривают на водяной бане досуха 500 мл испытуемой воды. Воду прибавляют в чашку порциями по мере испарения, а чашку защищают от загрязнения предохранительным колпачком. Затем чашку с сухим остатком выдерживают 1 ч в сушильном шкафу при 105-110 °С, охлаждают в эксикаторе и взвешивают на аналитических весах.
Воду считают соответствующей ГОСТ 6709-72, если масса сухого остатка будет не более 2,5 мг.
Определения содержания аммиака и аммонийных солей. В одну пробирку с притертой стеклянной пробкой вместимостью около 25 мл наливают 10 мл испытуемой воды, а в другую — 10 мл эталонного раствора, приготовленного следующим образом: 200 мл дистиллированной воды помещают в коническую колбу на 250-300 мл, прибавляют 3 мл 10% раствора NaOH и кипятят 30 мин, после чего раствор охлаждают. В пробирку с эталонным раствором прибавляют 0,5 мл раствора, содержащего 0,0005 мг NH4+. Затем в обе пробирки одновременно прибавляют по 1 мл реактива на аммиак (см. приложение 2) и перемешивают. Воду считают соответствующей стандарту, если наблюдаемая через 10 мин окраска содержимого пробирки будет не интенсивнее окраски эталонного раствора. Сравнение окраски производят по оси пробирок на белом фоне.
Проба на восстанавливающие вещества. 100 мл испытуемой воды доводят до кипения, прибавляют 1 мл 0,01 н. раствора KMnO4 и 2 мл разбавленной (1:5) H2SO4 и кипятят 10 мин. Розовая окраска испытуемой воды должна при этом сохраняться.
Деминерализация пресной воды ионообменным методом
При деионизации воды последовательно осуществляются процессы Н+ катионирования и ОН- анионирования, т. е. замещения содержащихся в воде катионов на ионы Н+ и анионов на ионы ОН-. Взаимодействуя друг с другом, ионы Н+ и ОН- образуют молекулу H2O.
Метод деионизации позволяет получать воду с более низким содержанием солей, чем обычная дистилляция, но при этом не удаляются неэлектролиты (органические загрязнения).
Выбор между дистилляцией и деионизацией зависит от жесткости исходной воды и расходов, связанных с ее очисткой. В отличие от дистилляции воды, при деионизации расход энергии пропорционален содержанию солей в очищаемой воде. Поэтому при высокой концентрации солей в исходной воде целесообразно вначале применять метод дистилляции, а затем доочистку осуществить деионизацией.
Иониты — твердые, практически нерастворимые в воде и органических растворителях вещества минерального или органического происхождения, природные и синтетические. Для целей деминерализации воды практическое значение имеют синтетические полимерные иониты — ионообменные смолы, отличающиеся высокой поглотительной способностью, механической прочностью и химической устойчивостью.
Деминерализацию воды можно осуществлять последовательным пропусканием водопроводной воды через колонку катионита в Н+ форме, затем через колонку анионита в ОН- форме. Фильтрат с катионита содержит при этом кислоты, соответствующие солям в исходной воде. Полнота удаления этих кислот анионитами зависит от их основности. Сильноосновные аниониты удаляют все кислоты почти полностью, слабоосновные не удаляют таких слабых кислот, как угольная, кремневая и борная.
Если эти кислотные группы допустимы в деминерализованной воде или их соли отсутствуют в исходной воде, то лучше применять слабоосновные аниониты, так как их последующая регенерация легче и дешевле, чем регенерация сильноосновных анионитов.
Для деминерализации воды в лабораторных условиях часто применяют катиониты марок КУ-1, КУ-2, КУ-2-8чС и аниониты марок ЭДЭ-10П, АН-1 и др. Иониты, поставляемые в сухом виде, измельчают и отсеивают зерна размером 0,2-0,4 мм при помощи набора сит. Затем их промывают дистиллированной водой декантацией, пока промывные воды не станут совершенно прозрачны. После этого иониты переносят в стеклянные колонки различных конструкций.
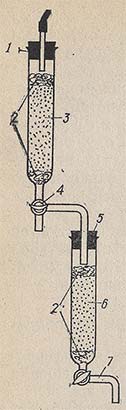
На рис. 62 изображена малогабаритная колонка для деминерализации воды. В нижнюю часть колонки помещают стеклянные бусы и поверх них стеклянную вату. Чтобы между зернами ионитов не попали пузырьки воздуха, колонку заполняют смесью ионита с водой. Воду по мере ее накопления спускают, но не ниже уровня ионита. Сверху иониты покрывают слоем стеклянной ваты и бусами и оставляют под слоем воды на 12-24 ч. Спустив воду с катионита, колонку заполняют 2 н. раствором HCl, оставляют на 12-24 ч, спускают HCl и катионит промывают дистиллированной водой до нейтральной реакции по метиловому оранжевому. Катионит, переведенный в Н+ форму, сохраняют под слоем воды. Аналогично переводят анионит в ОН- форму, выдерживая его в колонке после набухания в 1 н. растворе NaOH. Промывку анионита дистиллированной водой проводят до нейтральной реакции по фенолфталеину.
Деминерализация относительно больших объемов воды с раздельным применением ионитных фильтров может быть осуществлена в более крупной установке. Материалом для двух колонок высотой 700 и диаметром 50 мм может служить стекло, кварц, прозрачный пластик. В колонки помещают по 550 г подготовленного ионита: в одну — катионит в Н+ форме, в другую анионит — в ОН- форме. Водопроводная вода со скоростью 400-450 мл/мин поступает в колонку с катионитом, а затем проходит через колонку с анионитом.
Поскольку иониты постепенно насыщаются, необходимо контролировать работу установки. В первых порциях фильтрата, прошедшего через катионит, определяют кислотность титрованием щелочью по фенолфталеину. После того, как через установку пропустят около 100 л воды, или она проработает непрерывно 3,5 ч, следует взять вновь пробу воды из катионитной колонки и определить кислотность фильтрата. Если наблюдается резкое уменьшение кислотности, пропускание воды следует прекратить и провести регенерацию ионитов.
Катионит высыпают из колонки в большую банку с 5% раствором HCl и оставляют на ночь. Затем кислоту сливают, катионит переносят на воронку Бюхнера и промывают дистиллированной водой до отрицательной реакции на ион Cl- с AgNO3. Промытый катионит снова вводят в колонку.
Анионит регенерируют 5% раствором NaOH, промывают водой до отрицательной реакции по фенолфталеину, после чего вновь заполняют им колонку.
В настоящее время деминерализацию воды большей частью осуществляют методом смешанного слоя. Исходную воду пропускают через смесь катионита в Н+ форме и сильно- или слабоосновного анионита в ОН- форме. Этот метод обеспечивает получение воды высокой степени чистоты, но последующая регенерация ионитов требует больших затрат труда.
Для деионизации воды с применением смешанных ионитных фильтров смесь катионита КУ-2-8чС и анионита ЭДЭ-10П в объемном соотношении 1,25:1 загружают в колонку диаметром 50 мм и высотой 600-700 мм. В качестве материала для колонки предпочтителен плексиглас, а для подводящей и сточной трубок — полиэтилен.
Один килограмм смеси ионита может очистить до 1000 л однократно перегнанной воды.
Регенерацию отработанных смешанных ионитов производят раздельно. Смесь ионитов из колонки переносят на воронку Бюхнера и отсасывают до получения воздушно-сухой массы. Затем иониты помещают в делительную воронку такой вместимости, чтобы смесь ионитов занимала 1/4 ее объема. После этого в воронку добавляют до 3/4 объема 30% раствор NaOH и энергично перемешивают. При этом смесь ионитов благодаря их разной плотности (катионит 1,1, анионит 1,4) разделяется на слои. После этого катионит и анионит отмывают водой и регенерируют как указано выше.
В лабораториях, где потребность в глубоко обессоленной воде превышает 500-600 л/сутки, может быть использован серийно выпускаемый аппарат Ц 1913. Расчетная производительность 200 л/ч. Пропускная способность деионизатора за межрегенерационный период 4000 л. Масса комплекта 275 кг.
Деминерализатор снабжен системой автоматического отключения подачи водопроводной воды при понижении ее электрического сопротивления ниже допустимого значения и поплавковыми клапанами, позволяющими автоматически удалять воздух из колонок. Регенерация ионообменных смол производится путем обработки их непосредственно в колонках раствором NaOH или HCl.
Источник