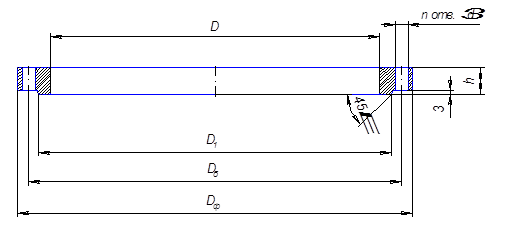ФАЗОВОЕ РАВНОВЕСИЕ В СИСТЕМЕ ЭТАНОЛ — ВОДА



ПОЛУЧЕНИЕ СПИРТА-СЫРЦА
Летучесть отдельных компонентов смеси характеризуют коэффициентом испарения (К= Y/X) —отношением концентрации данного вещества в паровой фазе Y к концентрации его в жидкой фазе X при равновесном состоянии фаз.
Летучая часть бражки состоит в основном, из воды и этилового спирта, поэтому в процессе выделения спирта бражку рассматривают как бинарную смесь этилового спирта и воды. Зависимость между составом паровой и жидкой фазы летучих веществ определяется законами Д. П. Коновалова и М. С. Вревского.
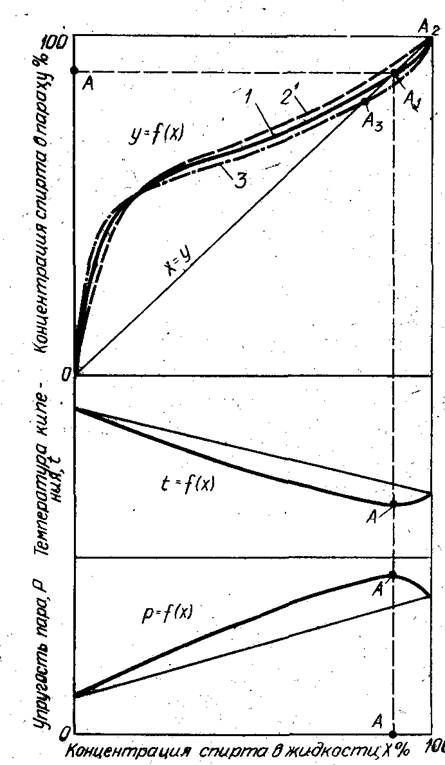
В верхней части рис. 1 линия 1 изображает зависимость равновесного состава пара У от состава жидкости X при атмосферном давлении и температуре кипения для смеси этиловый спирт — вода. Она представляет собой геометрическое место точек значений коэффициентов испарения этилового спирта Kэ.c = Y/X из водно-спиртовой смеси. При малых концентрациях спирта в смеси значения Kэ.c максимальны (около 13), при больших — минимальны (около 1).
Линия равновесного состава в точке А пересекает диагональ, следовательно, в этой точке состав паровой и жидкой фазы одинаковый. Эта точка получила название азеотропной точки, или точки нераздельного кипения. Для нее Y=X, или Kэ.c = 1. При нормальном давлении нераздельнокипящая смесь системы этиловый спирт — вода содержит 97,2 об.% (95,57 мас.%) этилового спирта при температуре кипения 78,15°С; при том же давлении температура кипения этилового спирта равна 78,3°С, а воды 100°С.
Рис. 1 Зависимость равновесного содержания пара. Температуры кипения и упругости пара от концентрации водно-спиртового раствора при давлении:
1 – атмосферное; 2 – ниже атмосферного; 3 – выше атмосферного.
В соответствии с законом Вревского при повышении давления растворы с низкой концентрацией спирта, примерно до 30— 40 мас.%, образуют пары с большим содержанием спирта, а растворы с высокой концентрацией спирта — пары с меньшим содержанием спирта, что наглядно показано в верхней части рис. 1 пунктирной линией. Из рисунка также видно, что с изменением давления сдвигается и положение азеотропной точки. Так, при давлении 93 кПа (температура кипения 27°С) нераздельнокипящая точка смещается вправо вплоть до Х= 100, т. е. при этом давлении пар всегда будет иметь большую концентрацию спирта, чем исходная жидкость (вплоть до 100%).
Анализируя положение кривой фазового равновесия, легко установить, что при атмосферном давлении пары над жидкостью будут обогащаться этиловым спиртом только до азеотропной тонки. Следовательно, путем ректификации (многократного испарения и конденсации) при атмосферном давлении можно достигнуть максимальной крепости спирта 97,2 об. %. Чтобы получить спирт большей крепости, необходимо уменьшить давление; тогда азеотропная точка сдвинется вправо, т. е. в область требующейся крепости. Этим приемом иногда пользуются на практике при получении абсолютного спирта.
Фазовое равновесие в бинарной смеси, этиловый спирт — вода при атмосферном давлении изучено В. Н. Стабниковым и О. Г. Мудравской. По их данным строят график фазового равновесия, который широко применяют для расчета процесса ректификации и анализа работы ректификационных колонн. В ряде случаев возникает необходимость иметь аналитическую зависимость указанного равновесия, которая по тем же данным установлена П. С. Цыганковым (табл.1).
| Интервалы концентраций, мол. % | Уравнения для Y, мол. % |
| 0—23 | Х/(0,014595 + 0,0773) |
| 23—55 | 0,395 Х + 45,52 |
| 55-66,5 | 0,5087Х + 39,27 |
| 66,5—82 | 0,6548X +29,56 |
| 82—89,4 . | 0,8113Х + 15,08 |
Наличие сухих веществ в водно-спиртовых растворах, как показано работами С. Е. Харина и В. М. Перелыгина, немного увеличивает концентрацию спирта в парах, однако в практических расчетах обычно пользуются кривой фазового равновесия для чистых водно-спиртовых растворов.
Источник
Теория фазового состояния водно-спиртовой смеси: температура, давление, концентрация
А никто не помнит где исходные данные лежат с которых Руди свой калькулятор ваял. Kotische, 14 Нояб. 16, 14:25
Посл. ред. 14 Нояб. 16, 21:32 от Чапаев1945
примерно такие же уравнения для расчета у Стабникова в приложенной книге.. Чапаев1945, 14 Нояб. 16, 19:42
Осталась самая малость: загнать уравнения в эксел. И я обязуюсь получить фактуру цифр, которые мы сгрузим в этот самый эксел, и проверим сходимость теории прошлого с практикой домашнего винокурения нынешнего веков!
Посл. ред. 14 Нояб. 16, 21:41 от игорь223
Таблицу или функцию соответствия четрыех параметров.
Когда три известны, а четвертый вычисляется игорь223, 14 Нояб. 16, 11:44
Осталась самая малость: загнать уравнения в эксел. И я обязуюсь получить фактуру цифр, которые мы сгрузим в этот самый эксел, и проверим сходимость теории прошлого с практикой домашнего винокурения нынешнего веков! игорь223, 14 Нояб. 16, 21:40
Загнать в эксел можно любое уравнение (ну почти) но где брать переменные для этого уравнения? То что ты получишь экспериментально боюсь нам не поможет.
Вот на скрине уравнение. Я даже не уверен, что есть Д у них. Давление при заданных параметрах молярных объемов спирта и воды? Далее что входит в уравнение — лямбды даны вроде по тексту, а J1 и J2 люто считаются по другим уравнениям. Они собирают какие то эксперементальные значения и оценивают их согласно уравнению? А что за значения? Нифига понять не получается))))
Короче, я не против составить что то в экселе, но я должен понимать ЧТО я делаю, а я эти уравнения не понимаю до конца. Они такое ощущение привели только верхушку айсберга своих расчетов, а по этим крохам воспроизвести их расчет не могу даже просто умозрительно. Уравнения в книге Стабникова тоже не сахар. Без примеров ничего не понимаю. Может кто то понимает, тогда поделитесь мыслью. Сплошь и рядом приводят только итоговые выкладки, а промежуточные расчеты не показывают))) А без них.
Можно обратится к Крелю где он показывал как высчитывать нужное нам экспериментально. Крель «Руководство по ректификации. Там где то со станицы 64 очень интересная для нас информация. Нужно почитать внимательно. Читаю.
Появятся мысли как посчитать искомое напишу. Если ответ и есть, то он у Креля. Стабников и Цыганков для меня закручены ядрено)))
Добавлено через 5мин.:
Осилишь? игорь223, 14 Нояб. 16, 21:40
Попробую найти путь.
Добавлено через 13мин.:
Вот интересный способ по эталонному веществу. Можно посчитать и посмотреть какая погрешность будет. Вроде все на первый взгляд решаемо. Скан Уравнение_Крель.
Или еще способ по уравнению Антуана. См. скан.
Добавлено через 1мин.:
Нужно попробовать посчитать заведомо известное значение и сравнить. Но это завтра а сейчас я спать))))
Посл. ред. 14 Нояб. 16, 23:05 от Чапаев1945
Источник
Процентное содержание спирта в парах и жидкости
В основу современной теории ректификации положены закономерности перегонки двойных смесей, которые установлены Д. П. Коноваловым и М. С. Вревским.
Первый закон Коновалова устанавливает зависимость между составом жидкой и паровой фаз в системе этанол — вода, а второй — положение азеотропной точки на кривой, устанавливающей зависимость между упругостью пара Р (МПа) и составом жидкой смеси X (мас %):
Р = f(Х).
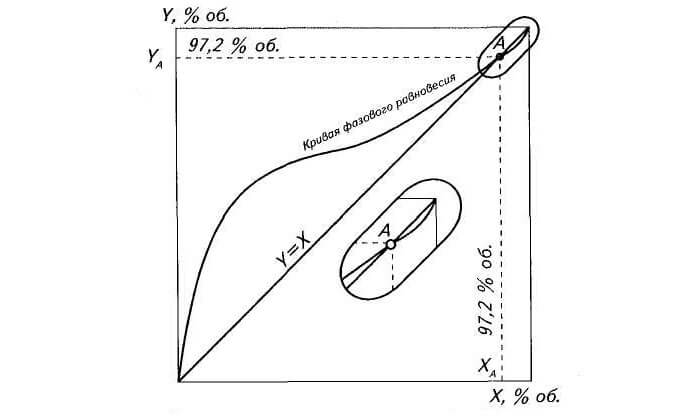
На рисунке ниже изображена кривая равновесной бинарной системы этиловый спирт — вода при нормальном давлении и температуре кипения смеси. На горизонтальной оси этого графика приведено содержание этанола х в жидкой фазе (мас. %), а на вертикальной оси — в паровой фазе у (мас. %).
Кривая равновесия системы этиловый спирт — вода при нормальном давлении:
х, у — концентрация спирта в парах и в жидкости соответственно
Кривая равновесия располагается выше диагонали (х = у) от начала координат до точки А, что свидетельствует об обогащении паровой фазы спиртом на указанном участке кривой равновесия. График представляет собой геометрическое место точек коэффициентов испарения этанола, которые наглядно характеризуют его летучесть в зависимости от состава жидкой фазы.
После точки А кривая равновесия проходит несколько ниже диагонали до правой верхней точки Б диаграммы. Следовательно, обогащение пара спиртом при содержании его в смеси более 95.57 мас. % невозможно. Лишь изменение давления в системе ниже нормального позволяет получать более крепкий спирт. В этом случае кривая равновесия располагается выше диагонали, вплоть до точки Б.
Законы Вревского указывают направление, в котором сдвигается равновесие в смеси этанол—вода при изменении давления в системе. Так, при давлении в системе 0,009 МПа и температуре кипения 27,92 С возможно получение безводного (абсолютного) спирта.
Таблица. Равновесие пар-жидкость смеси этиловый спирт-вода. Состав кипящей водно-спиртовой жидкости, образующегося из нее пара и температура кипения этой жидкости при атмосферном давлении.
Источник
Теоретические основы процесса ректификации и описание технологической схемы
Аннотация
Крашенинникова Е.В. Расчет ректификационной установки для разделения бинарной смеси этиловый спирт-вода. – Озёрск: ФГАОУ ВПО «УрФУ имени первого Президента России Б.Н. Ельцина» , 2010. – 50 с., 14 ил. Библиография – 10 назв.
В данной курсовой работе проведен расчет ректификационной колонны непрерывного действия с ситчатыми тарелками для разделения смеси этиловый спирт-вода производительностью 5000 кг/час по исходной смеси. Выполнен материальный и тепловой балансы, проведен гидравлический расчет, определены основные размеры аппарата и подобраны нормализованные конструктивные элементы. Подобраны испаритель и дефлегматор. Предложены способы повышения эффективности работы колонн с ситчатыми тарелками.
Задание на курсовую работу
Рассчитать ректификационную установку по следующим данным:
1. Тип аппарата: выбрать;
2. Разделяемая смесь: этиловый спирт – вода;
3. Производительность по сырью: 5 т/ч;
4. Концентрация НКК в:
· Дистилляте – 75% (мол.);
5. Давление греющего пара: 3 ат;
· Поступающего сырья – 10ºС;
· Воды, идущей на дефлегматор – 10ºС;
7. Давление в колонне: 1 ат.
Содержание
1 Теоретические основы процесса ректификации и описание технологической схемы
1.1 Теоретические основы процесса ректификации
1.2 Принцип работы ректификационного аппарата
1.3 Описание технологической схемы ректификационнй установки
2 Классификация и выбор ректификационных установок и вспомогательного оборудования
2.1 Классификация ректификационных установок по конструкции внутреннего устройства аппарата
2.2 Классификация ректификационных установок по периодичности действия
2.3 Классификация ректификационных установок по способу организации движения потоков контактирующих фаз
2.4 Выбор ректификационной установки
2.5 Колонны с ситчатыми тарелками для разделения смеси «этиловый спирт-вода»
2.6 Выбор вспомогательного оборудования
2.7 Выбор конструкционного материала
3 Материальный расчет колонны
3.1 Производительность колонны по дистилляту и кубовому остатку
3.2 Расчет оптимального флегмового числа и определение числа теоретических тарелок
3.3 Массовый поток пара в верхней и нижней частях колонны
3.4 Массовые расходы жидкости в верхней и нижней части колонны
4 Расчет диаметра колонны
4.1 Плотности компонентов
4.2 Скорость пара в колонне
4.3 Диаметр колонны
4.4 Характеристика тарелки (рис 8,9)
5 Расчет числа тарелок
5.1 Средний КПД тарелки
5.2 Высота колонны
6 Гидравлический расчет колонны
6.1 Гидравлическое сопротивление сухой тарелки
6.2 Гидравлическое сопротивление обусловленное силами поверхностного натяжения
6.3 Гидравлическое сопротивление газожидкостного слоя
6.4 Полное сопротивление тарелки
6.5 Суммарное гидравлическое сопротивление рабочей части колонны
7 Тепловой расчет колонны
7.1 Расход теплоты отдаваемой воде в дефлегматоре
7.2 Расход теплоты в кубе испарителе
7.3 Расход греющего пара
8 Конструктивный расчет
Введение
Ректификация – разделение жидких однородных смесей на составляющие вещества или группы составляющих веществ в результате взаимодействия паровой смеси и жидкой смеси. Это массообменный процесс, который осуществляется в большинстве случаев в противоточных колонных аппаратах с контактными элементами (насадки, тарелки), аналогичными используемыми в процессе абсорбции.
Возможность разделения жидкой смеси на составляющие её компоненты ректификацией обусловлена тем, что состав пара, образующегося над жидкой смесью, отличается от состава жидкой смеси в условиях равновесного состояния пара и жидкости.
Сущность процесса ректификации рассмотрена на примере разделения двухкомпонентной смеси по заданию на курсовую работу, где требуется рассчитать ректификационную установку для разделения смеси «этиловый спирт-вода».
Ректификационная установка даёт наиболее полное разделение смесей жидкостей, целиком или частично растворимых друг в друге. Процесс заключается в многократном взаимодействии паров с жидкостью – флегмой, полученной при частичной конденсации паров. В ректификационном аппарате снизу вверх движутся пары, а сверху подается жидкость, представляющая собой почти чистый НКК. При соприкосновении поднимающихся паров со стекающей жидкостью происходит частичная конденсация паров и частичное испарение жидкости. При этом из паров конденсируется преимущественно ВКК, а из жидкости испаряется преимущественно НКК. Таким образом, стекающая жидкость обогащается ВКК, а поднимающиеся пары обогащаются НКК, в результате чего выходящие из аппарата пары представляют собой почти чистый НКК. Эти пары поступают в конденсатор, называемый дефлегматором, и конденсируются. Часть конденсата, возвращаемая на орошение аппарата, называется флегмой, другая часть отводится в качестве дистиллята.
Как и во всех массобменных процессах эффективность ректификации зависит от поверхности контакта фаз. Для увеличения поверхности массобмена используют различные контактные устройства насадочного или барботажного типа. Наиболее распространенными ректификационными установками являются барботажные колонны с различными типами тарелок: колпачковыми, ситчатыми, провальными и т.п. Наиболее универсальны колонны с колпачковыми тарелками, но при разделении незагрязненных жидкостей в установках с постоянной нагрузкой, хорошо зарекомендовали себя аппараты с ситчатыми тарелками, отличающимися простотой конструкции и легкостью в обслуживании.
В данной курсовой работе рассмотрены основы процесса ректификации, классификация ректификационных колонн по конструкции внутреннего устройства, по периодичности действия и по способу организации движения потоков контактирующих фаз. Кроме того, представлены основные требования по выбору того или иного типа колонны. Согласно заданию на курсовую работу, в котором указаны компоненты бинарной смеси: этанол-вода, выбрана колонна с ситчатыми тарелками, и проведен её расчет по исходным данным, указанным в задании. Выполнен материальный и тепловой балансы, определены основные размеры аппарата и подобраны нормализованные конструктивные элементы.
Материальный расчет колонны
Расчет диаметра колонны
Плотности компонентов
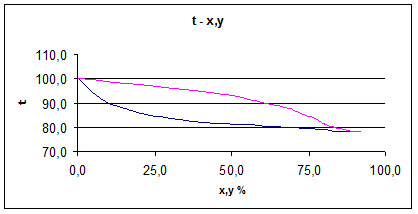
По диаграмме t — x, y* (рис 6), находим температуры исходной смеси, дистиллята и кубового остатка: tF = 86,80° C; tp = 77,50° C: tW = 96,0° C
Рис 6 – t-x,y диаграмма системы этиловый спирт – вода
Таблица 3 — Плотности компонентов при различных температурах, кг/м3
| t, ºC вещество | 86,80 | 77,50 | 96,0 |
| этанол | 739 | 732 | 727 |
| вода | 975 | 968 | 962 |
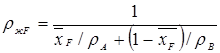
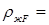

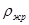
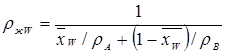
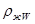
Средняя плотность жидкости в верхней и нижней части:
rвж = 0,5(rжF + rжр) (30)
rвж = 0,5×(903,34 + 772,20) = 837,77 кг/м3
rнж = 0,5(rжF + rжW) (31)
rнж = 0,5×(903,34 + 954,20) = 928,77 кг/м3
Плотность паров на питающей тарелке:
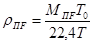
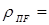
МпF = 0,362×46,1 + 0,638×18,0 = 28,136 кг/моль
Плотность паров в верхней части:
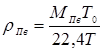
rпв = 29,94×273/[22,4×(273+79)] = 1,037 кг/м3
Плотность паров в нижней части:
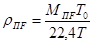
rпн = 28,68×273/[22,4×(273+82,5)] = 0,983 кг/м3
Скорость пара в колонне
Скорость пара в верхней части колонны:
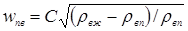
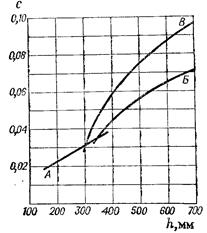
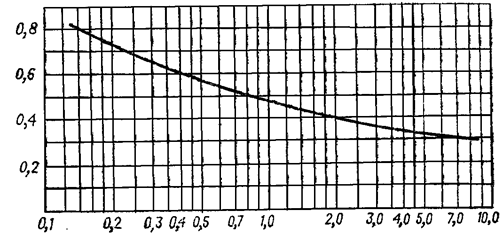
где С = 0,059 (при расстоянии между тарелками 400 мм) – коэффициент, зависящий от конструкции тарелок, расстояния между тарелками, рабочего давления в колонне, нагрузке колонны по жидкости (рис 7).
wпв = 0,059×[(837,70 – 1,037)/1,037]1/2 = 1,68 м/с
Рис 7 – Значение коэффициента С
А, Б – для колпачковых тарелок с круглыми колпачками; В – для ситчатых тарелок
Скорость пара в нижней части колонны:
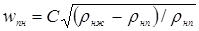
wпн = 0,059×[(928,77 – 0,983)/0,983]1/2 = 1,81 м/с
Диаметр колонны
· в верхней части:
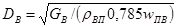
DB= [0,723 /(1,037×0,785×1,68)]1/2 = 0,73 м
Gв= 2604,13/3600 = 0,723 кг/с
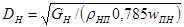
DH= [0,505/(0,983×0,785×1,81)]1/2 = 0,61 м
Gн= 1816,5/3600 = 0,505 кг/с
После определения диаметра колонны по уравнениям (37)-(38) уточним его в соответствии с имеющимися нормалями. Принимаем диаметр колонны 600 мм, тогда действительная скорость пара составит:
· в верхней части
wпв = 1,68×(0,73/0,6)2 = 1,044 м/с;
wпн = 1,81×(0,61/0,6)2 = 1,84 м/с.
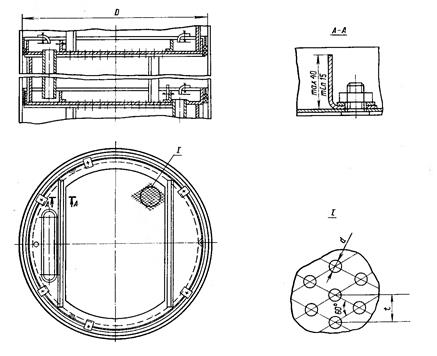
4.4 Характеристика тарелки (рис 8,9)
Принимаем тарелки типа ТС (ОСТ 26-01-108-85):
Исполнение I – неразборное;
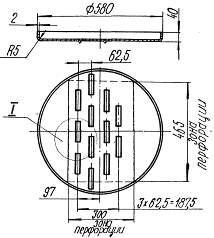
Диаметр тарелки – 580,00 мм (рис 9);
Высота тарелки – 40мм;
Свободное сечение колонны – 0,28 м2;
Рабочее сечение тарелки – 0,165 м2;
Свободное сечение тарелки – 0,51 м2;
Относительное свободное сечение тарелки (при dотверстий=5 мм) – 7,23%;
Шаг между отверстиями принимаем 13 мм;
Периметр слива – 0,570 м;
Сечение перелива – 0,012 м2;
Относительная площадь перелива – 4,1%;
Расстояние между тарелками – 300 мм;
Высота сливного порога – 30 мм;
Высота царги – 900 мм;
Число тарелок в царге – 3.
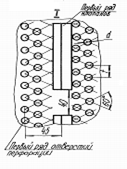
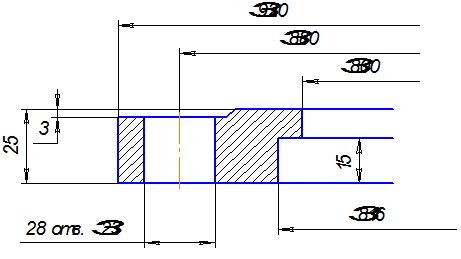
Рис 8 – Устройство ситчатых тарелок
Рис 9 – Основание тарелки по ОСТ 26-01-108-85
Расчет числа тарелок
Средний КПД тарелки
Вязкость жидкости на питающей тарелке:
lnm = х×lnmA + (1 – x)×lnmB (39)
где mА = 0,44 мПа×с – вязкость этанола;
mВ = 0,31 мПа×с – вязкость воды;
lnmж = 0,22×ln0,44 + (1 – 0,22)×ln0,31.
Откуда m = 0,33 мПа×с.
Коэффициент относительной летучести:
где рА = 1120 мм рт.ст. – давление насыщенного пара этанола;
рВ = 525 мм рт.ст. – давление насыщенного пара воды.
Произведение am = 2,13×0,33 = 0,704
По диаграмме для приближенного определения КПД тарелки (рис 10) находим значение h=0,56.
Рис 10 – Диаграмма для приближенного определения КПД тарелки
Тогда число тарелок:
· в верхней части колонны
· в нижней части колонны
Высота колонны
Принимаем расстояние между тарелками Нт = 300 мм, тогда высота нижней и верхней части составит:
Нн = (6 – 1)×0,3 = 1,5 м;
Нв = (Nв – 1)Нт = (12 – 1)×0,3 = 3,3 м.
Толщина тарелки – 0,04 м;
Высота сепарационного пространства – 0,7 м;
Высота кубового пространства – 2,3 м;
Высота опоры – 1,2 м;
Общая высота колонны:
Н = 1,2 + 2,3 + 0,7 + 18·0,04+ 3,3 + 1,5 =9,6 м
Тепловой расчет колонны
Расход греющего пара
Принимаем пар с давлением 0,3 МПа, для которого теплота конденсации
r = 2171 кДж/кг, тогда
Gп = 1362,52 / 2171 = 0,63 кг/c
Средняя разность температур в кубе испарителе
Dtср = tп – tw (59)
Dtср = 167 – 99 = 68° C
Ориентировочное значение коэффициента теплопередачи
К = 300 Вт/(м2×К), тогда требуемая поверхность теплообмена.
F = 1362,52×103/(300×68) = 66 м2
Принимаем стандартный кожухотрубчатый теплообменник с диаметром кожуха 600 мм и длиной труб 4 м, для которого поверхность теплообмена равна 75 м2 (Приложение Д).
Конструктивный расчет
Корпус колонны диаметром до 1000 мм изготовляют из отдельных царг (Приложение Б), соединяемых между собой с помощью фланцев.
S > pD/(2[s]j – p) + c (61)
где [s] = 138 МПа – допускаемое напряжение для стали [3c394];
j = 0,8 – коэффициент ослабления сварного шва;
с = 0,001 мм – поправка на коррозию [3с394].
S > 0,1×0,8/(2×138×0,8 – 0,1) + 0,001 = 0,003 м
Принимаем толщину обечайки s=8мм
Наибольшее распространение в химическом машиностроении получили эллиптические отбортованные днища по ГОСТ 6533 – 78.
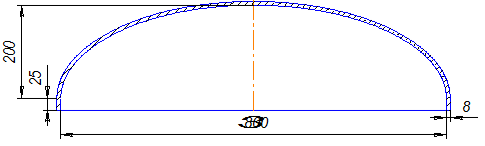
· Толщину стенки днища (рис 11) принимаем равной толщине стенки обечайки sд = s = 8 мм.
Рис 11 – Днище колонны
h = 40 мм – высота борта днища;
Масса днища mд = 16,9 кг.
Объем днища Vд = 0,086 м3.
Соединение обечайки с днищами осуществляется с помощью плоских приварных фланцев по ОСТ 26–428–79 (рис 12).
Подсоединение трубопроводов к аппарату осуществляется с помощью штуцеров.
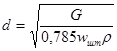
где wшт – скорость среды в штуцере.
Принимаем скорость жидкости wшт=1 м/с, газовой смеси wшт=25 м/с
Штуцер для входа исходной смеси
d1,2 = (1,39/0,785×1·903,34)0,5 = 0,044 м
принимаем d1 = d2 = 50 мм
Штуцер для входа флегмы
d3 = (1,8×0,34/0,785×1×772,20)0,5 = 0,033 м
принимаем d3 = 40 мм
Штуцер для выхода кубового остатка
d3 = (1,05/0,785×1×954,2)0,5 = 0,037 м
принимаем d4 = 40 мм
Штуцер для выхода паров
d3 = (0,72/0,785×25×1,037)0,5 = 0,188 м
принимаем d5 = 200 мм
Штуцер для входа паров
d6 = (0,5/0,785×25×0,983)0,5 = 0,17 м
принимаем d4 = 200 мм
Все штуцера должны быть снабжены плоскими приварными фланцами по ГОСТ 12820-80. Конструкция фланца приводится на рисунке 13, а размеры в таблице 4.
Рис 13 – Фланец штуцера
Таблица 4 – Размеры приварного фланца штуцера
| dусл | D | D2 | D1 | h | n | d |
| 40 | 130 | 100 | 80 | 13 | 4 | 14 |
| 50 | 140 | 110 | 90 | 13 | 4 | 14 |
| 200 | 315 | 280 | 258 | 18 | 8 | 18 |
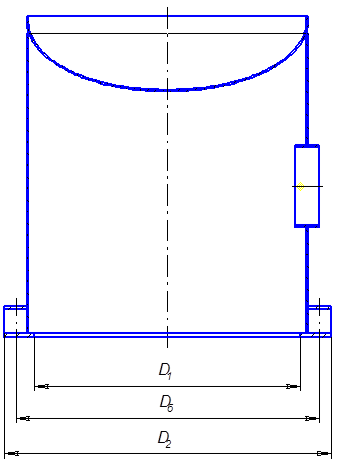
Аппараты вертикального типа с соотношением Н/D > 5, размещаемые на открытых площадках, оснащают так называемыми юбочными цилиндрическими опорами, конструкция которых приводится на рисунке 14.
Рис 14 – Опора юбочная
· Ориентировочная масса аппарата.
mоб = 0,785(Dн2-Dвн2)Нобρ (63)
где Dн = 0,616 м – наружный диаметр колонны;
Dвн = 0,6 м – внутренний диаметр колонны;
Ноб = 9,6 м – высота цилиндрической части колонны
ρ = 7900 кг/м3 – плотность стали
mоб = 0,785(0,6162-0,62)9,6·7900 = 952,55 кг
mт = 18·16,0 = 288,0 кг
m = 16,0 кг – масса одной тарелки
· Общая масса колонны
Принимаем, что масса вспомогательных устройств (штуцеров, измерительных приборов, люков и т.д.) составляет 10% от основной массы колонны, тогда
mк = mоб + mт + 2mд (65)
mк = 1,1(952,55 + 288,0 +2·16,9) = 1401,79 кг≈1402 кг
Масса колонны заполненной водой при гидроиспытании
Масса воды при гидроиспытании:
mв = 1000(0,785D2Hц.об + 2Vд) (66)
mв = 1000(0,785·0,62·9,6 + 2·0,086) = 2884,96 кг≈2885 кг
ректификационный колонна ситчатый этанол вода
Максимальный вес колонны
mmax = mк + mв (67)
mmax = 1402 + 2885 = 4280 кг = 0,042 МН
Принимаем внутренний диаметр опорного кольца D1 = 0,55 м, наружный диаметр опорного кольца D2 = 0,8 м.
Источник