- Фенолы
- Классификация фенолов
- По числу гидроксильных групп:
- Строение фенолов
- Химические свойства фенолов
- 1.1. Взаимодействие с раствором щелочей
- 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
- 2. Реакции фенола по бензольному кольцу
- 2.1. Галогенирование
- 2.2. Нитрование
- 3. Поликонденсация фенола с формальдегидом
- 4. Взаимодействие с хлоридом железа (III)
- 5. Гидрирование (восстановление) фенола
- Получение фенолов
- 1. Взаимодействие хлорбензола с щелочами
- 2. Кумольный способ
- 3. Замещение сульфогруппы в бензол-сульфокислоте
- Фенолы
- Фенол взаимодействует с бромной водой бензолом
Фенолы
Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
Классификация фенолов
По числу гидроксильных групп:
- фенолы с одной группой ОН — содержат одну группу -ОН. Общая формула CnH2n-7OH или CnH2n-6O.
- фенолы с двумя группами ОН — содержат две группы ОН. Общая формула CnH2n-8(OH)2 или CnH2n-6O2.
| Соединения, в которых группа ОН отделена от бензольного кольца углеродными атомами – это не фенолы, а ароматические спирты: |
Строение фенолов
В фенолах одна из неподеленных электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца, это является главной причиной отличия свойств фенола от спиртов.
Химические свойства фенолов
| Сходство и отличие фенола и спиртов. |
Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода.
Отличия:
- фенол не реагирует с галогеноводородами: ОН- группа очень прочно связана с бензольным кольцом, её нельзя заместить;
- фенол не вступает в реакцию этерификации, эфиры фенола получают косвенным путем;
- фенол не вступает в реакции дегидратации.
- фенол обладает более сильными кислотными свойствами и вступает в реакцию со щелочами.
1. Кислотные свойства фенолов
| Фенолы являются более сильными кислотами, чем спирты и вода, т. к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается. |
Раствор фенола в воде называют «карболовой кислотой», он является слабым электролитом.
1.1. Взаимодействие с раствором щелочей
В отличие от спиртов, фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты.
| Например, фенол реагирует с гидроксидом натрия с образованием фенолята натрия |
Так как фенол – более слабая кислота, чем соляная и даже угольная, его можно получить из фенолята, вытесняя соляной или угольной кислотой:
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Фенолы взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются феноляты. При взаимодействии с металлами фенолы ведут себя, как кислоты.
| Например, фенол взаимодействует с натрием с образованием фенолята натрия и водорода . |
2. Реакции фенола по бензольному кольцу
| Наличие ОН-группы в бензольном кольце (ориентант первого рода) приводит к тому, что фенол гораздо легче бензола вступает в реакции замещения в ароматическом кольце. |
2.1. Галогенирование
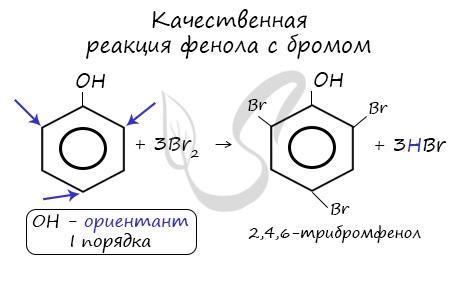
| Фенол легко при комнатной температуре (без всякого катализатора) взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол). |
2.2. Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов.
| Например, при нитровании фенола избытком концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота): |
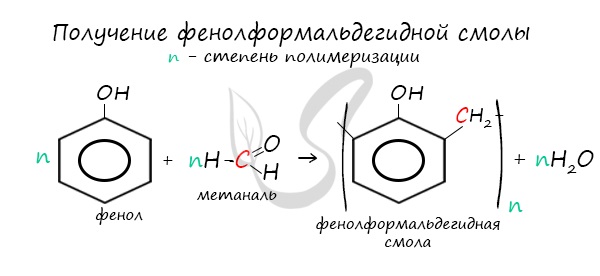
3. Поликонденсация фенола с формальдегидом
С формальдегидом фенол образует фенолоформальдегидные смолы.
4. Взаимодействие с хлоридом железа (III)
При взаимодействии фенола с хлоридом железа (III) образуются комплексные соединения железа, которые окрашивают раствор в сине-фиолетовый цвет. Это качественная реакция на фенол.
5. Гидрирование (восстановление) фенола
Присоединение водорода к ароматическому кольцу.
Продукт реакции – циклогексанол, вторичный циклический спирт.
Получение фенолов
1. Взаимодействие хлорбензола с щелочами
При взаимодействии обработке хлорбензола избытком щелочи при высокой температуре и давлении образуется водный раствор фенолята натрия.
При пропускании углекислого газа (или другой более сильной кислоты) через раствор фенолята образуется фенол.
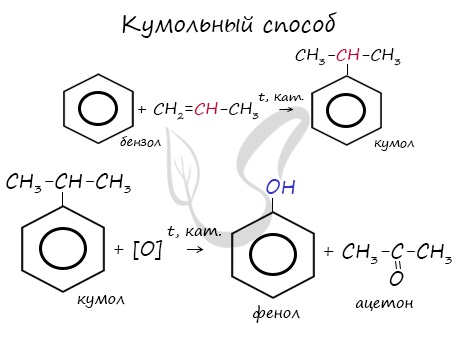
2. Кумольный способ
Фенол в промышленности получают из каталитическим окислением кумола.
Первый этап процесса – получение кумола алкилированием бензола пропеном в присутствии фосфорной кислоты:
Второй этап – окисление кумола кислородом. Процесс протекает через образование гидропероксида изопропилбензола:
Суммарное уравнение реакции:
3. Замещение сульфогруппы в бензол-сульфокислоте
Бензол-сульфокислота реагирует с гидроксидом натрия с образованием фенолята натрия:
Получается фенолят натрия, из которого затем выделяют фенол:
Источник
Фенолы
Фенолы — кислородсодержащие ароматические соединения, в молекулах которых содержится одна или несколько гидроксильных групп (OH), присоединенных к бензольному кольцу.
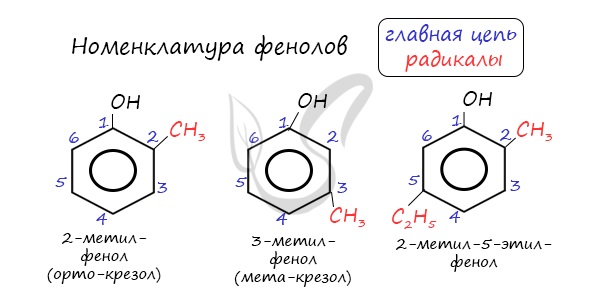
Номенклатура фенолов
Нумерацию атомов углерода в молекуле фенола начинают в такой последовательности, чтобы заместители получили наименьшие номера (идут кратчайшим путем). В основе названия принято сохранять тривиальное название «фенол».
Напомню, что гидроксильная группа является ориентантом I порядка (орто-, пара-ориентант). Поэтому реакции галогенирования, нитрования протекают в орто- и пара-положениях.
Получение фенолов
При гидролизе галогенбензолов происходит обмен: гидроксогруппа встает на место атома галогена.
Этим способом получают 95% всего производимого фенола. В ходе этой реакции кумол (изопропилбензол) подвергают окислению, в результате получается фенол и ацетон.
Химические свойства фенолов
Щелочные металлы (Li, Na, K) способны вытеснять водород из фенолов с образованием солей — фенолятов. В отличие от алифатических одноатомных спиртов, фенолы способны вступать в реакцию с щелочами (KOH, LiOH, NaOH)
Реакция фенола с бромной водой является качественной: в ходе нее выпадает белая взвесь — осадок трибромфенола.
Реакция между фенолом и азотной кислотой происходит по типу замещения. В бензольном кольце появляется новый радикал — нитрогруппа. Важно учитывать, что OH группа фенола является ориентантом I порядка: замещение идет в орто-, пара-положении.
При гидрировании разрываются двойные связи бензольного кольца, образуется циклогексанол.
В промышленности получила широкое распространение реакция поликонденсации фенола с формальдегидом, приводящая к образованию смолообразных полимеров (фенолформальдегидные смолы) и воды.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Фенол взаимодействует с бромной водой бензолом
4) гидроксидом натрия
5) азотной кислотой
6) оксидом кремния (IV)
Фенолы- кислородсодержащие органические соединения, в молекуле которых гидроксогруппа связанна непосредственно с бензольным кольцом. Фенолы реагируют с щелочными металлами, а также со щелочами. Вступают в реакции по бензольному кольцу: галогенирование и нитрование в 2,4,6 положениях.
Фенол реагирует с
3) гидроксидом натрия
6) оксидом углерода(IV)
Фенолы — кислородсодержащие органические соединения, в молекуле которых гидроксогруппа связанна непосредственно с бензольным кольцом. Фенолы как и спирты реагируют с щелочными металлами, а также со щелочами. Вступают в реакции по бензольному кольцу: галогенирование и нитрование в 2,4,6 положениях. И конечно же реакция горения — взаимодействие с кислородом. Правильный ответ: 1,3,5
Фенол реагирует с
3) гидроксидом натрия
6) оксидом углерода(IV)
Как и другие органические соединения, окисляется кислородом; реагирует со щелочами и натрием по гидроксильной группе фенола.
Верны ли следующие суждения о феноле?
А. Фенол взаимодействует с бромной водой.
Б. Для фенола характерны основные свойства.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Фенол реагирует с бромной водой (образование в данном случае белого осадка 2,4,6-трибромфенола — качественная реакция на фенол)- поскольку это ароматическое соединение, содержащее сильную донорную группу. Фенолы обладают более выраженными кислотными свойствами, чем, спирты, соответственно — их основные свойства слабые (например, фенол реагирует с соляной кислотой только в жестких условиях).
здравствуйте, прорешивая данную работу, мои дети нашли некоторую неточность в формулировке ответа, а именно:
взаимодействие с бромной водой качественная реакция на кратные связи( алкены, алкины, алкадиены, циклоалкены, непредельные кислоты, при этом происходит разрыв ПИ связи).
взаимодействуют с Br2 алканы, ФЕНОЛЫ, амины, реакция замещения с образованием промежуточного карбокатиона.
пожалуйста, объясните нашу ошибку) определения взяты с учебника.
спасибо огромное за ваш сайт, очень помогает !
При реакции фенола с бромом действительно не происходит разрыва ПИ связей — происходит реакция электрофильного замещения с образованием белого осадка 2,4,6-трибромфенола, поэтому её тоже можно считать качественной реакцией.
Какое органическое соединение реагирует с натрием, гидроксидом калия и бромной водой?
1) диметиловый эфир
Фенол реагирует с натрием, гидроксидом калия это реакция замещения водорода в гидроксогруппе на атом металла. Реагирует с бромной водой, в отличие от бензола, реакция замещения протекает в бензольном кольце.
Верны ли следующие утверждения о феноле?
А. Фенол проявляет свойства сильной кислоты.
Б. Фенол реагирует как с бромной водой, так и с азотной кислотой.
1) Верно только А
2) Верно только Б
3) Верны оба утверждения
4) Оба утверждения неверны
Фенол это производное бензола, в котором атом водорода замещен на гидроксогруппу. В гидроксогруппе происходит реакции замещения водорода на атом металла , в этом проявляются кислотные свойства фенола. Фенол является очень слабой кислотой. При пропускании через раствор фенолятов углекислого или сернистого газов выделяется фенол — такая реакция доказывает, что фенол — более слабая кислота, чем угольная и сернистая Реагирует с бромной водой и азотной кислотой, реакция замещения протекает в бензольном кольце.
Источник