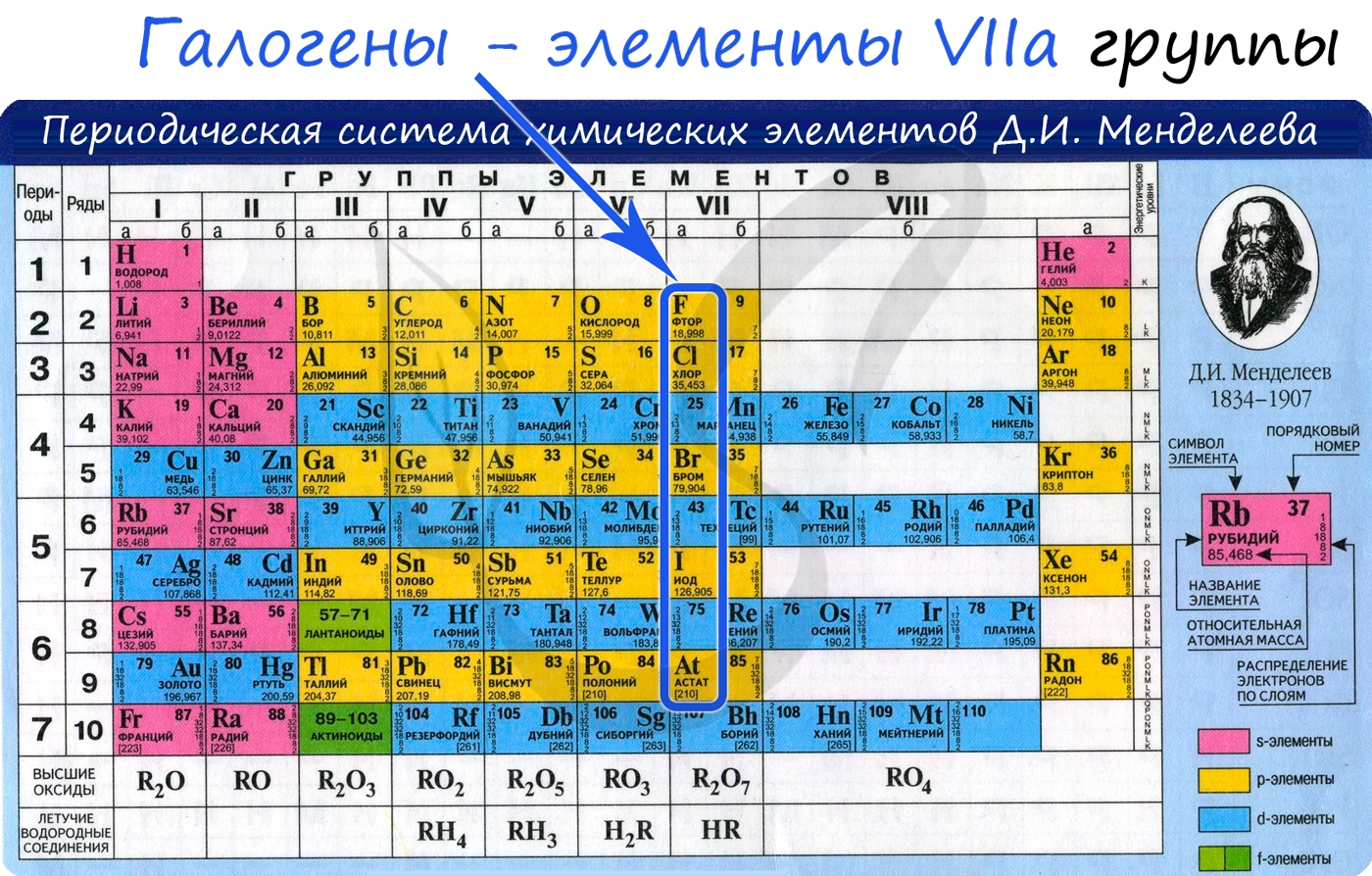
Подгруппа VII a. Галогены

Общая электронная конфигурация внешнего энергетического уровня — nS 2 nP 5 .
С возрастанием порядкового номера элементов увеличиваются радиусы атомов, уменьшается электроотрицательность, ослабевают неметаллические свойства (увеличиваются металлические свойства);
Галогены — сильные окислители, окислительная способность элементов уменьшается с увеличением атомной массы.
| Символ элемента | F | Cl | Br | I | At |
| Порядковый номер | 9 | 17 | 35 | 53 | 85 |
| Строение внешнего электронного слоя | 2s 2 2p 5 | 3s 2 3p 5 | 4s 2 4p 5 | 5s 2 5p 5 | 6s 2 6p 5 |
| Энергия ионизации, эв | 17,42 | 12,97 | 11,84 | 10,45 | |
| Относительная электроотрицательность (ЭО) | 4,0 | 3,0 | 2,8 | 2,5 | |
| Радиус атома, нм | 0,064 | 0,099 | 0,114 | 0,133 | – |
| Степени окисления | -1 | -1, +1, +3, +5, +7 | -1, +1, +3 +5, +7 | -1, +1, +3, +5, +7 | – |
Молекулы галогенов состоят из двух атомов.
С увеличением атомной массы окраска становится более темной, возрастают температуры плавления и кипения, а также плотность.
Фтор получают электролизом расплава гидрофторида калия KHF2 (разлагается лишь HF):
Анод: 2F — — 2ē → F2
В промышленности хлор в основном получают электролизом водного раствора хлорида натрия:
В лаборатории хлор получают действием различных окислителей на соляную кислоту:
Аналогично получают бром и иод, окисляя НВr, НI или их соли:
Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к йоду.
Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в атмосфере фтора самовоспламеняются, выделяя большое количество теплоты:
Без нагревания фтор реагирует и со многими неметаллами (H2, S, С, Si, Р) — все реакции при этом сильно экзотермические:
При нагревании фтор окисляет все другие галогены (их степень окисления +1):
При облучении фтор реагирует даже с инертными (благородными) газами:
Взаимодействие фтора со сложными веществами также протекает очень энергично:
Химические свойства Сl2
Свободный хлор реагирует со всеми простыми веществами, за исключением кислорода, азота и благородных газов:
Реакция замещения и присоединения с углеводородами:
Хлор способен при нагревании вытеснять бром или иод из их соединений с водородом или металлами:
Обратимо реагирует с водой:
Сl2 + Н2О↔ НСl + НСlO (хлорная вода)
Сl2 + 2NаОН → NаСl + NаСlO + Н2О (на холоде),
ЗСl2 + 6КОН → 5КСl + КClO3 + ЗН2О (при нагревании).
По химической активности бром занимает промежуточное положение между хлором и иодом. Взаимодействует со многими простыми веществами:
Бром, так же, как и хлор, растворяется в воде, и, частично реагируя с ней, образует так называемую «бромную воду»:
При растворении в растворах щелочей на холоду происходит образование бромида и гипобромита
2NaOH + Br2 =NaBr + NaBrO + H2O
При повышенных температурах (около 100°С) — бромида и бромата:
При реакции брома с растворами иодидов выделяется свободный иод:
Br2+ 2KI = I2+ 2KBr.
С органическими веществами, имеющими двойную или тройную связь. Обесцвечивание бромной воды – качественная реакция на непредельное соединение:
C2H4 + Br2 = C2H4Br2.
Йод существенно отличается по химической активности от остальных галогенов. Он не реагирует с большинством неметаллов, а с металлами медленно реагирует только при нагревании.
Взаимодействие же йода с водородом происходит только при сильном нагревании, реакция является эндотермической и сильно обратимой:
Йод практически в воде не растворим и не способен ее окислять даже при нагревании; по этой причине не существует «йодной воды».
Но йод способен растворяться в растворах иодидов с образованием комплексных анионов:
Образующийся раствор называется раствором Люголя.
Сероводород H2S, тиосульфат натрия Na2S2O3 и другие восстановители восстанавливают его до I — :
Хлор и другие сильные окислители в водных растворах переводят его в IO3 — :
Адсорбируясь на крахмале, йод окрашивает его в темно-синий цвет- качественная реакция на йод.
Таким образом, химическая активность галогенов последовательно уменьшается от фтора к йоду. Каждый галоген в ряду F — I может вытеснять последующий из его соединений с водородом или металлами, т.е. каждый галоген в виде простого вещества способен окислять галогенид-ион любого из последующих галогенов.
Источник
Химические свойства галогенов
Содержание:
К данным химическим элементам относят элементы VII группы главной подгруппы – фтор, хлор, бром, йод.
Отличительными особенностями галогенов является резко выраженные свойства неметаллов, или металлоидов. На внешнем энергетическом уровне у данных элементов семь электронов, то есть он считается не завершенным. В связи с этим они могут активно присоединять электроны для его завершения.
Химическая активность галогенов ослабевает сверху вниз в группе и с увеличением атомного радиуса – от фтора к йоду. Таким образом, самым сильным окислителем является фтор, его степень окисления всегда равна -1. У остальных галогенов могут быть степени окисления в пределах от -1 до +7.
Рассмотрим химические свойства галогенов на определенных примерах.
- При взаимодействии с металлами галогены образуют соли. Реакции происходят в зависимости от степени активности того или иного элемента.
- Фтор, как сильнейший окислитель, реагирует с металлами в нормальных условиях, а при высоких температурах способен взаимодействовать даже с неактивными металлами – серебром, золотом, платиной. Алюминий и цинк способны гореть в атмосфере фтора.
Другие галогены взаимодействуют с металлами при высоких температурах. К примеру, при высыпании в колбу с хлором измельченной в порошок сурьмы частички ее воспламеняются на лету, производя впечатление «огненного дождя». Колба наполняется при этом тяжелым белым дымом хлористой сурьмы.
Медь, взятая в виде пучка тонкой проволоки и предварительно нагретая на воздухе, при погружении в хлор раскаляется и сгорает, наполняя колбу бурым дымом. Бурый дым представляет собой частички хлорной меди.
Йод также вступает в реакции с металлами. Если растертый в ступке йод смешать с порошком алюминия, то через некоторое время сама собой начнется реакция соединения. Активизируется процесс в присутствии воды.
Реакция сопровождается появлением пламени. Продукт реакции – йодистый алюминий получается в виде тяжелого дыма, окрашенного примешивающимися к нему парами йода в фиолетовый цвет.
Галогены взаимодействуют с некоторыми неметаллами – водородом, серой, фосфором, кремнием. С кислородом и азотом непосредственно не реагирует.
- Фтор, при обычных условиях, реагирует практически со всеми неметаллами с выделением тепла. С водородом реакция протекает с взрывом.
Другие галогены реагируют с неметаллами при нагревании. С водородом соединяется бром, образуя бромистый водород. В соединениях с водородом и металлами бром является одновалентным.
При нагревании фтор может окислять другие галогены. Например, при взаимодействии фтора и хлора образуется при комнатной температуре бесцветный токсичный тяжелый газ с сильным раздражающим запахом – фторид хлора (I).
Галогены способны восстанавливать менее активные галогены из растворов галогенидов металлов. В эти реакции не вступает фтор, так как из-за высокой активности в растворе начинает немедленно реагировать с водой.
Взаимодействие со сложными веществами.
- Галогены могут взаимодействовать с щелочными растворами. Реакции протекают по-разному при высоких и низких температурах. При взаимодействии хлора со щелочами на холоде образуется смесь хлоридов и гипохлоритов.
Cl2 + 2KOH → KCl + KClO + H2O
В горячем растворе щелочи происходит реакция, при которой образуются хлорид калия и хлорат калия или бертоллетова соль.
Реакция с водой сопровождается выделением атомарного водорода.
Взаимодействие хлора с водой протекает в два этапа. Во-первых, хлор реагирует с водой с образованием хлорной и хлорноватистой кислоты.
Источник
Галоген реагирует с водой
Взаимодействие с металлами. 
Галогены в этой реакции проявляют окислительные свойства.
Взаимодействие с водородом.При обычных условиях фтор реагирует с водородом в темноте со взрывом, взаимодействие с хлором протекает на свету, бром и йод реагируют только при нагревании, причем реакция с йодом обратима.
Галогены в этой реакции проявляют окислительные свойства.
Взаимодействие с неметаллами. С кислородом и азотом галогены непосредственно не взаимодействуют, реагируют с серой, фосфором, кремнием, проявляя окислительные свойства, химическая активность у брома и йода выражена слабее, чем у фтора и хлора:
Взаимодействие с водой. Галогены реагируют со многими сложными веществами. С водой фтор и остальные галогены реагируют по-разному:
Hal + H2O = HHal + HHalO.
Эта реакции является реакцией диспропорционирования, где галоген одновременно является окислителем и восстановителем.
Взаимодействие со щелочами. Также галогены диспропорционируют в растворах щелочей:
Cl2 + KOH = KClO + KCl (на холоде);
3Cl2 + 6KOH = KClO3 + 5KCl + 3Н2О (при нагревании).
Гипобромид-ион существует только при температуре ниже 0 °С, гипойодит-ион в растворах не существует.
Взаимодействие с сероводородом. Галогены способны отнимать водород от других веществ:
Реакция замещения водорода в предельных углеводородах:
Реакция присоединения к непредельным углеводородам:
Взаимное замещение галогенов. 
Источник
Галогены
Галогены (греч. hals — соль + genes — рождающий) — химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.
Общая характеристика элементов VIIa группы
От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 5 :
- F — 2s 2 2p 5
- Cl — 3s 2 3p 5
- Br — 4s 2 4p 5
- I — 5s 2 5p 5
- At — 6s 2 6p 5
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов в возбужденном состоянии.
Природные соединения
- NaCl — галит (каменная соль)
- CaF2 — флюорит, плавиковый шпат
- NaCl*KCl — сильвинит
- 3Ca3(PO4)2*CaF2 — фторапатит
- MgCl2*6H2O — бишофит
- KCl*MgCl2*6H2O — карналлит
Простые вещества — F2, Cl2, Br2, I2
Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают электролизом водного раствора хлорида натрия.
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте — HF — был впервые получен фтор.
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.
В лабораторных условиях галогены могут быть получены следующими реакциями.
- Реакции с металлами
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере фтора самовоспламеняются.
Реакции с неметаллами
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.
F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность 😉
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром — F — )
Br2 + I2 → IBr3 (бром более электроотрицателен, чем йод — Br — )
Реакции с водой
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
Хлор реагирует с водой обратимо, образуя хлорную воду — смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.
Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами — только при нагревании.
Реакции с щелочами
Cl2 + NaOH → NaCl + NaClO + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Галогеноводороды
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF — фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl — хлороводород (газ), соляная кислота (жидкость)
- HBr — бромоводород, бромоводородная кислота
- HI — йодоводород, йодоводородная кислота
- HAt — астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI — газы, хорошо растворимые в воде.
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
HF — является слабой кислотой, HCl, HBr, HI — сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
KOH + HCl → KCl + H2O (реакция нейтрализации)
Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.
В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с плавиковой кислотой.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник