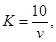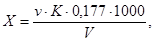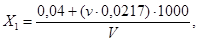- 1. МЕТОДЫ ОТБОРА ПРОБ
- 2. ЙОДОМЕТРИЧЕСКИЙ МЕТОД
- 3. МЕТОД ОПРЕДЕЛЕНИЯ СВОБОДНОГО ОСТАТОЧНОГО ХЛОРА ТИТРОВАНИЕМ МЕТИЛОВЫМ ОРАНЖЕВЫМ
- 4. МЕТОД РАЗДЕЛЬНОГО ОПРЕДЕЛЕНИЯ СВОБОДНОГО ХЛОРА, СВЯЗАННОГО МОНОХЛОРАМИНА И ДИХЛОРАМИНА ПО МЕТОДУ ПЕЙЛИНА
- Гост хлор активный питьевая вода
- 1. МЕТОДЫ ОТБОРА ПРОБ
- 2. ЙОДОМЕТРИЧЕСКИЙ МЕТОД
1. МЕТОДЫ ОТБОРА ПРОБ
1.1 . Пробы воды отбирают по ГОСТ 24481 * и ГОСТ 2874 **.
* На территории Российской Федерации действует ГОСТ Р 51593-2000.
** На территории Российской Федерации действует ГОСТ Р 51232-98.
1.2 . Объем пробы воды для определения содержания активного хлора не должен быть менее 500 см 3 .
1.3 . Пробы воды не консервируют. Определение следует проводить немедленно после отбора пробы.
2. ЙОДОМЕТРИЧЕСКИЙ МЕТОД
Метод основан на окислении йодида активным хлором до йода, который титруют тиосульфатом натрия. Озон, нитриты, окись железа и другие соединения в кислом растворе выделяют йод из йодистого калия, поэтому пробы воды подкисляют буферным раствором с pH 4,5.
Йодометрический метод предназначен для анализа воды с содержанием активного хлора более 0,3 мг/дм 3 при объеме пробы 250 см 3 . Метод может быть рекомендован также для окрашенных и мутных вод.
2.2 . Аппаратура, материалы и реактивы
Посуда мерная лабораторная стеклянная по ГОСТ 1770, ГОСТ 29169 и ГОСТ 29251, вместимостью: колбы 100 и 1000 см 3 ; пипетки без делений 5, 10, 25 см 3 ; бюретка с краном 25, 50 см 3 ; микробюретка 5 см 3 .
Колбы конические с пришлифованными пробками вместимостью 250 см 3 по ГОСТ 25336.
Калий йодистый по ГОСТ 4232, х. ч. в кристаллах.
Вода дистиллированная по ГОСТ 6709.
Кислота уксусная ледяная по ГОСТ 61.
Калий двухромовокислый по ГОСТ 4220.
Кислота серная по ГОСТ 4204.
Крахмал растворимый по ГОСТ 10163.
Натрий углекислый кристаллический по ГОСТ 84.
Натрий серноватистокислый (тиосульфат натрия) по ГОСТ 27068.
Все реактивы, используемые в анализе, должны быть квалификации «чистые для анализа» (ч. д. а.).
2.3 . Подготовка к анализу
2.3.1 . Приготовление 0,1 н раствора серноватистокислого натрия
25 г тиосульфата натрия Na 2 S 2 O 3 · 5H 2 O растворяют в свежепрокипяченной и охлажденной дистиллированной воде, добавляют 0,2 г углекислого натрия (Nа2СО3) и доводят объем до 1 дм 3 .
2.3.2 . Приготовление 0,01 н раствора серноватистокислого натрия
100 см 3 0,1 н. раствора тиосульфата натрия разбавляют свежепрокипяченной и охлажденной дистиллированной водой, добавляют 0,2 г углекислого натрия и доводят раствор до 1 дм 3 . Раствор применяют при содержании активного хлора в пробе более 1 мг/дм 3 .
2.3.3 . Приготовление 0,005 н. раствора серноватистокислого натрия
50 см 3 0,1 н. раствора тиосульфата натрия разбавляют свежепрокипяченной и охлажденной дистиллированной водой, добавляют 0,2 г углекислого натрия и доводят раствор до 1 дм 3 . Раствор применяют при содержании активного хлора в пробе менее 1 мг/дм 3 .
2.3.4 . Приготовление 0,01 н. раствора калия двухромовокислого
0,4904 г двухромовокислого калия К2Сr 2 О7, взвешенного с точностью до ± 0,0002 г, перекристаллизованного и высушенного при 180 °C до постоянной массы, растворяют в дистиллированной воде и доводят объем до 1 дм 3 .
2.3.5 . Приготовление 0,5 %-ного раствора крахмала
0,5 г растворимого крахмала смешивают с небольшим объемом дистиллированной воды, приливают к 100 мл кипящей дистиллированной воды и кипятят несколько минут. После охлаждения консервируют, добавляя хлороформ или 0,1 г салициловой кислоты.
2.3.6 . Приготовление буферного раствора pH 4,5
102 см 3 1 М уксусной кислоты (60 г ледяной уксусной кислоты в 1 дм 3 воды) и 98 см 3 1 М раствора уксуснокислого натрия (136,1 г уксуснокислого натрия СН3СОONа · 3Н2О в 1 дм 3 воды) наливают в мерную колбу вместимостью 1 дм 3 и доводят до метки дистиллированной водой (предварительно прокипяченной и охлажденной до 20 ° C , свободной от двуокиси углерода).
2.3.7 . Поправочный коэффициент 0,01 н. раствора серноватисто-кислого натрия определяют по 0,01 н раствору двухромовокислого калия следующим образом: в коническую колбу и с пришлифованной пробкой помещают 0,5 г йодистого калия, проверенного на отсутствие йода, растворяют в 2 см 3 дистиллированной воды, прибавляют 5 см 3 серной кислоты (1:4), затем 10 см 3 0,01 н. раствора двухромовокислого калия, добавляют 80 см 3 дистиллированной воды, закрывают колбу пробкой, перемешивают и ставят в темное место на 5 мин. Выделившийся йод титруют тиосульфатом натрия в присутствии 1 см 3 крахмала, прибавленного в конце титрования.
2.3.8 . Поправочный коэффициент ( K ) (0,01; 0,005 н. растворов серноватистокислого натрия) вычисляют по формуле
где v — количество серноватистокислого натрия, израсходованное на титрование, см 3 .
В коническую колбу насыпают 0,5 г йодистого калия, растворяют его в 1 — 2 см 3 дистиллированной воды, затем добавляют буферый раствор в количестве, приблизительно равном полуторной величине щелочности анализируемой воды, после чего добавляют 250 — 500 см 3 анализируемой воды. Выделившийся йод оттитровывают 0,005 н. раствором тиосульфата натрия из микробюретки до появления светло-желтой окраски, после чего прибавляют 1 см 3 0,5 %-ного раствора крахмала и раствор титруют до исчезновения синей окраски. При определении щелочности воду предварительно дехлорируют с помощью тиосульфата натрия в отдельной пробе.
При концентрации активного хлора менее 0,3 мг отбирают для титрования большие объемы воды.
Содержание суммарного остаточного хлора ( X ), мг/дм 3 вычисляют по формуле
где v — количество 0,005 н. раствора тиосульфата натрия, израсходованное на титрование, см 3 ;
K — поправочный коэффициент нормальности раствора тиосульфата натрия;
0,177 — содержание активного хлора, соответствующее 1 см 3 0,005 н. раствора тиосульфата натрия;
V — объем пробы воды, взятый для анализа, см 3 .
3. МЕТОД ОПРЕДЕЛЕНИЯ СВОБОДНОГО ОСТАТОЧНОГО ХЛОРА
ТИТРОВАНИЕМ МЕТИЛОВЫМ ОРАНЖЕВЫМ
Метод основан на окислении свободным хлором метилового оранжевого, в отличие от хлораминов, окислительный потенциал которых недостаточен для разрушения метилового оранжевого.
3.2 . Аппаратура, материалы, реактивы
Посуда мерная лабораторная стеклянная по ГОСТ 1770 и ГОСТ 29251 вместимостью: колбы мерные 100 и 1000 см 3 ; микробюретка с краном 5 см 3 .
Чашки фарфоровые выпарительные по ГОСТ 9147.
Кислота соляная по ГОСТ 3118, плотностью 1,19 г/см 3 .
Метиловый оранжевый (пара-диметиламиноазобензолсульфокислый натрий) по ТУ 6-09-5171.
Вода дистиллированная по ГОСТ 6709.
Все реактивы, применяемые для анализа, должны быть квалификации чистые для анализа (ч. д. а.).
3.3 . Подготовка к анализу
3.3.1. Приготовление 0,005 %-ного раствора метилового оранжевого
50 мг метилового оранжевого растворяют в дистиллированной воде в мерной колбе и доводят дистиллированной водой до 1 дм 3 . 1 см 3 этого раствора соответствует 0,0217 мг свободного хлора.
3.3.2. Приготовление 5 н. раствора соляной кислоты
В мерную колбу наливают дистиллированную воду, затем медленно добавляют 400 см 3 соляной кислоты HCl и доводят дистиллированной водой до 1 дм 3 .
100 см 3 анализируемой воды помещают в фарфоровую чашку, добавляют 2 — 3 капли 5 н. раствора соляной кислоты и, помешивая, быстро титруют раствором метилового оранжевого до появления неисчезающей розовой окраски.
Содержание свободного остаточного хлора ( X 1 ), мг/дм 3 , вычисляют по формуле
где v — количество 0,005 %-ного раствора метилового оранжевого, израсходованного на титрование, см 3 ;
0,0217 — титр раствора метилового оранжевого;
0,04 — эмпирический коэффициент;
V — объем воды, взятый для анализа, см 3 .
По разности между содержанием суммарного остаточного хлора, определенного методом титрования, метилоранжевым, находят содержание хлораминового хлора (Х2):
4. МЕТОД РАЗДЕЛЬНОГО ОПРЕДЕЛЕНИЯ СВОБОДНОГО ХЛОРА,
СВЯЗАННОГО МОНОХЛОРАМИНА И ДИХЛОРАМИНА ПО МЕТОДУ ПЕЙЛИНА
Метод основан на способности разных видов хлора превращать в определенных условиях восстановленную бесцветную форму диэтилпарафенилендиамина в полуокисленную окрашенную форму, которую восстанавливают опять до бесцветной ионами двухвалентного железа. Используются серия титрований раствором соли Мора для определения свободного хлора, монохлорамина и дихлорамина в присутствии диэтилпарафенилендиамина, как индикатора. Свободный хлор образует окраску индикатора в отсутствии йодистого калия, монохлорамин дает окраску в присутствии очень маленьких количеств йодистого калия (2 — 3 мг), а дихлорамин образует окраску лишь в присутствии больших количеств KI (около 1 г) и при стоянии раствора в течение 2 мин. По количеству раствора соли Мора, израсходованному на титрование, определяют содержание того вида активного хлора, за счет которого образуется окрашенная форма индикатора.
4.2 . Аппаратура, материалы, реактивы
Посуда мерная стеклянная лабораторная по ГОСТ 1770 и ГОСТ 29251 вместимостью: колбы мерные 100 и 1000 см 3 ; цилиндры мерные 5 и 100 см 3 ; микробюретки 1 и 2 см 3 .
Колбы конические вместимостью 250 мл; склянки из темного стекла вместимостью 100 — 200 см 3 .
Двойная сернокислая соль закиси железа и аммония (соль Мора) по ГОСТ 4208.
Калий йодистый по ГОСТ 4232.
Калий фосфорнокислый однозамещенный по ГОСТ 4198, х. ч.
Кислота серная по ГОСТ 4204.
Натрий фосфорнокислый двузамещенный безводный по ГОСТ 11773.
Трилон Б (комплексон III, двунатриевая соль этилендиаминтетрауксусной кислоты) по ГОСТ 10652.
Вода дистиллированная по ГОСТ 6709.
Диэтилпарафенилендиамин оксалат или сульфат.
Все реактивы, применяемые для анализа, должны быть квалификации «чистые для анализа» (ч. д. а.).
4.3.1. Приготовление стандартного раствора соли Мора
1,106 г соли Мора Fe(NH 4 )2(SO 4 )2 · 6H 2 O растворяют в дистиллированной воде, подкисляют 1 см 3 25 %-ного раствора серной кислоты H 2 SO 4 и доводят свежепрокипяченной и охлажденной дистиллированной водой до 1 дм 3 . 1 см 3 раствора соответствует 0,1 мг активного хлора. Если определение проводится в 100 см 3 воды, то количество миллилитров соли Мора, израсходованное на титрование, соответствует мг/дм 3 хлора, или монохлорамина или дихлорамина. Раствор устойчив в течение месяца. Хранить его следует в темном месте.
4.3.2. Приготовление фосфатного буферного раствора
К 2,4 г фосфорнокислого натрия двузамещенного Na 2 HPO 4 и 4,6 г фосфорнокислого калия однозамещенного КН2РО4 приливают 10 см 3 0,8 %-ного раствора трилона Б и доводят дистиллированной водой до 100 см 3 .
4.3.3. Приготовление индикатора диэтилпарафенилендиамин (оксалат или сульфат) 0,1 %-ного раствора
0,1 г диэтилпарафенилендиамина оксалата (или 0,15 г соли сульфата) растворяют в 100 см 3 дистиллированной воды с добавлением 2 см 3 10 %-ного раствора серной кислоты. Раствор индикатора следует хранить в склянке из темного стекла.
4.4.1. Определение содержания свободного хлора
В коническую колбу для титрования помещают 5 см 3 фосфатного буферного раствора, 5 см 3 раствора индикатора диэтилпарафенилендиамин оксалата или сульфата и приливают 100 см 3 анализируемой воды, раствор перемешивают. В присутствии свободного хлора раствор окрашивается в розовый цвет, его быстро титруют из микробюретки стандартным раствором соли Мора до исчезновения окраски, энергично перемешивая. Расход соли Мора, пошедший на титрование (А, см 3 ), соответствует содержанию свободного хлора, мг/дм 3 .
При наличии в анализируемой воде значительных количеств свободного хлора (более 4 мг/дм 3 ) для анализа следует брать менее 100 см 3 воды, так как большие количества активного хлора могут разрушить полностью индикатор.
4.4.2. Определение содержания монохлорамина
В колбу с оттитрованным раствором добавляют кристаллик (2 — 3 мг) йодистого калия, раствор перемешивают. В присутствии монохлорамина мгновенно появляется розовая окраска, которую тотчас же оттитровывают стандартным раствором соли Мора. Количество миллилитров соли Мора, пошедших на титрование (B, см 3 ), соответствует содержанию монохлорамина, мг/дм 3 .
4.4.3. Определение содержания дихлорамина
К оттитрованному раствору после определения содержания монохлорамина вновь добавляют около 1 г йодистого калия, перемешивают до растворения соли и оставляют раствор стоять в течение 2 мин. Появление розовой окраски свидетельствует о наличии в воде дихлорамина. Раствор титруют стандартным раствором соли Мора до исчезновения окраски. Расход соли Мора (С, см 3 ) соответствует содержанию дихлорамина, мг/дм 3 .
Содержание суммарного остаточного активного хлора ( X 3 ), мг/дм 3 , вычисляют по формуле
где А — содержание свободного хлора, мг/дм 3 ;
В — содержание монохлорамина, мг/дм 3 ;
С — содержание дихлорамина, мг/дм 3 .
1. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 25.10.72 № 1967
2. ВВЕДЕН ВПЕРВЫЕ
3. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Источник
Гост хлор активный питьевая вода
Методы определения содержания остаточного активного хлора
Drinking water. Methods for determination of сhlorine residual content
Дата введения 1974-01-01
1. УТВЕРЖДЕН и ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 25.10.72 N 1967
2. ВВЕДЕН ВПЕРВЫЕ
3. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка
Обозначение НТД, на который дана ссылка
4. Ограничение срока действия снято Постановлением Госстандарта СССР от 25.12.91 N 2120
5. ПЕРЕИЗДАНИЕ. Ноябрь 2009 г.
Настоящий стандарт распространяется на питьевую воду и устанавливает методы определения содержания остаточного активного хлора.
1. МЕТОДЫ ОТБОРА ПРОБ
* На территории Российской Федерации действует ГОСТ Р 51593-2000.
** На территории Российской Федерации действует ГОСТ Р 51232-98.
1.2. Объем пробы воды для определения содержания активного хлора не должен быть менее 500 см .
1.3. Пробы воды не консервируют. Определение следует проводить немедленно после отбора пробы.
2. ЙОДОМЕТРИЧЕСКИЙ МЕТОД
2.1. Сущность метода
Метод основан на окислении йодида активным хлором до йода, который титруют тиосульфатом натрия. Озон, нитриты, окись железа и другие соединения в кислом растворе выделяют йод из йодистого калия, поэтому пробы воды подкисляют буферным раствором с рН 4,5.
Йодометрический метод предназначен для анализа воды с содержанием активного хлора более 0,3 мг/дм при объеме пробы 250 см . Метод может быть рекомендован также для окрашенных и мутных вод.
2.2. Аппаратура, материалы и реактивы
Посуда мерная лабораторная стеклянная по ГОСТ 1770, ГОСТ 29169 и ГОСТ 29251, вместимостью: колбы мерные 100 и 1000 см ; пипетки без делений 5, 10, 25 см ; бюретка с краном 25, 50 см ; микробюретка 5 см .
Колбы конические с пришлифованными пробками вместимостью 250 см по ГОСТ 25336.
Калий йодистый по ГОСТ 4232, х.ч., в кристаллах.
Вода дистиллированная по ГОСТ 6709.
Кислота уксусная ледяная по ГОСТ 61.
Калий двухромовокислый по ГОСТ 4220.
Кислота серная по ГОСТ 4204.
Крахмал растворимый по ГОСТ 10163.
Натрий углекислый кристаллический по ГОСТ 84.
Натрий серноватистокислый (тиосульфат натрия) по ГОСТ 27068.
Все реактивы, используемые в анализе, должны быть квалификации «чистые для анализа» (ч.д.а.).
2.3. Подготовка к анализу
2.3.1. Приготовление 0,1 н. раствора серноватистокислого натрия
25 г тиосульфата натрия 

2.3.2. Приготовление 0,01 н. раствора серноватистокислого натрия
100 см 0,1 н. раствора тиосульфата натрия разбавляют свежепрокипяченной и охлажденной дистиллированной водой, добавляют 0,2 г углекислого натрия и доводят раствор до 1 дм . Раствор применяют при содержании активного хлора в пробе более 1 мг/дм .
2.3 3. Приготовление 0,005 н. раствора серноватистокислого натрия
50 см 0,1 н. раствора тиосульфата натрия разбавляют свежепрокипяченной и охлажденной дистиллированной водой, добавляют 0,2 г углекислого натрия и доводят раствор до 1 дм . Раствор применяют при содержании активного хлора в пробе менее 1 мг/дм .
2.3.4. Приготовление 0,01 н. раствора двухромовокислого калия
0,4904 г двухромовокислого калия 
2.3.5. Приготовление 0,5%-ного раствора крахмала
0,5 г растворимого крахмала смешивают с небольшим объемом дистиллированной воды, приливают к 100 cм кипящей дистиллированной воды и кипятят несколько минут. После охлаждения консервируют, добавляя хлороформ или 0,1 г салициловой кислоты.
2.3.6. Приготовление буферного раствора рН 4,5
102 cм 1 М уксусной кислоты (60 г ледяной уксусной кислоты в 1 дм воды) и 98 cм 1 М раствора уксуснокислого натрия (136,1 г уксуснокислого натрия 
2.3.7. Поправочный коэффициент 0,01 н. раствора серноватистокислого натрия определяют по 0,01 н. pacтвopy двухромовокислого калия следующим образом: в коническую колбу и с пришлифованной пробкой помещают 0,5 г йодистого калия, проверенного на отсутствие йода, растворяют в 2 cм дистиллированной воды, прибавляют 5 cм серной кислоты (1:4), затем 10 cм 0,01 н. раствора двухромовокислого калия, добавляют 80 cм дистиллированной воды, закрывают колбу пробкой, перемешивают и ставят в темное место на 5 мин. Выделившийся йод титруют тиосульфатом натрия в присутствии 1 cм крахмала, прибавленного в конце титрования.
2.3.8. Поправочный коэффициент ( ) (0,01; 0,005 н. растворов серноватистокислого натрия) вычисляют по формуле:

где — количество серноватистокислого натрия, израсходованное на титрование, cм .
2.4. Проведение анализа
В коническую колбу насыпают 0,5 г йодистого калия, растворяют его в 1-2 cм дистиллированной воды, затем добавляют буферный раствор в количестве, приблизительно равном полуторному значению щелочности анализируемой воды, после чего добавляют 250-500 cм анализируемой воды. Выделившийся йод оттитровывают 0,005 н. раствором тиосульфата натрия из микробюретки до появления светло-желтой окраски, после чего прибавляют 1 cм 0,5%-ного раствора крахмала и раствор титруют до исчезновения синей окраски. При определении щелочности воду предварительно дехлорируют с помощью тиосульфата натрия в отдельной пробе.
При концентрации активного хлора менее 0,3 мг отбирают для титрования большие объемы воды.
2.5. Обработка результатов
Содержание суммарного остаточного хлора ( ), мг/дм , вычисляют по формуле

где — количество 0,005 н. раствора тиосульфата натрия, израсходованное на титрование, cм ;
— поправочный коэффициент нормальности раствора тиосульфата натрия;
0,177 — содержание активного хлора, соответствующее 1 cм 0,005 н. раствора тиосульфата натрия;
— объем пробы воды, взятый для анализа, cм .
Источник