- Большая Энциклопедия Нефти и Газа
- Гваякол
- Гваякол — сильный и безопасный ароматизатор
- Свойства
- Меры предосторожности
- Применение
- Гваякол
- Получение
- Применение
- Безопасность
- Полезное
- Смотреть что такое «Гваякол» в других словарях:
- Гваякол
- Смотреть что такое «Гваякол» в других словарях:
- Экология СПРАВОЧНИК
- Информация
- Гваякол
Большая Энциклопедия Нефти и Газа
Гваякол
Гваякол и вообще простейшие неполные эфиры многоатомных фенолов в некоторой степени растворимы в воде. [1]
Гваякол и псевдобутилен в присутствии BF3 — 0 ( C2H6) 2 при комнатной температуре очень плохо взаимодействуют. [2]
Гваякол и циклогексен в отношении 1: 1 в присутствии 5 % BF3 0 ( С2Н6) 2 в течение 10 дней не вступают в реакцию, и циклогексен количественно регенерируется. [3]
Гваякол с дивинилом и BF3 — 0 ( C2HS) 2 при температуре от 13 до 25 реагирует менее энергично, чем описанные фенолы. Встряхивание реакционной смеси не сопровождается выделением тепла, гваякол постепенно растворяется и через сутки при температуре ниже 0 смесь представляет подвижную жидкость. При перегонке с водяным паром отгоняются небольшие количества непрореагировавшего гваякола и остается в виде мазеобразной жидкости смесь бутенильных производных эфирного типа, которые не растворяются в 5 % — ной КОН, обесцвечивают бромную воду и раствор перманганата. Индивидуальные соединения не выделены. При нагревании смеси на кипящей водяной бане, после стояния в течение суток при температуре ниже 0, получается вязкая масса, которая на воздухе постепенно твердеет, но легко размягчается и тянется в красивые нити темно-коричневого цвета. Растворяется в ацетоне, бензоле, эфире. [4]
Гваякол и циклогексен в отношении 1: 1 в присутствии 5 % BF3 — O ( C2H5) 2 в течение 10 дней не вступают в реакцию, и циклогексен количественно регенерируется. Увеличение продолжительности нагревания до 12 часов повышает общий выход продуктов реакции до 94 % в основном за счет фенольных соединений. [5]
Гваякол с дивинилом и BF3 0 ( G2H5) 2 при — 13 до 25 С реагирует менее энергично, чем описанные фенолы. [6]
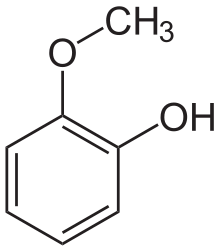
Гваякол — метиловый эфир пирокатехина. Кристаллическое вещество; обладает сильным характерным запахом. Плохо растворим в воде. Содержится в буковом дегте, креозоте. [7]
Гваякол был впервые выделен при перегонке гваяковой смолы; он может быть получен синтетически из о-анизидина через диазосоединение. С) получают с выходом 95 % при метилировании пирокатехина димегилсуль-фатом в присутствии щелочи. [8]
Гваякол был впервые выделен при перегонке гваяковой смолы; он может быть получен синтетически из о-анизидина через диазосоединение. С) получают с выходом 95 % при метилировании пирокатехина диметилсуль-фатом в присутствии щелочи. [9]
Гваякол растворяется, приблизительно, в 60 частях воды; легко растворим в спирте и эфире. [10]
Гваякол и вообще простейшие неполные эфнры многоатомных фенолов в некоторой Степени растворимы в воде. [11]
Гваякол сплавляют с хлоралгидратом в присутствии катализаторов ( КгСО3, Na3PO4 и др.) и полученный З — метокси-4 — оксифенил-трихлорметилкарбннол гидролизуют до — З — метокси-4 — оксифенил-глнокеа-ля. Последний подвергают восстановительному аминироаанию с нзопропиламином и никелем Ренея. [12]
Гваякол получен в 1826 г. из древесного дегтя. В буковом дегте, особо широко добываемом в горах Шварцвальда в Германии, содержится до 90 % гваякола в смеси с другими фенолами. Выделяют его фракционной перегонкой. [13]
Гваякол засасывают в аппарат для обезвоживания и при температуре 50 — 70 и вакууме 66 7 — 86 7 кн / м2 отгоняют воду до температуры 112 — 116 в парах. [15]
Источник
Гваякол — сильный и безопасный ароматизатор
Гваякол — неорганическое соединение, 
Соединение имеет природное происхождение, впервые выделено из смолы гваякового дерева, но в незначительных количествах его можно обнаружить практически во всех натуральных продуктах: мясе, грибах, хлебе, капусте, луке, помидорах, лимоне, пиве, кофе, чае, роме, касторовом масле и пр. Его много в продуктах сухой перегонки древесины, в дегте. Почти в любом природном запахе можно найти гваякол, а в запахе дыма от костра, копченостей и ванили ароматическая составляющая гваякола — определяющая.
Для нужд промышленности реактив получают в результате химического синтеза из пирокатехина С6Н4(ОН)2 и диметилсульфата (CH3)2SO4 или из о-анизидина CH3OC6H4NH2.
 |  |
| Гваякол имп 99%, фасовка 250 гр | Квадратная банка из темного стекла, 1000 мл |
Свойства
2-метоксифенол — порошкообразное вещество с бесцветными, беловатыми, сероватыми или желтоватыми кристалликами, чувствительными к свету и темнеющими на воздухе. Запах резкий, характерный, похож на запах дыма. Вкус жгучий. Реактив слабо растворим в воде, хорошо в спирте, хлороформе, эфирах, жирных маслах. Почти не растворим в петролейном эфире. Легко плавится уже при совсем незначительном нагревании (выше +29 °С). Горит, не взрывается, токсичен.
Вступает в химические реакции с кислотами, щелочами и их растворами, с серой и йодом, хлорным железом.
Меры предосторожности
Реактив опасен при проглатывании, раздражает кожу, слизистые оболочки глаз и органов дыхания. Может вызывать онемение кожи, привести к развитию экземы. Способен накапливаться в организме.
Гваякол следует хранить в герметичных, защищенных от света сосудах, например, в темных банках с плотной завинчивающейся крышкой. Температура хранения — ниже комнатной, лучше всего сосуд с веществом хранить в холодильнике.
В различной научно-популярной и околонаучной литературе нередко можно встретить тезис о том, что использование гваякола в пищевых продуктах очень опасно. Один из основных аргументов: он входит в состав креозота, которым пропитывают шпалы. При этом авторы забывают одно немаловажное обстоятельство: в пищу реактив добавляется как ароматизатор, и обладая очень интенсивным запахом, используется в микроскопических количествах (миллионные доли грамма на килограмм продукта). Его допустимая суточная норма вообще не регламентируется в силу того, что человек физически не может потребить такое количество реагента, которое может оказать хоть сколько-то ощутимое воздействие на здоровье.
Применение
• Добавка, ароматизатор «запах бекона» в пищепроме. Входит в состав синтетического ванилина.
• В фармацевтике используется для производства некоторых лекарственных препаратов, например, папаверина, фтивазида.
• Сырье для получения искусственных ароматизаторов и душистых веществ: ванилина, эвгенола и изоэвгенола —запаха гвоздики и санталидола — запаха сандала.
• В стоматологии входит в состав средств для обработки и дезинфекции корневых каналов.
• В медицине — востребован при изготовлении некоторых лекарств (таблетки, капсулы, порошки, растворы, эмульсии, мази) для лечения туберкулеза, цистита, пневмонии, бронхита, диареи и др. Обладает выраженным антисептическим эффектом.
Источник
Гваякол
Гваякол — бесцветные, с сильным своеобразным запахом, легко плавящиеся (т. плав. 28,5 °C, т. кип. 205 °C) кристаллы монометилового эфира пирокатехина, темнеющие на воздухе и на свету, хорошо растворимые в этаноле, эфире, хлороформе, ледяной уксусной кислоте, растворах щелочей и плохо — в воде и петролейном эфире. Содержится в продуктах сухой перегонки древесины лиственных и хвойных пород, высококипящих погонах букового дёгтя, а также в продуктах перегонки гваяковой смолы.
Получение
В промышленности получают метилированием пирокатехина метилсерной кислотой, диметилсульфатом или метанолом, а также диазотированием о-анизидина с последующим разложением диазосоединения водой в присутствии CuSO4.
Получают частичным метилированием пирокатехина или диазотированием o-анизидина с разложением водой образовавшегося диазосоединения.
Применение
Применяют для синтеза душистых веществ — ванилина, эвгенола, изоэвгенола, санталидола, и лекарственных препаратов, напр. фтивазида и папаверина. Служит искусственным ароматизатором пищевых продуктов, как аромат «бекона».
Безопасность
Гваякол вызывает анестезию кожи, экзему, раздражает глаза и дыхательные пути; ПДК — 20 мг/м³.В стоматологии входит в состав некоторых препаратов для антисептической обработки корневых каналов.
- Дополнить статью (статья слишком короткая либо содержит лишь словарное определение).
- Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое «Гваякол» в других словарях:
ГВАЯКОЛ — ГВАЯКОЛ, Guajacolum (Ф VII), монометиловый эфир бренцкатехипа, СвН4(ОН). .(ОСН3) (1, 2), является главной составной частью креозота, из которого и получается путем повторной фракционной перегонки; поступает в продажу или в виде бесцветных или… … Большая медицинская энциклопедия
ГВАЯКОЛ — бесцветная жидкость приятного запаха; получается при сухой перегонке гваяколовой смолы; при обработке хлороформом и едким кали переходит в ванилин. Словарь иностранных слов, вошедших в состав русского языка. Павленков Ф., 1907. ГВАЯКОЛОВОЕ ДЕРЕВО … Словарь иностранных слов русского языка
ГВАЯКОЛ — СН3ОС6Н4ОН, бесцветные кристаллы, tпл 28,5 .С. Сырье в синтезе душистых веществ (ванилина, эвгенола, санталидола) … Большой Энциклопедический словарь
гваякол — сущ., кол во синонимов: 2 • фенол (15) • эфир (40) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
гваякол — бесцветные кристаллы, tпл 28,5ºC. Сырьё в синтезе душистых веществ (ванилина, эвгенола, санталидола). * * * ГВАЯКОЛ ГВАЯКОЛ, СН3ОС6Н4ОН, бесцветные кристаллы, tпл 28,5 °С. Сырье в синтезе душистых веществ (ванилина, эвгенола, санталидола) … Энциклопедический словарь
гваякол — gvajakolis statusas T sritis chemija formulė HOC₆H₄OCH₃ atitikmenys: angl. guaiacol rus. гваякол ryšiai: sinonimas – 2 metoksifenolis … Chemijos terminų aiškinamasis žodynas
Гваякол — органическое соединение с сильным характерным запахом. Г. монометиловый эфир пирокатехина: бесцветные кристаллы, tпл 28,4 °С; tkип 205 °С. Г. хорошо растворим в спирте, хлороформе, плохо в петролейном эфире; растворяет иод и серу. Хлорное … Большая советская энциклопедия
Гваякол — водородистый гваяцил, пирогваяковая кислота метиловый эфир пирокатехина (ортодиоксибензола) С6Н4(ОСН3)ОН. Получается при сухой перегонке гваяковой смолы, ванилиново известковой соли с известью, при нагревании смеси пирокатехина и метил… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
гваякол — гваякол, гваяколы, гваякола, гваяколов, гваяколу, гваяколам, гваякол, гваяколы, гваяколом, гваяколами, гваяколе, гваяколах (Источник: «Полная акцентуированная парадигма по А. А. Зализняку») … Формы слов
ГВАЯКОЛ — (2 метоксифенол), мол. м. 124,13; бесцв. кристаллы со своеобразным запахом, темнеющие на воздухе и на свету; т. плавления 28,5 … Химическая энциклопедия
Источник
Гваякол
Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона. — С.-Пб.: Брокгауз-Ефрон . 1890—1907 .
Смотреть что такое «Гваякол» в других словарях:
ГВАЯКОЛ — ГВАЯКОЛ, Guajacolum (Ф VII), монометиловый эфир бренцкатехипа, СвН4(ОН). .(ОСН3) (1, 2), является главной составной частью креозота, из которого и получается путем повторной фракционной перегонки; поступает в продажу или в виде бесцветных или… … Большая медицинская энциклопедия
ГВАЯКОЛ — бесцветная жидкость приятного запаха; получается при сухой перегонке гваяколовой смолы; при обработке хлороформом и едким кали переходит в ванилин. Словарь иностранных слов, вошедших в состав русского языка. Павленков Ф., 1907. ГВАЯКОЛОВОЕ ДЕРЕВО … Словарь иностранных слов русского языка
ГВАЯКОЛ — СН3ОС6Н4ОН, бесцветные кристаллы, tпл 28,5 .С. Сырье в синтезе душистых веществ (ванилина, эвгенола, санталидола) … Большой Энциклопедический словарь
гваякол — сущ., кол во синонимов: 2 • фенол (15) • эфир (40) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
гваякол — бесцветные кристаллы, tпл 28,5ºC. Сырьё в синтезе душистых веществ (ванилина, эвгенола, санталидола). * * * ГВАЯКОЛ ГВАЯКОЛ, СН3ОС6Н4ОН, бесцветные кристаллы, tпл 28,5 °С. Сырье в синтезе душистых веществ (ванилина, эвгенола, санталидола) … Энциклопедический словарь
Гваякол — Гваякол бесцветные, с сильным своеобразным запахом, легко плавящиеся (т. плав. 28,5 °C, т. кип. 205 °C) кристаллы монометилового эфира пирокатехина, темнеющие на воздухе и на свету, хорошо раство … Википедия
гваякол — gvajakolis statusas T sritis chemija formulė HOC₆H₄OCH₃ atitikmenys: angl. guaiacol rus. гваякол ryšiai: sinonimas – 2 metoksifenolis … Chemijos terminų aiškinamasis žodynas
Гваякол — органическое соединение с сильным характерным запахом. Г. монометиловый эфир пирокатехина: бесцветные кристаллы, tпл 28,4 °С; tkип 205 °С. Г. хорошо растворим в спирте, хлороформе, плохо в петролейном эфире; растворяет иод и серу. Хлорное … Большая советская энциклопедия
гваякол — гваякол, гваяколы, гваякола, гваяколов, гваяколу, гваяколам, гваякол, гваяколы, гваяколом, гваяколами, гваяколе, гваяколах (Источник: «Полная акцентуированная парадигма по А. А. Зализняку») … Формы слов
ГВАЯКОЛ — (2 метоксифенол), мол. м. 124,13; бесцв. кристаллы со своеобразным запахом, темнеющие на воздухе и на свету; т. плавления 28,5 … Химическая энциклопедия
Источник
Экология СПРАВОЧНИК
Информация
Гваякол
Гваякол, ч.; едкий натр, 40% и 0,01 М растворы.[ . ]
Содержание гваякола в анализируемом объеме пробы находят по градуировочному графику, который строят по данным измерения оптической плотности растворов шкалы.[ . ]
Комбинация ТЭА и гваякола в дистиллированной воде обеспечивает эффективность поглощения NO, > 90%, но этот раствор может быть использован только в течение семи дней, поскольку после этого срока он приобретает окраску, и эффективность поглощения N02 снижается [37].[ . ]
Ксиленол, крезол и гваякол дают такую же реакцию; хинон окрашивает индикаторный слой в зеленый цвет.[ . ]
Стандартный раствор гваякола. Готовят растворением точного количества гваякола в 0,01 М растворе едкого натра (см. с. 32). Рабочие стандартные растворы с содержанием 10 и 1 м1кг/мл готовят соответствующим разбавлением исходного раствора 0,01 М раствором едкого натра. Стандартные растворы устойчивы в течение 1 сут.[ . ]
Определению не мешают гваякол, дихлорэтан, толуол.[ . ]
Фенол, крезолы, ксилолы, гваякол, тимол и некоторые другие соединения этой группы можно отделить от остальных фенолов и других мешающих веществ, присутствующих, в пробе, отгонкой с водяным паром при определенных условиях. Летучие фенолы являются основным компонентом фенольных сточных вод, и вместе с ними они попадают в-канализационную сеть и в поверхностные воды, загрязняя их. В концентрациях, равных нескольким миллиграммам на 1 л, они могут влиять на биологическую жизнь рек. Некоторые из фенолов в концентрациях порядка нескольких микрограммов на 1 л являются причиной неприятного хлорфенольного запаха и привкуса, появляющихся при хлорировании поверхностных вод в процессе водоподготовки.[ . ]
Метод основан на взаимодействии гваякола с- п-нитрофенилдиазони-ем в щелочной среде с образованием продукта реакции, окрашенного в розовый цвет. По интенсивности окраски определяют содержание гваякола; фенол дает желто-оранжевую окраску. Крезол и эфиры пирогаллола дают также розовую окраску.[ . ]
Предельно допустимая концентрация гваякола (рекомендуемая) 20 мг/м3.[ . ]
Основной стандартный раствор гваякола с содержанием 100 мкг/мл. Растворяют 0,01 г гваякола в мерной колбе емкостью 100 мл в 0,01 н. растворе едкого натра.[ . ]
Активность пероксидазы выражается количеством гваякола, который окисляется Н2О2 под влиянием пероксидазы 0,001 мл крови. Для этого экстинцию опытной пробы переводят согласно калибровочной кривой в количество гамм пероксидазы, делят на четыре (разведение крови для ры6 около 1 :250) и на 30 млн. (время инкубирования) и выражают активность пероксидазы в гваякольных единицах на минуту.[ . ]
Рабочий стандартный раствор с содержанием 10 мкг/мл гваякола готовят в день анализа разбавлением основного раствора 0,01 н. раствором едкого натра.[ . ]
Принцип метода. Метод основан на реакции азосочетания гваякола с диазотированным п-нитроанилином с образованием окрашенных в розовый цвет растворов2.[ . ]
Нэш 1 [392 ] улучшил абсорбцию N02 щелочным раствором путем добавления гваякола, по-видимому, тоже выступающего в роли вспенивающего средства.[ . ]
Т. Г. Лапина использовала ТСХ для раздельного определения в воздухе фенолов — гваякола, фенола и о-, м-, я-крезолов [83]. Отбор проб воздуха в этом случае производят в поглотитель с дистиллированной водой. К поглотительному раствору добавляют солянокислый раствор паранитродиазобензола и щелочь. Раствор нейтрализуют кислотой, проводят экстракцию эфиром и затем наносят эфирный раствор на пластинку, покрытую слоем силикагеля. Окрашенные пятна переносят в коническую колбу, заливают спиртом и раствор подщелачивают.[ . ]
К группе летучих фенолов относят простой фенол С6Н5ОН, три крезола, шесть ксиленолов, гваякол, тимол и многие их замещен-» ные. Относительно того, переходят ли в отгон или не переходят нафтолы и пирокатехин, литературные данные противоречивы. Наши исследования показали, что в обычных условиях проведения отгонки а-нафтол отгоняется на 65 %, ß-нафтол — на 50 % и пирокатехин — на 10%. Если определение заканчивать методом с применением 4-аминоантипирина, то следует учитывать, что опти».[ . ]
К группе летучих фенолов относятся: простой фенол Се ОН, три крезола, шесть ксиленолов, гваякол, тимол и многие их замещенные. Частично с паром отгоняются пирокатехин и а-нафтол.[ . ]
Деструкция лигнина происходит с образованием следующих мономерных соединений: фенола, пирокатехина, гваякола, ванилина и других ароматических соединений, содержащих гидроксильную группу (Криульков, Каплин, 1968). Лигнин, фенолы, углеводороды, жиры, особенно при повышенных концентрациях, образуют большое количество промежуточных продуктов распада, из которых могут возникать новые, более устойчивые соединения (гумусовые вещества, битумоиды). Скорость их распада в водоеме значительно отличается от исходных соединений.[ . ]
Обычно в водном дистилляте находятся метанол, уксусная кислота и ацетон; в дегте — фенолы, преимущественно гваякол, и нейтральные продукты еще неизвестной природы. Выход метанола из лигнинов твердых пород обычно больше, чем выход из мягких пород, вероятно, вследствие более высокого содержания метоксилов у первых.[ . ]
При перегонке с цинковой пылыо щелочного лигнина из початков кукурузы Филлипс [577] в фенольной фракции нашел гваякол и 1-пропил-З-метокси-4-оксибензол. Нейтральная фракция при окислении перманганатом калия дала анисовую кислоту. Выделение фенилпропанового производного укрепило гипотезу о том, что по крайней мере в части лигнин-ной молекулы находится боковая цепь с тремя углеродами в мета-положении к метоксильной группе и в пара-положении к гидроксильной группе.[ . ]
При более сложной и длительной обработке смоляных масел можно получать медицинский креозот, содержащий 50—60% гваякола и ¡креозола; это — маслообразная прозрачная жидкость, сильно преломляющая свет, с резким запахом и едким вкусом.[ . ]
Аттестованная характеристика — массовая концентрация компонента, мкг/мл: фенола 99,6, о-крезола 500, .«-крезола 502 и гваякола 497.[ . ]
Химические свойства. Благодаря наличию гидроксильной группы реакционноспособен. Со щелочью образует растворимый в воде гваяколят; реагирует с окислителями.[ . ]
В фенольной фракции, полученной при сухой перегонке щелочного лигнина из кукурузных стеблей, Бриджер [576] нашел, кроме фенола, о-крезола, гваякола и креозола, р-крезол и 3,5-ксиленол.[ . ]
Многие лекарственные препараты изготовляются в СССР из продуктов химической переработки дерева: скипидар, камфора, аспирин, уимол, креозот, гваякол, искусственная вата. Из продуктов древесины изготовляются краски, лаки. Скипидар употребляют и как лекарство, и как материал для получения автола и синтетической камфоры. Из продуктов химической переработки древесины сосновых пней готовят мыло. Продуктом переработки пневого осмола является скипидар, применяемый в резиновой и бумажной промышленности. Из дерева мы получаем уксусную кислоту, которая является пищевым продуктом и вспомогательным материалом в производстве автомобильных и других лаков, в фармацевтической и текстильной промышленности.[ . ]
В результате варки как соединения VIII, так и соединения XXXIV [45] основным продуктом реакции оказалась 0-стирилсульфокислота XXXVIL Наряду с ней обнаружены гваякол, пирокатехин и в значительном количестве метансульфокислота.[ . ]
Всеми признано, что элементарное ядро лигнина представляет собой гваяциловый остаток, так как близко совпадает по своим свойствам с такими соединениями, как гваякол, эвгенол, ванилик и другими подобными фенолами гваяцилового расположения. Возможной формой строения элемента лигнина является производная а-фенилпропана.[ . ]
Превращение пинорезинола в сульфокислоты было почти количественное. Хлороформенный экстракт содержал менее 1 % исходного вещества, и в нем обнаружены следы пирокатехина и гваякола.[ . ]
Впоследствии были предприняты попытки повысить эффективность поглощения щелочного метода добавлением к поглотительному раствору некоторых соединений: И-соли (0,2 г/л) и три-этаноламина (ТЭА) (1 г/л) [31]; гваякола [32, 33]. Степень поглощения N02 при этом увеличивается с 35 до 95%.[ . ]
Нами использована более точная и простая методика определения пероксидазной активности крови — метод Баха и Зубковой. Принцип методики заключается в том, что перекись водорода в присутствии пероксидазы разлагает растворенный в воде гваякол. Продукты окисления гваякола определяются колориметрически. По их количеству судят об активности фермента.[ . ]
Силилирование должно понижать время удерживания фенольного соединения в данных условиях благодаря частичному блокированию межмолекулярных водородных связей введенными триметилсилиль-ными группами. С) и более продолжительное время удерживания. Но, так как в результате сили-лирования повышается молекулярный вес, в некоторых случаях можно ожидать увеличения времени удерживания даже при отсутствии влияния водородных связей. Преимущества силилирования можно видеть на примере такого нелетучего теплостойкого соединения, как галловая кислота.[ . ]
Филлипс [574], Филлипс и Госс [575] подвергли деструктивной перегонке при пониженном давлении лигнины, извлеченные из соломы и других однолетних растений, и получили 28,3% масла. Окисление фракции, летучей с водяным паром, дало анисовую кислоту, в то время как в нелетучей фракции определили нонакозан.[ . ]
Дегидрирование лигнина с серой или селеном было мало успешным [310, 589]. Филлипс [590] обрабатывал щелочной лигнин початков кукурузы селеном при 300—340° и получил 12,9% масла, которое было разделено на различные фракции. Единственными идентифицированными продуктами были небольшое количество гваякола и З-метокси-4-оксифенил-пропана. Также было найдено некоторое количество неидентифицированных селенсодержащих органических продуктов.[ . ]
В природе ванилин встречается в стручках ванили, произрастающей в тропической полосе, в количестве 1,5—2,5%- С развитием тонкой химической технологии ванилин стали получать синтетически из различных химических веществ. Так, известны способы получения ванилина из эвгенола, пирокатехина, гваякола и других веществ. Однако все эти сырьевые источники являются дорогостоящими и дефицитными, поэтому, естественно, идут поиски более доступных и близких по своему строению веществ для синтеза ванилина. Лигнин и в особенности лигносульфонаты сульфитного щелока или барды спиртовых заводов оказалось возможным использовать для этих целей. Исходя из формулы сульфитированного лигнина (лигносульфонаты), можно легко представить возможность получения ванилина из этих продуктов.[ . ]
Алкилами здесь являются метил, этил и пропил.[ . ]
Токсическое действие. Анизол в 10 раз менее ядовит, чем фенол, и слабее раздражает кожу. Пары фенетола действуют, в основном, наркотически; наряду с этим наблюдается значительное возбуждающее действие на нервную систему животных, напоминающее действие паров фенола. По-видимому, летучесть слишком мала, чтобы пары могли вызывать серьезные отравления. Наибольшее значение в производственных условиях имеют гваякол и монобензиловый эфир гидрохинона.[ . ]
Из этих веществ Гибберт и его сотрудники при этанолизе лигнина выделили вещество (87) и производное соединение (85).[ . ]
Источник