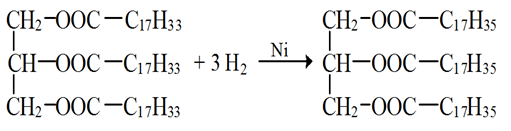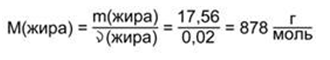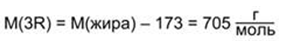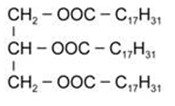- Сложные эфиры — номенклатура, получение, химические свойства. Жиры. Мыла
- Жиры, масла
- Физические свойства жиров
- Химические свойства жиров
- Химические свойства жиров с водой
- Физические свойства жиров
- Получение жиров
- Химические свойства жиров
- Применение жиров
- Примеры решения задач
- Номенклатура жиров
- Физические свойства жиров
- Химические свойства жиров
- 1.1. Кислотный гидролиз
- 1.2. Щелочной гидролиз — омыление жиров
- 2. Гидрирование (гидрогенизация) ненасыщенных жиров
- 3. Мыло и синтетические моющие средства
Сложные эфиры — номенклатура, получение, химические свойства. Жиры. Мыла
Важнейшими представителями сложных эфиров являются жиры.
Жиры, масла
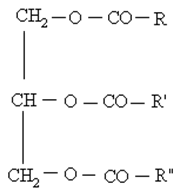
Жиры – это сложные эфиры глицерина и высших одноатомных карбоновых кислот. Общее название таких соединений – триглицериды или триацилглицерины, где ацил – остаток карбоновой кислоты -C(O)R. В состав природных триглицеридов входят остатки насыщенных кислот (пальмитиновой C15H31COOH, стеариновой C17H35COOH) и ненасыщенных (олеиновой C17H33COOH, линолевой C17H31COOH). Высшие карбоновые кислоты, которые входят в состав жиров имеют всегда четное количество атомов углерода (С8 – С18) и неразветвленный углеводородный остаток. Природные жиры и масла – это смеси глицеридов высших карбоновых кислот.
Состав и строение жиров могут быть отражены общей формулой:
Этерификация — реакция образования сложных эфиров.
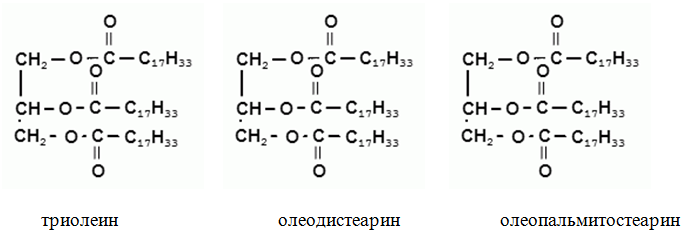
В состав жиров могут входить остатки как предельных, так и непредельных карбоновых кислот в различных сочетаниях.
В обычных условиях жиры, содержащие в своем составе остатки непредельных кислот, чаще всего бывают жидкими. Их называют маслами. В основном, это жиры растительного происхождения — льняное, конопляное, подсолнечное и другие масла (исключения пальмовое и кокосовое масла – твердые в обычных условиях). Реже встречаются жидкие жиры животного происхождения, например рыбий жир. Большинство природных жиров животного происхождения при обычных условиях – твердые (легкоплавкие) вещества и содержат в основном остатки предельных карбоновых кислот, например бараний жир.
Состав жиров определяет их физические и химические свойства.
Физические свойства жиров
Жиры нерастворимы в воде, не имеют четкой температуры плавления и значительно увеличиваются в объеме при плавлении.
Агрегатное состояние жиров твердое, это связано с тем, что в состав жиров входят остатки предельных кислот и молекулы жиров способны к плотной упаковке. В состав масел, входят остатки непредельных кислот в cis – конфигурации, следовательно плотная упаковка молекул невозможна, и агрегатное состояние – жидкое.
Химические свойства жиров
Жиры (масла) являются сложными эфирами и для них характерны реакции сложных эфиров.
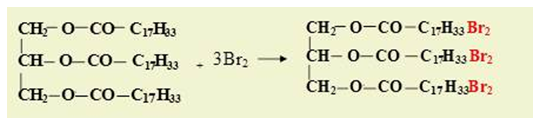
Понятно, что для жиров, содержащих остатки ненасыщенных карбоновых кислот, характерны все реакции непредельных соединений. Они обесцвечивают бромную воду, вступают в другие реакции присоединения. Наиболее важная в практическом плане реакция – гидрирование жиров. Гидрированием жидких жиров получают твердые сложные эфиры. Именно эта реакция лежит в основе получения маргарина — твердого жира из растительных масел. Условно этот процесс можно описать уравнением реакции:
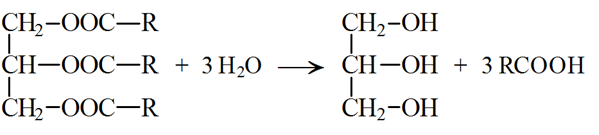
Все жиры, как и другие сложные эфиры, подвергаются гидролизу:
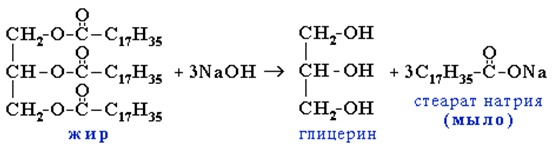
Гидролиз сложных эфиров- обратимая реакция. Чтобы сместить равновесие в сторону образования продуктов гидролиза, его проводят в щелочной среде (в присутствие щелочей или Na2CO3). В этих условиях гидролиз жиров протекает обратимо, и приводит к образованию солей карбоновых кислот, которые называются мылами. Гидролиз жиров в щелочной среде называют омылением жиров.
При омылении жиров образуются глицерин и мыла – натриевые и калиевые соли высших карбоновых кислот:
Омыление – щелочной гидролиз жиров, получение мыла.
Мыла – смеси натриевых (калиевых) солей высших предельных карбоновых кислот (натриевое мыло – твердое, калиевое — жидкое).
Мыла являются поверхностно-активными веществами (сокращенно: ПАВами, детергентами). Моющее действие мыла связано с тем, что мыла эмульгируют жиры. Мыла образуют мицеллы с загрязняющими веществами (условно — это жиры с различными включениями).
Липофильная часть молекулы мыла растворяется в загрязняющем веществе, а гидрофильная часть оказывается на поверхности мицеллы. Мицеллы заряжены одноименно, следовательно отталкиваются, при этом загрязняющее вещество и вода превращается в эмульсию (практически – это грязная вода).
В воде также происходит гидролиз мыла, при этом создается щелочная среда.
Мыла нельзя использовать в жесткой и морской воде, так как образующиеся при этом стеараты кальция (магния) в воде нерастворимы.
Источник
Химические свойства жиров с водой
На нашем сайте собрано более 100 бесплатных онлайн калькуляторов по математике, геометрии и физике.
Основные формулы, таблицы и теоремы для учащихся. Все что нужно, чтобы сделать домашнее задание!
Не можете решить контрольную?!
Мы поможем! Более 20 000 авторов выполнят вашу работу от 100 руб!
Жиры и масла (жидкие жиры) – важные природные соединения. Все жиры и масла растительного происхождения почти целиком состоят из сложных эфиров глицерина (триглицеридов). В этих соединениях глицерин этерифицирован высшими карбоновыми кислотами.
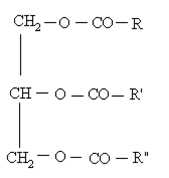
Жиры имеют общую формулу:
Здесь R, R’, R’’ – углеводородные радикалы.
Три гидроксогруппы глицерина могут быть этерифицированы либо только одной кислотой, например пальмитиновой или олеиновой, либо двумя или тремя различными кислотами:
Основные предельные кислоты, образующие жиры – пальмитиновая С15Н31СООН и стеариновая С17Н35СООН; основные непредельные кислоты – олеиновая С17Н33СООН и линолевая С17Н31СООН.
Физические свойства жиров
Жиры, образованные предельными кислотами, — твердые вещества, а непредельными – жидкие. Все жиры очень плохо растворимы в воде.
Получение жиров
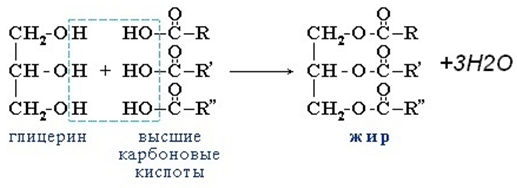
Жиры получают по реакции этерификации, протекающей между трехатомным спиртом глицерином и высшими карбоновыми кислотами:
Химические свойства жиров
Среди реакций жиров особое место занимает гидролиз, который можно осуществить действием как кислот, так и оснований:
а) кислотный гидролиз
б) щелочной гидролиз
Для масел (жидких жиров) характерны реакции присоединения:
— гидрирование (реакция гидрирования (гидрогенизации) лежит в основе получения маргарина)
Мерой ненасыщенности остатков кислот, которые входят в состав жиров, служит йодное число, выражаемое массой йода (в граммах), который может присоединиться по двойным связям к 100г жира. Йодное число важно при оценке высыхающих масел.
Масла (жидкие жиры) также подвергаются реакциям окисления и полимеризации.
Применение жиров
Жиры нашли широкое применение в пищевой промышленности, фармацевтике, в производстве масел и различных косметических средств, в производстве смазочных материалов.
Примеры решения задач
| Задание | Растительное масло массой 17,56 г нагрели с 3,36 г гидроксида калия до полного исчезновения масляного слоя. При действии избытка бромной воды на полученный после гидролиза раствор образуется только одно тетрабромпроизводное. Установите возможную формулу жира. |
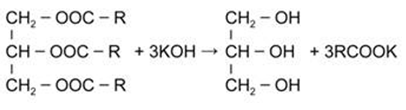
| Решение | Запишем в общем виде уравнение гидролиза жира: |
На 1 моль жира при гидролизе приходится 3 моль гидроксида калия. Найдем количество вещества гидроксида калия и жира, причем, количество жира втрое меньше:
Зная количество и массу жира, можно найти его молярную массу:
На три углеводородных радикала R кислот приходится 705 г/моль:
Зная, что тетрабромпроизводное получено только одно, можно сделать вывод, что все кислотные остатки одинаковы и содержат по 2 двойные связи. Тогда получаем, что в каждом радикале содержится 17 атомов углерода, это радикал линолевой кислоты:
Возможная формула жира:
| Задание | Напишите две возможные формулы жира, имеющего в молекуле 57 атомов углерода и вступающего в реакцию с иодом в соотношении 1:2. В составе жира имеются остатки кислот с четным числом углеродных атомов. |
| Ответ | Общая формула жиров: |
где R, R’, R» — углеводородные радикалы, содержащие нечетное число атомов углерода (еще один атом из кислотного остатка входит в состав группы -СО-). На долю трех углеводородных радикалов приходится 57- 6 = 51 атом углерода. Можно предположить, что каждый из радикалов содержит по 17 атомов углерода.
Поскольку одна молекула жира может присоединить две молекулы иода, то на три радикала приходится две двойные связи или одна тройная. Если две двойные связи находятся в одном радикале, то в состав жира входят остаток линолевой кислоты (R = С17Н31) и два остатка стеариновой кислоты (R’ = R» = С17Н35). Если две двойные связи находятся в разных радикалах, то в состав жира входят два остатка олеиновой кислоты (R = R’ = С 17H33) и остаток стеариновой кислоты (R» = С17Н35). Возможные формулы жира:
Источник
Номенклатура жиров
Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой. Все животные жиры, кроме рыбьего – твёрдые. | Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими. Все растительные жиры, кроме пальмового масла – жидкие. |
Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
1.1. Кислотный гидролиз
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин |
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
| Например, при гидролизе тристеарата глицерина гидроксидом натрия образуется стеарат натрия . |
2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
| Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина: |
| Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира. |
3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca 2+ и Mg 2+ дают с высшими кислотами нерастворимые в воде соли.
| Например, тристеарат глицерина взаимодействует с сульфатом кальция |
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Спирт реагирует с серной кислотой с образованием алкилсульфата .
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Источник