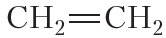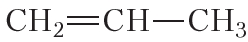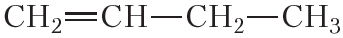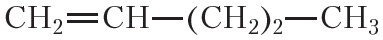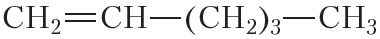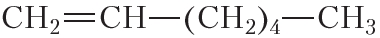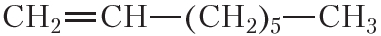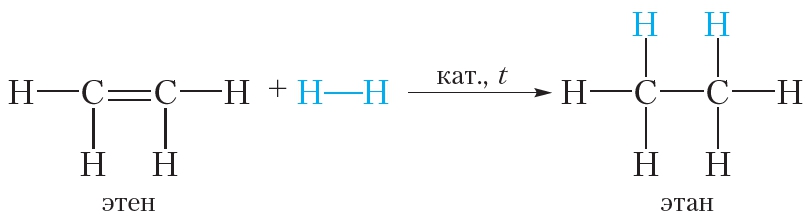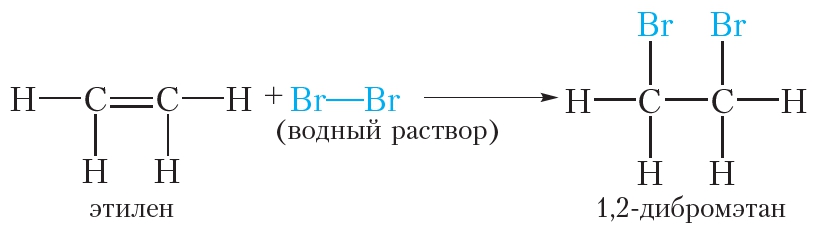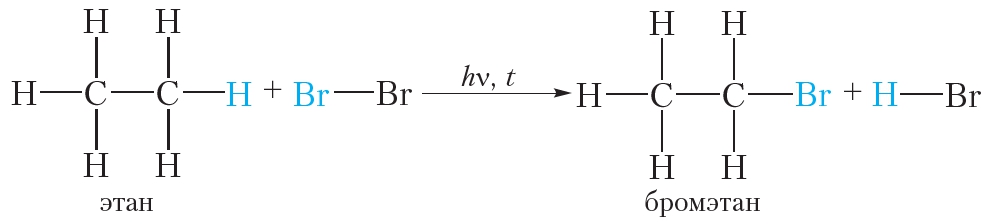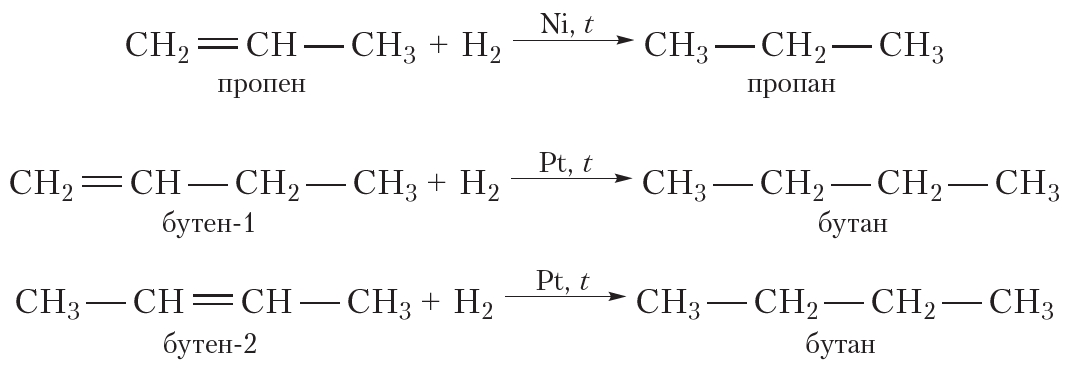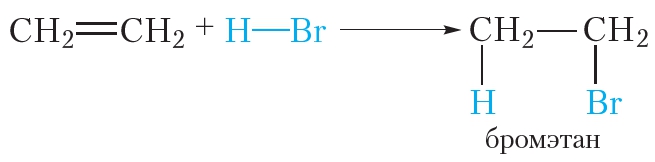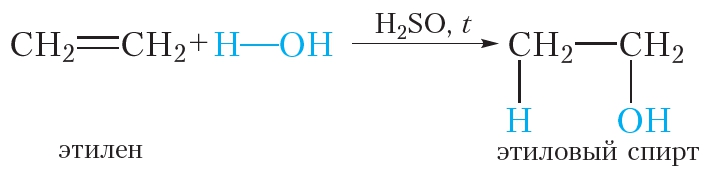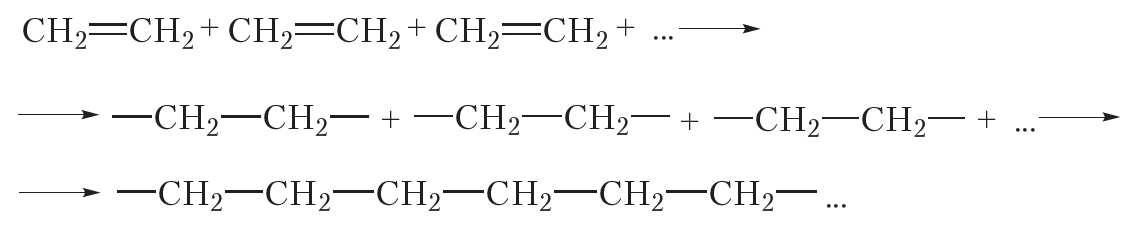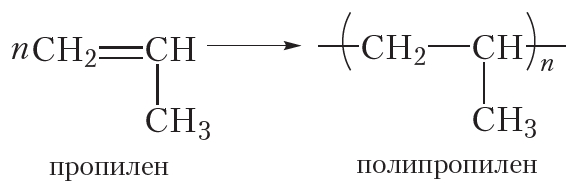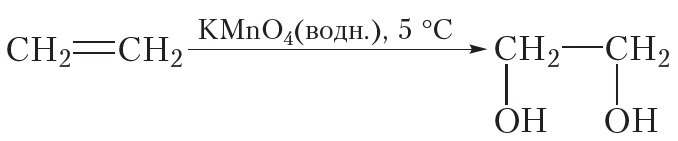§ 15. Физические и химические свойства алкенов
| Сайт: | Профильное обучение |
| Курс: | Химия. 10 класс |
| Книга: | § 15. Физические и химические свойства алкенов |
| Напечатано:: | Гость |
| Дата: | Четверг, 21 Октябрь 2021, 19:09 |
Оглавление
Физические свойства
По физическим свойствам алкены мало отличаются от алканов с тем же числом атомов углерода в молекуле. Так, алкены с числом атомов углерода в молекуле 2—4 при комнатной температуре являются бесцветными газами. Алкены с числом атомов углерода в молекуле от 5 до 17 — жидкости. Алкены с ещё бóльшим числом атомов углерода в молекуле (от 18 и более) представляют собой твёрдые вещества. Температуры кипения некоторых алкенов неразветвлённого строения приведены в таблице 15.1.
Таблица 15.1. Температуры кипения алкенов
Температура кипения (tкип, °С)
Так же, как и алканы, алкены нерастворимы в воде, но хорошо растворяются в органических растворителях.
Плотность алкенов меньше, чем у воды.
Химические свойства
Благодаря наличию в молекуле π-связи реакционная способность алкенов намного выше, чем у алканов. Напомним, что для алканов характерны реакции замещения. Для алкенов характерными являются реакции присоединения:
Эти реакции сопровождаются разрывом π-связи, так как она менее прочная, чем σ-связь.
В реакции присоединения алкены вступают в более мягких условиях, чем алканы в реакции замещения. Реакции замещения для алкенов нехарактерны.
Реакции присоединения
1. Галогенирование. Присоединение галогенов
Алкены так же, как и алканы, взаимодействуют с галогенами. Однако в случае алкенов происходит реакция присоединения, а не замещения. Сравним эти реакции.
Бромирование этилена (реакция присоединения ):
Бромирование этана (реакция замещения ):
Этилен реагирует с водным раствором брома (бромной водой) при обычных условиях, в то время как реакция этана с бромом возможна только в жёстких условиях — при нагревании или ультрафиолетовом облучении.
При пропускании этилена через бромную воду протекает реакция присоединения брома по двойной связи. В результате оранжевый раствор брома обесцвечивается.
В молекуле этана нет двойных связей, поэтому при пропускании этана через бромную воду химическая реакция не протекает и раствор брома остаётся оранжевым.
Следовательно, реакция с бромной водой является качественной реакцией на двойную связь.
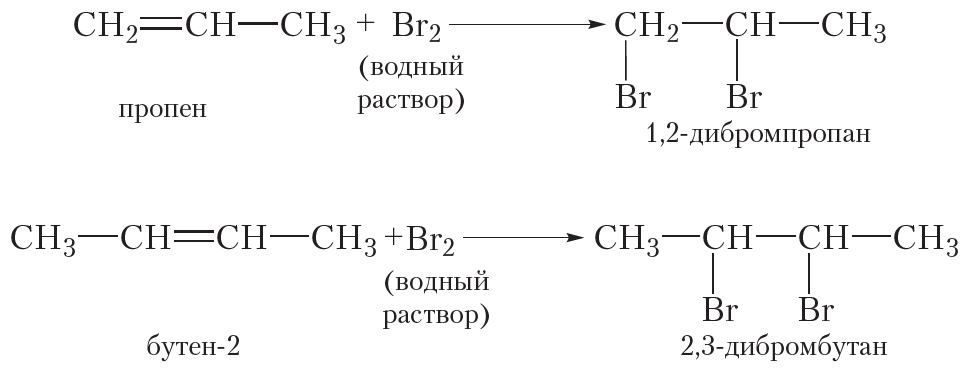
Подобно этилену, другие алкены легко присоединяют бром, обесцвечивая бромную воду:
2. Гидрирование. Присоединение водорода
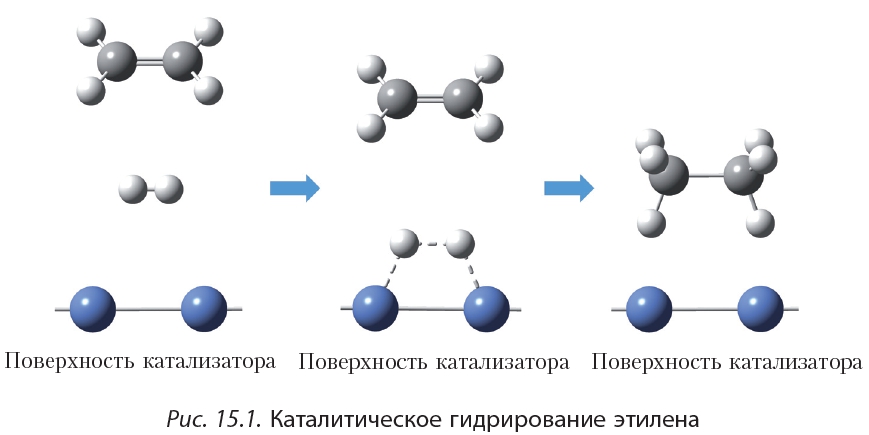
Присоединение водорода к органическому веществу называется реакцией гидрирования. При обычных условиях алкены не присоединяют водород. Для протекания реакции необходим катализатор (Pt или Ni).
В результате гидрирования алкенов образуются алканы. В начале данного параграфа приведено уравнение реакции гидрирования этена. Приведём уравнения реакций гидрирования некоторых других алкенов:
Как вы уже знаете, катализатор ускоряет протекание химической реакции, но сам при этом не расходуется. Роль катализатора в реакции гидрирования заключается в том, чтобы ослабить химическую связь в молекуле водорода и, таким образом, активировать эту молекулу для реакции присоединения:
3. Гидрогалогенирование. Присоединение галогеноводородов
Алкены могут вступать в реакции присоединения не только с простыми, но и со сложными веществами. Например, этилен легко присоединяет бромоводород:
Реакции присоединения галогеноводородов к органическим веществам называются реакциями гидрогалогенирования. Эти реакции протекают при обычных условиях.
4. Гидратация. Присоединение воды
Гидратацией называется реакция присоединения воды к органическому веществу. При нагревании в присутствии катализатора (H2SO4) этилен присоединяет воду. При этом образуется этиловый спирт:
Реакция полимеризации
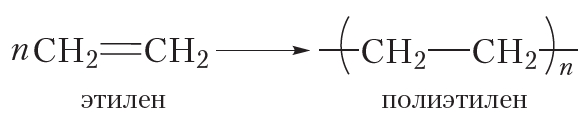
За счёт раскрытия двойных связей отдельные молекулы этилена могут соединяться друг с другом, образуя длинные цепи. Схематично этот процесс можно изобразить так:
В результате соединения сотен или даже тысяч молекул этилена образуется одна гигантская молекула — полимер. Протекающая реакция называется реакцией полимеризации.
Более кратко процесс полимеризации этилена можно выразить следующим уравнением:
Полимеризоваться могут и другие алкены, в частности пропилен:
Исходное вещество в реакции полимеризации называется мономером, а продукт — полимером. Молекулы полимера также называют макромолекулами.
Число мономерных звеньев в молекуле полимера называется степенью полимеризации. В формуле полимера степень полимеризации обозначают индексом «n».
Полиэтилен и полипропилен нам хорошо знакомы. Из полиэтилена изготавливают полиэтиленовую плёнку, посуду, предметы домашнего обихода и т. д. Полипропилен очень похож на полиэтилен и отличается от него только повышенной прочностью и термостойкостью. Из полипропилена изготавливают плёнку для теплиц, корпуса автомобильных аккумуляторов и многое другое. Со многими полимерами вы познакомитесь далее.
Реакции окисления
1. Горение. Взаимодействие с кислородом
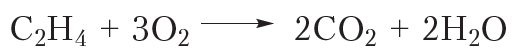
Так же, как и алканы, алкены горят с образованием углекислого газа и воды:
Приведём уравнение реакции горения алкенов в общем виде:
2. Неполное окисление. Реакция с KMnO4
Окисление алкенов может протекать и без разрушения углеродного скелета. Так, при пропускании этилена через разбавленный водный раствор перманганата калия (KMnO4) фиолетового цвета окраска исчезает. Перманганат калия расщепляет π-связь в молекуле этилена, при этом σ-связь между атомами углерода сохраняется. Протекание этой реакции отобразим не с помощью уравнения, а упрощённо в виде схемы. Схема реакции окисления этилена водным раствором перманганата калия выглядит следующим образом:
Из схемы видно, что π-связь в ходе данной реакции раскрывается, к атомам углерода присоединяются две кислородсодержащие группы — OH , то есть этилен окисляется. В результате образуется этиленгликоль, представитель многоатомных спиртов.
Написание схем часто оказывается более удобным, чем уравнений, поэтому их широко используют в органической химии.
Так же, как и реакция с бромной водой, реакция с раствором перманганата калия является качественной реакцией на двойную связь. В результате данной реакции наблюдается обесцвечивание фиолетового раствора перманганата калия.
Характерными для алкенов являются реакции присоединения по двойной связи. При этом происходит расщепление π -связи. Алкены могут присоединять галогены, водород, галогеноводороды, воду.
Реакция полимеризации — это многократно повторяющаяся реакция присоединения. В результате этой реакции образуются гигантские молекулы полимеров, широко применяемых в нашей жизни.
Низкомолекулярное вещество, из которого синтезируют полимер, называется мономером; число мономерных звеньев в макромолекуле полимера называется степенью полимеризации.
Реакции обесцвечивания бромной воды и раствора перманганата калия являются качественными реакциями на двойную связь.
Вопросы и задания
1. Напишите уравнения реакций присоединения к этилену и пропилену: а) водорода; б) хлора. Назовите продукты реакций. Как на практике можно различить метан и этилен?
2. Напишите уравнение реакции бромоводорода с бутеном-2 . Назовите продукт реакции.
3. К бромной воде добавили избыток раствора гексена-1 в гептане. Какие явления будут наблюдаться при этом? Напишите уравнение протекающей реакции.
4. Напишите схему реакции взаимодействия пропилена с водным раствором перманганата калия.
5. В результате полимеризации этилена получен полимер массой 140 г, содержащий 1,505 ∙ 10 22 макромолекул. Вычислите: а) среднюю молярную массу полимера; б) степень полимеризации.
6. После пропускания через склянку с бромной водой (избыток) 20 дм 3 (н. у.) смеси этана и этилена масса склянки увеличилась на 20 г. Определите объём (н. у.) этана в смеси газов.
7*. Напишите схемы реакций, с помощью которых можно получить 2,2,3,3-тетраметилбутан из 2-метилбутена .

Источник
Acetyl
Это пилотный ролик из серии об органических реакциях.
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Источник |