- Сероводород
- Сероводород
- Строение молекулы и физические свойства
- Способы получения сероводорода
- Химические свойства сероводорода
- Сероводород H2S и сульфиды- химические свойства
- Сульфиды — получение и химический свойства
- Сероводород (H2S) Свойства, риски и использование
- Где производится сероводород?
- Физико-химические свойства
- Реактивность и опасности
- ингаляция
- Контакт с кожей
- Зрительный контакт
- приложений
- 1- Производство серы
- 2- Аналитическая химия
- 3- Другое использование
Сероводород
Сероводород
Строение молекулы и физические свойства
Сероводород H2S – это бинарное соединение водорода с серой, относится к летучим водородным соединениям. Следовательно, сероводород бесцветный ядовитый газ, с запахом тухлых яиц. Образуется при гниении. В твердом состоянии имеет молекулярную кристаллическую решетку.
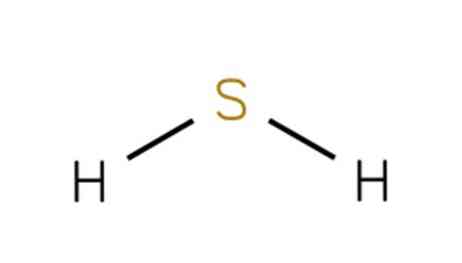
Геометрическая форма молекулы сероводорода похожа на структуру воды — уголковая молекула. Но валентный угол H-S-H меньше, чем угол H-O-H в воде и составляет 92,1 о .
Способы получения сероводорода
1. В лаборатории сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
Например , при действии соляной кислоты на сульфид железа (II):
FeS + 2HCl → FeCl2 + H2S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
Еще один лабораторный способ получения сероводорода – нагревание парафина с серой.
Видеоопыт получения и обнаружения сероводорода можно посмотреть здесь.
2. Также сероводород образуется при взаимодействии растворимых солей хрома (III) и алюминия с растворимыми сульфидами. Сульфиды хрома (III) и алюминия необратимо гидролизуются в водном растворе.
Например: х лорид хрома (III) реагирует с сульфидом натрия с образованием гидроксида хрома (III), сероводорода и хлорида натрия:
Химические свойства сероводорода
1. В водном растворе сероводород проявляет слабые кислотные свойства. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
Например , сероводород реагирует с гидроксидом натрия:
H2S + 2NaOH → Na2S + 2H2O
H2S + NaOH → NaНS + H2O
2. Сероводород H2S – очень сильный восстановитель за счет серы в степени окисления -2. При недостатке кислорода и в растворе H2S окисляется до свободной серы (раствор мутнеет):
В избытке кислорода:
3. Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Например, бром и хлор окисляют сероводород до молекулярной серы:
H2S + Br2 → 2HBr + S↓
H2S + Cl2 → 2HCl + S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
Например , азотная кислота окисляет сероводород до молекулярной серы:
При кипячении сера окисляется до серной кислоты:
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Например , оксид серы (IV) окисляет сероводород:
Соединения железа (III) также окисляют сероводород:
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
Серная кислота окисляет сероводород либо до молекулярной серы:
Либо до оксида серы (IV):
4. Сероводород в растворе реагирует с растворимыми солями тяжелых металлов : меди, серебра, свинца, ртути, образуя черные сульфиды, нерастворимые ни в воде, ни в минеральных кислотах.
Например , сероводород реагирует в растворе с нитратом свинца (II). при этом образуется темно-коричневый (почти черный) осадок, нерастворимый ни в воде, ни в минеральных кислотах:
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видеоопыт взаимодействия сероводорода с нитратом свинца можно посмотреть здесь.
Источник
Сероводород H2S и сульфиды- химические свойства
Физические свойства сероводорода:
Газ, бесцветный, с запахом тухлых яиц, ядовит, растворим в воде (в 1V H2O растворяется 3V H2S при н.у.); t°пл. = -86°C; t°кип. = -60°С.
Получение сероводорода:
1) Из простых веществ: H2 + S t° → H2S
2) Реакцией обмена: FeS + 2HCl→FeCl2 + H2S
Химические свойства сероводорода:
1) Раствор H2S в воде – слабая двухосновная кислота.
Сероводородная кислота образует два ряда солей — средние (сульфиды) и кислые (гидросульфиды).
2) Взаимодействует с основаниями:
3) Качественная реакция на сероводород и растворимые сульфиды — образование темно-коричневого (почти черного) осадка PbS:
4) H2S проявляет очень сильные восстановительные свойства:
5) Сероводород окисляется кислородом:
при недостатке O2
6) Серебро при контакте с сероводородом чернеет:
Сульфиды — получение и химический свойства
Получение сульфидов:
1) Многие сульфиды получают нагреванием металла с серой:
Hg + S → HgS (при комнатной температуре)
2) Растворимые сульфиды получают действием сероводорода на щелочи:
3) Нерастворимые сульфиды получают обменными реакциями:
Химические свойства сульфидов:
1) Растворимые сульфиды сильно гидролизованы, вследствие чего их водные растворы имеют щелочную реакцию:
S 2- + H2O ↔ HS — + OH —
2) Нерастворимые сульфиды можно перевести в растворимое состояние действием концентрированной HNO3:
3) Водорастворимые сульфиды растворяют серу с образованием полисульфидов:
Полисульфиды при окислении превращаются в тиосульфаты, например:
Источник
Сероводород (H2S) Свойства, риски и использование
сероводород это общее название сероводорода (H2S). Это можно рассматривать как гидразидную кислоту в растворе (H2S (aq)).
Рассмотрение сульфгидрильной кислоты дано несмотря на низкую растворимость в воде этого химического соединения. Его структура представлена на рисунке 1 (EMBL-EBI, 2005).
Поэтому сероводород мало растворим в воде. При растворении образует кислый сульфид-ион или гидросульфид (HS — ). Водный раствор сероводорода или сероводорода бесцветен и при воздействии воздуха медленно окисляет элементарную серу, которая не растворяется в воде.
Сера Дианион С2 — существует только в сильно щелочных водных растворах; Это исключительно основной с рКа> 14.
H2S возникает практически там, где элементарная сера вступает в контакт с органическим материалом, особенно при высоких температурах. Сероводород представляет собой ковалентный гидрид, химически связанный с водой (H2O), поскольку кислород и сера производятся в той же группе, что и периодическая таблица.
Это часто происходит, когда бактерии разрушают органическое вещество в отсутствие кислорода, например, в болотах и канализации (наряду с процессом анаэробного сбраживания). Это также происходит в вулканических газах, природном газе и некоторых колодезных водах..
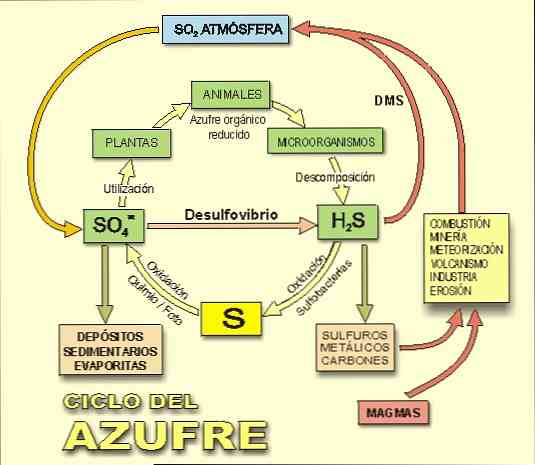
Также важно помнить, что сероводород является центральным участником серного цикла, биогеохимического цикла серы на Земле (рисунок 2)..
Как упомянуто выше, восстанавливающие серу и сульфатвосстанавливающие бактерии получают энергию окисления из водорода или органических молекул в отсутствие кислорода путем восстановления серы или сульфата до сероводорода.
Другие бактерии выделяют сероводород из аминокислот, которые содержат серу. Несколько групп бактерий могут использовать сероводород в качестве топлива, окисляя его до элементарной серы или сульфата, используя кислород или нитрат в качестве окислителя..
Чистые серные бактерии и зеленые серные бактерии используют сероводород в качестве донора электронов при фотосинтезе, в результате чего образуется элементарная сера.
Фактически, этот режим фотосинтеза старше, чем режим цианобактерий, водорослей и растений, который использует воду в качестве донора электронов и выделяет кислород (База данных метаболома человека, 2017).
- 1 Где производится сероводород?
- 2 Физические и химические свойства
- 3 Реактивность и опасности
- 3.1 Вдыхание
- 3.2 Контакт с кожей
- 3.3 Попадание в глаза
- 4 использования
- 4.1 1- Производство серы
- 4.2 2- Аналитическая химия
- 4.3 3- Другое использование
Где производится сероводород?
Сероводород (H2S) встречается в природе в сырой нефти, природном газе, вулканических газах и горячих источниках. Это также может быть результатом бактериальной деградации органического вещества. Это также произведено человеческими и животными отходами.
Бактерии, обнаруженные во рту и желудочно-кишечном тракте, вырабатывают сероводород из бактерий, которые расщепляют материалы, содержащие растительные или животные белки..
Сероводород также может возникать в результате промышленной деятельности, такой как пищевая промышленность, коксовые печи, крафт-бумаги, кожевенные заводы и нефтеперерабатывающие заводы (Агентство по регистрации токсичных веществ и заболеваний, 2011 г.).
Физико-химические свойства
Сероводород — бесцветный газ с сильным запахом тухлых яиц. Водный раствор сероводорода бесцветный без характерного аромата.
Соединение имеет молекулярную массу 34,1 г / моль, водный раствор имеет плотность 1,334 г / мл. Он имеет температуру плавления -82 ° С и температуру кипения -60 ° С. Он слабо растворяется в воде и способен растворять всего 4 грамма на литр этого растворителя при 20 ° C (Royal Society of Chemistry, 2015).
Сероводород реагирует как кислота и как восстановитель. Он взрывается при контакте с дифторидом кислорода, пентафторидом брома, трифторидом хлора, оксидом дихлорида и фульминатом серебра. Он может воспламениться и взорваться под воздействием медного порошка в присутствии кислорода..
Он может реагировать аналогичным образом с другими порошкообразными металлами. Воспламеняется при контакте с оксидами и пероксидами металлов (пероксид бария, триоксид хрома, оксид меди, диоксид свинца, диоксид марганца, оксид никеля, оксид серебра, диоксид серебра, триоксид таллия, пероксид натрия, оксид ртути, оксид кальция).
Зажигается броматом серебра, гипохлоритом свинца (II), хроматом меди, азотной кислотой, оксидом свинца (IV) и оксидом. Он может воспламениться, если пройдет через ржавые железные трубы. Экзотермически реагирует с основаниями.
Тепло реакции с кальцинированной содой, гидроксидом натрия, гидроксидом калия, гидроксидом бария может вызвать возгорание или взрыв непрореагировавшего участка в присутствии воздуха / кислорода (HYDROGEN SULFIDE, 2016).
Реактивность и опасности
H2S считается стабильным соединением, хотя он легко воспламеняется и чрезвычайно токсичен.
Смесь тяжелее воздуха и может перемещаться на значительное расстояние от источника возгорания и обратно. Может образовывать взрывоопасные смеси с воздухом в широком диапазоне.
Он также вступает в взрывную реакцию с пентафторидом брома, трифторидом хлора, трийодидом азота, трихлоридом азота, дифторидом кислорода и хлоридом фенилдиазония.
При нагревании до разложения он выделяет высокотоксичные пары оксидов серы. Несовместим со многими материалами, включая сильные окислители, металлы, сильную азотную кислоту, пентафторид брома, трифторид хлора, трийодид азота, трихлорид азота, дифторид кислорода и хлорид фенилдиазония.
Сероводород (H2S) несет ответственность за многие случаи профессионального токсического воздействия, особенно в нефтяной промышленности. Клинические эффекты Н2S зависит от его концентрации и продолжительности воздействия.
H2S немедленно приводит к смертельному исходу, когда концентрации превышают 500-1000 частей на миллион (ppm), но воздействие более низких концентраций, таких как 10-500 ppm, может вызывать различные респираторные симптомы, начиная от ринита до острой дыхательной недостаточности..
H2S также может поражать несколько органов, вызывая временные или постоянные нарушения в нервной, сердечно-сосудистой, почечной, печеночной и гематологической системах..
Представлен случай профессионального воздействия H2Это приводит к поражению нескольких органов, острой дыхательной недостаточности, организации пневмонии и шока, сходных с острым сепсисом. В этом случае у пациента также развилось легкое обструктивное и рестриктивное заболевание легких и периферическая невропатия (Al-Tawfiq, 2010).
ингаляция
В случае вдыхания выносите его на улицу и держите в покое в удобном для дыхания положении. Если не дышите, примените искусственное дыхание. Если дыхание затруднено, обученный персонал должен дать кислород.
Контакт с кожей
При попадании на кожу ее следует промыть большим количеством воды. Жидкость под давлением может вызвать обморожение. В случае воздействия жидкости под давлением зону замораживания следует немедленно нагреть теплой водой, не превышающей 41 ° C..
Температура воды должна быть терпимой к нормальной коже. Прогревание кожи следует поддерживать в течение не менее 15 минут или до тех пор, пока в пораженный участок не вернется нормальная окраска и ощущение. В случае массивного воздействия одежду снимают во время душа теплой водой.
Зрительный контакт
В случае попадания в глаза тщательно промыть глаза водой не менее 15 минут. Держите веки открытыми и подальше от глазных яблок, чтобы убедиться, что все поверхности тщательно промыты..
Проглатывание не считается возможным путем воздействия. Во всех остальных случаях требуется немедленная медицинская помощь (Praxair, 2016).
приложений
1- Производство серы
Установка извлечения серы Claus состоит из печи сгорания, котла-утилизатора, конденсатора серы и ряда каталитических ступеней, каждая из которых использует подогрев, слой катализатора и конденсатор серы. Обычно используются две или три каталитические стадии.
Процесс Клауса превращает сероводород в элементарную серу посредством двухстадийной реакции.
Первая стадия включает контролируемое сгорание исходного газа для превращения приблизительно одной трети сероводорода в диоксид серы и некаталитическую реакцию сероводорода, не сгоревшего с диоксидом серы..
На второй стадии реакции Клауса сероводород и диоксид серы реагируют на катализаторе с образованием серы и воды.
Количество воздуха для горения строго контролируется, чтобы максимизировать извлечение серы, то есть поддержание соответствующей реакционной стехиометрии от сероводорода 2: 1 до диоксида серы через последующие реакторы.
Как правило, извлечение серы может достигать 97% (Национальная медицинская библиотека США, 2011).
2- Аналитическая химия
Уже более века сероводород играет важную роль в аналитической химии, в качественном неорганическом анализе ионов металлов..
В этих анализах ионы тяжелых металлов (и неметаллов) осаждаются (например, Pb (II), Cu (II), Hg (II), As (III)) из раствора после воздействия H2S. Полученный осадок снова растворяется с некоторой селективностью и, таким образом, идентифицируется.
3- Другое использование
Это соединение также используется для отделения оксида дейтерия или тяжелой воды от обычной воды с помощью процесса сульфида Гирдлера..
Ученые из Университета Эксетера обнаружили, что клеточное воздействие небольшого количества сероводорода может предотвратить повреждение митохондрий.
Когда клетка подвергается стрессу из-за болезни, ферменты притягиваются к клетке, образуя небольшое количество сероводорода. Это исследование может иметь больше последствий в профилактике инсультов, болезней сердца и артрита (Stampler, 2014).
Сероводород может обладать антивозрастными свойствами, блокируя разрушительные химические вещества в клетке, имея свойства, подобные ресвератролу, антиоксиданту, обнаруженному в красном вине.
Источник