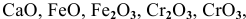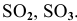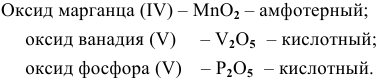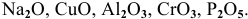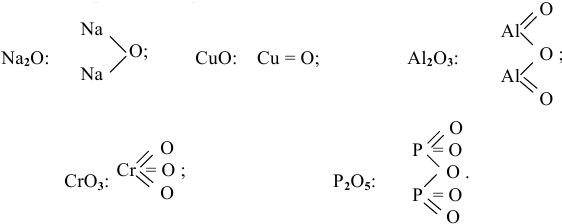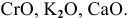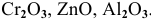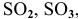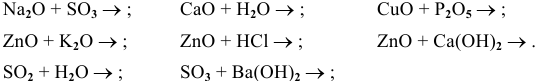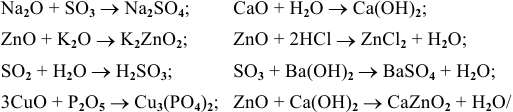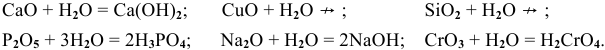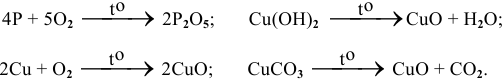- Как составить реакции с оксидами (алгоритм) методическая разработка по химии (8 класс) на тему
- Скачать:
- Предварительный просмотр:
- По теме: методические разработки, презентации и конспекты
- Конспект уроков химии в технологии деятельностного метода 8 класс «Взаимодействие оксидов неметаллов с водой»; 11 класс «Гидролиз неорганических веществ как пример ионных реакций»
- Задачи с решениями по оксидам
- Типовые задачи с решениями по оксидам
- Задача 1
- Задача 2
- Задача 3
- Задача 4
- Задача 5
- Задача 6
- Задача 7
- Задача 8
Как составить реакции с оксидами (алгоритм)
методическая разработка по химии (8 класс) на тему
Этот алгоритм поможет легко и просто составить уравнения.
Скачать:
| Вложение | Размер |
|---|---|
| kak_sostavit_reakcii_s_oksidami.doc | 157 КБ |
Как сдать ЕГЭ на 80+ баллов?
Репетиторы Учи.Дома помогут подготовиться к ЕГЭ. Приходите на бесплатный пробный урок, на котором репетиторы определят ваш уровень подготовки и составят индивидуальный план обучения.
Бесплатно, онлайн, 40 минут
Предварительный просмотр:
Как составить реакции с оксидами
Реакция 1. Основный оксид + кислотный оксид → соль
Тип реакции – реакция соединения .
Чтобы составить уравнение этой реакции, надо проделать следующие действия:
- Определить идёт ли реакция?
Реакция осуществима, если оксид металла образован элементами из IA и II A групп.
- Определить по формуле кислотного оксида химическую формулу соответствующей ему кислоты, формулу кислотного остатка и его валентность.
- Определить по формуле основного оксида валентность металла.
- Составить по валентностям формулу соли.
- Записать уравнение реакции и подобрать в нем коэффициенты.
Пример: Написать уравнение реакции: MgO + N 2 О 5 → .
Действуем по плану:
- Складываем (в уме или на черновике) формулы кислотного оксида и воды:
- Определяем формулу кислотного остатка NO 3 , валентность I (равна количеству Н в кислоте).
- По формуле MgO легко находится валентность магния – II.
- Составляем формулу соли: Mg(NO 3 ) 2
- Записываем, уравнение реакции и подбираем в нем коэффициенты:
MgO + N 2 O 5 → Mg(NО 3 ) 2
Реакция 2. основный оксид + кислота → соль + вода
Тип реакции — реакция обмена .
Составить уравнение этой реакции проще, чем уравнение реакции 1, потому что формула кислоты нам уже известна; зная ее, просто получить и формулу кислотного остатка, и его валентность.
Дальше поступаем так же, как и в предыдущем примере. При составлении уравнения реакции не забудем, что выделяется вода!
Пример: Составьте уравнение реакции между оксидом алюминия и хлороводородной кислотой.
- Вспомним формулу хлороводородной кислоты — НСl, её остаток Сl (хлорид) имеет валентность I.
- По периодической системе Д.И. Менделеева установим, что валентность алюминия III и формула его оксида Аl 2 Оз.
- Составим формулу продукта реакции — соли (хлорида алюминия): АlСlз.
- Запишем уравнение реакции и подберем в нем коэффициенты:
Аl 2 Оз + 6HCl → АlСlз + 3H 2 O
Реакция 3. Кислотный оксид + основание → соль + вода
Тип реакции — реакция обмена .
Для составления уравнения такой реакции следует выполнить действия:
- По формуле кислотного оксида определить формулу его кислоты, формулу кислотного остатка и его валентность (точно так же, как и при составлении реакции 1).
- По формуле гидроксида найти валентность металла: это просто, ведь она равна числу гидроксогрупп (ОН). Если формула гидроксида неизвестна, ее придется составить, используя таблицу растворимости.
- Дальше поступаем, как и в предыдущих примерах: надо составить формулу соли, записать уравнение реакции (не забыть про воду!) и подобрать коэффициенты.
Пример: Составьте уравнение реакции, происходящей при пропускании углекислого газа через известковую воду.
- Вспомним, что углекислый газ — это оксид углерода (IV) СО 2 , а известковой водой называется водный раствор гидроксида кальция Са(ОН) 2 .
- Определим, что оксиду углерода (IV) соответствует угольная кислота Н 2 СО з ; ее кислотный остаток СОз (карбонат) имеет валентность II.
- Не представляет труда вывести формулу продукта реакции — карбоната кальция СаСОз.
- Осталось составить уравнение реакции: СаО + СО 2 → СаСОз.
Реакция 4. Основный оксид + вода → основание
Тип реакции — реакция соединения .
Определить идёт ли реакция?
Реакция осуществима, если оксид металла образован элементами из IA и II A групп.
Составить уравнение этой реакции не составит труда, если вы умеете составлять формулы оснований и оксидов.
Пример: Написать уравнение реакции: Н 2 O + Na 2 O → .
Н 2 O + Na 2 O → 2NaOH
Реакция 5. Кислотный оксид + вода → кислота
Тип реакции — реакция соединения .
Определить идёт ли реакция?
Реагируют все оксиды, кроме оксида кремния SiO 2 .
Составление уравнения этой реакции: п о формуле кислотного оксида определить формулу его кислоты, точно так же, как и при составлении реакции 1).
Пример: Написать уравнение реакции: Н 2 O + N 2 О 5 → .
По теме: методические разработки, презентации и конспекты
Предлагаемая презентация с анимационными эффектами и подсказками может помочь восьмикласснику научиться выполнять задания данного вида при изучении темы «Свойства оксидов». Предназначена для.
Предлагаемая презентация с помощью анимационных эффектров и «подсказок» поможет восьмиклассникам закрепить умение выполнять задания данного вида при изучении темы «Химические свойства оснований». През.
Цели:Образовательная: продолжить формирование у учащихся понятия о классификации химических реакций в органической и неорганической химии.Развивающая: развитие аналитического и синтетического мышления.
Технологическая карта урока по химии « Типы химических реакций по числу и составу исходных и полученных веществ.».
Создание условий для репродуктивного усвоения материала, умения сравнивать и анализировать.Организовать деятельность учащихся по изучению классификации химических реакций по количеству исх.
Алгоритм решения задач для обучающихся.
План урока «Классификация химических реакций» содержит цели и задачи изучаемого материала. Описаны основные этапы и методы учебного процесса.
Источник
Конспект уроков химии в технологии деятельностного метода 8 класс «Взаимодействие оксидов неметаллов с водой»; 11 класс «Гидролиз неорганических веществ как пример ионных реакций»
Конспект урока химии в технологии деятельностного метода
Мы предлагаем разработку урока химии в технологии деятельностного метода по теме:
«Взаимодействие оксидов неметаллов с водой». 8 класс
Деятельностная цель : формирование способности учащихся к новому способу действия, применимого как в рамках образовательного процесса, так и при решении проблем в реальных жизненных ситуациях.
Образовательная: научить учащихся, используя алгоритмы составлять уравнения реакций оксидов металлов и оксидов неметаллов с водой. Определять состав и выводить формулы продуктов реакции, определять типы соответствующих реакций.
Воспитательная: развивать у обучающихся научное мировоззрение, на основе химического знания. Развивать умения строго, логично и аргументировано обосновывать ответы и делать соответствующие выводы. Развивать умения анализировать информацию и использовать её для получения нового знания.
Развивающая: развивать у учащихся способности к самостоятельному добыванию знаний, умения выводить и пользоваться соответствующими алгоритмами, общими схемами, применять полученные знания на практике в новых ситуациях и включать их в общую систему знаний
Оборудование: карточки для самостоятельной работы, печатные таблицы и алгоритмы.
Организовать демонстрацию опыта – растворение оксида углерода в водном растворе метилоранжевого и изменение цвета индикатора.
Открыть все тайны вещества учитель нам поможет!
Ведь мир химический так сложен и необъясним!
Ну, вот ответьте мне, мы это с вами можем?
А вот ещё вопрос: мы этого хотим?
Ответы на вопросы:
Актуализация знаний и фиксация затруднения в пробном действии
Источник
Задачи с решениями по оксидам
Типовые задачи с решениями по оксидам
Задача 1
Назвать следующие оксиды:
Решение:
Рекомендую самостоятельно составить подобную задачу и решить ее.
Задача 2
Найти эмпирические формулы следующих оксидов: оксид марганца (IV), оксид ванадия (V), оксид фосфора (V). К какой группе оксидов относится каждый из них?
Решение:
Рекомендую самостоятельно составить подобную задачу и решить ее.
Задача 3
Привести графические формулы следующих оксидов:
Решение:
Графическая формула показывает порядок, в котором атомы соединены в молекуле. В графической формуле единица химической связи (валентности) изображается черточкой:
Рекомендую самостоятельно составить подобную задачу и решить ее.
Задача 4
К каким типам относятся следующие оксиды: 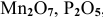
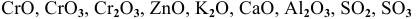
Решение:
К основным оксидам относятся оксиды металлов с ярко выраженными металлическими свойствами, проявляющими низкие валентности, в основном I и II:
К амфотерным оксидам относятся оксиды металлов со слабо выраженными металлическими свойствами. Обычно эти металлы находятся в каждом периоде на границе между неметаллами и металлами с ярко выраженными металлическими свойствами:
К кислотным оксидам относятся оксиды неметаллов, а также оксиды металлов, проявляющих высокие валентности, в основном V, VI, VII: 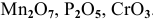
Рекомендую самостоятельно составить подобную задачу и решить ее.
Задача 5
Составить уравнения следующих химических реакций:
Решение:
Рекомендую самостоятельно составить подобную задачу и решить ее.
Задача 6
Какие из перечисленных оксидов будут взаимодействовать с водой: 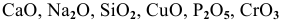
Решение:
С водой взаимодействуют кислотные оксиды, за исключением 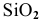
оксид щелочного или щелочно-земельного металла + 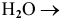
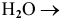
Рекомендую самостоятельно составить подобную задачу и решить ее.
Задача 7
Какие из оксидов будут реагировать попарно: 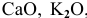
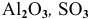
Решение:
Рекомендую самостоятельно составить подобную задачу и решить ее.
Задача 8
Как можно получить следующие оксиды: 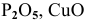
Решение:
Эти задачи взяты со страницы решения задач по неорганической химии:
Возможно эти страницы вам будут полезны:





















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Источник