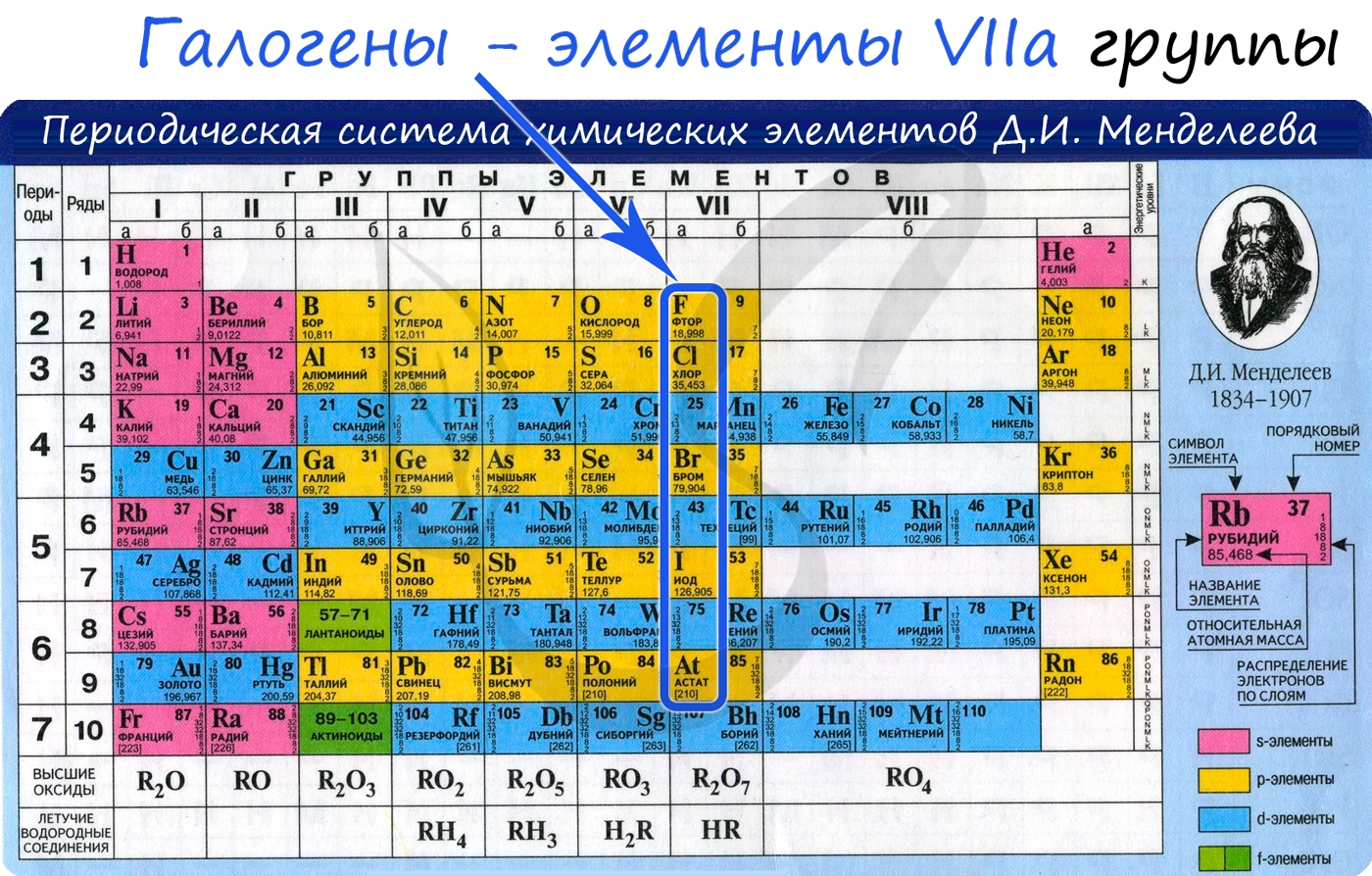
Галогены
Галогены (греч. hals — соль + genes — рождающий) — химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.
Общая характеристика элементов VIIa группы
От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 5 :
- F — 2s 2 2p 5
- Cl — 3s 2 3p 5
- Br — 4s 2 4p 5
- I — 5s 2 5p 5
- At — 6s 2 6p 5
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов в возбужденном состоянии.
Природные соединения
- NaCl — галит (каменная соль)
- CaF2 — флюорит, плавиковый шпат
- NaCl*KCl — сильвинит
- 3Ca3(PO4)2*CaF2 — фторапатит
- MgCl2*6H2O — бишофит
- KCl*MgCl2*6H2O — карналлит
Простые вещества — F2, Cl2, Br2, I2
Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают электролизом водного раствора хлорида натрия.
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте — HF — был впервые получен фтор.
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.
В лабораторных условиях галогены могут быть получены следующими реакциями.
- Реакции с металлами
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере фтора самовоспламеняются.
Реакции с неметаллами
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.
F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность 😉
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром — F — )
Br2 + I2 → IBr3 (бром более электроотрицателен, чем йод — Br — )
Реакции с водой
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
Хлор реагирует с водой обратимо, образуя хлорную воду — смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.
Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами — только при нагревании.
Реакции с щелочами
Cl2 + NaOH → NaCl + NaClO + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Галогеноводороды
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF — фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl — хлороводород (газ), соляная кислота (жидкость)
- HBr — бромоводород, бромоводородная кислота
- HI — йодоводород, йодоводородная кислота
- HAt — астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI — газы, хорошо растворимые в воде.
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
HF — является слабой кислотой, HCl, HBr, HI — сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
KOH + HCl → KCl + H2O (реакция нейтрализации)
Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.
В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с плавиковой кислотой.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Как взаимодействует фтор с водой
Взаимодействие с металлами. 
Галогены в этой реакции проявляют окислительные свойства.
Взаимодействие с водородом.При обычных условиях фтор реагирует с водородом в темноте со взрывом, взаимодействие с хлором протекает на свету, бром и йод реагируют только при нагревании, причем реакция с йодом обратима.
Галогены в этой реакции проявляют окислительные свойства.
Взаимодействие с неметаллами. С кислородом и азотом галогены непосредственно не взаимодействуют, реагируют с серой, фосфором, кремнием, проявляя окислительные свойства, химическая активность у брома и йода выражена слабее, чем у фтора и хлора:
Взаимодействие с водой. Галогены реагируют со многими сложными веществами. С водой фтор и остальные галогены реагируют по-разному:
Hal + H2O = HHal + HHalO.
Эта реакции является реакцией диспропорционирования, где галоген одновременно является окислителем и восстановителем.
Взаимодействие со щелочами. Также галогены диспропорционируют в растворах щелочей:
Cl2 + KOH = KClO + KCl (на холоде);
3Cl2 + 6KOH = KClO3 + 5KCl + 3Н2О (при нагревании).
Гипобромид-ион существует только при температуре ниже 0 °С, гипойодит-ион в растворах не существует.
Взаимодействие с сероводородом. Галогены способны отнимать водород от других веществ:
Реакция замещения водорода в предельных углеводородах:
Реакция присоединения к непредельным углеводородам:
Взаимное замещение галогенов. 
Источник
Химические свойства фтора
Большая энергия связей между атомом фтора и атомами других элементов является следствием большой электроотрицательности фтора и маленьким размером его атома. Благодаря малой энергии связи молекула фтора легко диссоциирует на атомы и энергия активации реакций со фтором обычно не велика, поэтому процессы с участием фтора протекают очень быстро.
Для фтора характерно:
1. Отсутствие положительных степеней окисления в соединениях с другими элементами.
2. Чрезвычайно низкая энергия активации реакций.
3. Большое выделение энергии при переходе молекулы фтора в анионы F – .
4. Стремление максимально использовать валентные электроны партнеров. Именно в соединениях со фтором реализуются высшие степени окисления многих элементов: BiF5, SF6, IF7, OsF7, CuF3 и др.
Итак, фтор – сильнейший окислитель. По образному выражению академика А. Е. Ферсмана его можно назвать “всесъедающим”.
Щелочные металлы, свинец, железо и большинство порошков других металлов загораются в атмосфере фтора при комнатной температуре. На некоторые металлы (алюминий, железо, никель, медь, цинк, марганец, магний) фтор на холоде не действует из-за образования поверхностной пленки фторидов, защищающей металл от дальнейшего взаимодействия. Поэтому сплавы этих металлов или никеля используют для хранения фтора. Однако при нагревании фтор реагирует со всеми металлами, в т.ч. с золотом и платиной.
Со многими неметаллами (водород, йод, бром, сера, фосфор, мышьяк, сурьма, углерод, кремний, бор) фтор взаимодействует на холоде; реакции протекают со взрывом или с образованием пламени.
С серой, фосфором и сурьмой фтор взаимодействует даже при температуре жидкого воздуха (-190 °C):
С водородом фтор взаимодействует уже при температуре -252 °C
Криптон взаимодействует с фтором под действием электрического разряда, а ксенон горит в атмосфере фтора ярким пламенем.
С кислородом фтор реагирует при низких тепературах в электрических разрядах с образованием эндотермических фторидов кислорода. O2 + F2 = O2F2, -190 °C, электрич. разряд.
При нагревании с фтором реагирует хлор с образованием ClF и ClF3. Бром и йод при взаимодействии с фтором образуют следующие соединения: BrF, BrF3, BrF5, IF, IF3, IF5, IF7.
При нагревании фтор вступает в реакцию и с азотом:
Непосредственно фтор не реагирует только с углеродом (в виде алмаза), гелием, неоном и аргоном.
В реакциях с фтором в роли восстановителей выступают такие вещества как азотная и серная кислоты:
Под действием фтора разлагается вода:
0 °C: H2O(тв) + F2 = HF + HOF (фтороксигенат водорода)
В атмосфере фтора горят такие стойкие вещества, как стекло (в виде ваты), асбест, кварц:
Катализатором этой реакции является вода. С совершенно сухим кварцем или стеклом фтор не взаимодействует.
Источник
Насколько опасен фтор в воде
На уроках химии все мы изучали периодическую таблицу Менделеева. Одним из элементов в этой большой и сложной таблице под номером 9 был фтор. Много ли Вы знаете о нем?
Мы контактируем с этим интересным элементом каждое утро и вечер, когда чистим зубы, а также едим яблоки, рыбу, морепродукты, пьем молоко и чай. Фтор участвует в формировании костей, для усваивания железа, влияет на здоровье волос и ногтей. Казалось бы, чем больше фтора, тем крепче кости, тем белее зубы и длиннее волосы.
А вы знаете, что с древнегреческого языка «фтор» переводится как вред, разрушение. Недостаток, также как и переизбыток фтора, негативно влияет на наш организм, появляется усталость, тошнота, головные боли, снижается иммунитет. Основным источником поступления фтора в организм в больших количествах является фторированная вода.
Полезна ли фторированная вода, давайте взвесим все «за» и «против».
Фтор приносит пользу только тогда, когда его количество находится на оптимальном уровне. Суточная норма фтора в организме составляет 2-3 мг для взрослого человека.
Плюсы пить фторированную воду:
1. Оптимальное количество фтора укрепляет зубы, предотвращает кариес.
2. Повышается иммунная система, человек реже болеет и легче переносит вирусные заболевания.
3. Костный скелет становится крепче, лучше растут волосы и ногти. Снижается риск нарушения осанки.
4. Фтор участвует в кровеносной системе. Благодаря ему образуются лейкоциты, быстрее заживают раны.
Еще ученые в древнем Риме утверждали: «Все есть яд и все есть лекарство, одна лишь доза определяет, будет ли яд лекарством, или лекарство ядом». Недостаток фтора также как и их переизбыток, приводит к серьезным заболеваниям. Поэтому в России и других странах мира строго регламентируется норма фтора, которая может содержаться в питьевой воде. По нормам ВОЗ содержание фтора не должно превышать 1,5 мг/л.
Минусы пить воду со фтором:
1. Избыток фтора приводит к такому заболеванию как флюороз (меняется форма зубов и цвет, зубы начинают чернеть и разрушаться).
2. Переизбыток фтора также влияет на структуру костей и суставов. Фтор в концентрациях больше или меньше нормы приводит к разрушению нашего скелета.
3. Фтор влияет на мозговую деятельность. Исследования показывают, что чем больше фтора в организме, тем меньше его IQ.
4. Фторированная вода является причиной заболевания щитовидной железы.
5. Последние исследования ученых выявили: чем больше фтора накапливается в организме мужской половины человечества, тем выше у них бесплодие.
Каждый год ученые проводят эксперименты и делают все новые и новые выводы. Кто знает, что они откроют через 5 лет? Зачем рисковать и надеяться, что фторированная вода не повлияет на нас и наше здоровье.
Мы советуем внимательно относиться к вопросам вашего здоровья, пить только очищенную воду и регулярно проверяться у врачей.
Источник