- ЛЁГКАЯ, КАК ВОЗДУХ, ЖИДКАЯ, КАК ВОДА
- Как рыба в воде. Может ли человек дышать жидкостью и зачем это нужно
- Основные агрегатные состояния вещества
- Агрегатные состояния вещества
- Твердое состояние
- Жидкое состояние
- Газообразное состояние
- Фазовые переходы: изменение агрегатных состояний вещества
- График фазовых переходов
- Решение задач по фазовым переходам
- Сублимация и десублимация
- Влажность воздуха: испарение и конденсация
- Как влажность влияет на человека
ЛЁГКАЯ, КАК ВОЗДУХ, ЖИДКАЯ, КАК ВОДА
Кандидат химических наук А. ЕФРЕМКИН.
Проведём простой опыт: возьмём пластиковую бутылку, нальём в неё немного чистой воды, закроем крышкой и встряхнём. На поверхности воды появится множество пузырьков, но буквально через несколько мгновений они исчезнут. А теперь добавим в бутылку чуть-чуть мыла (можно взять жидкость для мытья посуды), снова закроем крышкой и энергично взболтаем содержимое. Воздушная, переливающаяся всеми цветами радуги пена заполнит бутылку доверху. И вам придётся долго ждать, пока она осядет.
Что же такое содержится в мыле, что влияет на способность воды образовывать пену?
Давайте для начала рассмотрим, как устроена молекула мыла.
Она, подобно мифологическому Кентавру, состоит из двух частей с совершенно разными свойствами. «Голова» молекулы взята у гидрофильного вещества, то есть такого, которое любит воду (слово «гидрофильный» происходит от греческих слов ύδωρ — читается «хидор» —вода и φιλία — читается «филиа»—любовь). Длинный хвостик в молекуле мыла позаимствован у жира. Жиры воды «боятся» и не растворяются в ней, поэтому их называют гидрофобными (от греческого слова φόβoς — читается «фобос» — страх).
Когда такие молекулы попадают в воду, они выстраиваются вдоль границы, разделяющей воду и воздух таким образом, что водолюбивые «головы» погружены в воду, а водобоязливые «хвостики» торчат в воздух. Получается, что поверхность воды покрыта тончайшей мыльной плёнкой.
Мыло называют поверхностно-активным веществом. Оно снижает поверхностное натяжение воды, то есть ослабляет силы, притягивающие молекулы поверхностного слоя друг к другу. Именно из-за высокого поверхностного натяжения чистой воды из неё не удаётся получить устойчивую пену: пузыри почти мгновенно «схлопываются» в капли. Мыло поразительным образом меняет картину: даже небольшое его количество уменьшает поверхностное натяжение почти втрое!
Когда мы встряхиваем бутылку с мыльным раствором, пузырьки воздуха как бы обволакиваются слоем молекул мыла. Мыльные пузыри поднимаются на поверхность, соприкасаются друг с другом — и вот уже образовалась пена: лёгкая, ячеистая структура из множества многогранников.
В XIX веке изучением строения мыльной пены всерьёз увлёкся бельгийский учёный Жозеф Плато. Он первым обратил внимание на то, что в каждом ребре, разделяющем пенные многогранники, всегда сходятся три плёнки, ни больше и ни меньше. Оказалось, что сами плёнки — двойные, а рёбра между ними — это каналы, заполненные жидкостью. Пена оседает, потому что вода понемногу стекает по каналам вниз.
Ж. Плато нашёл способ поставить мыльные плёнки на службу математике. Он опускал в мыльный раствор проволочные рамки различной конфигурации и наблюдал, какую форму принимает мыльная плёнка. Эти опыты способствовали развитию пространственной геометрии (стереометрии). Заметим, что из-за поверхностного натяжения площадь мыльной плёнки стремится к минимуму. Поэтому мыльные пузыри, выдуванием которых увлекаются и дети и взрослые, имеют почти идеальную сферическую форму.
Пена состоит из множества пузырей, которые соприкасаются друг с другом. Наиболее выгодной формой мыльного пузыря в составе пены с точки зрения минимизации поверхностного натяжения оказался додекаэдр. Он напоминает угловатый шар, образованный из 12 соединённых гранями пятиугольников.
ЧТО УМЕЕТ ДЕЛАТЬ ПЕНА
Прежде всего, мыльная пена — отличное средство для очистки поверхностей от грязи. Частички грязи, содержащие жир, водой не смачиваются. Попробуйте отмыть испачканные чем-то жирным руки просто тёплой водой. Результат, скорее всего, будет неудовлетворительным. А если руки как следует намылить, молекулы мыла прилипнут своими гидрофобными «хвостами» к молекулам жира и образуют вокруг частичек грязи тонкую оболочку из мыльной плёнки. После этого грязь легко оторвётся от кожи и смоется водой.
У обычного мыла, сделанного из натурального жира и щёлочи, есть один существенный недостаток: оно плохо мылится в жёсткой воде. Поэтому жидкости для мытья посуды, стиральные порошки, шампуни и другие средства бытовой химии сейчас делают на основе синтетических поверхностно-активных веществ, которым жёсткая вода нипочём.
Мыльная пена освоила и другие «профессии». Например, её используют при добыче минеральной руды, чтобы отделить полезный минерал от пустой породы. Такой метод называют флотацией. Пену применяют при бурении скважин, при тушении пожаров, для удаления разлившейся нефти.
Пену создаёт не только мыло. Поверхностно-активными свойствами обладают и другие вещества, в том числе белки. Например, взбитые сливки сохраняют воздушную структуру благодаря белкам молока.
ОПЫТ С ПОВЕРХНОСТНЫМ НАТЯЖЕНИЕМ
Наполним стакан водой до краёв. Аккуратно добавим сверху ещё несколько капель воды. Её уровень поднимется чуть выше краёв стакана, но вода не выльется, словно удерживаемая тонкой плёнкой. Откуда берётся эта плёнка? Её создают молекулы воды, расположенные на поверхности, на границе с воздухом. Они более прочно связаны друг с другом, чем молекулы в толще воды, потому что силы, действующие на них сверху, со стороны воздуха, гораздо слабее сил, действующих на них снизу.
Поверхностная плёнка настолько прочна, что может выдержать вес небольшого металлического предмета, например иголки или канцелярской скрепки.
Осторожно опустите скрепку на поверхность воды. Она будет плавать до тех пор, пока вода не смочит металл. Для удобства можно положить скрепку на полоску рыхлой бумаги, вырезанную, скажем, из бумажного полотенца. Бумага намокнет и опустится на дно, а скрепка останется на поверхности. Чтобы опыт получился, скрепка обязательно должна быть сухой. А если её смазать жиром — результат гарантирован.
С поверхностным натяжением связаны явления смачивания и подъёма жидкости по тонким трубкам — капиллярам.
Из всех жидкостей самое большое поверхностное натяжение у ртути, поэтому маленькие капли ртути имеют форму почти идеальных шариков.
Источник
Как рыба в воде. Может ли человек дышать жидкостью и зачем это нужно
Недавно Научно-технический совет государственного Фонда перспективных исследований одобрил «проект по созданию технологии спасения подводников свободным всплытием с использованием метода жидкостного дыхания», реализацией которого должен заняться московский Институт медицины труда (на момент написания статьи руководство института было недоступно для комментариев). «Чердак» решил разобраться, что скрывается за таинственным словосочетанием «жидкостное дыхание».
Наиболее впечатляюще жидкостное дыхание показано в фильме Джеймса Кэмерона «Бездна».
Правда, в таком виде опыты на людях еще никогда не проводились. Но в целом ученые не сильно уступают Кэмерону по части исследования этого вопроса.
Первым, кто показал, что млекопитающие в принципе могут получать кислород не из смеси газов, а из жидкости, был Йоханнес Килстра (Johannes Kylstra) из медицинского центра университета Дьюка (США). Вместе с коллегами он в 1962 году опубликовал работу «Мыши как рыбы» (Of mice as fish) в журнале Transactions of American Society for Artificial Internal Organs.
Килстра и его коллеги погружали мышей в физраствор. Чтобы растворить в нем достаточное для дыхания количество кислорода, исследователями «вгоняли» газ в жидкость под давлением до 160 атмосфер — как на глубине 1,5 километра. Мыши в этих экспериментах выживали, но не очень долго: кислорода в жидкости было достаточно, а вот сам процесс дыхания, втягивания и выталкивания жидкости из легких требовал слишком больших усилий.
Стало понятно, что нужно подобрать такую жидкость, в которой кислород будет растворяться намного лучше, чем в воде. Требуемыми свойствами обладали два типа жидкостей: силиконовые масла и жидкие перфторуглероды. После экспериментов Леланда Кларка (Leland Clark), биохимика из медицинской школы университета Алабамы, в середине 1960-х годов выяснилось, что оба типа жидкостей можно использовать для доставки кислорода в легкие. В опытах мышей и кошек полностью погружали и в перфторуглероды, и в силиконовые масла. Однако последние оказались токсичны — подопытные звери погибали вскоре после эксперимента. А вот перфторуглероды оказались вполне пригодны для использования.
Перфторуглероды были впервые синтезированы в ходе Манхэттенского проекта по созданию атомной бомбы: ученые искали вещества, которые бы не разрушались при взаимодействии с соединениями урана, и они проходили под кодовым названием «вещества Джо» (Joe’s stuff). Для жидкостного дыхания они подходят очень хорошо: «вещества Джо» не взаимодействуют с живыми тканями и прекрасно растворяют газы, в том числе кислород и углекислый газ при атмосферном давлении и нормальной температуре человеческого тела.
Килстра и его коллеги исследовали технологию жидкостного дыхания в поисках технологии, которая бы позволяла людям погружаться и всплывать на поверхность, не опасаясь развития кессонной болезни. Быстрый подъем с большой глубины с запасом сжатого газа очень опасен: газы лучше растворяются в жидкостях под давлением, поэтому по мере того, как водолаз всплывает, растворенные в крови газы, в частности азот, образуют пузырьки, которые повреждают кровеносные сосуды. Результат может быть печальным, вплоть до смертельного.
В 1977 году Килстра представил в Военно-морское министерство США заключение, в котором писал, что, по его расчетам, здоровый человек может получать необходимое количество кислорода при использовании перфторуглеродов, и, соответственно, их потенциально возможно использовать вместо сжатого газа. Ученый указывал, что такая возможность открывает новые перспективы для спасения подводников с больших глубин.
Эксперименты на людях
На практике техника жидкостного дыхания, к тому времени получившая название жидкостной вентиляции легких, была применена на людях всего один раз, в 1989 году. Тогда Томас Шаффер (Thomas Shaffer), педиатр из медицинской школы Темпльского университета (США), и его коллеги использовали этот метод для спасения недоношенных младенцев. Легкие зародыша в утробе матери заполнены жидкостью, а когда человек рождается и начинает дышать воздухом, тканям легких на протяжении всей оставшейся жизни не дает слипаться смесь веществ, называемая легочным сурфактантом. У недоношенных младенцев он не успевает накопиться в нужном количестве, и дыхание требует очень больших усилий, что чревато летальным исходом. В тот раз, правда, жидкостная вентиляция младенцев не спасла: все трое пациентов вскоре умерли, однако этот печальный факт был отнесен на счет других причин, а не на счет несовершенства метода.
Больше экспериментов по тотальной жидкостной вентиляции легких, как эта технология называется по-научному, на людях не проводилось. Однако в 1990-х годах исследователи модифицировали метод и проводили на пациентах с тяжелым воспалительным поражением легких эксперименты по частичной жидкостной вентиляции, при которой легкие заполняются жидкостью не полностью. Первые результаты выглядели обнадеживающими, но в конечном счете до клинического применения дело не дошло — оказалось, что обычная вентиляция легких воздухом работает не хуже.
Патент на фантастику
В настоящее время исследователи вернулись к идее использования полной жидкостной вентиляции легких. Однако фантастическая картина водолазного костюма, в котором человек будет дышать жидкостью вместо специальной смеси газов, далека от реальности, хотя и будоражит воображение публики и умы изобретателей.
Так, в 2008 году отошедший от дел американский хирург Арнольд Ланде (Arnold Lande) запатентовал водолазный костюм с использованием технологии жидкостной вентиляции. Вместо сжатого газа он предложил использовать перфторуглероды, а избыток углекислоты, которая будет образовываться в крови, выводить при помощи искусственных жабр, «воткнутых» прямо в бедренную вену водолаза. Изобретение получило некоторую известность после того, как о нем написало издание The Inpependent.
Как считает специалист по жидкостной вентиляции из Шербрукского университета в Канаде Филипп Мишо (Philippe Micheau), проект Ланде выглядит сомнительным. «В наших экспериментах (Мишо и его коллеги проводят эксперименты на ягнятах и крольчатах со здоровыми и поврежденными легкими — прим. «Чердака») по тотальному жидкостному дыханию животные находятся под анестезией и не двигаются. Поэтому мы можем организовать нормальный газообмен: доставку кислорода и удаление углекислого газа. Для людей при физической нагрузке, такой как плавание и ныряние, доставка кислорода и удаление углекислоты будут проблемой, так как выработка углекислоты в таких условиях выше нормы», — прокомментировал Мишо. Ученый также отметил, что технология закрепления «искусственных жабр» в бедренной вене ему неизвестна.
Главная проблема «жидкостного дыхания»
Более того, Мишо считает саму идею «жидкостного дыхания» сомнительной, поскольку для «дыхания» жидкостью человеческая мускулатура не приспособлена, а эффективная система насосов, которая бы помогала закачивать и выкачивать жидкость из легких человека, когда он двигается и выполняет какую-то работу, до сих пор не разработана.
«Я должен заключить, что на современном этапе развития технологий невозможно разработать водолазный костюм, используя метод жидкостной вентиляции», — считает исследователь.
Однако применение этой технологии продолжает исследоваться для других, более реалистичных целей. Например, для помощи утонувшим, промывания легких при различных заболеваниях или быстрого понижения температуры тела (применяется в случаях реанимации при остановке сердца у взрослых и новорожденных с гипоксически-ишемическим поражением мозга).
Екатерина Боровикова
Источник
Основные агрегатные состояния вещества
О чем эта статья:
Агрегатные состояния вещества
Чтобы разобраться с тем, какими бывают агрегатные состояния, предлагаю по ходу чтения статьи заполнять таблицу.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
Лед, вода и водяной пар — это все три агрегатных состояния одного вещества. Лед — твердое состояние, вода — жидкая, пар — газообразное. Для каждого вещества существует три состояния.
Твердое состояние
Его очень легко представить — это любой предмет, который мы встречаем в жизни. В этом состоянии тело сохраняет форму и объем. Расстояние между молекулами, приблизительно равно размеру самих молекул, которые, в свою очередь, расположены очень структурированно.
Такая структура называется кристаллической решеткой — из-за четкой структуры молекулам сложно двигаться, и они просто колеблются около своих положений.
Заполняем нашу табличку
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
Жидкое состояние
В этом состоянии сохраняется объем, но не сохраняется форма. Например, если перелить молоко из кувшина в стакан, то молоко, имевшее форму кувшина, примет форму стакана. Кстати, в корове у молока тоже была другая форма.

Расстояние между молекулами в жидком состоянии чуть больше, чем в твердом, но все равно невелико. При этом частицы не собраны в кристаллическую решетку, а расположены хаотично. Молекулы почти не двигаются, но при нагревании жидкости делают это более охотно.
Вспомните, что происходит, если залить чайный пакетик холодной водой — он почти не заваривается. А вот если налить кипяточку — чай точно будет готов.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
Газообразное состояние
В жизни мы встречаем газообразное состояние вещества, когда чувствуем запахи. Запах очень легко распространяется, потому что газ не имеет ни формы, ни объема (он занимает весь предоставленный ему объем), состоит из хаотично движущихся молекул, расстояние между которыми больше, чем размеры молекул.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
занимают предоставленный объем
больше размеров молекул
хаотичное и непрерывное
С агрегатными состояниями разобрались, ура! Но до сих пор неясно, каким образом у каждого вещества их целых три, и как одно переходит в другое. Для этого узнаем, что такое фазовые переходы.
Фазовые переходы: изменение агрегатных состояний вещества
При изменении внешних условий (например, если внутренняя энергия тела увеличивается или уменьшается в результате нагревания или охлаждения) могут происходить фазовые переходы — изменения агрегатных состояний вещества.
Фазовые переходы интересны тем, что все живое не Земле существует лишь благодаря тому, что вода умеет превращаться в лед или пар. С кристаллизацией, плавлением, парообразованием и конденсацией связаны многие процессы металлургии и микроэлектроники.
На схеме — названия всех фазовых переходов:

Переход из твердого состояния в жидкое — плавление;
Переход из жидкого состояния в твердое — кристаллизация;
Переход из газообразного состояния в жидкое — конденсация;
Переход из жидкого состояния в газообразное — парообразование;
Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
График фазовых переходов
Если взять процесс превращения льда в воду, воды — в пар, и обратные действия, то мы получим очень информативный график.
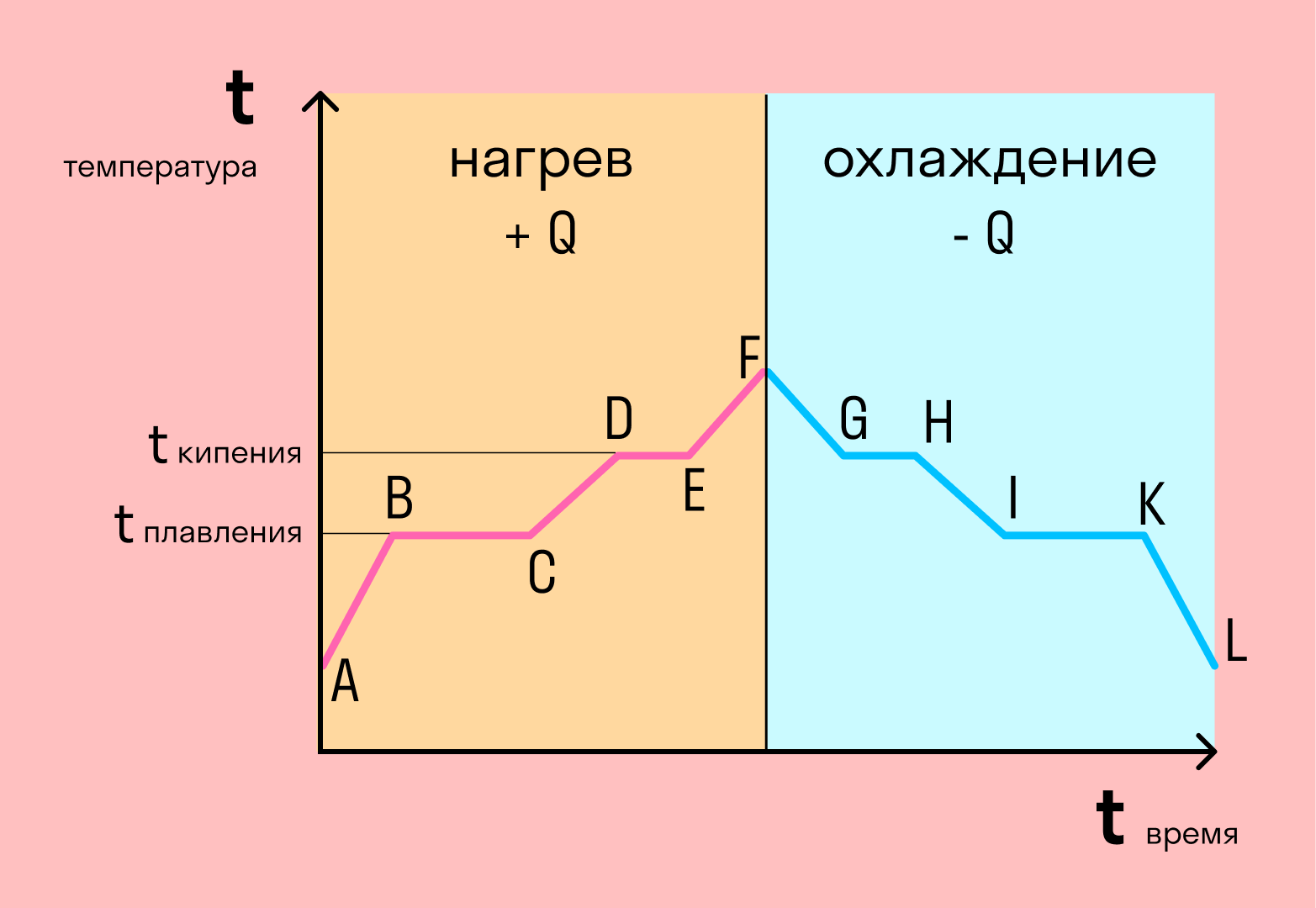
Разбираемся по шагам. Сначала взяли лед, конечно, при отрицательной температуре, потому что при нуле лед начинает плавиться. Нагрели лед до температуры плавления (до 0 градусов).
- AB — нагревание льда
После того, как лед нагрелся до температуры плавления, он начинает плавиться. Плавление происходит при постоянной температуре тем дольше длится, чем больше масса плавящегося вещества. Еще этот процесс зависит от свойств самого вещества, но об этом немного позже.
- BC — плавление льда
Расправившись вещество уже в жидком состоянии снова начинает нагреваться, и температура увеличивается, пока не достигает температуры кипения. В данном случае нагревается вода — это значит, что ее температура кипения равна 100 градусам Цельсия.
- CD — нагревание воды
При 100 градусах вода кипит, пока не выкипит целиком. В данном случае процесс аналогично плавлению происходит при постоянной температуре. Данный процесс нельзя путать с испарением, потому что парообразование происходит при конкретной температуре, а испарение — при любой.
- DE — кипение (парообразование) воды
Далее полученный пар нагревается, но путем нагревания невозможно дойти до другого фазового перехода — можно пойти только обратно.
- EF — нагревание пара
Первый шаг в обратную сторону — охлаждение до температуры кипения.
- FG — охлаждение пара
Дойдя до температуры кипения (в данном случае 100 градусов), пар начинает переходить в жидкое состояние. Этот процесс также происходит при постоянной температуре.
- GH — конденсация пара
Сконденсировавшись, вода охлаждается, пока не начнет замерзать.
- HI — охлаждение воды
Кристаллизуется (замерзает) вода при той же температуре, что и плавится лед — 0 градусов. Кристаллизация также происходит при постоянной температуре.
- IK — кристаллизация воды
После кристаллизации лед охлаждается.
- KL — охлаждение льда
С нагреванием и охлаждением все совсем просто — мы либо передаем теплоту телу (веществу), и оно идет на увеличение температуры, либо тело отдает тепло и охлаждается.
В остальных процессах температура не меняется. Это связано с тем, что количество теплоты не всегда зависит от температуры. Формулы для всех процессов выглядят так:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
m — масса [кг]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Плавление
Кристаллизация
Q — количество теплоты [Дж]
λ — удельная теплота плавления вещества [Дж/кг]
m — масса [кг]
Парообразование
Конденсация
Q — количество теплоты [Дж]
L — удельная теплота парообразования вещества [Дж/кг]
m — масса [кг]
Решение задач по фазовым переходам
С теорией разобрались — а теперь давайте практиковаться!
Задачка раз. Температура медного образца массой 100 г повысилась с 20 °С до 60 °С. Какое количество теплоты получил образец? Удельную теплоёмкость меди считать равной 380 Дж/(кг умножить на °С)
Сначала нужно перевести массу в килограммы:
Берем формулу количества теплоты для нагревания вещества:
Q = 380 * 0,1*(60-20) = 1520 Дж
Ответ: образец получил 1520 Дж
Задачка два. Какое количество теплоты необходимо для плавления 2,5 т стали, взятой при температуре плавления? Удельная теплота плавления стали λ=80кДж/кг. Теплопотерями пренебречь.
Сначала нужно перевести массу в килограммы и удельную теплоту в Дж/кг:
80 кДж/кг = 80000 Дж/кг
Берем формулу количества теплоты для плавления вещества:
Q = 80000*2500 = 200 000 000 Дж = 200 МДж
Ответ: для плавления 2,5 т стали необходимо 200 МДж теплоты.
Сублимация и десублимация
Мы уже рассказали про такие процессы, как сублимация и десублимация.
- Переход из твердого состояния в газообразное, минуя жидкое — сублимация (возгонка);
- Переход из газообразного состояния в твердое, минуя жидкое — десублимация.





