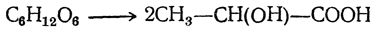Амины
Амины — органические соединения, продукты замещения атомов водорода в аммиаке NH3 различными углеводородными радикалами. Функциональная группой аминов является аминогруппа — NH2.
Классификация аминов
По числу углеводородных радикалов амины подразделяются на первичные, вторичные и третичные.
Запомните, что основные свойства аминов выражены тем сильнее, чем больше электронной плотности присутствует на атоме азота. Однако, у третичных аминов три углеводородных радикала создают значительные затруднения для химических реакций.
Таким образом, у третичных аминов основные свойства выражены слабее, чем у вторичных аминов. Основные свойства возрастают в ряду: третичные амины (слабые основные свойства) → первичные амины → вторичные амины (основные свойства хорошо выражены).
Номенклатура и изомерия аминов
Названия аминов формируются путем добавления суффикса «амин» к названию соответствующего углеводородного радикала: метиламин, этиламин, пропиламин, изопропиламин, бутиламин и т.д. В случае если радикалов несколько, их перечисляют в алфавитном порядке.
Общая формула предельных аминов CnH2n+3N. Атомы углерода находятся в sp3 гибридизации.
Для аминов характерна структурная изомерия: углеродного скелета, положения функциональной группы и изомерия аминогруппы.
Получение
- Нагревание галогеналканов с аммиаком
В основе этой реакции лежит замещение атома галогена в галогеналканах на аминогруппу, при этом образуются амин и соль аммония.
При такой реакции нитрогруппа превращается в аминогруппу, образуется вода.
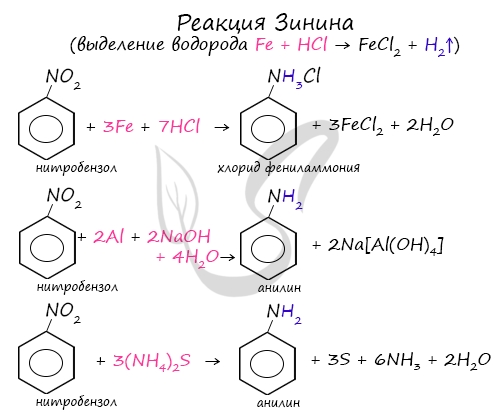
Знаменитой является предложенная в 1842 году Н.Н. Зининым реакция получения аминов восстановления ароматических нитросоединений (анилина и других). Она возможна в нескольких вариантах, главное, чтобы в начале реакции выделился водород.
Реакция сопровождается разрушением карбонильной группы и отщеплении ее от молекулы амида в виде воды.
Этим способом в промышленности получают гексаметилендиамин, используемый в изготовлении волокна — нейлон.
В промышленности амины получают реакцией аммиака со спиртами, в ходе которой происходит замещение гидроксогруппы на аминогруппу.
В ходе реакции галогеналканов с аммиаком, аминами, становится возможным получение первичных, вторичных и третичных аминов.
Химические свойства аминов
Как и аммиак, амины обладают основными свойствами, их растворы окрашивают лакмусовую бумажку в синий цвет.
В реакции с водой амины образуют гидроксиды алкиламмония, которые аналогичны гидроксиду аммония. Анилин с водой не реагирует, так как является слабым основанием.
Как основания, амины вступают в реакции с различными кислотами и образуют соли алкиламмония.
Данная реакция помогает различить первичные, вторичные и третичные амины, которые по-разному с ней взаимодействуют.
При конденсации первичных аминов с альдегидами и кетонами получают основания Шиффа, соединения, которые содержат фрагмент «N=C».
Соли аминов легко разлагаются щелочами (растворимыми основаниями). В результате образуется исходный амин, соль кислоты и вода.
При горении аминов азот чаще всего выделяется в молекулярном виде, так как для реакции азота с кислородом необходима очень высокая температура. Выделение углекислого газа и воды обыкновенно при горении органических веществ.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Молочная кислота
Молочная кислота СН3—СН(ОН)—СООН (α-оксипропионовая, этилиденмолочная) содержит асимметрический атом углерода и поэтому может существовать, в оптически изомерных формах.
Молочная кислота может быть получена различными синтетическими способами, но при всех этих синтезах кислота получается в виде оптически недеятельной, т. е. всегда получаются равные количества правого и левого изомеров. То же наблюдается и во всех других случаях, когда путем синтетических реакций получаются вещества, содержащие асимметрический атом углерода.
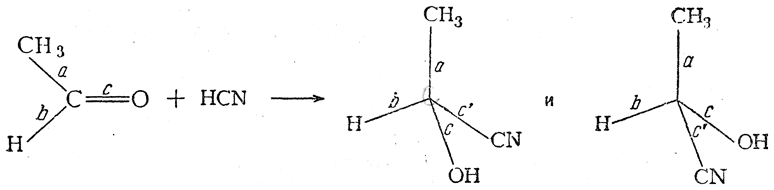
Причина обязательного образования оптически недеятельных соединений при синтетических реакциях может быть показана на следующих примерах:
Как видно из приведенной схемы, при действии цианистоводородной кислоты на уксусный альдегид анион CN – может атаковать π-связь карбонильной группы равновероятно как с одной, так и с другой стороны плоскости, в которой расположены σ-связи а, b и с молекулы кетона. В результате должны образоваться равные количества оптически изомерных молекул оксинитрилов.
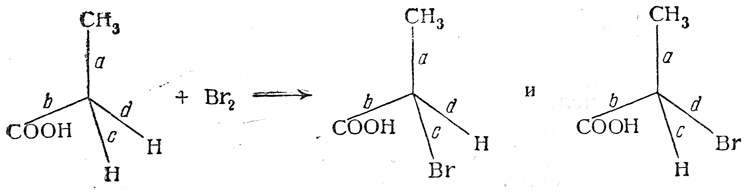
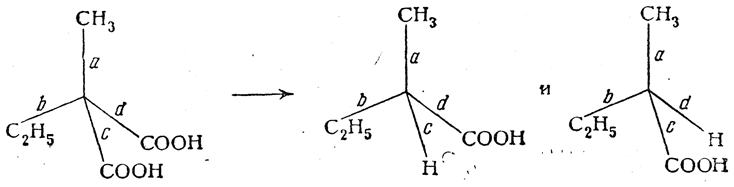
Точно так же в тех случаях, когда асимметрический атом углерода появляется в результате реакций замещения
вероятности образования молекул оптических антиподов совершенно одинаковы, что и должно вести к образованию оптически недеятельных смесей или рацемических соединений.
Значительные количества молочной кислоты образуются при действии щелочей на водные растворы простейших сахаристых веществ (моноз). Так, например, из смеси глюкозы и фруктозы («инвертный» сахар) можно получить до 60% молочной кислоты. И в этом случае образуется недеятельная молочная кислота.
Наиболее важным источником получения молочной кислоты является процесс молочнокислого брожения, которому легко подвергаются растворы многих сахаристых веществ (молочного сахара, тростникового сахара, виноградного сахара и др.). Брожение является результатом жизнедеятельности бактерий молочнокислого брожения, зародыши которых всегда находятся в воздухе. Протеканием этого процесса и объясняется наличие молочной кислоты в кислом молоке, откуда она была впервые выделена Шееле (1780). Молочнокислое брожение сахарных растворов лучше всего протекает под действием чистых культур молочнокислых бактерий (Bacillus Delbrückii) при температуре 34—45° С, с добавкой необходимых для жизни бактерий минеральных веществ, а также мела или карбоната цинка. Последние добавки вводятся для нейтрализации свободной кислоты, так как при сколько-нибудь значительной концентрации кислоты бактерии погибают и брожение прекращается.
Молочнокислое брожение является одним из процессов, протекающих при изготовлении масла (из скисшего молока), при созревании сыра, квашении капусты, при силосовании кормов и пр. Уравнение процесса молочнокислого брожения имеет вид:
Для молочнокислого брожения, как и для спиртового, доказано существование особого энзима, зимазы молочнокислого брожения, могущего вызывать брожение и без живых бактерий (Бухнер и Мейзенгеймер).
Обычно молочнокислое брожение приводит к образованию оптически недеятельной молочной кислоты, однако часто при этом получается кислота, обладающая слабым правым или левым вращением.
Чистая левовращающая молочная (D-молочная) кислота может быть получена брожением сахаристых веществ при посредстве особого возбудителя брожения (Bacillus acidi laevolactici). Правовращающий изомер молочной кислоты (L-молочная) был открыт Либихом (1847) в мясном экстракте и получил названиемясомолочной кислоты. Правовращающая молочная кислота всегда содержится в мышцах животных.
Обыкновенная (недеятельная) молочная кислота, часто называемая «молочной кислотой брожения», долгое время была известна лишь в виде густой жидкости. Осторожным выпариванием в высоком вакууме (0,1—0,5 мм рт. ст.) можно получить ее в безводном состоянии в виде кристаллической массы, плавящейся при 18° С. Из солей i-молочной кислоты характерной является хорошо кристаллизующаяся цинковая соль, содержащая три молекулы воды (С3Н5О3)2Zn ∙ 3Н2О.
Различие свойств недеятельной молочной кислоты и оптически деятельных кислот и их солей показывает, что недеятельное вещество представляет собой не смесь, а рацемическое соединение обеих (D— и L-) кислот или их солей (лактатов).
Правовращающая (L-молочная) и левовращающая (D-молочная) кислоты представляют собой расплывающиеся на воздухе призмы с т. пл. 25—26° С. Они обладают равным, но противоположным оптическим вращением (в 10%-ном растворе [α]D 15°C =±3,82° и в 2,5%-ном [α]D 15°C =±2,67°). При продолжительном нагревании до 130—150°С оптически деятельные изомеры рацемизуются и дают ангидриды недеятельной молочной кислоты. Цинковые соли оптически деятельных изомеров молочной кислоты кристаллизуются только с двумя молекулами воды (C3H5O3)2Zn ∙ 2H2O и обе обладают совершенно одинаковой растворимостью в воде (1 : 175 при 15° С), отличной от растворимости недеятельной соли (1 : 50 при 10° С).
Оптически недеятельная молочная кислота может быть разделена на оптически деятельные изомеры с помощью плесневых грибков, а также кристаллизацией молочнокислых солей оптически деятельных алкалоидов: стрихнина, хинина или морфина.
Особенно легко (даже при высушивании в вакууме) идет выделение воды с превращением в лактид, являющийся гомологом гликолида.
Молочная кислота брожения находит значительное применение в технике, например в протравном крашении, в кожевенном производстве, в бродильных производствах (для предохранения от попадающих из воздуха посторонних бактерий), а также в медицине (80%-ный сироп; относительная плотность 1,21 — 1,22).
Источник
Карбоновые кислоты
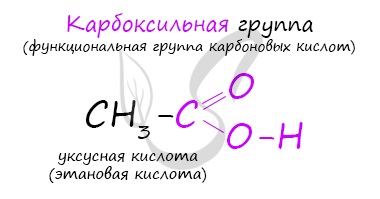
Карбоновые кислоты — класс органических соединений, молекулы которых содержат одну или несколько карбоксильных групп COOH.
Имеют разнообразное промышленное применение и большое биологическое значение. Общая формула одноосновных карбоновых кислот CnH2nO2 .
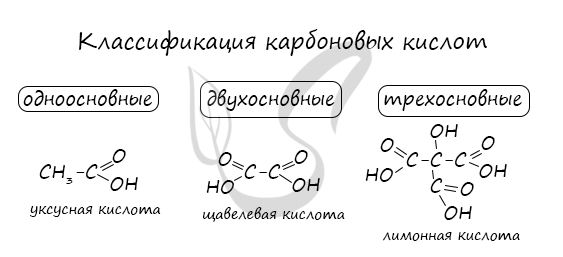
Классификация карбоновых кислот
По количеству карбоксильных групп в молекуле карбоновые кислоты подразделяются на:
- Одноосновные — 1 карбоксильная группа
- Двухосновные — 2 карбоксильных группы
- Трехосновные — 3 карбоксильных группы
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
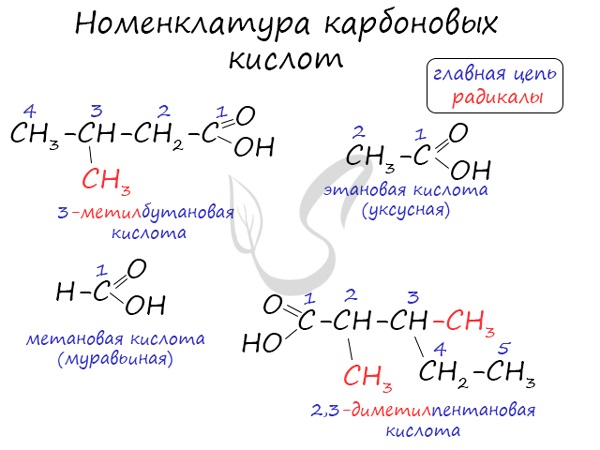
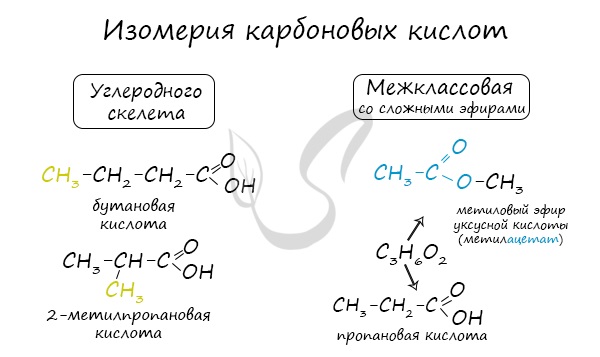
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
Многие карбоновые кислоты имеют тривиальные названия. Наиболее известные:
- Метановая — HCOOH — муравьиная кислота
- Этановая — CH3-COOH — уксусная кислота
- Пропановая — C2H5-COOH — пропионовая кислота
- Бутановая — C3H7-COOH — масляная кислота
- Пентановая — C4H9-COOH — валериановая кислота
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
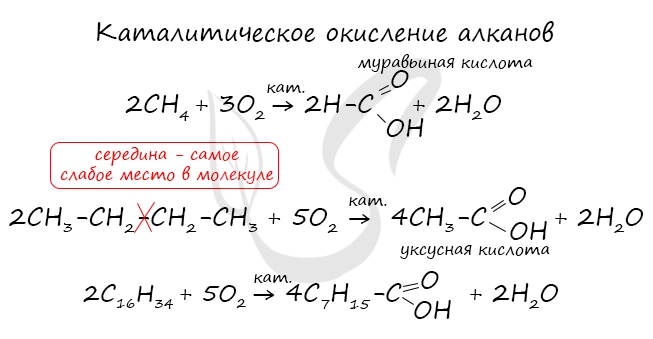
Получение карбоновых кислот
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
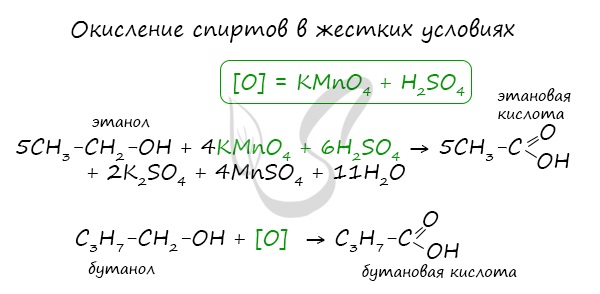
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
При окислении альдегиды образуют соответствующие карбоновые кислоты. Окисление можно проводить качественной реакцией на альдегиды — реакцией серебряного зеркала.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
Окисление альдегидов также может быть успешно осуществлено другим реагентом — свежеосажденным гидроксидом меди II. В результате такой реакции образуется осадок кирпично-красного цвета оксида меди I.
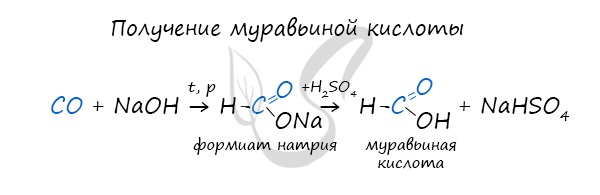
Существует специфический способ получения муравьиной кислоты, который заключается в реакции твердого гидроксида щелочного металла с угарным газом под давлением и температуре 200°С — образуется формиат (соль муравьиной кислоты).
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
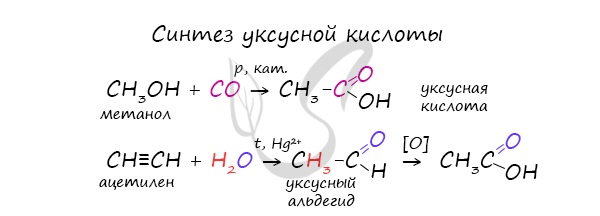
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
Галогенирование происходит по типу замещения в радикале, который соединен с карбоксильной группой. Напомню, что наиболее легко замещается водород у третичного, чуть сложнее — у вторичного, и значительно сложнее — у первичного атома углерода.
Сила карбоновых кислот тем выше, чем меньше электронной плотности сосредоточено на атоме углерода в карбоксильной группе. Поэтому самая слабая из трех кислот — уксусная, чуть сильнее — хлоруксусная, за ней — дихлоруксусная и самая сильная — трихлоруксусная.
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
Сложные эфиры
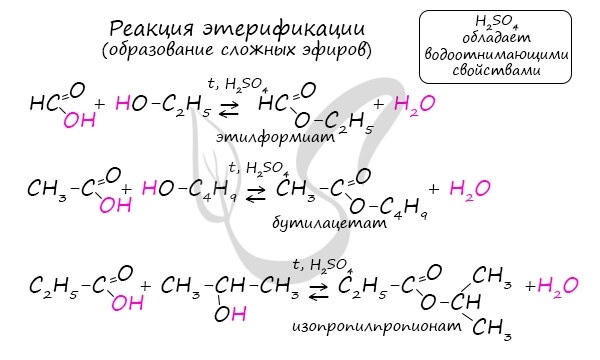
Получение сложных эфиров происходит в реакции этерификации (лат. aether — эфир), заключающейся во взаимодействии карбоновой кислоты и спирта.
Названия сложных эфиров формируются в зависимости от того, какой кислотой и каким спиртом эфир образован. Примеры:
- Метановая кислота + метанол = метиловый эфир метановой кислоты (метилформиат)
- Этановая кислота + этанол = этиловый эфир уксусной кислоты (этилацетат)
- Метановая кислота + этанол = этиловый эфир метановой кислоты (этилформиат)
- Пропановая кислота + бутанол = бутиловый эфир пропионовой кислоты (бутилпропионат)
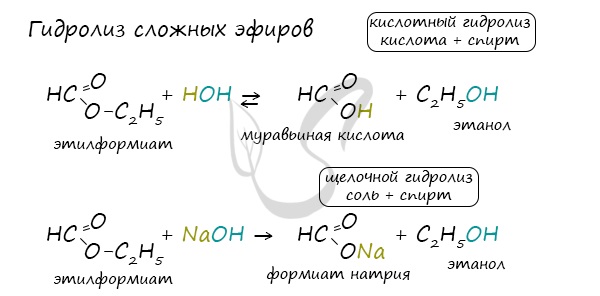
Для сложных эфиров характерной реакцией является гидролиз — их разложение. Возможен щелочной гидролиз, при котором образуется соль кислоты и спирт, и кислотный гидролиз, при котором образуются исходные спирт и кислота.
Кислотный гидролиз протекает обратимо, щелочной — необратимо. Реакция щелочного гидролиза по-другому называется реакция омыления, и напомнит о себе, когда мы дойдем до темы жиров.
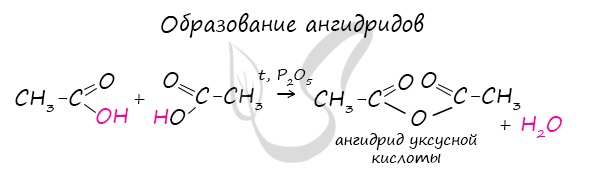
Ангидриды
Ангидриды — химические соединения, производные неорганических и органических кислот, образующиеся при их дегидратации.
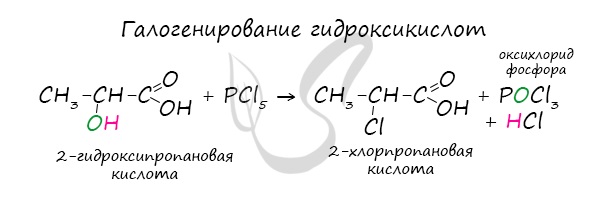
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
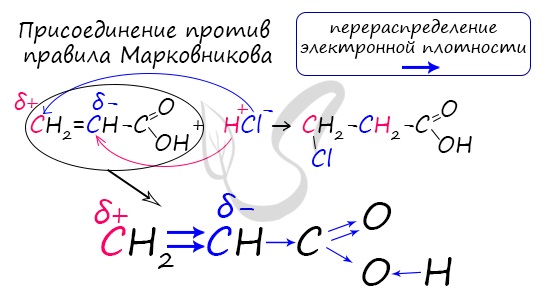
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник