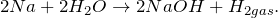Натрий: способы получения и химические свойства
Натрий — это щелочной металл, серебристо-белого цвета. Легкий, очень мягкий, низкая температура плавления.
Относительная молекулярная масса Mr = 22,990; относительная плотность по твердому состоянию d = 0,968; относительная плотность по жидкому состоянию d = 0, 27; tпл = 97,83º C; tкип = 886º C.
Способ получения
1. Натрий получают в промышленности электролизом расплава гидроксида натрия, в результате образуется натрий, кислород и вода:
4NaOH → 4Na + O2↑ + 2H2O
Качественная реакция
Качественная реакция на натрий — окрашивание пламени солями натрия в желтый цвет .
Химические свойства
Натрий — активный металл; на воздухе реагирует с кислородом и покрывается оксидной пленкой. Воспламеняется при умеренном нагревании; окрашивает пламя газовой горелки в темно-красный цвет.
1. Натрий — сильный восстановитель . Поэтому он реагирует почти со всеми неметаллами :
1.1. Натрий легко реагирует с галогенами с образованием галогенидов:
2Na + I2 = 2NaI
1.2. Натрий реагирует с серой с образованием сульфида натрия:
2Na + S = Na2S
1.3. Натрий активно реагирует с фосфором и водородом . При этом образуются бинарные соединения — фосфид натрия и гидрид натрия:
3Na + P = Na3P
2Na + H2 = 2NaH
1.4. С азотом натрий реагирует при температуре 100º С и электрическом разряде с образованием нитрида:
1.5. Натрий реагирует с углеродом с образованием карбида:
1.6. При взаимодействии с кислородом при температуре 250–400º C натрий образует пероксид натрия:
2. Натрий активно взаимодействует со сложными веществами:
2.1. Натрий реагирует с водой . Взаимодействие натрия с водой приводит к образованию щелочи и водорода:
2Na 0 + 2 H2 O = 2 Na + OH + H2 0
2.2. Натрий взаимодействует с кислотами . При этом образуются соль и водород.
Например , натрий реагирует с разбавленной соляной кислотой :
2Na + 2HCl = 2NaCl + H2 ↑
2.3. Натрий может реагировать с аммиаком , при этом образуются амид натрия и водород:
2.4. Н атрий может взаимодействовать с гидроксидами:
Например , натрий взаимодействует с гидроксидом натрия при температуре 600º С:
2Na + 2NaOH = 2Na2O + H2
Источник
Натрий
Натрий — элемент 3-го периода и IA-группы Периодической системы, порядковый номер 11. Электронная формула атома [10Ne]3s 1 , степени окисления +1 и 0. Имеет малую электроотрицательность (0,93), проявляет только металлические (основные) свойства. Образует (как катион) многочисленные соли и бинарные соединения. Почти все соли натрия хорошо растворимы в воде.
В природе — пятый по химической распространенности элемент (второй среди
металлов), встречается только в виде соединений. Жизненно важный элемент для всех организмов.
Натрий, катион натрия и его соединения окрашивают пламя газовой горелки в ярко-желтый цвет (качественное обнаружение).
Натрий Na. Серебристо-белый металл, легкий, мягкий (режется ножом), низкоплавкий. Хранят натрий в керосине. С ртутью образует жидкий сплав — амальгаму (до 0,2 % Na).
Весьма реакционноспособный, во влажном воздухе натрий медленно покрывается гидроксидной пленкой и теряет блеск (тускнеет):
Натрий химически активен, сильный восстановитель. Воспламеняется на воздухе при умеренном нагревании (>250 °С), реагирует с неметаллами:
2Na + O2 = Na2O2 2Na + H2 = 2NaH
2Na + CI2 = 2NaCl 2Na + S = Na2S
6Na + N2 = 2Na3N 2Na + 2C = Na2C2
Очень бурно и с большим экзо-эффектом натрий реагирует с водой:
2Na + 2H2O = 2NaOH + Н2^ + 368 кДж
От теплоты реакции кусочки натрия расплавляются в шарики, которые начинают беспорядочно двигаться из-за выделения Н2. Реакция сопровождается резкими щелчками вследствие взрывов гремучего газа (Н2 + O2). Раствор окрашивается фенолфталеином в малиновый цвет (щелочная среда).
В ряду напряжений натрий стоит значительно левее водорода, из разбавленных кислот НС1 и H2SO4 вытесняет водород (за счет Н20 и Н ).
Получение натрия в промышленности:
(см. также ниже получение NaOH).
Натрий применяется для получения Na2O2, NaOH, NaH, а также в органическом синтезе. Расплавленный натрий служит теплоносителем в ядерных реакторах, а газообразный — используется как наполнитель желтосветных ламп наружного освещения.
Оксид натрия Na2O. Основный оксид. Белый, имеет ионное строение (Na + )2O 2- . Термически устойчивый, при прокаливании медленно разлагается, плавится под избыточным давлением пара Na. Чувствителен к влаге и углекислому газу в воздухе. Энергично реагирует с водой (образуется сильнощелочной раствор), кислотами, кислотными и амфотерными оксидами, кислородом (под давлением). Применяется для синтеза солей натрия. Не образуется при сжигании натрия на воздухе.
Уравнения важнейших реакций:
Получение: термическое разложение Na2O2 (см.), а также сплавление Na и NaOH, Na и Na2O2:
2Na + 2NaOH = 2NaаO + H2 (600 °C)
2Na + Na2O2 = 2NaаO (130-200 °C)
Пероксид натрия Na2O2. Бинарное соединение. Белый, гигроскопичный. Имеет ионное строение (Na + )2O2 2- . При нагревании разлагается, плавится под избыточным давлением О2. Поглощает углекислый газ из воздуха. Полностью разлагается водой, кислотами (выделение О2 при кипячении — качественная реакция на пероксиды). Сильный окислитель, слабый восстановитель. Применяется для регенерации кислорода в изолирующих дыхательных приборах (реакция с СО2), как компонент отбеливателей ткани и бумаги. Уравнения важнейших реакций:
Получение: сжигание Na на воздухе.
Гидроксид натрия NaOH. Основный гидроксид, щелочь, техническое название едкий натр. Белые кристаллы с ионным строением (Na + )(OH — ). Расплывается на воздухе, поглощая влагу и углекислый газ (образуется NaHCО3). Плавится и кипит без разложения. Вызывает тяжелые ожоги кожи и глаз.
Хорошо растворим в воде (с экзо-эффектом, +56 кДж). Реагирует с кислотными оксидами, нейтрализует кислоты, вызывает кислотную функцию у амфотерных оксидов и гидроксидов:
Раствор NaOH разъедает стекло (образуется NaSiО3), корродирует поверхность алюминия (образуются Na[Al(OH)4] и Н2).
Получение NaOH в промышленности:
а) электролиз раствора NaCl на инертном катоде
б) электролиз раствора NaCl на ртутном катоде (амальгамный способ):
(освобождающуюся ртуть возвращают в электролизер).
Едкий натр — важнейшее сырье химической промышленности. Используется для получения солей натрия, целлюлозы, мыла, красителей и искусственного волокна; как осушитель газов; реагент в извлечении из вторичного сырья и очистке олова и цинка; при переработке руд алюминия (бокситов).
Источник
Уравнение реакции натрия с водой
Запишите уравнение реакции натрия с водой; дайте название продукту взаимодействия. Какую химическую связь называют ковалентной. Расскажите о процессе образования ковалентной связи с позиции метода валентных связей
Уравнение реакции натрия с водой, в результате которой образуется гидроксид натрия и выделяется водород, имеет вид:
Для описания ковалентной связи существуют два основных метода: метод валентных связей (МВС) и метод молекулярных орбиталей (ММО). Согласно первому из них связь осуществляется за счет пары электронов, находящихся на орбитали, образовавшейся за счет перекрывания двух атомных орбиталей.
Суть метода ММО заключается в следующем: в молекуле образуется собственная система молекулярных орбиталей, на которых находятся все электроны данной молекулы.
МВС можно рассматривать как современное развитие теории Льюиса, в соответствии с которой два атома совместно владеют одной или несколькими парами электронов. Известны два механизма образования такой связи: либо оба атома предоставляют в общее пользование по одному электрону, либо один атом (донор) предоставляет пару электронов, а другой (акцептор) — пустую орбиталь (донорно-акцепторный механизм). Результат один и тот же: две орбитали перекрываются, и на них находятся два электрона. Например, в ионе аммония три связи Н-N образованы перекрыванием одноэлектронных облаков, а четвертая — по донорно-акцепторному механизму. В результате все четыре связи неразличимы и равноценны.
В МВС ковалентная связь характеризуется насыщаемостью, поляризуемостью и направленностью.
Источник
Эксперимент «Натрий на воде»
Почему металл не тонет, а бегает по воде?
Можно ли заставить металл бегать по воде? Давайте проверим!
Меры предосторожности
Проводите опыт в защитных перчатках, очках и маске. Соблюдайте технику безопасности при работе с огнем и горючими предметами, а также активными металлами (литий, натрий, калий, рубидий, цезий).
Внимание! Не проводите этот опыт самостоятельно — только в присутствии профессионала!
Реагенты и оборудование:
- металлический натрий;
- 1%-й р-р фенолфталеина;
- 1%-й р-р индигокармина;
- 1%-й р-р тимолового синего;
- вода;
- кристаллизатор (3 шт.).
Пошаговая инструкция
В кристаллизаторы наливаем воду и добавляем растворы индикаторов: в первый кристаллизатор капаем фенолфталеин, во второй — индигокармин, а в третий — тимоловый синий. Добавляем по кусочку металлического натрия. Наблюдаем изменение окраски во всех трех кристаллизаторах.
Пояснение процессов
Натрий — очень активный металл, он способен вытеснять водород из воды. Реакция натрия и воды нередко сопровождается взрывом. Если маленький кусочек натрия бросить в кристаллизатор с водой и кислотно-основным индикатором, натрий будет быстро бегать по поверхности жидкости. При этом он будет плавиться, превращаясь в красивую «бусину», которая может даже загореться!
Почему натрий бегает
При взаимодействии с водой выделяется водород, который подталкивает натрий к «бегству».
Почему натрий плавится и загорается
Реакция натрия с водой сопровождается выделением огромного количества тепла — из-за этого металл плавится. Этой энергии реакции достаточно, чтобы поджечь выделяющейся водород!
Почему изменяется цвет растворов
Фенолфталеин, индигокармин и тимоловый синий являются кислотно-основными индикаторами, то есть веществами, которые изменяют свой цвет в зависимости от водородного показателя среды. При взаимодействии натрия с водой образуется гидроксид натрия, который является очень сильным основанием — так среда становится щелочной. Фенолфталеин меняет цвет от бесцветного к малиновому, индигокармин — от синего к зеленому, а тимоловый синий — от желтого к синему.
Источник
Реакция воды и натрия: что там происходит
Группа исследователей во главе с Павлом Юнгвиртом (Pavel Jungwirth) из Чешской академии наук в Праге (Чехия) провели эксперимент для изучения деталей детонации натрия в воде. Ученые засняли реакцию с помощью камер замедленной съемки и обнаружили удивительные подробности. Результаты исследования опубликованы в Nature Chemistry.
В ходе популярного эксперимента, известного еще с XIX века, в обычную воду опускают кусок натрия. Это вызывает мгновенную и бурную реакцию, а иногда, на радость школьников — и взрыв. Все дело в том, что натрий является одним из щелочных металлов. В «чистом виде» при комнатной температуре он представляет собой твердое вещество, которое, однако, можно резать ножом. Всем известна поваренная соль. В этом виде натрий стабилен, и мы не видим подобной реакции, к примеру, подсаливая суп, поскольку в соли натрий присутствует в виде хлорида. Чистые щелочные металлы – совсем другое дело. Когда они соприкасаются с водой, происходит реакция окисления. Электроны покидают металл, выделяется тепло и газ водород, который может воспламениться. Так описывает процесс хрестоматийная теория популярного эксперимента. Однако в ней все еще остаются белые пятна.
Чешские исследователи задались целью выяснить подробности этого процесса. Поначалу они опускали в воду небольшие кусочки натрия. Результаты оказались непредсказуемы: вспышка то происходила, то нет. Причиной нестабильности были незначительные колебания в размере и форме металла. Тогда ученые использовали смесь жидкого натрия и другого щелочного металла, калия. Это позволило исследователям производить капли одинаковой формы и величины.
Съемка со скорость тысяча кадров в секунду показала, что через пять миллисекунд, попав в воду, щелочной металл «съеживается», выпуская десятки и сотни «игл». Ученые предположили, что это происходит в силу того, что электроны из металла мгновенно уходят в воду, и в нем происходит накопление положительного заряда. Взаимное отталкивание положительно заряженных частиц разрывает металл, вызывая появление «игл». В свою очередь это увеличивает площадь металла, контактирующего с водой, вызывая бурную реакцию. Компьютерное моделирование, проведенное после эксперимента, подтвердило этот эффект, хотя и на примере значительно меньшего количества натрия из-за ограниченности вычислительной мощности.
Подробное объяснение природы этой реакции — которым, как ни странно, до сих пор никто не озаботился — может быть применено для предотвращения подобных взрывов на производственных объектах, использующих щелочные металлы, например, в некоторых видах ядерных реакторов, которые охлаждаются жидким металлом. Но это все уже прикладное, как признается руководитель группы исследователей — похоже, им, как и любым мальчишкам, нравится играть со взрывчатыми веществами.
И добавим о российских химических новостях — не так взрывчато, зато куда фундаментальнее — как сообщал недавно наш портал, российским химикам удалось получить титан с особо низкой радиактивностью, что может быть крайне полезным для экспериментов с элементарными частицами.
Источник