- ХИМИЯ НЕФТИ
- ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
- Понятие поверхностного натяжения
- Параметры влияющие на поверхностное натяжение
- Экспериментальное определение поверхностного натяжения
- Добыча нефти и газа
- Изучаем тонкости нефтегазового дела ВМЕСТЕ!
- Поверхностно-молекулярные свойства системы пласт-вода
- Молекулярно –поверхностные свойства системы нефть-газ-вода-порода
ХИМИЯ НЕФТИ
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Понятие поверхностного натяжения
называется термодинамическая характеристика поверхности раздела фаз, определенная как работа обратимого изотермического образования единицы плошали этой поверхности. Для жидкости поверхностное натяжение рассматривается как сила, действующая на единицу длины контура поверхности и стремящаяся сократить поверхность до минимума при заданных объемах фаз.
Нефть — это нефтяная дисперсная система, состоящая из дисперсной фазы и дисперсионной среды.
Поверхность частицы дисперсной фазы (например, ассоциат асфальтенов, глобула воды и т. п.) обладает некоторым избытком свободной поверхностной энергии Fs, пропорциональной площади поверхности раздела фаз S:
Величина σ может рассматриваться не только как удельная поверхностная энергия, но и как сила, приложенная к единице длины контура, ограничивающего поверхность, направленная вдоль этой поверхности перпендикулярно контуру и стремящаяся эту поверхность стянуть или уменьшить. Эта сила носит название .
Действие поверхностного натяжения можно наглядно представить в виде совокупности сил, стягивающих края поверхности к центру.
Длина каждой стрелочки вектора отражает величину поверхностного натяжения, а расстояние между ними соответствует принятой единице длины контура поверхности. В качестве размерности величины σ в равной мере используются как [Дж/м 2 ] = 10 3 [эрг/см 2 ], так и [Н/м] = 10 3 [дин/см].
В результате действия сил поверхностного натяжения жидкость стремится сократить свою поверхность, и если влияние силы земного притяжения незначительно, жидкость принимает форму шара, имеющего минимальную поверхность на единицу объема.
Поверхностное натяжение различно для разных групп углеводородов — максимально для ароматических и минимально для парафиновых. С увеличением молекулярной массы углеводородов оно повышается.
Большинство гетероатомных соединений, обладая полярными свойствами, имеют поверхностное натяжение ниже, чем углеводороды. Это очень важно, поскольку их наличие играет значительную роль в образовании водонефтяных и газонефтяных эмульсий и в последующих процессах разрушения этих эмульсий.
Параметры влияющие на поверхностное натяжение
Поверхностное натяжение существенно зависит от температуры и давления, а также от химического состава жидкости и соприкасающейся с ней фазы (газ или вода).
С повышением температуры поверхностное натяжение убывает и при критической температуре равно нулю. С увеличением давления поверхностное натяжение в системе газ — жидкость также снижается.
Поверхностное натяжение нефтепродуктов может быть найдено расчетным путем по уравнению:
Пересчет σ от одной температуры T0 к другой T можно проводить по соотношению:
Значения поверхностного натяжения для некоторых веществ.
Вещества, добавка которых к жидкости уменьшает ее поверхностное натяжение, называют поверхностно-активными веществами (ПАВ).
Поверхностное натяжение нефти и нефтепродуктов зависит от количества присутствующих в них поверхностно-активных компонентов (смолистых веществ, нафтеновых и других органических кислот и т. п.).
Нефтепродукты с малым содержанием поверхностно-активных компонентов имеют наибольшее значение поверхностного натяжения на границе с водой, с большим содержанием — наименьшее.
Хорошо очищенные нефтепродукты имеют высокое поверхностное натяжение на границе с водой.
С поверхностными силами на границе раздела твердой и жидкой фаз связаны явления смачивания и капиллярные явления, на которых основаны процессы миграции нефти в пластах, подъем керосина и масла по фитилям ламп и масленок и т. д.
Экспериментальное определение поверхностного натяжения
Для экспериментального определения поверхностного натяжения нефтей и нефтепродуктов применяются различные методы.
Первый метод (а) основан на измерении силы, необходимой для отрыва кольца от поверхности раздела двух фаз. Эта сила пропорциональна удвоенной силе окружности кольца. При капиллярном методе (б) измеряют высоту подъема жидкости в капиллярной трубке. Недостатком его является зависимость высоты подъема жидкости не только от величины поверхностного натяжения, но и от характера смачивания стенок капилляра исследуемой жидкостью. Более точной разновидностью капиллярного метода является метод висячей капли (в), основанный на измерении массы капли жидкости, отрывающейся от капилляра. На результаты измерения влияют плотность жидкости и размеры капли и не влияет угол смачивания жидкостью твердой поверхности. Этот метод позволяет определять поверхностное натяжение в сосудах высокого давления.
Наиболее распространенным и удобным способом измерения поверхностного натяжения является способ наибольшего давления пузырьков или капель (г), что объясняется простотой конструкции, высокой точностью и независимостью определения от смачивания.
Этот способ основан на том, что при выдавливании пузырька воздуха или капли жидкости из узкого капилляра в другую жидкость поверхностное натяжение σ на границе с той жидкостью, в которую выпускается капля, пропорционально наибольшему давлению, необходимому для выдавливания капли.
Поверхностное натяжение о входит в выражение для так называемого парахора П — величины, связывающей молекулярную массу М углеводородов и плотность их в жидкой фазе ρж и в парах ρп:
Парахор углеводородов зависит от структуры их молекул: с увеличением числа боковых цепей, двойных связей, ароматических и нафтеновых циклов величина парахора уменьшается. При одинаковой температуре кипения углеводородов парахор уменьшается в следующем порядке: парафины — олефины — нафтены — ароматические углеводороды.
Источник
Добыча нефти и газа
Изучаем тонкости нефтегазового дела ВМЕСТЕ!
Поверхностно-молекулярные свойства системы пласт-вода
Нефтяной пласт представляет собой залежь осадочных пород в виде тела с огромным скоплением капиллярных каналов и трещин, поверхность которых очень велика. Поэтому закономерности движения нефти в пласте и её вытеснения из пористой среды зависят также и от свойств пограничных слоёв соприкасающихся фаз и процессов, происходящих на поверхности контакта нефти, газа и воды с породой.
На формирование залежей углеводородов оказывает влияние количество остаточной воды в залежи (остаточная водонасыщенность, SB), которая в свою очередь зависит от свойств воды и углеводородов и от природы поверхности горной породы. Под природой поверхности понимаются гидрофильность – способность вещества смачиваться водой и гидрофобность – способность вещества не смачиваться водой.
Физико-химические свойства поверхностей раздела фаз и закономерности их взаимодействия характеризуются рядом показателей – поверхностным натяжением на границе раздела фаз, явлениями смачиваемости и растекания, работой адгезии и когезии, теплотой смачивания.
Поверхностное натяжение s – избыток свободной энергии сосредоточенной на одном квадратном сантиметре площади поверхностного слоя на границе раздела двух фаз. По поверхностному натяжению пластовых жидкостей на различных поверхностях раздела можно судить о свойствах соприкасающихся фаз, закономерностях взаимодействия жидких и твёрдых тел, процессах адсорбции, количественном и качественном составе полярных компонентов в жидкости, интенсивности проявления капиллярных сил и т.д.
Поверхностное натяжение связано с такими понятиями как свободная энергия поверхностного слоя жидкости и сила поверхностного натяжения.
Свободная энергия поверхности:
где s – поверхностное натяжение;
s – суммарная поверхность двух фаз.
Сила поверхностного натяжения – сила, действующая на единицу длины периметра взаимодействия двух фаз (линию смачивания):

где 
Коэффициент поверхностного натяжения s зависит от давления, температуры, газового фактора, свойств флюидов.
Если поверхностное натяжение между двумя жидкостями, газом и жидкостью можно измерить, то на поверхности раздела породы-жидкости и породы-газа измерить трудно. Поэтому для изучения поверхностных явлений на границе порода-жидкость пользуются косвенными методами изучения поверхностных явлений: измерением работы адгезии и когезии, исследованием явлений смачиваемости и растекаемости, изучением теплоты смачивания.
Смачиванием называется совокупность явлений на границе соприкосновения трёх фаз, одна из которых обычно является твёрдым телом и две другие – не смешиваемые жидкости или жидкость и газ.
Капля жидкости может растекаться по поверхности, если поверхность хорошо смачивается, а если поверхность плохо смачивается, то капля растекаться не будет.
Интенсивность смачивания характеризуется величиной краевого угла смачивания Q, образованного поверхностью твёрдого тела с касательной, проведённой к поверхности жидкости из точки её соприкосновения с поверхностью (рис. 5.1).
Рис. 5.1. Форма капли, обусловленная поверхностными натяжениями на различных границах соприкасающихся фаз.
Краевой угол Q измеряется в сторону более полярной фазы (в данном случае в сторону воды). Принято условно обозначать цифрой 1 водную фазу, цифрой 2 – углеводородную жидкость или газ, цифрой 3 – твёрдое тело.
Предполагая, что краевой угол Q отвечает термодинамическому равновесию, получим уравнение, впервые выведенное Юнгом:
s2,3 = s3,1 +s1,2 × cosQ, (5.3)
откуда получим выражение для краевого угла Q:

Если s23 > s13, то 0
Если s23 > s13, то -1
Существуют также переходные поверхности (т.н. амфотерные), которые хорошо смачиваются как полярными, так и неполярными системами.
К гидрофильным поверхностям относятся силикаты, карбонаты, окислы железа. К гидрофобным поверхностям – парафины, жиры, воск, чистые металлы.
Краевой угол смачивания зависит от строения поверхности, адсорбции жидкостей и газов, наличия ПАВ, температуры, давления, электрического заряда.
Поверхностные явления описываются также работой адгезии.
Адгезия – прилипание (сцепление поверхностей) разнородных тел. Когезия – явление сцепления поверхностей разнородных тел, обусловленной межмолекулярным или химическим взаимодействием.
Работа адгезии оценивается уравнением Дюпре:
Wa = s1,2 + s2,3+ s1,3. (5.5)
Используя соотношения (5.3) и (5.5), мы получим уравнение Дюпре-Юнга:
Wa = s1,2(1+cosQ). (5.6)
s2,3 – s1,3= s1,2cosQ (5.7)
следует, что при смачивании свободная энергия единицы поверхности твёрдого тела уменьшается на величину s1,2cosQ, которую принято называть натяжением смачивания.
Работа когезии Wк характеризует энергетические изменения поверхностей раздела при взаимодействии частиц одной фазы.
Из уравнения (5.6) следует, что на отрыв жидкости от поверхности твёрдого тела при полном смачивании (когда cosQ=0) затрачивается работа, необходимая для образования двух жидких поверхностей – 2sжг, т.е. Wк = 2sж г, где 2sжг – поверхностное натяжение жидкости на границе с газом.
Это значит, что при полном смачивании жидкость не отрывается от поверхности твёрдого тела, а происходит разрыв самой жидкости, т.е. при полном смачивании s1,2 £ s1,3 .
Подставив в уравнение Юнга значения работ адгезии и когезии, получим:

Из этого уравнения следует, что смачиваемость жидкостью твёрдого тела тем лучше, чем меньше работа когезии (и поверхностное натяжение жидкости на границе с газом).
Для характеристики смачивающих свойств жидкости используют также относительную работу адгезии z=Wа/Wк.
Ещё одна характеристика, используемая для описания поверхностных явлений – теплота смачивания.
Установлено, что при смачивании твёрдого тела жидкостью наблюдается выделение тепла, так как разность полярностей на границе твёрдое тело–жидкость меньше, чем на границе с воздухом. Для пористых и порошкообразных тел теплота смачивания обычно имеет значение от 1 до 125 кДж/кг и зависит от степени дисперсности твёрдого тела и полярности жидкости.
Теплота смачивания характеризует степень дисперсности твёрдого тела и природу его поверхности. Большее количество теплоты выделяется при смачивании той жидкостью, которая лучше смачивает твёрдую поверхность.
Источник
Молекулярно –поверхностные свойства системы нефть-газ-вода-порода



Нефтесодержащие горные породы имеют огромную удельную поверхность, которая контактирует в пласте с нефтью, газом и водой.
В порах и трещинах горной породы также находятся в контакте не смешивающиеся друг с другом жидкости- вода и нефть.
Суммарная поверхность их раздела также большая. Исходя из этого, на многие прцессы разработки нефтяных и газовых залежей значительное влияние оказывают поверхностные явления, происходящие в пласте на границе разделов твердой поверхности породы с жидкостями и газами самих несмешивающихся жидкостей.
Молекулярно- поверхностные свойства раздела фаз пластовых систем (нефть-газ-вода) изучают по величине поверхностного натяжения жидкостей на границах с жидкостями (нефть, вода) и газом, по избирательной смачиваемости системы, по величине работы адгезии и теплот смачивания горных пород пластовыми жидкостями.
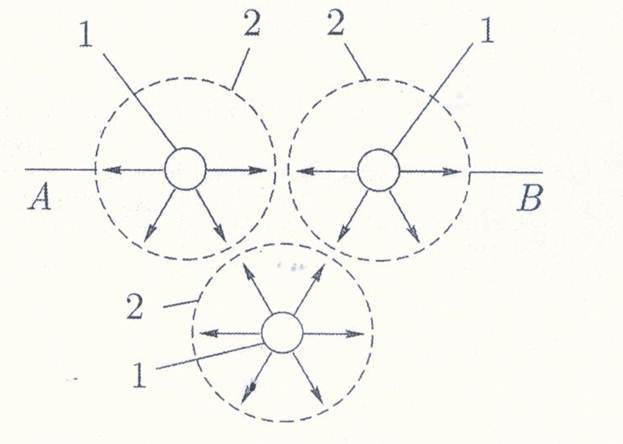
В жидкости между молекулами присутствуют силы взаимного сцепления, которые находятся в равновесном состоянии (рис. 10) и свободно могут передвигаться в любом направлении.
Рис. 10.Схема возникновения молекулярного давления: 1 – молекула; 2 –область молекулярного притяжения.
Силы, действующие на молекулы, находятся в поверхностном слое (АВ) или на поверхности раздела двух несмешивающихся жидкостей и вдоль поверхности раздела.
Молекулы, которые находятся на поверхности раздела двух фаз, обладают избытком энергии по сравнению с энергией молекул, находящихся во внутренних слоях жидкости.
При этом поверхностный слой жидкости оказывает большое давление, называемое молекулярным давлением. Для воды оно доходит до 1000 МПа.
Давление поверхностного слоя вызывает появление сил реакции, которые противодействуют молекулярному давлению и называются силами поверхностного натяжения. Поверхностное натяжение можно охарактеризовать как работу, необходимую для образования единицы новой поверхности:
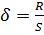
Где R – работа, Дж; S – вновь образованная поверхность, м 2. ; 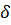
В нефтяном пласте поверхностное натяжение может быть на границах таких фаз: нефть-вода, нефть-газ, нефть-порода, вода-газ, вода-порода, газ-порода.
Поверхностное натяжение всегда изменяется на границе раздела двух фаз. Поверхностное натяжение разных фаз на границе их раздела неодинаковое за счет различного содержания полярных компонентов.
В таблице 1 показаны значения поверхностного натяжения некоторых жидкостей на границе с воздухом и водой при температуре 20 о С.
Поверхностное натяжение на границе двух фаз зависит от температуры и давления. Поверхностное натяжение жидкости на границе с воздухом уменьшается с повышением температуры. Поверхностное натяжение жидкости при критической температуре становится равным нулю, и вся жидкость превращается в газ. Поверхностное натяжение жидкости уменьшается с повышением давления.
Поверхностное натяжение жидкостей на границе сгазом понижается с повышением температуры и давления. В то же время поверхностное натяжение нефти на границе с водой практически не зависит от давления и температуры
На поверхностное натяжение нефти на границе с водой в большей степени влияют поверхностно-активные вещества .ПАВ в нефти являются нафтеновые кислоты, асфальтосмолистые вещества, меркаптаны. Тиофены и др., в молекулах которых атомы расположены несимметрично. Такие вещества способны адсорбироваться на поверхности раздела и снижать поверхностное натяжение.
Взаимная растворимость жидкостей обусловлена содержанием в нмх ПАВ. Чем меньше взаимная растворимость жидкостей, тем выше поверхностное натяжение на границе их раздела: чем больше взаимная растворимость жидкости, тем меньше поверхностное натяжение. В тех случаях, когда растворенные вещества уменьшают взаимную растворимость жидкостей, тогда поверхностное натяжение на границе раздела жидкостей увеличивается. Такие вещества называют ПАВ.
Источник