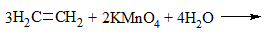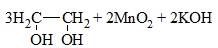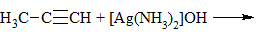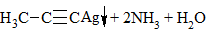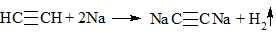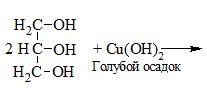Химия, Биология, подготовка к ГИА и ЕГЭ
Качественные реакции органической химии
В качественном анализе используют легко выполнимые, характерные химические реакции, при которых наблюдается появление или исчезновение окрашивания, выделение или растворение осадка, образование газа и др. Реакции должны быть как можно более селективны и высокочувствительны.
Это означает, что качественные реакции — это реакции с ощутимым эффектом -цвет, запах, изменение состояния вещества. «Селективность» — означает, что желательно, чтобы такая реакция на данный класс веществ или на данное вещество была уникальна. Высокая чувствительность — даже очень небольшое количество вещества должно проявляться в такой реакции.
С уникальностью в органической химии немного проблематично, но тем не менее, есть достаточно много реакций для определения того или иного вещества .
Итак, классы органических соединений и соответствующие им качественные реакции:
| Класс органических соединений | Качественные реакции |
| Алканы | У алканов нет качественных реакций. Их определяют методом исключения |
| Алкены | 1. Обесцвечивание бромной воды: 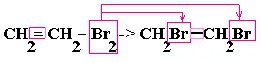 2. Изменение окраски раствора 2. Изменение окраски раствора 3СH2=CH2 + 2 KMnO4 + 4H2O → 3C2H4(OH)2 + 2 MnO2 + 2KOH |
| Циклоалканы | Обесцвечивание бромной воды: 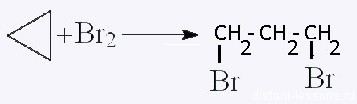 |
| Алкины | 1. Обесцвечивание бромной воды, 2. Образование ацетиленидов серебра и меди:  3. Изменение окраски перманганата калия: (KMnO4 → MnO2) C2H2 → HOOC-COOH |
| Алкадиены | Т.к. алкадиены содержат 2 двойные связи, то они так же как и алкены, обесцвечивают бромную воду |
| Арены | 1. Взаимодействие с бромом (в присутствии катализатора) 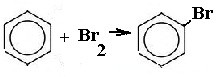
|
| Спирты | Реакция с оксидом меди — в осадок выпадает медь: 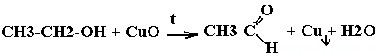 |
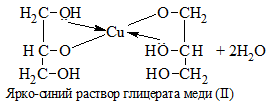
| Многоатомные спирты | С гидрокисдом меди (II) — Cu(OH)2 образуется комплекс синего цвета |
| Альдегиды | Реакция «серебряного зеркала» и реакция «медного зеркала»: 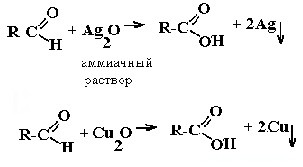 |
| Кислоты органические | Дают окрашенные соли тяжелых металлов — см. таблицу растворимости |
| Амины | Качественных реакций нет (только анилин — имеет характерный запах) |
Как вы видите, все вещества, имеющие кратные связи (кратные=двойные и тройные), обесцвечивают бромную воду. Многие из них изменяют окраску раствора перманганата калия. Поэтому эти вещества надо разделять по их индивидуальным, характерным только для них качественным реакциям.
Здесь перечислены самые основные качественные реакции органической химии. Если говорить о высокомолекулярных соединениях — белках, жирах, углеводах, то для них качественные реакции определяются функциональными группами, входящими в состав. Зная функциональную группу, вы легко сможете подобрать реактив, т.к. в таблице они разобраны именно по классам.
Источник
помогите с вопросами по химии
А1. Функциональная группа карбоновых кислот называется
1) карбонильной
2) гидроксильной
3) карбоксильной
4) сложноэфирной
А2. Реагирует с аммиачным раствором оксида серебра, давая реакцию «серебряного зеркала» , следующая кислота
1) метановая
2) этановая
3) пальмитиновая
4) олеиновая
A3. Обесцвечивает бромную воду следующая кислота
1) пальмитиновая
2) олеиновая
3) стеариновая
4) уксусная
А4. Укажите формулу непредельной кислоты
1) C15H31COOH
2) СН3СООН
3) НСООН
4) C17H31COOH
А5. С увеличением числа атомов углерода в молекулах предельных одноосновных кислот их растворимость в воде
1) уменьшается
2) увеличивается
3) увеличивается незначительно
4) не изменяется
А6. Укажите формулу кислоты, являющейся альдегидокислотой
1) С17Н31СООН
2) НСООН
3) СНзСООН
4) C15H31COOH
А7. Уксусная кислота не реагирует со следующим металлом
1) Zn
2) Мg
3) Сu
4) Са
А8.Уксусная кислота не взаимодействует с
1) NaHC03
2) Na2Si03
3) NaOH
4) С02
А9. Напишите уравнение реакции оксида магния с уксусной кислотой. Ответ дайте в виде суммы коэффициентов в уравнении реакции
1) 5
2) 7
3) 6
4) 4
А10. В ходе реакции этерификации карбоновые кислоты реагируют
1) с металлами
2) с основаниями
3) со спиртами
4) с кислотами
All. Олеиновая кислота не взаимодействует с раствором
1) брома
2) ацетата натрия
3) гидроксида натрия
4) перманганата калия
А12. Определите вещество X в следующей схеме превращений:
метанол → X→ уксусная кислота
1) этилформиат
2) этаналь
3) метаналь
4) метилацетат
А13. Избыток муравьиной кислоты прореагировал с 200 г 6,1%-ного раствора силиката натрия. Определите массу образовавшегося осадка.
1) 7,8 г
2) 8,3 г
3) 15,6 г
4) 16,8 г
А14. В ходе реакции 46 г уксусной кислоты с 46 г этанола в присутствии концентрированной серной кислоты образовалось 54 г этилацетата. Определите выход реакции этерификации.
1) 0,84 2) 0,82
3) 0,80 4) 0,78
А15. Смесь гидрокарбоната натрия и карбоната натрия полностью прореагировала с 300 г 14%-ного раствора уксусной кислоты. При этом выделилось 11,2 л (н. у. ) газа. Определите массовую долю карбоната натрия в исходной смеси
1) 0,44 2) 0,46,
3) 0,54 4) 0,56
А1. Функциональная группа карбоновых кислот называется
3) карбоксильной
А2. Реагирует с аммиачным раствором оксида серебра, давая реакцию «серебряного зеркала» , следующая кислота
1) метановая
A3. Обесцвечивает бромную воду следующая кислота
2) олеиновая
А4. Укажите формулу непредельной кислоты
4) C17H31COOH
А5. С увеличением числа атомов углерода в молекулах предельных одноосновных кислот их растворимость в воде
1) уменьшается
А6. Укажите формулу кислоты, являющейся альдегидокислотой
2) НСООН
А7. Уксусная кислота не реагирует со следующим металлом
3) Сu
А8.Уксусная кислота не взаимодействует с
4) С02
А9. Напишите уравнение реакции оксида магния с уксусной кислотой. Ответ дайте в виде суммы коэффициентов в уравнении реакции MgO + 2CH3COOH —> (CH32COO)2Mg + H2O
1) 5
А10. В ходе реакции этерификации карбоновые кислоты реагируют
3) со спиртами
All. Олеиновая кислота не взаимодействует с раствором
2) ацетата натрия
А12. Определите вещество X в следующей схеме превращений:
метанол → X→ уксусная кислота
4) метилацетат
А13. Избыток муравьиной кислоты прореагировал с 200 г 6,1%-ного раствора силиката натрия. Определите массу образовавшегося осадка.
1) 7,8 г
А14. В ходе реакции 46 г уксусной кислоты с 46 г этанола в присутствии концентрированной серной кислоты образовалось 54 г этилацетата. Определите выход реакции этерификации.
3) 0,80
Источник
Некоторые темы органической химии для подготовки к ЕГЭ
Задание 25. Качественные реакции (подробно)
1. Как распознать алкены и стирол (в случае стирола в реакции вступает только двойная связь боковой цепи, а не бензольное кольцо)
1) + Br2 (бромная вода) → обесцвечивание раствора (реакция протекает в обычных условиях)
2) + KMnO4 (водный раствор) → обесцвечивание раствора, образование осадка MnO2 бурого цвета:
Раствор перманганат калия фиолетового цвета. В результате реакции окраска исчезает, образуется осадок MnO2 бурого цвета.
2. Как распознать алкины
1) + Br2 (бромная вода) → обесцвечивание раствора (реакция протекает в обычных условиях):
2) + KMnO4 (водный раствор) → обесцвечивание раствора, образование осадка MnO2 бурого цвета:
3C2H2 + 8KMnO4 → 3K2C2O4 + 8MnO2 + 2KOH + 2H2O (K2C2O4 — соль щавелевой кислоты)
3) + [Ag(NH3)2]OH → выпадение осадка в случае концевой тройной связи:
4) + Металл → выпадение осадка и выделение водорода в случае концевой тройной связи
3. Как распознать бензол
1) Бензол горит коптящим пламенем из-за большого содержания углерода.
Благодаря устойчивой ароматической системе бензол не вступает в реакции с водным раствором Br2 и раствором KMnO4.
4. Как распознать одноатомные спирты
1) + CuO → наблюдаем выделение металлической меди:
CH3-CH2-OH + CuO → CH3-CHO + Cu + H2O (t, окисление спиртов до альдегидов)
С основаниями одноатомные спирты не взаимодействуют.
5. Как распознать многоатомные спирты
1) + Cu(OH)2 → растворение голубого осадка и появление ярко-синей окраски раствора:
С щелочами многоатомные спирты не взаимодействуют.
6. Как распознать фенолы
1) + Br2 → выпадение белого осадка 2,4,6-трибромфенола
2) + FeCl3 → раствор фиолетового цвета
7. Как распознать альдегиды
1) + [Ag(NH3)2]OH → восстановление металлического серебра
2) + Cu(OH)2 → выпадение осадка Cu2O кирпично-красного цвета
8. Как распознать карбоновые кислоты
1) раствор лакмуса → изменение окраски на красную
2) + Na2CO3/NaHCO3  → выделение газа CO2
9. Как распознать соли высших карбоновых кислот
1) + HCl (любая сильная кислота) → появление хлопьев нерастворимых высших кислот
10. Как отличить муравьиную кислоту от уксусной
Муравьиная кислота содержит и альдегидную группу тоже, следовательно, возможны реакции, характерные альдегидам:
1) + [Ag(NH3)2]OH → восстановление металлического серебра и выделение газа (так как кислота окисляется до CO2)
2) + Cu(OH)2 → выпадение осадка Cu2O кирпично-красного цвета и выделение газа (так как кислота окисляется до CO2).
11. Как распознать низшие амины
1) раствор лакмуса → изменение окраски на синюю (так как среда раствора щелочная)
1) раствор фенолфталеина → изменение окраски на малиновую
12. Как распознать анилин
1) + Br2 → выпадение белого осадка 2,4,6-триброманилина
13. Как распознать белок
1) + HNO3 → желтое окрашивание (ксантопротеиновая реакция)
2) + Cu(OH)2 → фиолетовое окрашивание (биуретовая реакция)
14. Как распознать глюкозу C6H12O6
1) + Cu(OH)2 → растворение голубого осадка и появление ярко-синей окраски раствора (реакция на несколько гидроксильных групп)
2) + Cu(OH)2 → при нагревании образуется осадок Cu2O красного цвета (реакция на альдегидную группу)
3) + [Ag(NH3)2]OH → восстановление металлического серебра
15. Как распознать крахмал
1) + I2 → появление синей окраски.
Источник
Обесцвечивать бромную воду будут кислоты
При сгорании 4,00 г органического соединения образовалось 4,48 л углекислого газа (н.у.) и 2,88 г воды. Вещество обесцвечивает бромную воду и вступает в реакцию с раствором гидроксида бария при нагревании, один из продуктов имеет формулу
На основании данных условия задания:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции этого вещества с раствором гидроксида бария при нагревании (используйте структурные формулы органических веществ).
Общая формула вещества
Запишем схему реакции горения:
Определим количества вещества атомов углерода, водорода и кислорода:
Откуда,
Получаем, что
Простейшая формула исходного вещества
Формула может являться и молекулярной. Это могут быть, например, непредельная карбоновая кислота или сложный эфир.
Искомое вещество обесцвечивает бромную воду, значит, молекула содержит кратную углерод-углеродную связь.
Искомое вещество вступает в реакцию с раствором гидроксида бария при нагревании, один из продуктов имеет формулу Из этого можно сделать вывод, что искомое вещество − сложный эфир непредельной кислоты, содержащей три атома углерода.
Значит, искомое вещество − это этиловый эфир пропеновой кислоты.
Его структурная формула
Запишем уравнение реакции этого вещества с раствором гидроксида бария при нагревании :
| Критерии оценивания выполнения задания | Баллы |
|---|---|
| Ответ правильный и полный, содержит следующие элементы: • правильно произведены вычисления, необходимые для установления молекулярной формулы вещества и записана молекулярная формула вещества; • записана структурная формула органического вещества, которая отражает порядок связи и взаимное расположение заместителей и функциональных групп в молекуле в соответствии с условием задания; • с использованием структурной формулы органического вещества записано уравнение реакции, на которую даётся указание в условии задания Источник |