- Оформите таблицу эталонные свойства веществ алмаз вода
- Предмет химии. Вещества — ГДЗ Габриелян Сладков 8 класс рабочая тетрадь
- Шкала твердости Мооса
- Основные свойства минералов определитель (Таблица)
- Основные свойства минералов
- Таблица определитель минералов их свойства, формула, генезис
- Алмаз, описание, характеристики, свойства и происхождение
- Алмаз, описание, характеристики, свойства и происхождение.
- Алмаз, характеристики, описание, кристаллическая решетка, химический состав:
- Образование и происхождение алмазов:
- Механические, оптические, химические и иные свойства алмаза:
- Физические свойства алмаза:
- Огранка алмаза:
- Оценка алмаза как ювелирного камня:
Оформите таблицу эталонные свойства веществ алмаз вода
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
ПРОВЕРЬТЕ СВОИ ЗНАНИЯ
Упражнение 1. В чём разница между веществом и материалом? В том, что материал очень часто представляет собой композицию нескольких веществ. Например, различные сплавы металлов― это материал, а сам металл и отдельные компоненты сплавов ― это вещества.
Упражнение 2. Что такое термопластичность? Способность некоторых веществ или материалов при нагревании легко изменять форму и сохранять её после прекращения нагревания.
Как это свойство пластмасс используют в промышленности. При изготовлении различных пластмассовых изделий.
Упражнение 3. Приведите примеры физических свойств некоторых веществ, которые используются в качестве эталонных. Температурная шкала, предложенная шведским астрономом и метеорологом Андерсом Цельсием, основана на физических свойствах воды: температуре замерзания и кипения. Ноль в современной шкале Цельсия ― точка плавления льда (и замерзания воды), а 100 градусов ― точка кипения воды (и конденсации ее паров) при давлении 1 атм.
Источник
Предмет химии. Вещества — ГДЗ Габриелян Сладков 8 класс рабочая тетрадь
Часть 1
1. Химия изучает:
2. Вещество это —
то, из чего состоят физические тела.
3. Признаки, по которым одни вещества отличаются от других,
— это свойства , например: агрегатное состояние, цвет, запах, плотность и т.д.
4. Существует взаимосвязь: свойство вещества — применение вещества.
Например, для стекла:
2) изготовление хрусталя
5. Вещества состоят из молекул , которые, в свою очередь, образованы из атомов . Определенный вид атомов называют химическим элементом . Всего известно 120 химический элементов.
6. Химический элемент существует в трех формах.
Часть 2
1. Установите соответсвие между понятием и примером.
2. Вычеркните лишнее:
колба, приборка, химический стакан, мензурка, ступка , мерный цилиндр, кристаллизатор.
Укажите признак, общий для оставшихся объектов.
3. Составьте задание, аналогичное предыдущему.
Вычеркните лишнее — приборка, мерная колба, цилиндр, штатив.
4. Заполните таблицу «Физические свойства вещества». В качестве примеров опишите вещества, используемые на кухне.
5. Укажите прилагательные, которые характеризуют свойства воды.
6. Заполните таблицу «Сравнение физических свойств газообразных веществ».
7. Заполните таблицу «Сравнение физических свойств меди и железа».
8. Составьте кроссворд о свойствах и применении какого-либо вещества (по своему выбору).
9. На примере химического элемента водорода укажите правильную последовательность (1-2-3) перечисленных понятий от единичного к общему. Конкретизируте ее, используя слова и рисунки моделей частиц.
3) Вещество — это то, из чего состоят физические тела.
1) Атом — это химически неделимая частица.
2) Молекула — это наименьшая частица вещества.
10. Выражения, являющиеся синонимами понятия «химический элемент».
2) вид одинаковых молекул
3) вид атомов, имеющих одинаковые свойства
4) простые вещества
5) названия видов атомов
Ответ: 1, 3
11. Установите соответствие между формой существования химического элемента и рисунками моделей частиц.
12. Проанализируйте рисунки и впишите пропущенные слова.
На рисунках изображено две молекулы сложных веществ, образованных из двух химических элементов.
13. Отметьте фразы, в которых говорится о сере как о химическом элементе. Из букв, соответствующих правильным ответам, вы составите название химического элемента, соединения которого используют для обеззараживания воды: хлор .
В тех фразах, которые вы не выбрали, речь идет о сере как о простом вещества .
Источник
Шкала твердости Мооса
Шкала Мооса (минералогическая шкала твёрдости) представляет собой качественную порядковую шкалу, характерезующую стойкость различных минералов к царапанию. Используется для определения относительной твердости образцов минералов.
Основана на способности более твердого материала царапать более мягкий материал.
Шкала содержит 10 минералов в качестве эталонных, упорядочивая их в порядке возрастания твердости от очень мягкого (тальк) до очень твердого (алмаз).
Все минералы из таблицы, кроме алмаза, относительно распространены и их легко или недорого получить.
Если минерал царапет эталон, значит его твердость — выше, если он царапается эталоном — ниже.
Шкала Мооса создана в 1812 году и названа в честь изобретателя немецкого геолога и минеролога Фридриха Мооса. С тех пор было изобретено множество различных методов определения твердости: метод Бринеля, Кнупа, Роквелла, Шора, Виккерса.
Определение твердости по Моосу — это относительное целочисленное сравнение устойчивости к царапинам.
Другие методы измерения твердости оперируют устойчивостью к вдавливанию. Для испытаний используется «Индентор» который вдавливается в исследуемый образец с тщательно измеренной силой. Затем размер или глубина выемки на образце и величина силы используются для расчета значения твердости. Поскольку в каждом из этих тестов используются разные аппараты и разные расчеты, их нельзя сравнивать напрямую друг с другом.
Шкала Мооса получила широкое распространение т.к. метод определения твердости прост в исполнении, недорог и люди быстро его понимают.
Несмотря на недостаточную точность, шкала актуальна для полевых геологов, которые используют её для грубой идентификации минералов когда исследуются легко идентифицируемые образцы или когда нет возможности использовать более сложные тесты.
Некоторые используют легкодоступные предметы для быстрого испытания. Например геолог может иметь карманный нож, которым можно определить является ли образец тверже или мягче чем значение 5-6,5 по Моосу.
Ниже представлена расширенная таблица веществ, минералов, драгоценных камней:
| Вещество или минерал | Твердость по Моосу |
|---|---|
| Пирофиллит, молибденит | 1-2 |
| Боксит, уголь | 1-3 |
| Лимонит | 1-5 |
| Лед, сахар, галлий, стронций, индий, олово, барий, таллий, свинец, графит | 1,5 |
| Гипс, кальций | 1,5-2 |
| Сера | 1,5-2,5 |
| Сильвит, глауконит, кадмий, селен | 2 |
| Каменная соль, киноварь, хлорит, висмут, янтарь | 2-2,5 |
| Мусковит | 2-3 |
| Серебро, золото, галенит, медь, биотит, слюда | 2,5-3 |
| Алюминий, известняк, кальцит, борная кислота, нитрофоска | 3 |
| Арагонит, витерит, ангидрит | 3-3,5 |
| Жемчуг, латунь, мышьяк | 3-4 |
| Серпентин | 3-5 |
| Сфалерит, родохрозит, малахит, доломит, куприт, халькопирит, азурит, барит | 3,5-4 |
| Сидерит, пирротин, доломит | 3,5-4,5 |
| Флюорит, бронза фосфористая | 4 |
| Мрамор | 4-5 |
| Зубная эмаль, асбест, апатит, марганец, цирконий , палладий , обсидиан | 5 |
| Титанит, монацит | 5-5,5 |
| Нефрит, уранинит, ильменит, энстатит, керамогранит (полированный) | 5-6 |
| Магнетит | 5-6,5 |
| Нефелин, авгит, арсенопирит, актинолит, бустамит, кобальтит | 5,5-6 |
| Родонит, диопсид, опал, железняк красный | 5,5-6,5 |
| Титан, германий , ниобий , родий , уран | 6 |
| Рутил, пирит, пренит, плагиоклаз, ортоклаз, амазонит, андезин, анортоклаз, бенитоит, гельвин, иридий | 6-6,5 |
| Кремний | 6,5 |
| Яшма | 6,5-7 |
| Агат, цоизит, эпидот, касситерит, пиролюзит | 6-7 |
| Марказит | 6-7,5 |
| Гранит, танзанит, сподумен, оливин, жадеит, аксинит, хризопраз, жадеит | 6,5-7 |
| Силлиманит, гранат | 6,5-7,5 |
| Кварц, каменная галька, аметист, авантюрин, форстерит, осмий, силикон, рений , ванадий | 7 |
| Турмалин, кордиерит, альмандин, борацит, кордиерит, данбурит | 7-7,5 |
| Циркон, андалузит, эвклаз, гамбергит, сапфирин | 7,5 |
| Изумруд , закаленная сталь, вольфрам, шпинель, берилл, бериллий, аквамарин, красный берилл, ганит, пейнит | 7,5-8 |
| Топаз, Фианит | 8 |
| Хризоберилл, александрит, холтит | 8,5 |
| Керамогранит (неполированный) | 8,5 |
| Корунд, рубин, сапфир, алунд, хром | 9 |
| Муассанит, бор | 9,5 |
| Карборунд | 9-10 |
| Алмаз, карбонадо | 10 |
© 2014-2021 Все права на материалы, находящиеся на сайте, охраняются в соответствии с законодательством РФ.
Источник
Основные свойства минералов определитель (Таблица)
Минералы — это относительно конкретные и достаточно устойчивые химические соединения и самородные элементы, характеризующиеся строго постоянным внутренним строением. Обычно к минералам относят природные образования, возникшие в результате физико-химических процессов в недрах и на поверхности земной коры.
На текущее время известно до 4000 минералов.
Основные свойства минералов
В данной таблице учтены физичесике и химичесике как основные (химизм, строение, минеральные агрегаты, твердость, плотность, спайность, излом, цвет, черта, блеск, генезис), так и дополнительные (магнитные и электрические свойства, гигроскопичность, запах, вкус, горючесть, упругость, ковкость, радиоактивность) свойства и приведены сведения относительно практического использования минералов.
Сингония – это классификация кристаллографических групп симметрии, кристаллов и кристаллических решёток в зависимости от системы координат (координатного репера); группы симметрии с единой координатной системой объединяются в одну сингонию. Кристаллы, принадлежащие к одной и той же сингонии, имеют подобные углы и рёбра элементарных ячеек.
Спайность – это способность минералов раскалываться (расщепляться) по параллельным ровным блестящим поверхностям, именуемым плоскостям спайности. Спайность — свойство исключительно кристаллических минералов.
Излом – это поверхности раскола, ориентированные вопреки спайности. Различают раковистый (халцедон, кремень, кварц), занозистый (селенит, асбест), зернистый (горные породы), землистый (боксит, лимонит, ступенчатый (ортоклаз, галенит) и другие поверхности излома.
Черта (цвет черты) — это след, который остается на неглазурованной фарфоровой пластинке (бисквите), если чертить по ней минералом.
Таблица определитель минералов их свойства, формула, генезис
Минерал, формула Разновидности (Р.)
Сингония (С.) Формы нахождения в природе (Ф.)
Источник
Алмаз, описание, характеристики, свойства и происхождение
Алмаз, описание, характеристики, свойства и происхождение.
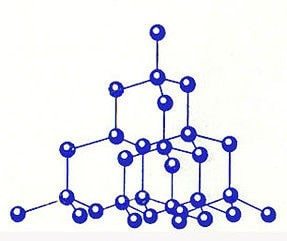
Алмаз представляет собой твердую аллотропную форму углерода, атомы которого имеют кубическую гранецентрированную кристаллическую решетку.
Алмаз, характеристики, описание, кристаллическая решетка, химический состав:
Алмаз (от др.-греч. ἀδάμας «несокрушимый», через араб. ألماس [’almās] и тур. elmas) – минерал, кубическая аллотропная форма углерода . Химическая формула алмаза – C.
Алмаз – это природный минерал, состоящий из углерода и кристаллизующийся в кубической сингонии.
Наряду с графитом , алмазом существуют еще много аллотропных форм углерода. Например, графен , фуллерен , углеродные нанотрубки и т.д. Свойства данных веществ совершенно отличаются друг от друга.
Алмаз является самым твердым природным материалом на Земле.
Алмаз – редкий, но вместе с тем довольно широко распространённый минерал. К настоящему времени алмазы найдены на всех континентах Земли, в том числе и в Антарктиде.
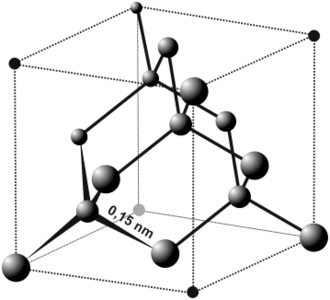
Алмаз представляет собой твердую аллотропную форму углерода , атомы которого имеют кубическую гранецентрированную кристаллическую решетку. При этом, каждый атом углерода в структуре алмаза расположен в центре тетраэдра, вершинами которого служат четыре ближайших атома.
Таким образом, в алмазе каждый атом углерода связан с четырьмя другими атомами. В алмазе связи сформированы sp 3 гибридными орбиталями. Такая связь является наиболее прочной. Именно прочная связь атомов углерода и отсутствие свободного электрона объясняет высокую твёрдость алмаза. Из всех известных веществ алмаз также имеет наибольшее количество атомов на единицу объема, поэтому он одновременно и самый твердый, и наименее сжимаемый.
Наоборот, в графите – другой аллотропной форме углерода, каждый атом углерода связан с тремя атомами аналогичными атомами и имеет один свободный электрон. В графите межатомные связи сформированы sp 2 гибридными орбиталями. Связи между атомами углерода в графите формируются в одной плоскости. Связи между плоскостями графита слабы. Это и обуславливает высокую мягкость графита и свойство слоев графита легко отделяться (отслаиваться) друг от друга.
При нормальных условиях (т.е. комнатной температуре и нормальном давлении), а также высоких давлениях алмаз может существовать неограниченно долго. При комнатной температуре и давлении другая твердая форма углерода, известная как графит, также является химически стабильной формой, но алмаз почти никогда не превращается в нее. И только в вакууме или в инертном газе при повышенных температурах – при 2000 о С алмаз постепенно переходит в графит.
Алмазы бывают совершенно разных цветов и оттенков: от стального серого, белого до коричневого и черного цветов. Редко встречаются бесцветные и прозрачные камни. Это обусловлено тем, что природный алмаз может содержать небольшое количество дефектов и примесей (около одного на миллион атомов углерода). Небольшие количества дефектов или примесей окрашивают алмаз в синий (примеси бора), желтый (примеси азота), коричневый (дефекты кристаллической решетки), зеленый (радиационное воздействие), фиолетовый, розовый, оранжевый, красный или серые цвета. Вместе с тем, химически чистый и структурно совершенный алмаз прозрачен и не имеет оттенка или цвета.
Алмаз также обладает относительно высокой оптической дисперсией (способностью рассеивать свет разных цветов).
Твердость алмаза и его высокая оптическая дисперсия способствует его использованию в качестве драгоценного камня. В отличие от многих других драгоценных камней, он хорошо подходит для ежедневного ношения из-за его устойчивости к царапинам. Поцарапать алмаз может только другой алмаз.
Огранённый алмаз называется бриллиантом.
Алмаз состоит из чистого углерода. В небольших количествах в нем присутствуют различные примеси других химических элементов (бор, азот, алюминий, кремний, кальций, магний и т.д.).
Образование и происхождение алмазов:
Большинство природных алмазов имеют возраст от 1 миллиарда до 3,5 миллиардов лет. Многие из них были сформированы на глубинах от 150 до 250 километров в мантии Земли , хотя некоторые из них формировались на глубине около 800 километров.
Под высоким давлением и температурой углеродсодержащие жидкости растворяли минералы в породе и заменяли их алмазами.
Алмазы образовывались из этой жидкости либо путем восстановления окисленного углерода (например, CO2 или CO3), либо путем окисления восстановленной фазы, такой как метан .
Гораздо позднее (десятки – сотни миллионов лет назад) они были вынесены на поверхность в результате извержений вулканов и отложились в магматических породах, известных как кимберлиты и лампроиты.
Механические, оптические, химические и иные свойства алмаза:
– алмаз представляет собой твердую форму чистого углерода. Твердость по шкале Мооса 10,
– твердость алмаза зависит от его чистоты, отсутствия дефектов кристаллической решетки и ориентации. Твердость выше для безупречных, чистых кристаллов , ориентированных в направлении по самой длинной диагонали кубической алмазной решетки. Поэтому алмазы могут быть поцарапаны и подвергаться обработке только другими алмазами,
– из всех известных веществ алмаз имеет наибольшее количество атомов на единицу объема, поэтому он одновременно и самый твердый , и наименее сжимаемый. У алмаза самый низкий коэффициент сжатия,
– имеет высокую плотность от 3,47-3,55 г/см³,
– обладает хрупкостью, легко раскалывается,
– имеет большой показатель преломления и относительно высокую оптическую дисперсию (способность рассеивать свет разных цветов). Эти свойства заставляют нанесенные при обработке алмаза грани блестеть, играя на свету,
– обладает наиболее высокой теплопроводностью среди всех твёрдых тел 900-2300 Вт/(м·К). Из-за этого алмаз на ощупь холодный,
– у алмаза очень низкий коэффициент трения по металлу,
– имеет самый высокий модуль упругости,
– на воздухе алмаз сгорает при 850-1000 °C, а в струе чистого кислорода горит слабо-голубым пламенем при 720-800 °C, полностью превращаясь в углекислый газ ,
– под действием солнечного света, а также под действием катодных, ультрафиолетовых и рентгеновских лучей алмазы начинают люминесцировать – светиться различными цветами. Именно это специфическое свойство алмаза позволяет его выявлять в породе,
– поверхность алмаза гидрофобна и липофильна, т.е. алмаз не смачивается водой, а хорошо смачивается маслом и жиром. Это свойство использует для того, чтобы отличить алмаз от подделки. Жир на подделке не смачивает поверхность полностью, а собирается в маленькие капельки. Кроме того, алмаз, смазанный жиром, прилипает к стеклу , а подделка – нет,
– алмазы химически стабильны. При комнатной температурой они не реагируют с кислоты и щелочами. Поверхность алмаза может окисляться только при температуре воздуха выше 850 °C. Алмаз также реагирует с газом фтора при температуре свыше 700 °C,
– лучепреломление алмаза таково, что, поместив бесцветный кристалл на страницу с печатным текстом, прочитать написанное не получится. Эта характеристика алмаза позволяет отличить подделку от оригинала. Также если посмотреть сквозь алмаз на солнце, то будет видна лишь тусклая точка,
– под действием радиоактивного излучения алмаз меняет окраску на насыщенный зеленый цвет.
Физические свойства алмаза:
| Наименование показателя: | Значение: |
| Длина связи С–С, нм | 0,15 |
| Плотность, г/см 2 | от 3,47 до 3,55 |
| Температура плавления (при давлении 11 ГПа), о С | 3700-4000 °C |
| Теплопроводность, Вт/(м·К) | от 900 до 2300 |
| Показатель преломления | от 2,417 до 2,419 (в желтом цвете), |
в других цветах – от 2,402 (красный цвет) до 2,465 (фиолетовый цвет).
Огранка алмаза:
Основными типами огранки алмаза являются:
– круглая (со стандартным числом 57 граней),
– фантазийная, к которой относятся такие виды огранки, как «овальная», «груша», «маркиза», «принцесса», «радиант», «сердце», «квадрат», «изумруд», « треугольник » и другие виды.
Форма огранки бриллианта зависит от формы исходного кристалла алмаза.
Оценка алмаза как ювелирного камня:
Ограненный алмаз называют бриллиантом (от фр. brillant «блестящий, сверкающий»). Ему придают специальную форму, максимально выявляющую его естественный блеск.
Лишь 60% добытых алмазов пригодны для ювелирной обработки. Все остальные алмазы находят применение в различных отраслях промышленности .
Все бриллианты оценивают по системе «4 C»:
– и carat (масса в каратах), что позволяет определить, насколько камень близок к совершенству.
В огранке (cut) алмаза ценится ее качество: насколько грани геометрически точны и пропорциональны друг другу. Идеальная огранка кодируется литерой «А», далее — Б, В, Г — по убыванию качества. В международной системе (GIA, Gemological Institute of America) идеальная огранка обозначена как Excellent, и по убыванию качества (Very Good, Good, Fair, Bad).
Чистота (clarity ) пожалуй самый существенный показатель качества бриллиантов: выражается она в наличии или отсутствии дефектов камня или посторонних включений. Бриллианты без изъянов называются бриллиантами чистой воды.
Цвет бриллианта также имеет значение. Особо ценятся бриллианты зеленого, фиолетового и черного цветов. Такие бриллианты встречаются очень редко.
Масса бриллиантов измеряется в каратах: 1 карат равен 0,2 грамма. Чем больше масса бриллианта, тем он стоит дороже.
Источник