- Оксид кальция: способы получения и химические свойства
- Способ получения
- Химические свойства
- Реакция оксида кальция с водой
- Реакция взаимодействия оксида кальция с водой.
- Уравнение реакции взаимодействия оксида кальция с водой:
- Мировая экономика
- Справочники
- Востребованные технологии
- Поиск технологий
- О чём данный сайт?
- О Второй индустриализации
- Оксид кальция с водой нагревание
- Гашение извести (реакция оксида кальция с водой)
- Структура, свойства и применение оксида кальция (CaO)
- формула
- структура
- свойства
- растворимость
- приложений
- Как ступка
- В производстве очков
- В горном деле
- Как средство для удаления силикатов
- Наночастицы оксида кальция
Оксид кальция: способы получения и химические свойства
Оксид кальция CaO — бинарное неорганическое вещество . Белый, гигроскопичный. Тугоплавкий, термически устойчивый, летучий при очень высоких температурах. Проявляет основные свойства.
Относительная молекулярная масса Mr = 56,08; относительная плотность для тв. и ж. состояния d = 3,35; tпл ≈ 2614º C; tкип = 2850º C.
Способ получения
1. Оксид кальция получается при разложении карбоната кальция при температуре 900 — 1200º C. В результате разложения образуется оксид кальция и углекислый газ:
2. В результате взаимодействия гидрида кальция и кислорода при температуре 300 — 400º С образуется оксид кальция и вода:
3. Оксид кальция можно получить сжиганием кальция в в кислороде при температуре выше 300º С:
2Ca + O2 = 2CaO
Химические свойства
1. Оксид кальция реагирует с простыми веществами :
Оксид кальция реагирует с углеродом (коксом) при температуре 1900 — 1950º С и образует угарный газ и карбид кальция:
CaO + 3C = CaC2 + CO
2. Оксид кальция взаимодействует со сложными веществами:
2.1. Оксид кальция взаимодействует с кислотами:
2.1.1. О ксид кальция с разбавленной соляной кислотой образует хлорид кальция и воду:
CaO + 2HCl = CaCl2 + H2O
2.1.2. Оксид кальция вступает во взаимодействие с разбавленной плавиковой кислотой с образованием фторида кальция и воды:
CaO + 2HF = CaF2↓ + H2O
2.1.3. Оксид кальция вступает в реакцию с разбавленной фосфорной кислотой, образуя фосфат кальция и воду:
2.2. Оксид кальция реагирует с оксидами:
2.2.1. Оксид кальция при комнатной температуре реагирует с углекислым газом с образованием карбоната кальция:
CaO + CO2 = CaCO3
2.2.2. Взаимодействуя с оксидом кремния при 1100 — 1200º С оксид кальция образует силикат кальция:
CaO + SiO2 = CaSiO3
2.3. Оксид кальция взаимодействует с водой при комнатной температуре, образуя гидроксид кальция:
Источник
Реакция оксида кальция с водой
Реакция взаимодействия оксида кальция с водой.
Уравнение реакции взаимодействия оксида кальция с водой:
Оксид кальция взаимодействует с водой . Процесс имеет название «гашение извести ».
Реакция оксида кальция с водой протекает при обычных условиях.
В результате реакции оксида кальция с водой образуется гидроксид кальция .
В ходе реакции оксида кальция с водой при стандартных условиях выделяется тепловая энергия (теплота) 65,27 кДж .
Термохимическое уравнение этой реакции имеет следующий вид:
CaO (т) + H2O (ж)= Ca(OH)2 (т) + 65,27 кДж; ΔH = -65,27 кДж/моль.
Таким образом, реакция оксида кальция с водой носит экзотермический характер.
Примечание: © Фото https://www.pexels.com, https://pixabay.com

Мировая экономика
Справочники
Востребованные технологии
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (106 484)
- Экономика Второй индустриализации России (102 475)
- Программа искусственного интеллекта ЭЛИС (27 490)
- Метан, получение, свойства, химические реакции (23 728)
- Этилен (этен), получение, свойства, химические реакции (22 795)
- Природный газ, свойства, химический состав, добыча и применение (21 165)
- Крахмал, свойства, получение и применение (20 570)
- Целлюлоза, свойства, получение и применение (19 414)
- Пропилен (пропен), получение, свойства, химические реакции (19 090)
- Прямоугольный треугольник, свойства, признаки и формулы (18 725)
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник
Оксид кальция с водой нагревание
Курс общей и неорганической химии
(для студентов биологического факультета (биофизиков)
и для студентов факультета биоинженерии и биоинформатики)
Программа курса. Материалы лекций. Презентации лекций. Программа сетевых контрольных мероприятий
Лектор — Загорский Вячеслав Викторович — ст.н.сотр., к.х.н., д.п.н.
Гашение извести
(реакция оксида кальция с водой)
Посмотреть видео:
Гашение извести — реакция взаимодействия оксида кальция [CaO] с водой [H 2 O]. Типичная реакция между основным оксидом щелочноземельного металла и воды. Продукт реакции — соответствующая щелочь. В данном случае гидроксид кальция [Ca(OH) 2 ].
В фарфоровую чашку поместили заранее приготовленную прокаливанием мела негашеную известь. При помощи пипетки прикапали в чашку несколько капель воды. В ходе реакции образовался рыхлый гидроксид кальция [Ca(OH) 2 ].
Автор и оператор
Загорский В.В.
Ассистент
Петрова Е.П.
Подготовка публикации
Мочалыгин А.Г.
Редактирование
Миняйлов В.В.


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
Источник
Структура, свойства и применение оксида кальция (CaO)
оксид кальция (CaO) является неорганическим соединением, которое содержит кальций и кислород в ионных формах (не путать с пероксидом кальция, CaO2). Это известно во всем мире как известь, слово, которое обозначает любое неорганическое соединение, которое содержит карбонаты, оксиды и гидроксиды кальция, а также другие металлы, такие как кремний, алюминий и железо..
Этот оксид (или известь) также в разговорной речи называют негашеной или гашеной известью, в зависимости от того, гидратирована она или нет. Известь является оксидом кальция, а гашеная известь — его гидроксидом. В свою очередь, известняк (известняк или затвердевшая известь) на самом деле является осадочной породой, состоящей в основном из карбоната кальция (CaCO3).
Это один из крупнейших природных источников кальция и является сырьем для производства оксида кальция. Как получается этот оксид? Карбонаты подвержены термическому разложению; нагревание карбонатов кальция при температуре выше 825 ° С, что приводит к образованию извести и углекислого газа.
Вышеприведенное утверждение можно описать следующим образом: CaCO3(s) → CaO (s) + CO2(G). Поскольку земная кора богата известняком и кальцитом, а в океанах и на пляжах имеются многочисленные морские раковины (сырье для производства оксида кальция), оксид кальция является относительно дешевым реагентом.
- 1 Формула
- 2 Структура
- 3 свойства
- 3.1 Растворимость
- 4 использования
- 4.1 В качестве раствора
- 4.2 При производстве очков
- 4.3 В майнинге
- 4.4 Как средство для удаления силикатов
- 5 наночастиц оксида кальция
- 6 Ссылки
формула
Химическая формула оксида кальция — СаО, в котором кальций подобен кислотному иону (акцептору электронов) Са 2+ , и кислород в качестве основного иона (донора электронов) ИЛИ 2— .
Почему кальций имеет +2 заряда? Потому что кальций принадлежит к группе 2 периодической таблицы (г-н Бекамбара) и имеет только два валентных электрона, доступных для образования связей, которые уступают атому кислорода.
структура
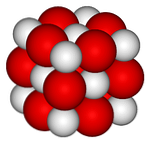
На верхнем изображении представлена кристаллическая структура (типа драгоценной соли) для оксида кальция. Объемные красные сферы соответствуют ионам Ca 2+ и белые сферы с ионами O 2- .
В этом кубическом кристаллическом расположении каждый ион Са 2+ окружен шестью ионами O 2- , закупорены в октаэдрических отверстиях, оставленных между ними большими ионами.
Эта структура максимально выражает ионный характер этого оксида, хотя заметное различие радиусов (красная сфера больше, чем белая) придает более слабую кристаллическую ретикулярную энергию по сравнению с MgO.
свойства
Физически это кристаллическое белое твердое вещество без запаха и с сильными электростатическими взаимодействиями, которые ответственны за его высокие температуры плавления (2572 ° C) и кипения (2850 ° C). Кроме того, он имеет молекулярную массу 55,958 г / моль и интересную способность быть термолюминесцентным.
Это означает, что кусок оксида кальция, подверженный воздействию пламени, может сиять интенсивным белым светом, известным на английском языке под названием центр внимания, или по-испански, легкий кальций. Ионы Са 2+ , при соприкосновении с огнем они вызывают красноватое пламя, как показано на следующем изображении.
растворимость
CaO является основным оксидом, который обладает сильным сродством к воде в той степени, в которой он поглощает влагу (это гигроскопичное твердое вещество), и немедленно реагирует с образованием гашеной извести или гидроксида кальция:
Эта реакция является экзотермической (выделяет тепло) из-за образования твердого тела с более сильными взаимодействиями и более стабильной кристаллической решеткой. Тем не менее, реакция является обратимой, если Ca (OH) нагревается2, обезвоживание и освещение гашеной извести; затем лайм «возрождается».
Полученный раствор является очень основным, и если он насыщен оксидом кальция, он достигает рН 12,8.
Кроме того, он растворим в глицерине и в растворах кислоты и сахара. Поскольку это основной оксид, он, естественно, имеет эффективные взаимодействия с кислотными оксидами (SiO2, в2О3 и вера2О3, например) растворим в их жидких фазах. С другой стороны, он нерастворим в спиртах и органических растворителях.
приложений
CaO широко используется в промышленности, а также для синтеза ацетилена (CH≡CH), для извлечения фосфатов из сточных вод и в реакции с диоксидом серы из газообразных отходов..
Другие применения оксида кальция описаны ниже:
Как ступка
Если оксид кальция смешан с песком (SiO2) и вода спекается с песком и медленно реагирует с водой с образованием гашеной извести. В свою очередь, СО2 воздуха растворяется в воде и вступает в реакцию с солью с образованием карбоната кальция:
CaCO3 Это более стойкое и более твердое соединение, чем CaO, в результате чего раствор (предыдущая смесь) затвердевает и фиксирует кирпичи, блоки или керамику между ними или на желаемой поверхности..
В производстве очков
Основным сырьем для производства стекол являются оксиды кремния, которые смешивают с известью, карбонатом натрия (Na2Колорадо3) и другие добавки, которые затем подвергают нагреванию, в результате чего получается стеклообразное твердое вещество. Это твердое вещество впоследствии нагревается и выдувается в любых фигурах.
В горном деле
Гашеная известь занимает больший объем, чем негашеная, благодаря взаимодействиям водородных связей (О-Н-О). Это свойство используется, чтобы разбить камни изнутри.
Это достигается путем наполнения их компактной смесью извести и воды, которая герметизирована, чтобы сосредоточить ее тепло и экспансивную силу в породе..
Как средство для удаления силикатов
CaO сплавляется с силикатами с образованием коалесцирующей жидкости, которая затем извлекается из сырья определенного продукта..
Например, железные руды являются сырьем для производства металлического железа и стали. Эти минералы содержат силикаты, которые являются нежелательными примесями для процесса и устраняются только что описанным способом..
Наночастицы оксида кальция
Оксид кальция можно синтезировать в виде наночастиц, варьируя концентрации нитрата кальция (Са (NO3)2) и гидроксид натрия (NaOH) в растворе.
Эти частицы являются сферическими, основными (а также твердыми на макроуровне) и имеют большую площадь поверхности. Следовательно, эти свойства выгодны каталитическим процессам. Что? В настоящее время следствие отвечает на этот вопрос.
Эти наночастицы были использованы для синтеза замещенных органических соединений, полученных из пиридинов, при разработке новых лекарств для проведения химических превращений, таких как искусственный фотосинтез, для очистки воды от тяжелых и вредных металлов, а также для фотокаталитические агенты.
Наночастицы могут быть синтезированы на биологической подложке, такой как листья папайи и зеленый чай, для использования в качестве антибактериального средства..
Источник