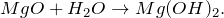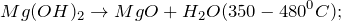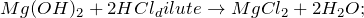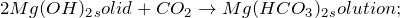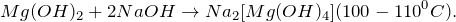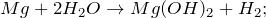- Оксид магния: способы получения и химические свойства
- Способ получения
- Химические свойства
- MgO + H2O = ? уравнение реакции
- В какие реакции вступает оксид магния
- Примеры реакций оксида магния
- Реакции MgO с кислотными оксидами
- Реакции с амфотерным оксидами:
- Как MgO реагирует с водой?
- Как оксид магния реагирует с водой?
- Acetyl
Оксид магния: способы получения и химические свойства
Оксид магния MgO — бинарное неорганическое вещество . Белый, тугоплавкий, термически устойчивый, не реагирует с водой. Проявляет основные свойства.
Относительная молекулярная масса Mr = 40,3; относительная плотность для тв. и ж. состояния d = 3,62; tпл ≈ 2825º C; tкип = 3600º C.
Способ получения
1. Оксид магния получается при разложении карбоната магния при температуре 350 — 650º C. В результате разложения образуется оксид магния и углекислый газ:
2. В результате разложения нитрата магния при температуре выше 300º С образуется оксид магния, оксид азота (IV) и кислород:
3. Гидроксид магния разлагается при 350-480º С с образованием оксида магния и воды:
4. Оксид магния можно получить путем разложения сульфата магния при температуре выше 1200º C, образуется оксид магния, кислород и оксид серы (IV):
5. Оксид магния можно получить сжиганием магния в в кислороде при 600 — 650º С:
2Mg + O2 = 2MgO
Химические свойства
1. Оксид магния реагирует с простыми веществами :
1.1. В результате реакции между оксидом магния и кальцием при температуре выше 400º С образуется магний и оксид кальция:
MgO + Ca = CaO + Mg
1.2. Оксид магния реагирует с углеродом при температуре выше 2000º С и образует магний и угарный газ:
MgO + C = Mg + CO
2. Оксид магния взаимодействует со сложными веществами:
2.1. Оксид магния взаимодействует с кислотами . При этом образуются соль и вода.
2.1.1. О ксид магния с разбавленной соляной кислотой образует хлорид магния и воду:
MgO + 2HCl = MgCl2 + H2O
2.3. Оксид магния взаимодействует с водой при 100 — 125º С, образуя гидроксид магния:
Источник
MgO + H2O = ? уравнение реакции
Помогите составить химическое уравнение по схеме MgO + H2O = ? Расставьте стехиометрические коэффициенты. Укажите тип взаимодействия. Запишите молекулярное уравнение реакции. Охарактеризуйте полученное соединение: укажите основные физические и химические свойства, способы получения.
В результате взаимодействия оксида магния с водой (MgO + H2O = ?) происходит образование нерастворимого в воде основания – гидроксида магния (соединение). Молекулярное уравнение реакции имеет вид:
Гидроксид магния представляет собой вещество белого цвета, кристаллы которого при нагревании разлагаются. Не растворяется в воде. Проявляет основные свойства, реагирует с кислотами, кислотными оксидами. В жестких условиях образует гидроксокомплексы. Поглощает углекислый газ из воздуха. Переводится в раствор солями аммония.
Кроме вышеописанного способа гидроксид магния получают растворением металла в воде:
а также по любой реакции, удовлетворяющей сокращенному-ионному уравнению
Источник
В какие реакции вступает оксид магния
Всё о химических свойствах оксида магния
Оксид магния — порошкообразное вещество, которое в природе встречается в форме минерала периклаз. Порошок этот очень тугоплавкий (расплав образуется при температуре свыше 2650 ⁰С).
Оксид магния легко впитывает влагу, благодаря чему он нашел широкое применение. Оксид магния применяется в пищевой промышленности (кодируется как пищевая добавка Е 530) против комкообразования и слеживания.
В медицине MgO используется как антацид (средство против повышенной кислотности в желудке), как слабительное или как вспомогательное вещество во многих лекарствах, которые выпускаются в форме таблеток.
Нашел MgO широкое распространение и как наполнитель в производстве резины, огнеупоров, цемента, а также в качестве мелкого абразива в электронной промышленности.
Интересное оптическое свойство порошка оксида магния обуслаливает его применение в качестве эталонного отражателя: в широком спектре его коэффициент отражения равен 1.
Одно из названий MgO — жженая магнезия, так как он получается при обжиге минералов магнезита и доломита:
Получить это вещество можно простым способом — взаимодействием магния и кислорода:
Будучи основным оксидом, MgO вступает в реакции с:
- водой, образуя гидроксид магния (о нюансах этой реакции расскажем чуть позже);
- с кислотами, образуя соли и воду;
- с кислотными оксидами, образуя сложные соли;
- c амфотерным оксидами при сплавлении образует сложные вещества — двойные оксиды.
Примеры реакций оксида магния
Растворение в кислотах:
- MgO + HCl (разб) → MgCl₂ + H₂O (для протекания реакции нужны неконцентрированные кислоты)
- MgO + H₂SO₄ → MgSO₄ + H₂O В реакциях с кислотами MgO показывает общие свойства оксидов (образуя соль и воду).
Реакции MgO с кислотными оксидами
MgO + SO₃ → MgSO₄ — образуется сульфат магния
MgO + СO₃ → MgСO₃ — образуется карбонат магния
Реакции с амфотерным оксидами:
Al₂O₃ + MgO → MgAl₂O₄
В этой реакции оксида магния с оксидом алюминия образуется алюминат магния (двойной оксид магния и алюминия). Реакция протекает при высокой температуре (свыше 1500 ⁰С).
Как MgO реагирует с водой?
Являясь основным оксидом, MgO взаимодействует с водой, образуя основание — гидроксид магния.
С холодной водой оксид магния реагирует очень медленно, но если реакцию проводить с водяным паром, реакция пойдет быстрее.
MgO + H₂O (вода в виде горячего пара) → Mg(OH)₂
В результате этой реакции образуется гидроксид магния
А вот если у экспериментатора есть полоска магния, можно провести очень зрелищный опыт:
- полоску металла частично опустить в стакан с водой;
- поджечь оставшуюся часть магния.
Mg + 2H₂O = Mg(OH)₂ + H₂↑
Горение магния продолжается даже в воде. При этом выделяющийся водород тоже вступает в реакцию горения.
Внимание! Не пытайтесь повторить этот опыт самостоятельно!
Источник
Как оксид магния реагирует с водой?
Как оксид магния реагирует в воде?
MgO + H2O → Mg (HO) 2.
Оксид магния реагирует с ионизированной водой с образованием гидроксида магния. Это комбинированная реакция. Эта реакция протекает при температуре, значительно превышающей комнатную, около 120 ° С, и ее можно обратить вспять путем повторного нагревания гидроксида магния.
Металлы магния не подвержены воздействию воды при комнатной температуре. Магний обычно является медленно реагирующим элементом, но реакционная способность увеличивается с увеличением уровня кислорода. Кроме того, магний реагирует с водяным паром с гидроксидом магния и газообразным водородом:
Mg (s) + 2H2O (г) -> Mg (OH) 2 (водн.) + H2 (г)
Магниевые пожары нельзя потушить водой. Магний продолжает гореть после истощения кислорода. Затем он реагирует с азотом из воздуха с образованием нитрида магния (Mg3N2). Когда предпринимаются попытки тушения пожаров магния водой, магний агрессивно реагирует с газообразным водородом. Чтобы предотвратить любое повреждение, магниевый огонь должен быть покрыт песком.
Оксид магния будет реагировать с водой, но кислотно-щелочное равновесие лежит далеко налево (что означает, что реакция благоприятствует MgO и H2O), частично потому, что MgO не очень растворим в воде. Продуктом реакции является Mg (OH) 2. Растворение MgO в воде сделает воду слабощелочной, но достаточно щелочной, чтобы ее можно было проверить лакмусовой бумагой.
Вот почему люди принимают MgO от изжоги. Он выделяет небольшие контролируемые количества ОН-, которые нейтрализуют избыток желудочной кислоты, пока либо не израсходуется MgO (когда вам нужно принять еще одну таблетку), либо кислота.
Химическое уравнение: MgO + H2O (горячая вода) = Mg (OH) 2
Комбинированная реакция должна реагировать в горячей воде.
Он не будет реагировать при нормальной температуре.
Он будет реагировать, но очень медленно из-за недостаточной растворимости оксида в воде. Небольшая часть будет образовывать гидроксид, который является основанием и может быть обнаружен путем погружения лакмусовой бумаги в раствор.
Источник
Acetyl
Это пилотный ролик из серии об органических реакциях.
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Источник |