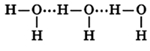- Описать химическое вещество вода
- Физические свойства воды
- Химические свойства воды
- Вода в жизнедеятельности человека. Водные растворы
- Вода (H2O)
- Физические свойства воды
- Строение молекулы воды
- Химические свойства воды
- Растворимость веществ в воде
- Что такое вода: агрегатные состояния, роль на Земле
- Что такое вода, химические названия
- Агрегатные состояния
- Строение в различных агрегатных состояниях
- Свойства
- Круговорот воды в природе
- Происхождение воды на планете
- Наука о воде
- Значение на Земле
- Применение
- Сколько жидкости в теле человека
- Основные функции
- Польза чистой питьевой воды
- Сколько нужно пить воды в день
- Процентное содержание в органах
- Признаки обезвоживания
- Запасы пресной воды
- Показатели качества
- 25 интересных фактов
- Заключение
Описать химическое вещество вода
Ключевые слова конспекта: вода, физические и химические свойства воды, водные растворы.
Физические свойства воды
Чистая вода — прозрачная жидкость, без цвета, вкуса и запаха, плотность 1 кг/л, температура кипения 100 °С при 1 атм, температура плавления 0°С. У воды высокая удельная теплоемкость — 4,12 кДж/кг К), поэтому она долго нагревается и медленно остывает. У воды большая теплота испарения. На испарение 1 г воды требуется 2,25 кДж теплоты.
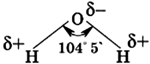
Атомы Н и О в молекуле воды соединены полярными ковалентными связями. На атоме водорода в молекуле Н2О имеется небольшой положительный заряд δ+, а на атоме кислорода — небольшой отрицательный δ-. Поскольку молекула воды имеет уголковое строение, она представляет собой двухполюсную частицу — диполь: 
Химические свойства воды
Вода реагирует со многими металлами по типу реакций замещения.
С наиболее активными металлами — от Li по Аl в ряду активности металлов при комнатной температуре протекают реакции замещения одного атома Н в молекуле Н2O. С магнием реакция идет при нагревании, с алюминием — после снятия защитной оксидной пленки. В реакции образуются гидроксиды металлов — соединения, содержащие гидроксогруппу ОН, и водород:
2Li + 2Н2O = 2LiOH + Н2↑,
Са + 2Н2O = Са(ОН)2 + Н2↑.
Менее активные металлы — Zn, Mo, W, Fe — взаимодействуют с водой при высокой температуре (400-600 °С). В этих реакциях образуются оксиды металлов и водород:
Zn + Н2O = ZnO + Н2↑,
3Fe + 4Н2O = Fe3O4 + 4Н2↑
Вода реагирует с оксидами активных металлов (реакция гидратации). При этом получаются растворимые в воде гидроксиды металлов — щелочи:
Na2O + Н2O = 2NaOH,
СаО + Н2O = Са(ОН)2.
Вода соединяется с оксидами многих неметаллов. При этом получаются растворимые в воде гидроксиды неметаллов — кислоты:
СO2 + Н2O = Н2СO3,
SO3 + Н2O = H2SO4.
Гидролиз — это обратимая реакция обмена, например соли с водой. При этом происходит расщепление молекул воды на Н и ОН, которые входят в состав двух новых веществ:
К2СO3 + Н2O = КНСО3 + КОН,
РСl3 + ЗН2O = Н3РО3 + ЗНСl.
Вода в жизнедеятельности человека. Водные растворы
Вода — жизненная среда всех живых организмов. Человек живет на суше, но его организм на 65-70% состоит из воды. Все процессы в живой клетке осуществляются в водной среде. В сутки человеку необходимо 2 л питьевой воды. Кроме того, вода нужна, чтобы варить пищу, стирать белье, умываться. Большие количества пресной воды расходуются в промышленности и сельском хозяйстве (растворитель). Отметим, что соленая вода морей и океанов для этих целей непригодна. Доля пресной воды в общих запасах воды на Земле составляет менее 3% от всех водных ресурсов.
Вода — химический реагент. Соединяясь с оксидами активных металлов, вода образует щелочи, а в реакциях с оксидами неметаллов дает кислоты — два больших и важных в деятельности человека класса веществ. Один из способов синтеза этилового спирта (этанола) C2H5OH — реакция этилена С2Н4 с водой:
Жесткость воды — это свойства воды, обусловленные содержанием в ней ионов Са 2+ , Mg 2+ , Fe 2+ . Если концентрация этих ионов велика, то воду называют жесткой, если мала — мягкой. При стирке с мылом в жесткой воде образуются осадки, часть мыла уходит в осадок и ухудшается качество ткани. Такая вода непригодна для охлаждения в радиаторах автомобилей, в паровых котлах и стиральных машинах. При нагревании жесткой воды образуется накипь, которая забивает трубы и ускоряет изнашивание механизмов. Различают временную и постоянную жесткость воды.
Временная или карбонатная жесткость вызвана присутствием растворенных гидрокарбонатов кальция Са(НСО3)2, магния Mg(HCO3)2 и железа Fe(HCO3)2. При кипячении воды гидрокарбонаты разлагаются с образованием осадка карбоната, и жесткость воды снижается:
Са(НСO3)2 = СаСО3↓ + СO2↓ + Н2O,
Fe(HCO3)2 = FeCO3↓ + CO2↓ + Н2O.
Другой способ устранения временной жесткости — действие известкового молока или соды:
Постоянная жесткость воды обусловлена присутствием в ней хлоридов, сульфатов и других растворимых солей кальция, магния и железа. Ее устраняют действием соды:
СаСl2 + Na2CO3 = СаСO3↓ + 2NaCl.
Водный раствор — разновидность раствора, в котором растворителем служит вода. Будучи превосходным растворителем, именно вода используется для приготовления большинства растворов в химии.
Вещества, которые плохо растворяются в воде, называют гидрофобными (‘боящимися воды’), а хорошо в ней растворяющиеся — гидрофильными (‘любящими воду’). Примером типичного гидрофильного соединения может служить хлорид натрия (поваренная соль).
Если вещество образует водный раствор, который хорошо проводит электрический ток, то он называется сильным электролитом; в противном случае — слабым.
Конспект урока по химии «Вода. Свойства воды. Водные растворы». Выберите дальнейшее действие:
Источник
Вода (H2O)
Оксид водорода (H2O), гораздо более известный всем нам под названием «вода», без преувеличения, является главной жидкостью в жизнедеятельности организмов на Земле, ибо все химико-билогические реакции проходят, либо с участием воды, либо в растворах.
Вода является вторым, после воздуха, самым важным веществом для организма человека. Прожить без воды человек может не более 7-8 суток.
Чистая вода в природе может существовать в трех агрегатных состояниях: в твердом — в виде льда, в жикдом, собственно вода, в газообразном — в виде пара. Таким разнообразием агрегатных состояний в природе больше не может похвастаться ни одно вещество.
Физические свойства воды
- при н.у. — это жидкость без цвета, запаха и вкуса;
- вода обладает высокой теплоёмкостью и низкой электропроводностью;
- температура плавления 0°C;
- температура кипения 100°C;
- максимальная плотность воды при 4°C равна 1 г/см 3 ;
- вода — хороший растворитель.
Строение молекулы воды
Молекула воды состоит из одного атома кислорода, который соединен с двумя атомами водорода, при этом связи O-H образуют угол в 104,5°, при при этом общие электронные пары смещены к атому кислорода, который более электроотрицателен по сравнению с атомами водорода, поэтому, на атоме кислорода формируется частичный отрицательный заряд, соответственно, на атомах водорода — положительный. Таким образом, молекулу воды можно рассматривать, как диполь.
Молекулы воды могут между собой образовывать водородные связи, притягиваясь противоположно заряженными частями (на рисунке водородные связи показаны пунктиром):
Формирование водородных связей объясняет высокую плотность воды, температуру ее кипения и плавления.
Количество водородных связей зависит от температуры — чем выше температура, тем меньшее кол-во связей образуется: в парах воды присутствуют только отдельные ее молекулы; в жидком состоянии — образуются ассоциаты (H2O)n, в кристаллическом состоянии каждая молекула воды связана с соседними молекулами четырьмя водородными связями.
Химические свойства воды
Вода «охотно» вступает в реакции с другими веществами:
- с щелочными и щелочноземельными металлами вода реагирует при н.у.:
- с менее активными металлами и неметаллами вода реагирует только при высокой температуре:
- с основными оксидами при н.у. вода реагирует с образованием оснований:
- с кислотными оксидами при н.у. вода реагирует с образованием кислот:
- вода является главным участником реакций гидролиза (подробнее см. Гидролиз солей);
- вода участвует в реакциях гидратации, присоединяясь к органическим веществам с двойными и тройными связями.
Растворимость веществ в воде
- хорошо растворимые вещества — в 100 г воды растворяется более 1 г вещества при н.у.;
- малорастворимые вещества — в 100 г воды растворяется 0,01-1 г вещества;
- практически нерастворимые вещества — в 100 г водры растворяется менее 0,01 г вещества.
Совершенно нерастворимых веществ в природе не существует.
При растворении многих веществ в воде вокруг их молекул образуется оболочка из молекул воды — такой «слоеный пирог» называется гидратом. После кристаллизации в составе таких комплексов сохраняются некоторая часть молекул воды, образуя кристаллогидрат:
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Источник
Что такое вода: агрегатные состояния, роль на Земле
Вода — самая удивительная и загадочная из всех жидкостей, существующих на Земле.
Учёные на протяжении многих столетий продолжают проводить исследования, находя новые интересные факты. Каждый человек знает, что без воды жизнь невозможна.
Вода участвует в формировании климата, для многих живых организмов является средой обитания. Её важность сложно недооценить. Не случайно, нашу планету называют голубой, именно вода покрывает 71 % поверхности земного шара.
В статье мы собрали самую важную и интересную информацию про воду: гипотезы её появления на нашей планете, особенности строения молекулы, агрегатные состояния, уникальные и необычные свойства.
Что такое вода, химические названия
Вода — это бинарное неорганическое соединение, химическая формула H2O.
При нормальных условиях представляет собой прозрачную, бесцветную жидкость, которая не имеет вкуса и запаха, текуча (принимает форму сосуда).
Молекула воды состоит из одного атома кислорода и двух атомов водорода, которые соединены между собой ковалентной связью. Никакие другие элементы таблицы Менделеева при соединении не образуют жидкости. Рассмотрим строение молекулы H2O на изображении.
Вода имеет несколько химических названий:
- оксид водорода;
- гидроксид водорода;
- монооксид дигидрогена;
- дигидромонооксид;
- гидроксильная кислота.
Агрегатные состояния
Из всех веществ, существующих на Земле, только вода может иметь три принципиально разных агрегатных состояния: жидкое, газообразное и твердое. Благодаря трём агрегатным состояниям происходит круговорот воды в природе и жизнь на Земле. Рассмотрим подробнее каждое агрегатное состояние.
- Жидкое (вода). В нормальных условиях вода является жидкостью. Образует мировой океан, реки, ручьи и т.д.
- Газообразное (водяной пар) — это бесцветный газ, не имеет вкуса и запаха. Испаряется с поверхности океанов, рек, болот, почвы, растений и поступает в воздух или образуется путём кипения жидкой воды или сублимации из льда. Сублимация — переход вещества из твёрдого состояния сразу в газообразное, минуя стадию плавления (перехода в жидкое состояние).
- Твердое (лёд). При температуре от нуля и ниже вода превращается в лёд. В холодное время года он сковывает реки и лужи, выпадает в виде осадков: снежинок, града, инея, образует ледяные облака. Встречается в виде ледников и айсбергов.
Строение в различных агрегатных состояниях
Жидкая вода, лёд и водяной пар имеют один и тот же состав, но разные состояния.
Рассмотрим строение молекулы на изображении.
Многочисленные исследования ученых подтверждают, что по структуре вода и лед близки друг к другу. Структура льда – это решетчатый каркас. Структура воды зависит от содержания разных веществ, которые в ней растворяются, а также от нерастворимых соединений и некоторых других факторов.
В воде возникают структуры, которые стали называть «кластерами» — группа атомов или молекул, которые представляют собой единую структуру, но внутри имеют свои индивидуальные особенности.
При температуре близкой к точке замерзания, молекулы жидкой воды собираются в небольшие группы, практически так, как в кристаллах. При температуре близкой к точке кипения они располагаются более свободно.
Свойства
Вода — уникальный природный компонент, который обладает рядом свойств. Рассмотрим основные:
- не имеет цвета, запаха и вкуса;
- распространенный растворитель;
- обладает высоким поверхностным натяжением, уступая в этом только ртути;
- имеет большую теплоту испарения (используется для терморегуляции);
- чистая вода — хороший изолятор;
- обладает большой теплоёмкостью (увеличение тепловой энергии вызывает лишь сравнительно небольшое повышение ее температуры);
- плотность в разных диапазонах температур меняется неодинаково.
Существуют необычные свойства. Например, в твердом виде вода легче, чем в жидком. Лёд не тонет в воде. В твёрдом состоянии частички воды располагаются по порядку, между ними остается много свободного пространства. Когда лёд тает, активность частичек повышается, свободное пространство заполняется. Жидкая форма становится более тяжелой, нежели твердая.
Такая уникальная способность даёт возможность любому водоёму не замерзать по всей глубине. Даже при самом сильном морозе температура воды у дна не опускается ниже +4 ᵒС. Все живые существа (рыбы и другие) могут спокойно пережить самую суровую зиму подо льдом.
Когда лёд тает, плотность увеличивается, и становится максимальной при температуре +4 ᵒС. В диапазоне от +4 ᵒС до +40 ᵒС плотность снижается, потом снова увеличивается. При понижении температуры ниже +4 ᵒС плотность уменьшается, т.е. при замерзании вода расширяется.
Горячая вода замерзает быстрее, чем холодная. Это связано с большей скоростью испарения и излучения тепла.
Теплоемкость и некоторые другие физические свойства воды тоже зависят от температуры неодинаково. Другие виды жидкостей не имеют таких особенностей – чтобы какой-то один параметр менялся по-разному на разных порогах температуры.
Круговорот воды в природе
Вода образует водную оболочку нашей планеты – гидросферу.
Её делят на Мировой океан, континентальные поверхностные воды и ледники, а также подземные водоёмы. Переходы H2O из одних частей гидросферы в другие составляют сложный круговорот воды на Земле
Круговорот воды в природе — это непрерывное движение воды в гидросфере Земли. В процессе этого обмена водная масса меняет агрегатное состояние: из жидкой или твердой превращается в газообразную и обратно.
Рассмотрим на примере.
- С поверхности океанов, морей, рек и суши вода в виде пара поднимается вверх.
- Высоко над землей он охлаждается и образует множество водяных капелек и льдинок. Из них образуются облака.
- В виде осадков вода возвращается на Землю.
Происхождение воды на планете
Возникновение воды на нашей планете является предметом научных споров. Существует 2 основные гипотезы:
- Космическое происхождение. Часть учёных считают, что вода появилась вследствие падающих метеоритов, астероидов, которые содержали воду.
- Земное происхождение. Другие учёные считают, что вода образовалась на Земле во время формирования, а не занесена с космоса.
Наука о воде
Изучением природных вод, явлений и процессов занимается наука Гидрология.
Первые упоминания о гидрологии появились на заре истории человечества около 6000 лет назад.
Начало гидрологических наблюдений в России относится к XV–XVI вв.: в записях русских летописцев сохранились сведения о свойствах воды, наводнениях, паводках, замерзании.
Значение на Земле
Без воздуха человек может прожить несколько секунд, без еды – несколько месяцев, без воды – максимум несколько суток. Снижение содержания воды в организме всего лишь на 2% может вызвать сильную слабость. При нехватке 8% уже может возникнуть серьезное недомогание, а при 12% – смерть.
Каждая клетка живого организма состоит из жидкости и нуждается в регулярном пополнении. Без воды не проживут ни люди, ни растения, ни животные.
Вода формирует климат, участвует в круговороте воды в природе, для многих живых организмов является средой обитания.
Применение
Все люди на планете прекрасно знают, что жизнь без воды невозможна. Любое начало жизни изначально зарождается в воде.
Человек применяет воду:
- для поддержании жизни (приготовления пищи, обеспечения организма водой);
- для бытовых нужд (гигиены, уборки и т. д);
- в сельском хозяйстве и животноводстве;
- промышленности (используется при производстве продуктов питания, чугуна, стали, резины и т. д);
- медицине;
- химии (в качестве реагента для химических реакций, опытов, исследований);
- рыболовстве;
- для транспортировки людей и грузов;
- для спорта;
- в земледелии;
- для пожаротушения;
- служит источником энергии (электростанции).
Сколько жидкости в теле человека
Эмбрион человека состоит из жидкости не менее, чем на 97%. Когда ребенок рождается, вода составляет около 80% его тела. В первые несколько суток после рождения этот показатель существенно снижается.
В дальнейшем содержание воды в организме человека постоянно уменьшается. В пожилом возрасте в теле человека доля воды не превышает 50-60%.
Как определить, сколько воды в теле человека?
Массу тела необходимо разделить на 3 и умножить на 2.
Стоит отметить, что расчет считается приблизительным (может отличаться на 5-10%) Так как количество воды зависит от возраста, пола, физической активности, состояния здоровья.
Основные функции
Вода необходима каждому живому существу. Каждый живой организм состоит из клеток. Ключевую роль выполняет вода. Она составляет около 70 процентов от её массы. Рассмотрим кратко основные функции.
- Растворитель. Большинство химических реакций протекают только в водной среде.
- Транспортная функция. Переносит питательные вещества из одной части в другую.
- Функция регенерации. С помощью воды удаляются ненужные продукты жизнедеятельности.
- Регулирует терморегуляцию. Защищает организм от перегрева и обеспечивает равномерное распределение тепла по организму.
- Все обменные процессы в организме регулируются водой.
Польза чистой питьевой воды
Врачи, диетологи и другие специалисты часто совершают ошибку, когда слишком много внимания уделяют разным продуктам питания и забывают про воду. Любые вещества, даже самые питательные и полезные, могут оказаться совершенно неэффективными, если нет растворителя, способного доставить их в нужные части тела. На Земле есть только один простой, надежный и распространенный растворитель – вода.
Вода участвует абсолютно во всех обменных процессах. И чтобы они протекали нормально, необходимо пить достаточное количество чистой воды. Именно воды, не чая, не напитков. Содержание разных примесей, консервантов и прочих веществ существенно меняют структуру, нормальное молекулярное состояние воды.
Изначально природой заложено употреблять чистую воду. Когда в организм вносится некая смесь, то пищеварительной системе приходится прикладывать много усилий, растрачивать много энергии, чтобы отделить все лишнее и получить воду. Кроме этого, высокое содержание сахара неизбежно провоцирует нарушение нормального обмена веществ.
Питьевая вода должна быть чистая, свежая, качественная, «живая». Т.е. это должна быть натуральная природная вода, которая при попадании в организм легко проникает во все клетки, служит эффективным растворителем. Она быстро доставляет все питательные вещества к тканям и органам.
Сколько нужно пить воды в день
Рекомендуется употреблять чистую воду без примесей 30-40 мл на 1 кг веса.
для женщины: 1,5 – 2 литра ежедневно;
для мужчины: 2,5 – 5 литров ежедневно.
Количество рекомендуемой нормы зависит от физической активности, климата и веса.
Процентное содержание в органах
Вода в теле человека находится в разных субстанциях и никогда не смешивается в единое целое.
Жидкости больше в тех клетках, в которых обмен веществ протекает более интенсивно. Рассмотрим таблицу № 1.
Таблица № 1. Процент содержания в органах человека
| Органы | Процент содержания |
| Мозг | 90 |
| Лёгкие | 86 |
| Печень | 86 |
| Кровь | 83 |
| Яйцеклетки | 90 |
| Кости | 72 |
| Кожа | 72 |
| Сердце | 75 |
| Желудок | 75 |
| Селезёнка | 77 |
| Почки | 83 |
| Мышцы | 75 |
Признаки обезвоживания
Если содержание воды резко меняется в одну или другую сторону, то это сразу сказывается на общем состоянии здоровья. Чрезмерное количество воды организм переносит намного легче, чем ее нехватку. Рассмотрим основные симптомы проявления нехватки воды в организме человека.
- Жажда – первый сигнал нехватки жидкости в организме.
- У человека возникают твердые каловые массы и запоры.
- Появляется усталость и слабость.
- Возникают головные боли и головокружения.
- Кожа становится сухой.
- Состояние может сопровождаться сильным упадком настроения (вплоть до тяжелой депрессии).
При длительном сохранении такого состояния могут возникнуть проблемы:
- с артериальным давлением;
- нарушением пищеварения;
- заболеваниями органов ЖКТ;
- может появиться диабет, ожирение (или наоборот – истощение, дистрофия);
- появляются зрительные и слуховые галлюцинации (при потери воды 10%);
- сильное обезвоживание может привести к смерти.
Проходя гидрологический цикл, вода может дополняться химическими элементами: ионами, растворенными газами, микроэлементами и т.д.
Воду квалифицируют по следующим признакам:
- по наличию и составу изотопов в молекуле;
- по степени растворения частиц солей и других примесей;
- по источнику;
- по взаимодействию с другими элементами и компонентами;
- по воздействию человека;
- по индивидуальным параметрам.
Рассмотрим некоторые виды на рисунке.
Запасы пресной воды
Несмотря на то, что Земля более, чем на 70% покрыта водой, лишь 1% является пресной (её солёность не превышает 0,5 ‰).
Более 2/3 запасов пресной воды на Земле хранится в ледниках. Крупнейшим водоёмом пресной воды считается озеро Байкал в России.
Показатели качества
В воде, которая течет из кранов современных городских квартир, могут содержаться вредные примеси. Такую воду стали называть словом «техногенная». В ней содержатся металлы, песок, глина, хлор и много чего еще.
Современные нормы очистки водопроводной питьевой воды предполагают использование хлорсодержащих реагентов, которые избавляют воду от инфекций. В дополнение рекомендуется использовать дополнительные методы очистки. Например, фильтры.
Большой популярностью в развитых странах пользуется бутилированная питьевая вода. Она является экологически чистым продуктом. Реализуется в гигиенически чистой ёмкости и соответствует всем установленным требованиям.
25 интересных фактов
Ученые постоянно исследуют оксид водорода, находя интересные факты.
- Лёд не тонет в воде. Дело в том, что плотность льда меньше чем, воды в жидком состоянии. Поэтому морские обитатели продолжают жизнедеятельность. Другие вещества увеличивают плотность при замерзании.
- Большинство загрязнений вымораживаются при образовании льда.
- Более 2/3 запасов пресной воды на Земле хранится в ледниках.
- Вёдра для воды изготавливают в форме конуса для того, чтобы их не разорвало при случайном замерзании воды.
- Теплоёмкость и некоторые другие физические свойства воды зависят от температуры не одинаково.
- Жидкая вода регулирует температуру Земли, водяной пар — влажность воздуха.
- Снег способен отражать лучи света на 75%, а вода только на 5%, поэтому снежные ночи такие светлые.
- В Антарктиде есть озеро с водой, в 11 раз солёнее морской. В нем настолько соленая вода, что не замерзает даже при — 50 С.
- Горячая вода имеет способность замерзать быстрее, чем холодная. Этот факт легко проверить самостоятельно.
- Лёд встречается на полюсах Луны, а также на полюсах Марса и Меркурия.
- В Антарктике находится самый холодный лёд, а вот самым теплым льдом считается Альпийский, так как его температура составляет 0 градусов по Цельсию.
- Температура кипения воды не всегда составляет 100 градусов по Цельсию. Показатель зависит от атмосферного давления. Например, на Эльбрусе — самой высокой вершине Европы (5642 м), — вода закипит при 80,8 °С.
- Примерно на каждые 100 метров вглубь к центру Земли температура кипения увеличивается на 3°C.
- Озеро Байкал — самое большое пресное озеро в мире.
- Для производства 1 тонны стали требуется 300 тонн воды.
- Учёные считают, что мировой океан изучен только на 2-7%.
- На 1 кг тела коровы приходится 600 грамм жидкости.
- В теле рыбы 70-80 процентов.
- В медузе больше 95 процентов.
- Растения на 50-90 процентов состоят из жидкости.
- Вода участвует в фотосинтезе растений.
- Бегемот употребляет около 250 литров воды в сутки.
- Древесное растение Эвкалипт в сутки поглощает из почвы и испаряет 320 л влаги.
- Верблюд способен выпить больше 100 литров воды менее, чем за 15 минут.
- Скалистая белка может жить без воды до 100 дней.
Заключение
Вода – удивительное вещество, обладающее химическими и физическими свойствами. Она формирует климат на планете, для многих живых организмов является средой обитания, необходима для фотосинтеза растений и жизнедеятельности всех живых организмов.
Источник