Экология СПРАВОЧНИК
Информация
Озерная вода
Воды озер по своему химическому составу и минерализации весьма разнообразны. В противоположность морской воде в озерных водах нет постоянства соотношений между основными ионами. Среди озер мира встречаются озера с весьма малой минерализацией (30 мг/л, оз. Онежское) и очень большой соленостью, значительно превышающей соленость морских вод (свыше 300 г/л).[ . ]
Воды открытых водоемов загрязнены гумусовыми веществами — сложными органическими соединениями, содержание которых в речных водах в среднем составляет 5—10 мг/л, в озерных водах колеблется от 1 до 150 мг/л. Природные воды содержат также коллоидные, мелкодисперсные и грубодисперсные примеси. Следует отметить и биологическое загрязнение водоемов (микроорганизмами, простейшими организмами, водорослями и др.).[ . ]
Воды, заполняющие естественные впадины на поверхности Земли, образуют озера. По сути это также водоемы с замедленным водообменом. В нелом на нашей планете запасы пресных озерных вод оценивают в 120 тыс. км3 [25].[ . ]
Вода мелких пресных водоемов (озер) имеет слоистую структуру. Для озер характерны сезонные и периодические процессы. Большое значение для формирования микробных ассоциаций имеют придонные иловые отложения. В то же время прибрежные зоны сходны с почвой. Содержание микроорганизмов в воде пресных водоемов ниже, чем в почвах и илах, но достаточно высоко (1,4 млн. клеток в 1 см3 воды и более). При анализе качественного состава микрофлоры обнаружены представители всех основных физиологических групп микроорганизмов, обеспечивающих круговорот азота, углерода, фосфора и других элементов. В озерной воде отмечается четкое вертикальное распределение бактерий. Максимальное количество бактерий отмечается в летний период, причем в некоторых озерах на значительной глубине (10 л), где было наибольшее количество отмерших водорослей.[ . ]
Озерные воды характеризуются очень большими колебаниями pH — от 1,7 в некоторых вулканических озерах до 12,0 в ряде закрытых озер, например в содовых озерах Восточной Африки и Южной Америки. Почти все озера, воды которых имеют pH меньше 4, располагаются в вулканических областях, куда поступают сильные неорганические кислоты, такие, в частности, как серная кислота. Низкие значения pH также обнаруживаются в природных водах, обогащенных растворенными органическими веществами, например в заболоченных озерах. Ионы Н+ в них образуются за счет совместного участия атмосферных осадков, серных бактерий, восстанавливающих суль-фат-ионы, и катионного обмена в торфяниках, слагающих борта этих водоемов и представленных сфагнумовым мхом. Обычные величины pH для открытых озер колеблются в пределах от 6 до 9, причем они сильно буферируются системой С02—НСОз—СО§ . Величина pH определяется соотношением между С02 и карбонат-ионом, или, точнее, соотношением ионов Н+, образующихся при диссоциации Н2С03, и ионов ОН , образующихся при гидролизе бикарбоната. Очень высокие величины pH встречаются там, где наблюдается абстракция большого количества С02, приводящая к смещению равновесия в системе С02—НСОз-СО -.[ . ]
В озерной воде бактерии кишечной палочки содержались в количестве (2-f-3)-l05 микробных тел в 1 л (мкр. т/л), из них 30% составляли E. Coli, остальные — бактерии Ehterobacter и Citrobacter. Количество энтерококков составляло (1—5)-104 мкр. т/ л с преобладанием видов Str. faecium и Str. faecalis.[ . ]
Химизм озерных вод Тургайской ложбины отличается необычайной пестротой (Муравлев, 1955).[ . ]
При оценке воды, выбранной для закачки в пласт, должно быть уделено внимание микроорганизмам ( бактерии, водоросли, планктон), которые часто встречаются в поверхностных морской п озерных водах преимущественно в теплое время года. 13 результате своей жнзне.ииюлыюстп бактерии, занесенные в пласт, могут вызвать процессы окисления л восстановления минеральных солен с выделением в порах грунта в твердой фазе соединений серы п желез.;:. Водоросли н микроорганизмы могут образовать в призабойной зоне биологическую пленку и снизить поглотительную способность нагнетательной скважины.[ . ]
Накопление озерного органического вещества происходит, как сказано выше, за счет поступления с водосборного бассейна (аллохтонное) и первичной продукции фотосинтезирующих озерных организмов — водорослей и высшей водной растительности (автохтонное). Содержание органического вещества в озерной воде обычно оценивается по концентрации в нем углерода. Общий органический углерод (TOC — total organic carbon) складывается из органического углерода взвесей (РОС — particulate organic carbon) и углерода растворенного органического вещества (DOC — dissolved organic carbon). Растворенное и взвешенное органическое вещество природных вод является основным регулятором метаболизма водных экосистем. Общий органический углерод по способности к биохимической деструкции подразделяется на лабильный (LOC — labile organic carbon), в первую очередь подвергающийся биохимическому окислению, и консервативный. Лабильная часть органического вещества формируется продуктами деструкции гидробионтов и их прижизненными выделениями (метаболитами). В больших озерах накопление лабильной фракции органического вещества происходит в основном за счет первичной продукции и метаболитов фитопланктона. Величина лабильной составляющей в пуле растворенного органического вещества характеризует интенсивность продукционно-де-струкционных процессов, а ее постоянство или резкие межгодовые колебания свидетельствуют о стабильности или дисбалансе экосистемы. Консервативная часть DOC — водное гуминовое вещество — представляет собой единый высокомолекулярный комплекс и формируется преимущественно аллохтонным органическим веществом.[ . ]
Активность озерной воды несколько выше, чем речной и лежит в пределах (8-65), Ю»10 Ки/л, что на 2-3 порядка величин ниже ДКб для питьевой воды.[ . ]
Почти все запасы озерных вод находятся в 16 наиболее крупных озерах. Так, объем озера Байкал — 23 тыс. км3 (51 % всех пресных вод СССР) — в 5 раз превышает суммарный годовой сток всех рек нашей страны.[ . ]
По минерализации воды различают пресные, солоноватые и соленые озера. Степень минерализации озерной воды кроме климатических условий зависит от наличия у озера стока. Верхней границей минерализации воды солоноватых озер считают 35°/00, озера с большим содержанием солей в воде относят к соляным.[ . ]
Химический состав озерных вод приведен в таблице 38. Как видно из этой таблицы, озеро Тыгиш — пресное, сухой остаток воды составляет 358 мг/л — 472 мг/л. Озера Большой Сунгуль и Червяное — солоноватые, сухой остаток воды в оз-.Большой Сунгуль колеблется от 1974 мг/л до 2791 мг/л, а в оз. Червяное — от 3199 мг/л до 5402 мг/л. Концентрация ионов кальция в воде этих трех водоемов примерно одинакова; основные различия в солевом составе воды обусловлены разным содержанием хлоридов, сульфатов, К, Na и Mg. Вода в озерах Большой Сунгуль и Червяное аномально обогащена бромом (1,6 — 4,2 мг/л), бором (1,0 -1,2 мг/л), йодом (0,6 — 0,8 мг/л), что является свидетельством значимого вклада в формирование ее качества разгрузки минерализованных подземных вод.[ . ]
Химический состав озерных вод находится в прямой зависимости от состава пород, слагающих водосбор и ложе озера. В целом рассматриваемые воды по их общему гидрохимическому облику являются типичными водами выщелачивания. Химический состав и общая минерализация их формируется в результате выщелачивания кристаллических пород водосбора водами местного стока. Тем не менее, минералогический состав пород в достаточной мере контрастно сказывается на наличии тех или иных компонентов ионного состава. Анионный состав озерных вод также во многих случаях формируется за счет выщелачивания горных пород.[ . ]
Химический состав озерных вод определяется составом воды питающих притоков и подземных вод. Обычно доминирующими являются ионы НСО , Са2+ и Л 2+; ионы вО -, С1 , №+и К+ содержатся в малых количествах; имеются и биогенные элементы. По питательности содержащихся в воде веществ различают три типа озер (классификация Тинемана): олиготрофный — с малым количеством питательных веществ, большими и средними глубинами.[ . ]
В природных водах озер Урала сурьма имеет ограниченное распространение. Она обнаруживается в водах гидрокарбонатных озер в небольшом количестве — от 0.009 до 0.3 мг/л. (ПДК по СанПиН № 4630-88). Сурьма в озерной воде, вероятно, природного происхождения, не превышает 0.007 мг/л во время весеннего привноса воды. В другое время практически не обнаруживается. В центре озера не отмечалась ни в одной пробе. Встречается только в районе Зимника, Штанной курье и в районе базы Миассово (табл. 11).[ . ]
Сильно минерализованные озерные воды также могут быть эффективно использованы для заводнения пластов. В них, как показали исследования АзНИИ ПД, при солености свыше 22° Б прекращается развитие микрофлоры.[ . ]
Содержание хлорид-ионов в воде природных водоемов варьирует в широких пределах. В речной и озерных водах, особенно в северных районах нашей страны (см. рис. 3.8), концентрация их невелика. Однако с увеличением минерализации воды абсолютное и относительное количество С1 возрастает;, в морях и большей части соляных озер он является главным анионом; в морской воде хлорид-ионы составляют 87% массы всех анионов. Объясняется это хорошей растворимостью хлоридов кальция, магния, натрия (см. п. 2.4.2.2) и малой растворимостью Са504 и СаС03. Поэтому с увеличением солесодержания в воде такие широко распространенные ионы, как БО и С03 (НСО ), достигая величин произведения растворимости в присутствии ионов Са2+ (см. п. 2.4.4), начинают выделяться в осадок, уступая» место иону С1 .[ . ]
Турбулентность втекающих вод. Контраст между плотностью озерной воды и воды притоков оказывает влияние на турбулентные движения вод в озере. При «чистом» поступлении энергии на поверхность земли (например, весной и летом или в дневные часы) воды рек и водотоков будут относительно более теплыми, чем озерные воды, вследствие ограниченной глубины водотоков. Эта разница температуры приводит к различию в плотности вод — втекающие в озеро воды должны иметь меньшую плотность, чем озерные воды, и по этой причине они будут стремиться подняться к поверхности. Если воды притока поступают в озеро на уровне его поверхности («перетекание» на рис. 2.29), то они вызовут незначительную турбулентность вод. Если же втекающие воды проникают на большую глубину, то в озере формируется струя, которая, обладая плавучестью, поднимается к поверхности до определенной глубины (рис. 2.30).[ . ]
Причиной мутности речных и озерных вод могут быть составные части почв и горных пород, вымываемые реками из своего русла, а также талые воды и ливневой смыв, т. е. твердые осадки, смываемые дождями с почвы лесов, полей, лугов и улиц населенных пунктов. Ливневой смыв в период сильных дождей повышает мутность воды в несколько раз. В больших водоемах помутнение воды происходит за счет взмучивания осадков со дна вследствие волнения в ветреную погоду, в результате массового развития одноклеточных водорослей и по другим причинам.[ . ]
Так как вытекающие из озера воды являются смесью речных и озерных вод, то растворенного вещества в них обычно меньше, чем в водах, втекающих в озеро, вследствие разбавления и синтеза биомассы в озере, если озерная вода не отличается значительной трофностью в сравнении с поступающей в озеро речной водой. Концентрация растворенных веществ увеличивается за счет испарения с поверхности озера, что особенно важно для тропических и субтропических регионов.[ . ]
Гидрооптические характеристики воды — цвет и прозрачность — являются чувствительными индикаторами физического и биохимического состояния озерных вод. Вместе с другими физическими показателями они могут быть использованы для выделения различных по происхождению водных масс и изучения их трансформаций в озере, как это делается в настоящее время в отношении водных масс водохранилищ (см. § 203), океанов и морей (см. § 77). Показатели прозрачности и цвета воды использованы для выделения в Ладожском и Онежском озерах водных масс речного происхождения, поверхностных, глубинных и придонных. Они могут служить также показателями для выделения зон загрязнения водоема сточными водами.[ . ]
Одним из самых главных параметров озерной воды является содержание в ней кислорода, так как кислород играет весьма существенную роль в метаболизме водных аэробных организмов. Привнос растворимого в воде кислорода из атмосферы и образование его путем фотосинтеза сбалансированы с его расходом на дыхание аэробных организмов. Результирующее распределение и динамика кислорода имеют первостепенное значение для наличия нутриентов и, следовательно, для органической продуктивности озер. Биологические и химические процессы при этом тесно взаимосвязаны.[ . ]
Таллин, 1973. т. 2, с. 33-96.[ . ]
Средний элементный состав поверхностных вод суши отличается от среднего элементного состава вод Мирового океана. Так, в океанических водах преобладают хлор и натрий, а в речных и озерных — гидрокарбонаты кальция и магния. Отмечаются различия и по степени концентрации ионного состава. Концентрация растворенных в воде солей определяет степень ее солености (жесткости). В океанических водах концентрация растворенных веществ в среднем в 175 раз превышает таковую в водах рек и озер. Из этого не следует, что не может быть сильно опресненных морских вод и сильно засоленных озерных и даже речных вод. Последний случай объясняется тем, что состав речной и озерной воды зависит главным образом от типа почвы и горных пород, через которые она протекает, а также от типа источника питания в виде поверхностного стока или грунтовых вод. Обычно в грунтовой воде содержится больше растворенных веществ, чем в водах поверхностного стока.[ . ]
Результаты вычислений индексов стабильности озерной воды сведены в табл. 1.14.[ . ]
Содержание гуминовых и фульвокислот в речных и озерных водах можно оценить по их цветности. Например, по нашим данным, интервал значений цветности вод бассейна Верхней Волги от 10 до 300° (в среднем 50—60°), а для вод Днепра и других рек, питающих Киевское водохранилище, по данным работы [14]—от 20 до 230°. Согласно корреляции, установленной в работе [15], 1 мг гумусовых веществ увеличивает цветность вод на 5°. Поэтому можно сделать вывод о том, что растворенные органические вещества, образующие прочные комплексные соединения с ионами металлов, вносят существенный вклад в макро-компонентный состав вод, так как в большинстве вод содержание фульвокислот превышает 10 мг/л. В этих условиях расчет степени насыщенности вод карбонатом кальция, по данным валового химического определения, без учета комплексообразования с растворенными органическими веществами вряд ли является правомерным.[ . ]
Метод может быть рекомендован для анализа речных и озерных вод с содержанием сульфатов до 40 мг БО /л, а также для анализа дождевых и снеговых вод, содержащих 1 —10 мг БО /л.[ . ]
В отличие от других металлов ионы №2 и Со2+ в природных водах подвержены гидролизу в меньшей степени. Вклад гидроксокомплексов для никеля становится ощутимым при pH > 6, а для кобальта — при рн > 9. В обоих случаях доминирующими гидроксоформами являются №(ОН)2 и Со(ОН)2. В речных и озерных водах степень закомплексованности никеля и кобальта обычно не превышает 40-50%. Однако несмотря на существенный вклад растворимых форм никеля и кобальта в общее содержание этих металлов в воде, подавляющая их часть переносится речными водами во взвешенном состоянии.[ . ]
Одними из биологических факторов, определяющих выживаемость лептоспир в воде, являются плотность и состав сопутствующей микрофлоры. В аналогичных опытах со стерильной водопроводной водой при pH 7,0 и температуре воды 25—27°С лептоспиры выживали в течение 30—33 дней. Добавление к водопроводной воде посторонней микрофлоры сокращало время выживания L. icterohaemorrhagiae почти вдвое [66]. В опытах по сохранению жизнеспособности L. icterohaemorrhagiae в длительно хранимой в лабораторных условиях озерной воде, зараженной воздушной микрофлорой в концентрации 1 млн. микробных тел в 1 мл, лептоспиры выживали 55 дней при 25—32°С [67]. В почве, загрязненной мочой инфицированных животных, лептоспиры обнаруживались в течение 15 дней [68].[ . ]
Наименьшей величиной окисляемости (—2 мг/л, 02) характеризуются артезианские воды. Окисляемость грунтовых вод зависит от глубины их залегания. Грунтовые незагрязненные воды имеют окисляемость, близкую-к окисляемости артезианских вод. Окисляемость чистых озерных вод в среднем составляет 5—8 мг/л кислорода; в речной воде она колеблется в широких пределах, доходя до 60 мг/л и более. Высокой окисляемостью воды отличаются реки, бассейны которых расположены в болотистых местностях. В болотных водах в некоторых случаях она достигает 400 мг/л.[ . ]
| Превращения фосфата [14]. Схематически изображены локализация фосфора в воде и обменные процессы между различными локализациями. Hayes и Phillips [22] предположили, что время цикла (время, необходимое для потери из фазы всего имеющегося фосфора) колеблется от 5 мин для обмена между растворенным неорганическим фосфатом и фитопланктоном до многих дней для некоторых других обменов. Самые медленные процессы, по-видимому,— это обмен между водой и осадком ( | 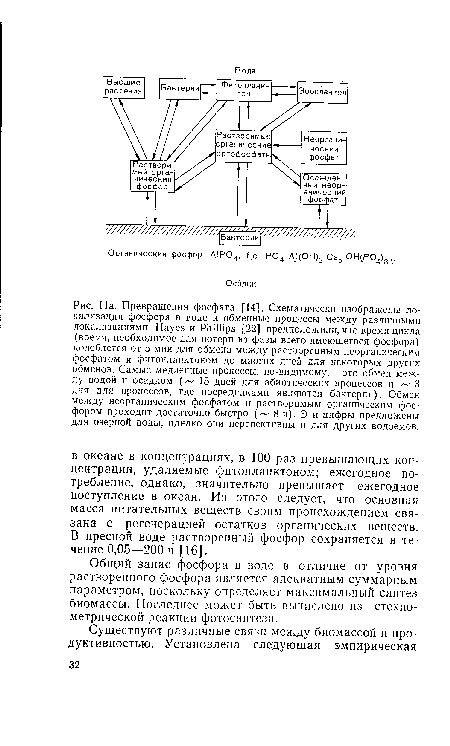 |
Результаты последних исследований показали, что практически во 1 ; типах природных вод присутствует растворенная газообразная ртуть и I имущественно в атомарном состоянии Н ° [316, 336, 445, 512]. Уровен : содержания значительно колеблется в разных типах вод. По первонач ным оценкам содержание газообразной ртути Н£° в природных водах > нивалось как 10—50 % от общего содержания [512]. Образование в повер I-стных водах Ня° и ее эмиссия в атмосферу является важным элементом >-бального биогеохимического цикла ртути.[ . ]
Гипопикнальные течения в озерах значительно менее вероятны, чем в морской обстановке, так как озерная вода и речная вода часто имеют одинаковую плотность. Правда, большая разница плотностей может быть вызвана различием температур или наличием взвешенного твердого стока в речной воде. Эти различия оказывают влияние на осадкообразующие гиперпикнальные потоки, из которых могут сформироваться подводные озерные каналы и намывные дельты, такие как в дельте Роны в Женевском озере [841,1162].[ . ]
Следует особо выделить две особенности озер. Первая состоит в их чувствительности к климату: древние озерные отложения, по-видимому, являются лучшими индикаторами палеоклимата. Вторая заключена в разнообразии осадочных фаций в вертикальном разрезе как результате колебаний биохимического режима озерной воды и непостоянства береговой линии. По этой причине, для того чтобы задокументировать весь набор обстановок осадконакопления, разрезы озерных отложений следует изучать буквально сантиметр за сантиметром.[ . ]
Наиболее длительное время сохраняют подвижность спермин у рыб, размножающихся в солоноватой и соленой воде. В солоноватой воде, оказывающей на половые клетки протективное действие, спермии остаются активными при нерестовых температурах в течение 15—25 мин (Гостеева, 1957; А. Турдаков, 1962; Дорошев, Горелов, 1964, и др.). Невысокая скорость, а также чередование периодов поступательного движения с временными замедлениями и остановками приводят к увеличению периода жизнедеятельности его спермиев на срок до нескольких часов. У двух других видов иссыккуль-ских рыб—османа и маринки—спермии в солоноватой озерной воде приходят в гораздо более активное движение, быстро расходуют энергию и прекращают поступательное движение уже через 5—25 мин (А. Турдаков, 1962, и неопубликованные данные). Такая разница у спермиев исеьгккульских рыб, размножающихся в сходных условиях, объясняется, вероятно, особенностями их нереста. Чебачок размножается большими стадами на ограниченных участках нерестилища, и присутствие в воде спермиев, длительное время сохраняющих подвижность и оплодотворяющую способность, содействует, очевидно, успешному осеменению выметываемой икры. Ооман и маринка не образуют в период нереста больших скоплений. Нерестовая группировка у них состоит из самки и одного или нескольких самцов. В этих условиях целесообразно активное движение спермиев в течение сравнительно короткого времени, сочетающееся с единовременным продуцированием большого количества спермы (см. табл. 5).[ . ]
Водоносный горизонт здесь состоит из средне- и мелкозернистых песков. Между инфильтрационным бассейном, в который подается озерная вода, и линией водозаборных скважин-расположены 13 наблюдательных скважин, из которых были отобраны пробы подземных вод через 2 мес. после чистки бассейна и начала очередного фильтроцикла.[ . ]
Согласно периодическим наблюдениям, родниковый сток в озеро Байкал оценивается в 63 млн. м3/год. В него входят холодные и термальные источники, так же, как и воды подземного стока в низовьях Северного Байкала в виде высачиваемых потоков и мочажин. Необходимо заметить, что температура шести термальных источников, питающих Байкал на северном побережье, с суммарным дебитом 1,6 млн. м3/год, превышает 80°С, что влияет на геотермальный и микробиологический режим озерной воды в прибрежной зоне.[ . ]
Экономические последствия этих условий прежде всего требуют внедрения более сложных технологических процессов и усовершенствованных установок для очистки воды. Другим важным фактором, однако, являются расходы, связанные с ¡временными, иногда весьма серьезными, нарушениями водоснабжения в больших городах и стоимостью срочных мер, принятие которых необходимо в таких случаях. В одном из больших городов Германской Демократической Республики, водоснабжение которого производится за счет и подпочвенных и поверхностных вод озера, длившееся всего несколько часов просачивание фенолов в систему водоснабжения от озера причинило ущерб более чем на 10 ООО немецких марок. Хотя в озерной воде концентрация фенолов, отгоняемых с паром, возросла лишь на несколько сотых миллиграмма, оказалось необходимым полностью переключить водоснабжение на подпочвенную воду, освободить и прочистить резервуары, содержащие чистую воду, промыть фильтрующие установки, ¡спустить профильтрованную воду и тщательно прочистить трубопровод.[ . ]
Культуры помещают в термостат при 30—35° и выдерживают до момента хорошего развития и обильного образования сероводорода. Далее эту же пробирку доверху заполняют озерной водой или расплавленной агаризированной (0.5% агара) средой Бавендама (№ 48). Пробирки хорошо встряхивают, чтобы мел распределился по всей среде, заражают испытуемым материалом или культурой пурпурных серобактерий. Затем пробирки закрывают корковыми пробками, охлаждают под струей холодной воды и выставляют на окно, выходящее на север или северо-восток. Уже через четыре-пять дней отмечается развитие пурпурных или зеленых серобактерий. В случае жидкой среды пурпурные бактерии вначале развиваются в виде сплошной розовой пленки, которая в дальнейшем спускается вглубь между агаром и стеклом пробирки, а жидкая среда теряет свою окраску.[ . ]
В фазу трансгрессии озера, продолжительностью 20-25 лет, когда отметка его уровня превышает 341 м, в прибрежной зоне формируется обратный уклон грунтового потока, обеспечивающий отток озерной воды в берега. Наибольший отток отмечается на участках неглубокого залегания грунтовых вод, в дельтах рек и других понижениях рельефа. Расход подземного потока из озера, определенный по уравнению Дарси, в пределах южного побережья оценивается в 28 млн. м3/год. Из них из Западного Балхаша только по низкому южному берегу отток составляет 19,1 млн. м3/год (2 л/с км), из Восточного — 8,9 млн. м3/год (0,89 л/с км).[ . ]
Водоснабжение большинства городов Урала, России в целом осуществлялось за счет поверхностных водоемов и водохранилищ. Подрусловые водозаборы на Чусовой, Белой, Урале и других реках также восполняются речными водами. С ростом промышленных городов увеличились потребности в воде во всем мире, и ее стало не хватать; к тому же значительно ухудшилось качество воды. Развитие промышленности, энергетики, строительства, широкое использование минеральных удобрений и ядохимикатов в сельском хозяйстве, проведение недостаточно эффективных природоохранных мероприятий привели к загрязнению водоемов и водохранилищ. В бассейнах Волги, Камы и Урала, в речных и озерных водах стали развиваться сине-зеленые водоросли, которые специалисты называют “раковой опухолью” планеты. К тому же в воду попадает огромное количество разнообразных органических соединений, нефтепродуктов, фенолов, которые в сочетании с хлор-ионом, тяжелыми металлами, радиоактивными элементами и другими компонентами образуют вредные токсичные вещества, вызывающие экологический иммунодефицит, аллергические, онкологические заболевания, болезни сердца и кишечно-желудочного тракта.[ . ]
В зависимости от местоположения ледниковые покровы делятся на три морфолого-динамических типа; наземный, плавучий, «морской». Наземные покровы залегают целиком на каменном ложе и имеют выпуклую форму; плавучие — на морской или озерной воде и обладают плоской поверхностью; «морские», сочетающие выпуклую поверхность над каменным ложем, опущенном ниже уровня моря, и горизонтальную, где окраинный лед оказывается на плаву. К плавучим покровам относятся шельфовые ледники, к «морским»— покровы Западной Антрактиды.[ . ]
Первый способ дает абсолютные значения и является полезным, например, при определении достаточности запаса кислорода для рыб. Второй способ, однако, позволяет оценить, сколько еще кислорода можно добавить в водную среду (или насколько озерные воды дефицитны по содержанию кислорода).[ . ]
Процессом, под влиянием которого трансформируется в течение почти сорока последних лет экосистема Ладожского озера, является антропогенное эвтрофирование. Инициирующую роль в эволюции экосистемы сыграло изменение содержания фосфора в озерной воде. Фосфор входит в состав нуклеиновых кислот, играет важную роль в записи генетической информации, в синтезе белка, в процессах хранения и передачи энергии и во многих других процессах, необходимых для жизни растений и животных. Природные поверхностные воды умеренной зоны северного полушария бедны фосфором вследствие специфики гидрохимических процессов в условиях повышенной увлажненности. Из трех основных компонентов, необходимых для построения живого вещества авто-трофных организмов (первичной продукции), — фосфора, азота и углерода — озерная экосистема строго лимитирована только в отношении фосфора, поступление которого в водоем связано исключительно с водным притоком (речным, грунтовым, атмосферными осадками). Нехватка азота и углерода в воде (Schindler, 1974) компенсируется за счет поступления этих элементов из атмосферы в процессе газообмена (углерод) или фиксации азота водорослями.[ . ]
Для исследованной территории характерно распространение кристаллических трудно растворимых пород. Коренные породы часто выходят на поверхность. Почвы — серые лесные и фрагментарные, маломощные. Промывной режим обусловил значительную выщелоченность почв и пород на водосборах. В результате озеру Большое Миассово свойственна минерализация от 183 до 240 мг/л. По нашим данным, по преобладающим ионам воды озера Большое Миассово относятся к гидрокарбонатному классу смешанного катионного состава, но среди катионов обычно незначительно преобладает кальций. Гидрохимический тип воды переходный между содовым (Г) и сульфатно-натриевым (II). В течение года химический состав и общая минерализация воды изменяются незначительно. Некоторое снижение минерализации воды наблюдается в период весеннего половодья и наибольшего наполнения озера талыми водами (апрель-май) и в период осеннего максимума дождей (сентябрь). Самая низкая минерализация отмечена в феврале. Минерализация в придонной воде несколько выше, чем в поверхностной. Общая жесткость озерной воды 1.83-2.77 мг-экв/л.[ . ]
Анализ проводился в стеклянных вертикальных (60 см) сосудах (в сечении 5 5 см2) при температуре 17-19°С. Для создания воздействия на вертикальное распределение A. salinus в опытные сосуды помещались: а) закрытые стаканчики (диаметр — 2 см, длина — 7 см) из крупного газа (0.25 мм) с живым G. lacustris (4 особи/стаканчик); б) стеклянные сосуды объемом 5 мл с гомогенатом A. salinus, закрытые сверху мелким газом N»76; в) стеклянные сосуды объемом 5 мл с гомогенатом G. lacustris, закрытые сверху мелким газом №76; г) электродвигатели (9 оборотов/мин) с лопастями для создания гидродинамического возмущения воды в верхнем слое опытных вертикальных сосудов. Для заполнения сосудов использовалась озерная вода с глубины 3 м с пелагиали (станция над глубиной 16 м), пропущенная через мелкий газ №76. Контроль — сосуды, в которых A. salinus не испытывал никакого воздействия. Проведены две серии экспериментов: а) при освещении, б) в темноте; все в трех повторностях. Достоверность различия между опытом и контролем оценивалась непараметрическим критерием Манна-Уитни в программе STATISTICA.[ . ]
Источник



