- Может ли вода оставаться жидкой при температуре ниже нуля?
- Давление
- Добавки
- Другие методы. Переохлаждённая вода
- Как почувствовать себя волшебником — мгновенная заморозка воды
- Переохлажденная жидкость
- Общие сведения
- Эксперимент в домашних условиях
- Похожие статьи
- Переохлажденная вода почему не замерзает
- Войти
- Это интересно! Переохлажденная вода.
- Вода может не замерзать при температуре ниже нуля градусов Цельсия
Может ли вода оставаться жидкой при температуре ниже нуля?
Да, может. Температура замерзания воды падает ниже нуля градусов по Цельсию, если вы оказываете на неё давление. И не только.
Это может произойти несколькими способами. Рассмотрим их далее.
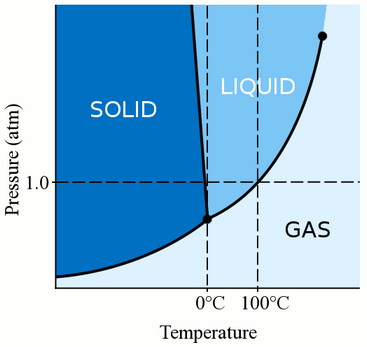
Давление
Прежде всего, фаза материала (будь то газ, жидкость или твёрдое вещество) сильно зависит как от его температуры, так и от давления.
Для большинства жидкостей давление поднимает температуру, при которой жидкость замерзает. Твёрдое тело образуется, когда свободные молекулы жидкости становятся достаточно медленными и достаточно близко располагаются друг к другу, чтобы сформировать стабильные связи, которые закрепляют их на месте. Когда мы оказываем давление на жидкость, мы заставляем молекулы сближаться. Поэтому они могут образовывать стабильные облигации и стать твёрдыми при более высокой температуре, чем температура замерзания при стандартном давлении.
Однако вода несколько уникальна.
Молекулы воды распространяются, когда они связываются в твёрдую кристаллическую структуру. Это действие делает лёд менее плотным, чем жидкостная вода, поэтому лёд плавает, а не тонет. Это действие молекул воды при замерзании также означает, что давление воды понижает температуру замерзания. Если вы примените достаточное давление (что затрудняет распространение молекул воды в твёрдую структуру), вы можете получить жидкую воду на несколько градусов ниже нуля градусов по Цельсию.
Добавки
Даже без давления вы можете получить жидкую воду при минусовой температуре, используя добавки. Такие добавки, как соль, могут помешать сформировать твёрдое тело и понизить температуру замерзания воды.
Соль состоит из сильных ионов натрия и хлора. Растворённые в воде, молекулы воды присоединяются к ионам соли, и поэтому не замерзают как охотно. По мере того, как вы добавляете больше соли в воду, точка замерзания продолжает падать, пока вода не достигнет насыщения и не сможет удерживать соль.
Если добавить достаточное количество соли, температура замерзания воды может упасть до -21 градуса Цельсия.
Этот факт означает, что вода при температуре -21 градус Цельсии может всё ещё быть жидкой (с достаточным количеством соли).
Это мощное свойство соли можно также использовать для того, чтобы дать льду превратиться обратно в воду. Посыпание солью ледяных тротуаров снижает температуру замерзания льда ниже температуры окружающей среды, и лёд тает.
Но посыпать солью обледеневшие дорожки не поможет, если температура окружающей среды ниже -21 градуса по Цельсию.
Воздействие соли на точку замерзания воды также оказывает глубокое воздействие на океаны Земли.
Другие методы. Переохлаждённая вода
Даже если вы не применяете давление и ничего не добавляете в воду, вы всё равно можете иметь жидкую воду при температуре ниже нуля градусов по Цельсию.
Для того, чтобы вода замёрзла до льда, ей нужно замёрзнуть, чтобы начать процесс. Эти отправные точки называются «центрами нуклеации». В большинстве случаев немного пыли, примесей или даже небольшие колебания в воде обеспечивают центры зарождения для замерзания воды. Но если ваша вода очень чистая и неподвижная, молекулам воды не на что кристаллизоваться. В результате вы можете охладить очень чистую воду ниже нуля градусов по Цельсию без замерзания.
Вода в таком состоянии называется «переохлаждённой».
Чистую воду можно переохладить до около -40 градус Цельсия.
Переохлаждённая вода удерживается от замерзания только отсутствием центров зарождения. Поэтому, как только появятся центры нуклеации (что может произойти от простой вибрации), супер-охлаждённая вода быстро замерзает.
Ледяной дождь — это естественный пример переохлаждённой жидкой воды. Как только дождь попадает на объект на поверхности Земли, объект обеспечивает центры нуклеации, и дождь замерзает до льда.
Какой обьект обеспечивает какие центры нуклеации? Что спрятано за этими терминами? — незнание!
Источник
Как почувствовать себя волшебником — мгновенная заморозка воды
Кто из нас в детстве не увлекался фокусами? Детство проходит, но вера в чудеса остается. Нехитрые приготовления, и вот вы уже творите настоящее волшебство. Немного научных знаний, ловкость рук и, главное, никакого мошенничества. Предлагаем вам поучаствовать в эксперименте, ход которого очень прост.
Процесс, который запечатлен на видео, называется мгновенной заморозкой воды. Для эксперимента вам понадобится очищенная вода. Конечно, дистиллированную воду достать проблематично, но для нашего случая вполне подойдет очищенная питьевая вода, которая продается в магазине. Пол-литровую бутылку необходимо поместить в морозильную камеру, температура в которой около -15 – 18 градусов. Когда спустя полтора-два часа вы достанете бутылку, вода в ней по-прежнему будет находиться в жидком состоянии, но ее температура будет значительно ниже нуля. Почему же она не замерзает? Все дело в том, что она не содержит в себе примесей, необходимых для кристаллизации льда и может находиться при температуре до минус 40 градусов в жидком состоянии. То есть она уже остыла и готова замерзнуть, но у нее нет для этого подходящих центров кристаллизации, вокруг которых происходит образование льда.
А вот с обычной пресной питьевой водой, содержащей, как правило, растворенные соли, такой трюк не получится. Она начнет замерзать уже в морозильной камере.
Но что же происходит, когда мы достаем бутылку из холода? Как показано на видео, экспериментатор встряхивает бутылку или прикасается к воде кусочком льда. От механического воздействия или соприкосновения с кристаллами льда переохлажденная вода начинает прямо на глазах превращаться в лед. Вода обретает тот самый недостающий центр кристаллизации и, поскольку ее температура значительно ниже нуля градусов, запускается цепная реакция — кристаллики льда пристраиваются друг к другу и постепенно заполняют собой весь объем бутылки.
Обязательно попробуйте сделать такое со своими друзьями или удивите детей! Это очень эффектный эксперимент, а главное, легко выполнимый в домашних условиях.
Источник
Переохлажденная жидкость
Переохлажденная жидкость — жидкий лед
Общие сведения
Переохлажденная жидкость (метастабильное состояние) – это такая жидкость, температура которой ниже температура кристаллизации при нормальном давлении. Причиной существования переохлажденных жидкостей при атмосферном давлении является отсутствие так называемых центров кристаллизации.
Центром кристаллизации в веществе называется зародыш твердого состояния в веществе, из которого возникает кристаллит – минимальный объем кристалла.
Переохлажденную жидкость можно получить двумя способами:
- Очень быстрое охлаждение – замедляет процессы диффузии веществе, которые являются необходимыми для перехода в твердое состояние. Говоря простым языком – охлаждения происходит настолько быстро, что молекулы не успевают выстроиться в кристаллическую решетку.
- Устранение центров кристаллизации. Производится посредством очистки жидкости от различных твердых примесей. Дело в том, что примеси значительно снижают работу, требуемую для образования кристаллического зародыша и потому приводят к быстрой кристаллизации всей массы вещества.
Эксперимент в домашних условиях
Суть простейшего эксперимента по переохлаждению воды состоит в том, чтобы использовать очищенную воду для дальнейшего охлаждения, хотя бы в морозильной камере холодильника. Так вода способна находиться в жидком состоянии вплоть до температуры -40°C. Далее, емкость с охлажденной водой достаточно встряхнуть, чтобы вода мгновенно замерзла. Еще более интересное зрелище можно наблюдать, если вылить данную воду в другую емкость. При соприкосновении переохлажденной жидкости с другой емкость – вода мгновенно будет замерзать.
Похожие статьи
Понравилась запись? Расскажи о ней друзьям!
Источник
Переохлажденная вода почему не замерзает
Войти
Авторизуясь в LiveJournal с помощью стороннего сервиса вы принимаете условия Пользовательского соглашения LiveJournal
Это интересно! Переохлажденная вода.
Если очень чистую воду охлаждать, предохраняя от сотрясений, то её можно переохладить, т. е. достигнуть температур ниже нуля без образования льда. Однако такая переохлаждённая вода малоустойчива — при внесении в неё кристаллика льда она затвердевает.
Особенно легко переохлаждаются отдельные капли воды, причём их самопроизвольное замерзание наступает тем труднее, чем они меньше. Так, при диаметрах от одного мм до одного мк температуры быстрого самопроизвольного замерзания водяных капель лежат в пределах от 24 до 38 °С. Поэтому облака даже при низких температурах состоят обычно не из частиц льда, а из капелек воды. Каждый см3 дождевого облака содержит от десятков до сотен капелек с диаметрами от 1 мк до 1 мм.
Некоторые растворённые в воде примеси существенно влияют на её способность к переохлаждению. Например, при небольшой добавке ацетона удавалось переохлаждать водяные капли до 72 °С. Подобные примеси имеются, вероятно, в крови холоднокровных животных, благодаря чему их организмы способны без вреда для себя переносить замораживание и последующее оттаивание. Напротив, у теплокровных животных способность крови к переохлаждению очень невелика. Происходящая при её замораживании кристаллизация воды вызывает разрывы тканей с их последующим омертвением.
При обычных условиях состояние жидкой воды является устойчивым. Напротив, переохлаждённая или перегретая вода находится в так называемом метастабильном состоянии. Последнее характеризуется тем, что само по себе оно более или менее устойчиво, но устойчивость эта легко нарушается под влиянием тех или иных воздействий. Если представить себе конус со слегка срезанной параллельно основанию вершиной, то устойчивое состояние вещества будет соответствовать такому конусу, стоящему на своём основании, а метастабильное — стоящему на вершине. Возможность более или менее длительного существования метастабильных состояний обусловлено затруднённостью возникновения при данных условиях зародышевых образований стабильной фазы рассматриваемого вещества.
Источник
Вода может не замерзать при температуре ниже нуля градусов Цельсия
С детства каждый помнит, что вода замерзает при температуре 0 градусов по Цельсию. Возможно, кто-то слышал и о том, что чистая пресная вода в очень чистом сосуде может находиться в жидком состоянии и при отрицательных температурах. Ученые в своих опытах доходили до температуры минус 40 градусов по Цельсию. Вода в жидком виде при отрицательной температуре носит название «переохлажденной», и при этом она находится в очень неустойчивом состоянии:
стоит появиться хоть одной посторонней частице, вокруг которой может образоваться кристалл льда, как тут же вся вода замерзает.
Группа ученых из института имени Вейцмана (Израиль) под руководством Игоря Любомирского выяснила, что переохлажденная вода замерзает при различных температурах в зависимости от того, положительно или отрицательно заряжена поверхность, с которой соприкасается вода. Соответствующая работа опубликована в журнале Science.
Основным предметом исследования израильских ученых стали пироэлектрические (обладающие поляризацией в отсутствие внешних воздействий) аморфные (не имеющие упорядоченной кристаллической структуры) твердые тела. Однажды Игорь Любомирский обнаружил, что если вода контактирует с поверхностью из подобного материала, то температура замерзания воды зависит от заряда поверхности.
Отрицательный заряд понижал температуру замерзания, а положительный повышал ее.
Обратив внимание на этот факт, ученые решили подробнее исследовать его. Используя мощные микроскопы, Игорь Любомирский и коллеги обнаружили, что капельки воды на кристаллах танталата лития (LiTaO3) и тонких пленках из титаната стронция (SrTiO3) замерзают при температуре -11 градусов. С изменением заряда с отрицательного на положительный температура замерзания повышалась на несколько градусов.
Используя метод рентгеноструктурного анализа, исследователи отметили, что положительно заряженные поверхности вызывают начало замерзания переохлажденной воды на границе «поверхность – вода», тогда как отрицательно заряженные поверхности влекут начало замерзания на поверхности «вода – воздух».
Комментируя свою работу, Игорь Любомирский признается, что не знает, почему изменение заряда так меняет свойства воды. «То, что мы теперь знаем, дает нам очень, очень, очень хорошую тему для размышлений», — приводит слова ученого National Public Radio.
Возможность контролировать температуру замерзания переохлажденной воды может быть весьма актуальной.
В частности, результаты работы израильских ученых могут найти свое применение в актуальных областях исследований:
— выживание холоднокровных животных;
— криоконсервация (методы хранения органов, тканей или отдельных клеток при пониженной температуре);
— защита сельскохозяйственных культур от замерзания;
— «посев» облаков (то есть целенаправленное изменение погоды для создания дождя в засушливых местах или вызывание дождя с целью уменьшения вероятности града).
Источник