Перманганат калия сульфат марганца вода реакция
Для выполнения задания используйте следующий перечень веществ: перманганат калия, сульфат марганца (II), вода, карбонат натрия, хлорид натрия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна окислительно восстановительная реакция, и запишите уравнение этой реакции. Составьте электронный баланс, укажите окислитель и восстановитель.
Для выполнения задания используйте следующий перечень веществ: перманганат калия, сульфат марганца (II), вода, карбонат натрия, хлорид натрия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Запишем уравнение реакции:
Составим электронный баланс:
Марганец в степени окисления +2 является восстановителем. Марганец в степени окисления +7 (или перманганат калия за счёт марганца в степени окисления +7) — окислителем.
| Критерии оценивания выполнения задания | Баллы | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ответ правильный и полный, содержит следующие элементы: — выбраны вещества, и записано уравнение окислительно-восстановительной реакции; Источник KMnO4 + MnSO4 = ? уравнение реакцииСрочно нужна помощь! Какие продукты образуются в результате взаимодействия перманганата калия с сульфатом марганца (II) (KMnO4 + MnSO4 = ?)? Укажите основные физические и химические свойства полученного соединения марганца, а также способы получения этой соли. Заранее, большое спасибо! В результате взаимодействия перманганата калия с сульфатом марганца (II) в горячей воде (KMnO4 + MnSO4 = ?) происходит образование средней соли – нитрата сульфата калия, серной кислоты, а также выпадение осадка черного цвета – оксида марганца (IV). Молекулярное уравнение реакции имеет вид: Запишем ионные уравнения, учитывая, что вода и оксид марганца (IV)на ионы не распадаются, т.е. не диссоциируют. Первое уравнение называют полным ионным, а второе – сокращенным ионным. Источник KMnO4 + MnSO4 + H2O = ? уравнение реакцииЗакончите уравнение реакции KMnO4 + MnSO4 + H2O = ? Расставьте стехиометрические коэффициенты. Запишите молекулярное и ионное уравнения реакции. Охарактеризуйте полученное нерастворимое в воде соединение: приведите его основные физические и химические свойства. Каким образом его можно получить в лаборатории? А в промышленности? В результате взаимодействия перманганата калия с водным раствором сульфата марганца (II) (KMnO4 + MnSO4 + H2O = ?) происходит образование средней соли сульфата калия, серной кислоты а также выпадение твердого оксида марганца (IV). Молекулярное уравнение реакции имеет вид: Запишем ионные уравнения, учитывая, что вода и оксиды на ионы не распадаются, т.е. не диссоциируют. Первое уравнение называют полным ионным, а второе – сокращенным ионным. Оксид марганца (IV) представляет собой твердое вещество черного цвета с коричневым оттенком, кристаллы которого при нагревании разлагаются. Не реагирует с водой. Из раствора осаждается в виде гидрата состава Источник AcetylЭто пилотный ролик из серии об органических реакциях. Наведите курсор на ячейку элемента, чтобы получить его краткое описание. Чтобы получить подробное описание элемента, кликните по его названию.
|
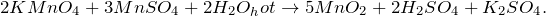
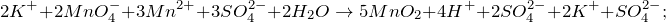
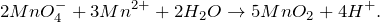
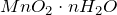 . Переводится в раствор действием концентрированных кислот. Проявляет окислительно-восстановительные свойства. В природе — самое распространенное соединение марганца (пиролюзит).
. Переводится в раствор действием концентрированных кислот. Проявляет окислительно-восстановительные свойства. В природе — самое распространенное соединение марганца (пиролюзит).