- Универсальное определение растворителя — 2021
- «Ил-2 Штурмовик» нового поколения — «Битва за Сталинград» и «Битва за Москву» #13
- Ключевые выводы: универсальный растворитель
- Универсальное определение растворителя
- Почему вода называется универсальным растворителем
- Алкахест как универсальный растворитель
- Другие важные растворители
- Почему нет универсального растворителя
- источники
- Экспоненциальный спад: определение и функция
- Универсальное желание: «Приятного аппетита»
- Хиллари Клинтон и Универсальное Здравоохранение
- Что такое универсальный растворитель?
- Что такое растворитель?
- Почему вода считается универсальным растворителем?
- Универсальный растворитель – определение и характеристики
- Универсальное определение растворителя
- Характеристики универсального растворителя
- полярность
- Высокая удельная теплоемкость
- Уникальные свойства плотности и температуры
- викторина
Универсальное определение растворителя — 2021
«Ил-2 Штурмовик» нового поколения — «Битва за Сталинград» и «Битва за Москву» #13
Технически, растворитель является компонентом раствора, присутствующего в большем количестве. Напротив, растворенные вещества присутствуют в меньшем количестве. В обычном использовании растворитель — это жидкость, которая растворяет химические вещества, такие как твердые вещества, газы и другие жидкости.
Ключевые выводы: универсальный растворитель
- Универсальный растворитель теоретически растворяет любой другой химикат.
- Истинного универсального растворителя не существует.
- Воду часто называют универсальным растворителем, потому что она растворяет больше химикатов, чем любой другой растворитель. Однако вода растворяет только другие полярные молекулы. Он не растворяет неполярные молекулы, включая органические соединения, такие как жиры и масла.
Универсальное определение растворителя
Универсальный растворитель — это вещество, которое растворяет большинство химических веществ.Вода называется универсальным растворителем, потому что она растворяет больше веществ, чем любой другой растворитель. Однако ни один растворитель, включая воду, не растворяет все химические вещества. Как правило, «подобное растворяет подобное». Это означает, что полярные растворители растворяют полярные молекулы, такие как соли. Неполярные растворители растворяют неполярные молекулы, такие как жиры и другие органические соединения.
Почему вода называется универсальным растворителем
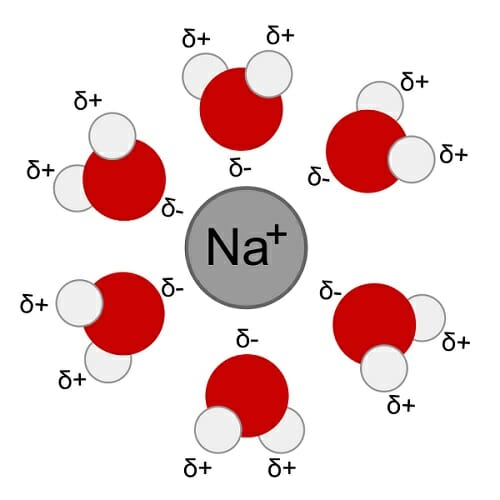
Вода растворяет больше химикатов, чем любой другой растворитель, потому что ее полярная природа дает каждой молекуле гидрофобную (боязливую воду) и гидрофильную (любящую воду) сторону. Сторона молекул с двумя атомами водорода имеет небольшой положительный электрический заряд, а атом кислорода несет небольшой отрицательный заряд. Поляризация позволяет воде привлекать много разных типов молекул. Сильное притяжение к ионным молекулам, таким как хлорид натрия или соль, позволяет воде разделить соединение на его ионы. Другие молекулы, такие как сахароза или сахар, не разрываются на ионы, а равномерно диспергируются в воде.
Алкахест как универсальный растворитель
Алкахест (иногда пишется alcahest) является гипотетическим истинно универсальным растворителем, способным растворять любое другое вещество. Алхимики искали легендарный растворитель, так как он мог растворить золото и найти полезное лекарственное применение.
Считается, что слово «алкахест» было придумано Парацельсом, который основывался на арабском слове «щелочь». Парацельс приравнивал алкахеста к философскому камню. Его рецепт для алкаэста включал едкую известь, спирт и карбонат калия (карбонат калия). Рецепт Парацельса не мог растворить все.
После Парацельса алхимик Франциск ван Гельмонт описал «ликер алкахест», который представлял собой своего рода растворяющуюся воду, способную разбить любой материал на его основное вещество. Ван Гельмонт также писал о «соляной щелочи», которая представляла собой едкий калиевый раствор в спирте, способный растворять многие вещества. Он описал смешивание соляной щелочи с оливковым маслом для получения сладкого масла, вероятно, глицерина.
Хотя alkahest не является универсальным растворителем, он все еще находит применение в химической лаборатории. Ученые используют рецепт Парацельса, смешивая гидроксид калия с этанолом для очистки лабораторной посуды. Затем посуду ополаскивают дистиллированной водой, чтобы она оставалась чистой.
Другие важные растворители
Растворители делятся на три широкие категории. Есть полярные растворители, такие как вода; неполярные растворители, такие как ацетон; и затем есть ртуть, специальный растворитель, который образует амальгаму. Вода — безусловно самый важный полярный растворитель. Существует несколько неполярных органических растворителей. Например, тетрахлорэтилен для химической чистки; ацеторы, метилацетат и этилацетат для клея и лака для ногтей; этанол для парфюмерии; терпены в моющих средствах; эфир и гексан для точечного удаления; и множество других растворителей, специфичных для их назначения.
Хотя чистые соединения могут быть использованы в качестве растворителей, промышленные растворители, как правило, состоят из комбинаций химических веществ. Этим растворителям присваиваются названия alphanumeroc. Например, растворитель 645 состоит из 50% толуола, 18% бутилацетата, 12% этилацетата, 10% бутанола и 10% этанола. Растворитель П-14 состоит из 85% ксилола и 15% ацетона. Растворитель RFG сделан с 75% этанолом и 25% бутанолом. Смешанные растворители могут влиять на смешиваемость растворенных веществ и улучшать растворимость.
Почему нет универсального растворителя
Алкахест, если бы он существовал, поставил бы практические проблемы. Вещество, которое растворяет все остальные, не может храниться, потому что контейнер будет растворен. Некоторые алхимики, включая Philalethes, обошли этот аргумент, заявив, что alkahest будет растворять материал только до его элементов. Конечно, по этому определению алкахест не сможет растворить золото.
источники
- Гутман В. (1976). «Влияние растворителя на реакционную способность металлоорганических соединений». Коорд. Химреагент оборот , 18 (2): 225. doi: 10.1016 / S0010-8545 (00) 82045-7.
- Лейнхард, Джон «No.1569 Алкахест». Университет Хьюстона.
- Philalethes, Eirenaeus. «Секрет бессмертного ликера под названием Алкахест или Игнис-Аква»
- Тиноко, Игнасио; Зауэр, Кеннет и Ван, Джеймс С. (2002) Физическая химия , Прентис Холл р. 134 ISBN 0-13-026607-8.
Экспоненциальный спад: определение и функция
Узнайте об экспоненциальном затухании, экспоненциальной функции, которая описывает, когда первоначальная сумма уменьшается на постоянную ставку в течение определенного периода времени.
Универсальное желание: «Приятного аппетита»
«Приятного аппетита» — это всеобщее желание, когда человек собирается есть. Это может буквально означать «хороший аппетит», но его цель — «приятного аппетита».
Хиллари Клинтон и Универсальное Здравоохранение
Узнайте, где Хиллари Клинтон стоит на здравоохранении. Посмотрите, какой план медицинского обслуживания она предложила в прошлом.
Источник
Что такое универсальный растворитель?
универсальный растворитель это вещество способно растворять широкий спектр растворенных веществ или химических веществ. Вещество, которое считается универсальным растворителем, является вода, а затем объясняет, почему в соответствии с его свойствами.
Если мы думаем о лимонаде, необходимы три ингредиента: вода, лимоны и сахар. Добавляя сахар, он легко растворяется в лимонаде, напитке, который использует воду в качестве основы..
Простой пример, как лимонад, служит для демонстрации свойств воды в действии. Вода известна как «универсальный растворитель» по преимуществу.
Однако, хотя вода является самым известным растворителем и одним из самых важных, она не является единственным растворителем, используемым в химической промышленности..
Что такое растворитель?
Растворитель — это просто вещество, которое может растворять другие молекулы и соединения, известные как растворенные вещества. Гомогенная смесь растворителя с растворенным веществом известна как раствор.
Растворитель всегда находится в жидком состоянии, в то время как растворенное вещество может присутствовать в твердом, жидком или газообразном состоянии..
Примерами растворителей являются вода, олово, спирт, молоко. Примерами растворенных веществ являются сахар, соль, уксусная кислота. Примером раствора является солевой раствор, образованный водой и солью.
Растворители являются частью различных применений, таких как фармацевтические препараты, синтетические материалы, краски и клеи.
Почему вода считается универсальным растворителем?
Наше тело работает через химические изменения, которые происходят на клеточном уровне. Точно так же растения и животные страдают химическими изменениями в своих организмах..
Эти изменения происходят в водных растворах или растворах, в которых вода является основным растворителем..
Поскольку вода обладает свойствами полярности (отрицательный и положительный заряд) и способностью образовывать водородные связи, она считается отличным растворителем.
Способность воды растворять большое разнообразие молекул является ключом для этих химических реакций, происходящих в организмах. Отсюда важность воды для жизни на планете..
Благодаря своей способности растворять большое количество растворенных веществ, больше, чем любая другая жидкость, вода известна как «универсальный растворитель». Важно отметить, что не все вещества хорошо растворяются в воде, например, масла.
Молекулы масел не имеют областей заряда ни положительных, ни отрицательных, поэтому они не притягиваются молекулами воды.
Молекулы воды состоят из атомов водорода и кислорода. Водород имеет положительный заряд, а кислород — отрицательный, что позволяет молекулам воды притягиваться ко многим различным типам молекул и, следовательно, способно растворять их.
Есть и другие свойства воды, такие как поверхностное натяжение, ее уникальная плотность и температура, которые позволяют воде быть отличным растворителем..
Вода существует в трех возможных формах, таких как газ, жидкость или твердое вещество, что обычно не встречается в других растворителях.
Источник
Универсальный растворитель – определение и характеристики
Универсальное определение растворителя
Вода это вещество, которое мы называем универсальным растворитель, Растворитель – это просто жидкость, в которой могут растворяться другие вещества, и причина, по которой вода получила ярлык универсального растворителя, заключается в том, что никакой другой растворитель не может растворить столько веществ, сколько может. Это в основном то, что делает его таким важным для жизни на земле. Кроме того, удивительно, что каждый водоем, найденный на земле, включая лед, поддерживает ту или иную форму жизни, которая адаптировалась к температуре и давлению, обнаруженному в этой форме воды.
Тот простой факт, что ученым всегда интересно находить воду, связанную с жизнью, на других планетах, многое говорит об этом, казалось бы, простом веществе. Вода является наиболее распространенным веществом в организмах и клетках. Конечно, есть много очевидных применений для воды, таких как питье, мытье и тушение пожаров, и это благодаря характеристикам, которыми он обладает, которые делают его универсальным растворителем. Вода очень важна для жизни, потому что для многих важных реакций в организме организмов необходима водная среда. Например, вода необходима для переваривания белков в аминокислоты, И в фотосинтез и пищеварение.
Характеристики универсального растворителя
полярность
Это большая часть того, почему вода является универсальным растворителем. Полярность – это неравномерность распределения электронов в молекула, что приводит к одной молекуле, имеющей две противоположные стороны; один отрицательный и один положительный. Теперь вода имеет молекулярную формулу H2O, поэтому каждая молекула воды имеет два атома водорода и один атом кислорода, как вы можете видеть на диаграмме ниже. Атомы водорода не находятся на противоположных сторонах друг друга, и они несут частичный положительный заряд. Это означает, что они создают положительно заряженную часть молекулы, в то время как кислородный конец создает отрицательно заряженную часть. Эта полярность означает, что вода может присоединяться и, следовательно, растворять полярные и ионные (заряженные) вещества.
Высокая удельная теплоемкость
Количество энергии, необходимое для повышения температуры одного грамма воды на 1 градус Цельсия, является ее удельной теплотой, и при одной калории на грамм она намного выше, чем удельная теплоемкость большинства жидкостей. Это хорошая новость для нас, так как мы на 60% состоим из воды, и мы не смогли бы выжить, если бы наши тела сильно и быстро остыли и нагрелись. Это также имеет решающее значение для выживания всех других организмов, в том числе водных организмов. Это означает, что океаны и реки не замерзают постоянно или не испаряются при изменении температуры. Если вода не может стабилизировать свою температуру, энергия, которая выделяется во время обмена веществ в живых организмах, может привести к перегреву и смерти.
Уникальные свойства плотности и температуры
Когда мы помещаем кубик льда в воду, он плавает, и, к счастью, то же самое относится и к айсбергу. Если бы лед был более плотным, чем вода, он бы постоянно замерзал наверху, а затем опускался, пока все водоемы не превратятся в лед, уничтожая всю жизнь. Вода также существует в виде газа, жидкости и твердого вещества в очень небольшом диапазоне температур, что означает, что мы можем найти ее во всех трех формах на Земле в зависимости от того, где мы находимся, и часто в одном и том же месте. Это не часто встречающаяся собственность.
- растворенное вещество – Это вещество, которое растворяется в другом растворителе.
- Ковалентная связь – Распределение электронов между атомами с образованием молекулы.
- Круговорот воды – Процесс циркуляции воды между различными элементами земли – атмосферой, землей и океанами.
- метаболизм – Все химические реакции, происходящие внутри живых организмов.
викторина
1. Вода считается полярной, потому что:A. У этого есть одна отрицательная сторона и другая, которая является положительной.B. Это универсальный растворитель.C. У него два атома водорода.D. Это самый плотный в твердой форме.
Ответ на вопрос № 1
верно. У воды есть сторона, которая немного положительна, и сторона, которая слегка отрицательна.
2. Что из следующего является силой, которая удерживает молекулы воды вместе?A. Ковалентные связи B. Ионные связиC. Полярные связиD. Водородные связи
Ответ на вопрос № 2
D верно. Водородные связи образуются между атомами кислорода и атомами водорода различных молекул воды.
3. Какое свойство относится к слипшимся молекулам воды?A. прилипание B. полярностьC. когезияD. Быть универсальным растворителем
Ответ на вопрос № 3
С верно. Силы сцепления, вызванные водородными связями, делают воду эластичной.
Источник