Тяжелые металлы в сточных водах.Продолжение
Медь. Медь является микроэлементом, содержится в организме человека, главным образом, в виде комплексных органических соединений и играет важную роль в процессах кроветворения. В организме человека медь участвует в образовании эритроцитов, высвобождении тканевого железа и развитии скелета, центральной нервной системы и соединительной ткани. Как недостаток, так и избыток меди в организме вызывает его заболевание. Во вредном воздействии избытка меди решающую роль играет реакция катионов Сu2+ с SH-группами ферментов. Изменения содержания меди в сыворотке и коже обуславливают явления депигментации кожи (витилиго). Отравление соединениями меди могут приводить к расстройствам нервной системы, нарушению функций печени и почек и др. Известны случаи группового отравления водой, содержащей от 4 до 60 мг/л меди. Это могло быть связано с эксплуатацией медных водопроводных труб при повышении щелочности воды. ПДК меди в питьевой воде составляет 1,0 мг/л, лимитирующий показатель вредности — органолептический.
Медь и ее соединения широко распространены в окружающей среде, и поэтому их часто обнаруживают в природных водах. Концентрации меди в природных водах обычно составляют десятые доли мг/л, в питьевой воде могут увеличиваться за счет вымывания из материалов труб и арматуры. Свойства меди в воде зависят от значения рН воды, концентрации в ней карбонатов, хлоридов и сульфатов. Медь придает воде неприятный вяжущий привкус в низких концентрациях, что и лимитирует ее содержание в питьевой воде. Это обстоятельство необходимо учитывать в технологии приготовления напитков, а также при выборе источника водоснабжения для производства бутилированной питьевой воды.
Железо. Железо входит в состав важнейших в биологическом отношении органических соединений – гемоглобина крови и ряда ферментов. Около 70% железа, содержащегося в организме человека, входит в состав гемоглобина. Основным физиологическим назначением железа является участие в процессе кроветворения. В природных водах железо встречается, как правило, в регионах месторождений. В малых концентрациях железо встречается практически во всех природных водах в поверхностных и подземных источниках. В болотной воде железа много, десятки миллиграммов на литр, вот почему она имеет коричневый «ржавый» оттенок. В сточные воды железо может попадать из травильных и гальванических цехов, участков подготовки металлических поверхностей, цехов крашения тканей и других производств. Концентрация железа в воде тесно связана с содержанием углекислоты — в кислой среде растворимость соединений железа увеличивается, а в щелочной уменьшается. В водной среде оно присутствует чаще всего в форме бикарбоната, закиси, сульфида. В силу гидрохимических закономерностей в подземных водах железо встречается в различных соотношениях с марганцем.
Вода подземных источников, соприкасаясь с железосодержащими горными породами, насыщается солями двухвалентного железа. Данные соединения железа являются самыми «коварными», поскольку они отличаются хорошей растворимостью и не задерживаются на фильтрах. Чистая, прозрачная вода, изливающаяся из скважины, постояв некоторое время на воздухе, буквально на глазах начинает мутнеть, приобретая характерную рыжевато-бурую окраску. Это происходит потому, что соединения двухвалентного железа, вступив в контакт с кислородом воздуха, окисляются и переходят в нерастворимую форму трехвалентного железа — осадок, называемый обычно ржавчиной.
Похожая история происходит и с водопроводной водой. Пройдя очистку на муниципальных водопроводных очистных сооружениях, вода обычно содержит небольшое количество железа, укладывающиеся в медицинские нормы, но проходя до конечного потребителя через многие километры труб распределительной водопроводной сети, она подвергается вторичному загрязнению, растворяя продукты коррозии стальных труб. В результате на выходе мы вновь имеем «железистую» воду с желтоватым оттенком. Насыщенная соединениями железа вода имеет не только неприятный вид.
Она портит запорную арматуру, оставляет ржавые подтеки не керамических поверхностях сантехники. Кроме того, медиками доказано, что вода с повышенным содержанием железа (свыше 0.3 мг/л) приводит к заболеваниям печени, увеличивает риск инфарктов, негативно влияет на репродуктивную функцию организма, а также служит причиной появления аллергических реакций. Повышенное содержание железа в воде создает благоприятные условия для развития железобактерий, особенно в подогретой воде. Эти микроорганизмы образуют ветвящиеся колоннии, которые осложняют работу гидротехнических сооружений. Продукты жизнедеятельности железобактерий являются канцерогенами. Железообраста-
ния внутри труб – идеальная среда для развития кишечной палочки, гнилостных бактерий, различных других микроорганизмов. Все это ухудшает химические и бактериологические показатели воды.
Анализ воды на содержание железа ведут по показателю «Железо общее». Железо образует два рода растворимых солей, образующих катионы Fe2+ и Fe3+, однако в растворе железо может находиться и во многих других формах, в частности: — в виде истинных растворов (аквакомплексов) [Fe(H2O)6]2+, содержащих железо (II). На воздухе железо (II) быстро окисляется до железа (III), растворы которого имеют бурую окраску из-за быстрого образования гидроксосоединений (сами растворы Fe2+ и Fe3+ практически бесцветны);
— в виде коллоидных растворов из-за пептизации (распада агрегированных частиц) гидроксида железа под воздействием органических соединений;
— в виде комплексных соединений с органическими и неорганическими лигандами.
К ним относятся карбонилы, ареновые комплексы (с нефтепродуктами и др. углеводородами) , гексацианоферраты [Fe(CN)6 ] 4- и др.
В нерастворимой форме железо может быть представлено в виде различных взвешенных в воде твердых минеральных частиц различного состава. Таким образом, поскольку соединения железа в воде могут существовать в различных формах, как в растворе, так и во взвешенных частицах, точные результаты могут быть получены только при определении суммарного железа во всех его формах, так называемого «общего железа».
Раздельное определение железа (II) и (III), их нерастворимых и растворимых форм, дает менее достоверные результаты относительно загрязнения воды соединениями железа, хотя иногда возникает необходимость определить железо в его индивидуальных формах. Перевод железа в растворимую форму, пригодную для анализа, проводят, добавляя к пробе определенное количество сильной кислоты (азотной, соляной, серной) до рН 1-2. Диапазон определяемых концентраций железа в воде — от 0,1 до 1,5 мг/л. Определение возможно и при концентрации железа более 1,5 мг/л после соответствующего разбавления пробы чистой водой. ПДК общего железа в питьевой воде составляет 0,3 мг/л, лимитирующий показатель вредности — органолептический.
Марганец. Содержание марганца в подземных водах, не связанных с месторождениями, достигает 0,7 мг/л, связанных с месторождениями, — до 300 мг/л и выше. В поверхностных водах наблюдаются концентрации марганца до 8 мг/л, чаще всего за счет экзогенного поступления. Биологи относят марганец к эссенциальным микроэлементам, поскольку он входит в состав многих ферментов, гормонов и витаминов, влияющих на процессы роста, размножения, кроветворения и формирование иммунитета. Всасывание марганца, поступающего в организм с питьевой водой, незначительно вследствие гидролиза катионов марганца и образования малорастворимых солей. По данным ВОЗ, содержание марганца в питьевой воде до 0,5 мг/л не приводит к нарушению здоровья человека. Однако присутствие марганца в таких концентрациях может быть неприемлемым для водопотребителей, поскольку вода имеет металлический привкус и окрашивает ткани при стирке. Отечественный норматив содержания марганца в питьевой воде — 0,1 мг/л., показатель вредности — органолептический
Источник
Железо в сточных водах

Большинство предприятий предпочитает сбрасывать сточные воды в систему городской канализации. Такие сточные воды по своим ингредиентам являются производственно-бытовыми и должны соответствовать ПДК. За несанкционированный сброс сверх ПДК, в том числе и железа в сточных водах предприятию грозит крупный штраф. Так как в дальнейшем сточная вода поступает на городские очистные сооружения, и содержание в стоках компонентов сверх норматива приводит к негативному воздействию на работу очистных сооружений, в том числе и на биологическую очистку сточных вод.
На содержание железа в сточных водах большое влияние оказывают микроорганизмы, обитающие, в том числе и в канализационных трубопроводах. Крупная эколого-трофическая группировка железо- марганцевых бактерий играет ключевую роль в глобальных биогеохимических круговоротах железа и марганца — элементов, которые широко распространены в земной коре и имеют огромное практическое значение в жизни человека. Прокариотические организмы, могут окислять или восстанавливать железо и марганец- составные элементы стальных трубопроводов. Таким образом, железобактерии играют важную роль в коррозии металлов. Повышенная коррозия старых канализационных трубопроводов вследствие жизнедеятельности железо-бактерий может приводить, в том числе и к превышению содержания железа в сточных водах.
Предприятиям, чтобы избежать штрафных санкций за превышение железа в сточных водах необходимо проводить проверку воды в специализированной лаборатории. Химический анализ проб воды необходимо так же проводить и для ливневых сточных вод. Железо в ливневой сточной воде обычно содержится в малой концентрации. При достаточном содержании в воде растворенного кислорода железо (II) с легкостью переходит в железо(III) и осаждается в виде гидроксида. Достоверный результат содержания железа в сточных водах может быть получен только при при определении суммарного содержания железа во всех его формах. В лаборатории химического исследования для определения суммарного содержания железа в сточных водах используется фотометрический метод с 1,10-фенантролином, а так же фотометрический метод с сульфосалицилатом натрия. Для определения малых концентраций железа в природных и питьевых водах в лаборатории «Экологический мониторинг» используется метод вольтамперометрического титрования.
Заказать определение железа в сточных водах можно оставив заявку на sales@chemanalytica.ru , или воспользовавшись формой обратной связи.
В нашей лаборатории вы также можете провести
Источник
Очистка сточных вод от железа
Содержание статьи
Очистка воды от железа
Общеизвестными токсичными компонентами являются соединения железа и другие тяжелые металлы. При выветривании и эрозии почвы этот металл попадает в пресную воду, содержание в ней не должно превышать 0,3 мг/л. В противном случае возможно обнаружение по запаху, привкусу металла, а при окислении жидкость из-за него приобретет коричневый оттенок, бурый осадок.
В виде связанных соединений, а именно гидрооксидов и солей, примеси поступают в стоки в результате производственной деятельности человека. Допустимые нормы могут быть превышены, и это опасно для здоровья человека.
Особым токсичным эффектом обладают их растворенные формы.
Биологические очистные сооружения соединения металлов (Ме) практически не удаляют. Имеет место лишь частичная их сорбция на биомассе активного ила.
При длительном их накоплении происходит образование прочных связей с белком биоценоза. В результате окислительная способность его ухудшается.
Поэтому организация процесса изъятия металлов из производственных сливов требует серьезной проработки метода очистки сточных вод.
На заключительном этапе обработки жидких отходов достаточно высокую степень изъятия солей металлов дает установка специальных сорбционных фильтров с применением угольных материалов.
Более подробно об очистке сточных вод от тяжелых металлов читайте в статье «Очистка сточных вод от металлов».
Черный металл
Металлы с неметаллами образуют соли, а с кислородом — окислы. Железо встречается в стоках гальванических цехов, шахтном производстве, и т.д. Оно постоянно находится в водах городских очистных сооружений.
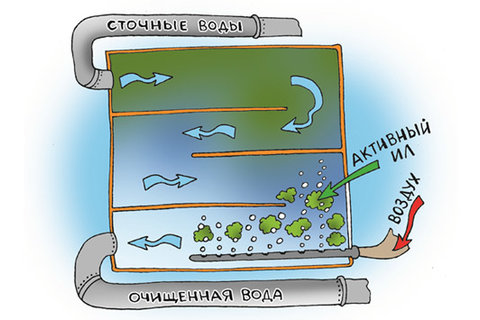
Степень удаления зависит от природы металла, начальной концентрации в загрязненных жидкостях, химических свойств дозы ила, времени взаимосвязи сточных вод с илом.
Устранение Fe в первичных отстойниках 0-25 %, а в аэротанках 75%.
Ответьте на 5 вопросов и получите ТКП
Ответьте на 5 вопросов и получите ТКП на очистные сооружения и гарантированную скидку
Соотношение нерастворимых и растворимых форм Fe разное для различных типов сточных вод и это необходимо определять экспериментально. Делать это нужно периодически на таких сооружениях биоочистки, где возникает токсическое «стрессирование» активного ила, которое вызывается соединениями растворенного железа и других металлов.
Предельно допустимые концентрации (ПДК) существуют только для растворимых форм, если указан ПДК общего содержания металла, например, общее железо, то в это понятие входит суммарное содержание в воде всех его растворимых валентных форм.
В процессе механической и биологической очистки нерастворимые соединения железа за счет осаждения и биосорбции хорошо выводятся из стоков, а растворимые удаляются меньшей долей.
Главными физико-химическими факторами , влияющими на интенсивность шокового воздействия металлов на активный ил, являются: температура, растворенный кислород, рН, жесткость и щелочность воды, присутствие загрязняющих агентов в воде, недостаток или дисбалансированный состав питательных веществ.
Главными биологическими факторами — рабочая доза активного ила (количество биомассы, на которую будет распространено действие токсических веществ); количество биополимерного геля, служащего детоксикатором; возраст и адаптационные свойства активного ила.
Чистим воду от железа
Удалить его возможно, превратив в нерастворимый элемент, сначала привести в Fe 3 , после пропустить через фильтр. К воде на производстве требования еще жёстче.
В жидкости железо представляет собой: двухвалентное Fe 2+ ,трехвалентное Fe 3 органическое, бактериальное.
1. Биологическая очистка
Представляет собой использование микроорганизмов – железобактерий. Благодаря этим бактериям закисное железо окисляется. Этот способ безопасный. После использования необходимо освободить воду от продуктов жизнедеятельности бактерий процессом адсорбции.
Минус — процесс долгий. Также требуются большие очистные емкости.
2. Окисление
Применяются окислители: хлор, кислород, перманганат калия. Этот метод используется на крупных водоочистных сооружениях.
3. Ионный обмен
Он более известен чем те, которые представлены выше и раньше использовался, чтоб умягчить жидкость. В современном мире используют высокомолекулярные соединения, образующиеся в результате реакции полимеризации, или концентрации химических веществ (стирола, этилена и т.д) — синтетические смолы, результативность улучшилась. Здесь применяются катионы, которые убирают Fe из воды в растворенном виде.
Минус — этот метод довольно сложный, потому что катионы уменьшают жёсткость воды.
Именно этот способ более эффективен. Но при подборе оптимальной комбинации ионообменных смол возникает сложность. Это необходимо для того, чтобы можно было работать с различными параметрами воды.
Простой способ избавится от Fe — это отстаивание жидкости на воздухе в течение времени, за которое оно станет осадком.
После жидкость нужно направить на лабораторный анализ. И из этих данных можно будет сделать вывод, какое водоочистное оборудование необходимо использовать для большей эффективности.
Источник