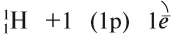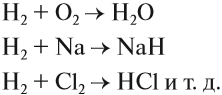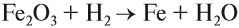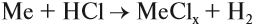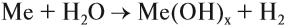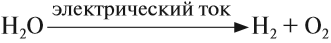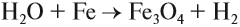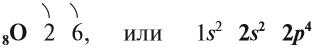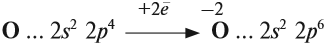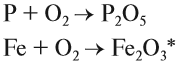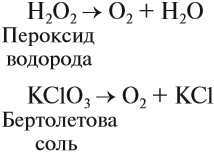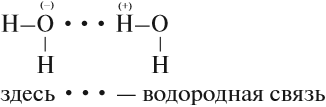Каким таким чудесным образом два ГАЗА (водород и кислород) при соединении становятся ЖИДКОСТЬЮ (водой)?!
Я понимаю, почему вода становится паром — увеличивается расстояние между молекулами при нагревании, а когда оно уменьшается от низких температур — жидкость вода становится твёрдым льдом. А вот как два газа превращаются в воду? В каких условиях возможно такое превращение? Я уже посмотрел, как сделать обратный процесс расщепления воды на два газа эл. током (электролиз) , и это понятно. Но как же СОЕДИНИТЬ два газа в жидкость-воду.
водород взаимодействует с водородом образуя пару и захватывают своей гравитацией
тепловые частицы . То же самое с двумя атомами кислорода .
Одна «тёплая» молекула кислорода взаимодействуя с двумя «тёплыми» молекулами водорода
образуют две молекулы воды HOH со сквозным движением элементарных частиц входящих
потоком в молекулу воды со стороны одного атома водорода и проходя через
кислород покидают вытесняются противоположным атомом водорода .
По сути водород в молекуле воды ведёт себя как двухвалентный элемент с разной
полярностью как и кислород .
Через молекулу воды проходит поток элементарных частиц
Вывод реакция между водородом и кислородом вытесняет тепловые частицы .
А двуокись углерода газ и движется винтом .
Ось углерод а лопасти кислород . можете проверить . поток движется восьмёркой
Справедливости ради, при сгорании водорода тоже получается газ, а уж после он конденсируется.
Ну и ваш холодильник только тем и занимается, что из одного единственного газа делает жидкость. После её испаряет и снова делает.
Эта.. . думаится, слипляютси лектрически — кисларод, панимашь, он чисто жаднай.. . а мож ишшо как.. . колдунизм метаморфознай!
Я Вам больше скажу — при соединении твердого вещества — углерода, и газа — кислорода, получается ГАЗ (углекислый) !
При соединении двух жидкостей — поликонденсата эпихлоргидрина с бисфенолом и перикиси этилена — получается твердый пластик, который мы называем эпоксидной смолой.
Происходит химическая реакция, образуются продукты химической реакции. Эти продукты могут иметь какие угодно физические свойства, ничем не похожие на свойства исходных веществ.
Физические свойства вещества зависят от его собственной структуры, и никак не зависят (или очень опосредовано зависят) от веществ, из которых оно получено.
Да, чудеса, да и только!
Наверное у атомов такие маленькие крючочки есть, и они друг за друга цепляются?:
Образуются молекулы нового вида — идет химическая реакция.
При соединении выделяется огромное кол-во энергии и происходит мини взрыв. Из этого взрыва образуется вода.
Чиркни спичкой и раздастся взрыв
«Да, чудеса, да и только!
Наверное у атомов такие маленькие крючочки есть, и они друг за друга цепляются?: »
Да, и петельки, за которые крючочки цепляются.
Источник
Водородная энергетика: начало большого пути
Ранее мы рассказывали про то, каким экологичным видом транспорта являются электробусы. Однако не упомянули один важный момент: c ростом числа электротранспорта городам потребуется больше электричества, которое зачастую получают экологически небезопасными способами. К счастью, сегодня мир научился получать энергию при помощи ветра, солнца и даже водорода. Новый материал мы решили посвятить последнему из источников и рассказать об особенностях водородной энергетики.
На первый взгляд, водород — идеальное топливо. Во-первых, он является самым распространенным элементом во Вселенной, во-вторых, при его сгорании высвобождается большое количество энергии и образуется вода без выделения каких-либо вредных газов. Преимущества водородной энергетики человечество осознало уже давно, однако применять ее в больших промышленных масштабах пока не спешит.
Водородные топливные элементы
Первый водородный топливный элемент был сконструирован английским ученым Уильямом Гроувом в 30-х годах XIX века. Гроув пытался осадить медь из водного раствора сульфата меди на железную поверхность и заметил, что под действием электрического тока вода распадается на водород и кислород. После этого открытия Гроув и работавший параллельно с ним Кристиан Шенбейн продемонстрировали возможность производства энергии в водородно-кислородном топливном элементе с использованием кислотного электролита.
Позже, в 1959 году, Фрэнсис Т. Бэкон из Кембриджа добавил в водородный топливный элемент ионообменную мембрану для облегчения транспорта гидроксид-ионов. Изобретением Бэкона сразу заинтересовалось правительство США и NASA, обновленный топливный элемент стал использоваться на космических аппаратах «Аполлон» в качестве главного источника энергии во время их полетов.

Водородный топливный элемент из сервисного модуля «Аполлонов», вырабатывающий электричество, тепло и воду для астронавтов. Источник: James Humphreys / Wikimedia Commons
Сейчас топливный элемент на водороде напоминает традиционный гальванический элемент с одной лишь разницей: вещество для реакции не хранится в элементе, а постоянно поставляется извне. Просачиваясь через пористый анод, водород теряет электроны, которые уходят в электрическую цепь, а сквозь мембрану проходят катионы водорода. Далее на катоде кислород ловит протон и внешний электрон, в результате чего образуется вода.

Принцип работы водородного топливного элемента. Источник: Geek.com
С одной топливной ячейки снимается напряжение порядка 0,7 В, поэтому ячейки объединяют в массивные топливные элементы с приемлемым выходным напряжением и током. Теоретическое напряжение с водородного элемента может достигать 1,23 В, но часть энергии уходит в тепло.
С точки зрения «зеленой» энергетики у водородных топливных элементов крайне высокий КПД — 60%. Для сравнения: КПД лучших двигателей внутреннего сгорания составляет 35-40%. Для солнечных электростанций коэффициент составляет всего 15-20%, но сильно зависит от погодных условий. КПД лучших крыльчатых ветряных электростанций доходит до 40%, что сравнимо с парогенераторами, но ветряки также требуют подходящих погодных условий и дорогого обслуживания.
Как мы видим, по этому параметру водородная энергетика является наиболее привлекательным источником энергии, но все же существует ряд проблем, мешающих ее массовому применению. Самая главная из них — процесс добычи водорода.
Проблемы добычи
Водородная энергетика экологична, но не автономна. Для работы топливному элементу нужен водород, который не встречается на Земле в чистом виде. Водород нужно получать, но все существующие сейчас способы либо очень затратны, либо малоэффективны.
Самым эффективным с точки зрения объёма полученного водорода на единицу затраченной энергии считается метод паровой конверсии природного газа. Метан соединяют с водяным паром при давлении 2 МПа (около 19 атмосфер, т. е. давление на глубине около 190 м) и температуре около 800 градусов, в результате чего получается конвертированный газ с содержанием водорода 55-75%. Для паровой конверсии необходимы огромные установки, которые могут быть применимы лишь на производстве.

Трубчатая печь для паровой конверсии метана — не самый эргономичный способ добычи водорода. Источник: ЦТК-Евро
Более удобный и простой метод — электролиз воды. При прохождении электрического тока через обрабатываемую воду происходит серия электрохимических реакций, в результате которых образуется водород. Существенный недостаток этого способа — большие энергозатраты, необходимые для проведения реакции. То есть получается несколько странная ситуация: для получения водородной энергии нужна… энергия. Во избежание возникновения при электролизе ненужных затрат и сохранения ценных ресурсов некоторые компании стремятся разработать системы полного цикла «электричество — водород— электричество», в которых получение энергии становится возможным без внешней подпитки. Примером такой системы является разработка Toshiba H2One.
Мобильная электростанция Toshiba H2One
Мы разработали мобильную мини-электростанцию H2One, преобразующую воду в водород, а водород в энергию. Для поддержания электролиза в ней используются солнечные батареи, а излишки энергии накапливаются в аккумуляторах и обеспечивают работу системы в отсутствие солнечного света. Полученный водород либо напрямую подается на топливные ячейки, либо отправляется на хранение во встроенный бак. За час электролизер H2One генерирует до 2 м 3 водорода, а на выходе обеспечивает мощность до 55 кВт. Для производства 1 м 3 водорода станции требуется до 2,5 м 3 воды.
Пока станция H2One не способна обеспечить электричеством крупное предприятие или целый город, но для функционирования небольших районов или организаций ее энергии будет вполне достаточно. Благодаря своей мобильности она может использоваться также как и временное решение в условиях стихийных бедствий или экстренного отключения электричества. К тому же, в отличие от дизельного генератора, которому для нормального функционирования необходимо топливо, водородной электростанции достаточно лишь воды.
Сейчас Toshiba H2One используется лишь в нескольких городах в Японии — к примеру, она снабжает электричеством и горячей водой железнодорожную станцию в городе Кавасаки.
Монтаж системы H2One в городе Кавасаки
Водородное будущее
Сейчас водородные топливные элементы обеспечивают энергией и портативные пауэр-банки, и городские автобусы с автомобилями, и железнодорожный транспорт (более подробно об использовании водорода в автоиндустрии мы расскажем в нашем следующем посте). Водородные топливные элементы неожиданно оказались отличным решением для квадрокоптеров — при аналогичной с аккумулятором массе запас водорода обеспечивает до пяти раз большее время полета. При этом мороз никак не влияет на эффективность. Экспериментальные дроны на топливных элементах производства российской компании AT Energy применялись для съемок на Олимпиаде в Сочи.
Стало известно, что на грядущих Олимпийских играх в Токио водород будет использоваться в автомобилях, при производстве электричества и тепла, а также станет главным источником энергии для олимпийской деревни. Для этого по заказу Toshiba Energy Systems & Solutions Corp. в японском городе Намиэ строится одна из крупнейших в мире станций по производству водорода. Станция будет потреблять до 10 МВт энергии, полученной из «зеленых» источников, генерируя электролизом до 900 тонн водорода в год.
Водородная энергетика — это наш «запас на будущее», когда от ископаемого топлива придется окончательно отказаться, а возобновляемые источники энергии не смогут покрывать нужды человечества. Согласно прогнозу Markets&Markets объем мирового производства водорода, который сейчас составляет $115 млрд, к 2022 году вырастет до $154 млрд. Но в ближайшем будущем массовое внедрение технологии вряд ли произойдет, необходимо еще решить ряд проблем, связанных с производством и эксплуатацией специальных энергоустановок, снизить их стоимость. Когда технологические барьеры будут преодолены, водородная энергетика выйдет на новый уровень и, возможно, будет так же распространена, как сегодня традиционная или гидроэнергетика.
Источник
Урок 12. Водород и кислород
Водород
Водород — самый распространённый химический элемент во Вселенной. Именно он составляет основу горючего вещества Звёзд.
Водород — первый химический элемент Периодической системы Менделеева. Его атом имеет простейшее строение: вокруг элементарной частицы «протон» (ядро атома) вращается один-единственный электрон:
Природный водород состоит из трех изотопов: протий 1 Н, дейтерий 2 Н и тритий 3 Н.
Задание 12.1. Укажите строение ядер атомов этих изотопов.
Имея на внешнем уровне один электрон, атом водорода может проявлять единственно возможную для него валентность I:
Вопрос. Образуется ли завершённый внешний уровень при приёме атомом водорода электронов?
Таким образом, атом водорода может и принимать, и отдавать один электрон, т. е. является типичным неметаллом. В любых соединениях атом водорода одновалентен.
Простое вещество «водород» Н2 — газ без цвета и запаха, очень лёгкий. Он плохо растворим в воде, но хорошо растворим во многих металлах. Так, один объём палладия Рd поглощает до 900 объёмов водорода.
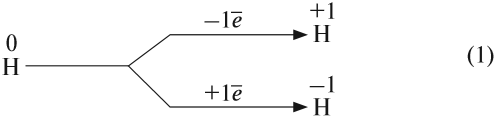
Схема (1) показывает, что водород может быть и окислителем, и восстановителем, реагируя с активными металлами и многими неметаллами:
Задание 12.2. Определите, в каких реакциях водород является окислителем, а в каких — восстановителем. Обратите внимание, что молекула водорода состоит из двух атомов.
Смесь водорода и кислорода является «гремучим газом», поскольку при поджигании её происходит сильнейший взрыв, который унёс многие жизни. Поэтому опыты, в которых выделяется водород, нужно выполнять подальше от огня.
Чаще всего водород проявляет восстановительные свойства, что используется при получении чистых металлов из их оксидов*:
* Аналогичные свойства проявляет алюминий (см. урок 10 — алюминотермия).
Разнообразные реакции происходят между водородом и органическими соединениями. Так, за счёт присоединения водорода (гидрирование) жидкие жиры превращаются в твёрдые (подробнее урок 25).
Водород можно получить разными способами:
- Взаимодействием металлов с кислотами:
Задание 12.3. Составьте уравнения таких реакций для алюминия, меди и цинка с соляной кислотой. В каких случаях реакция не идет? Почему? В случае затруднения см. уроки 2.2 и 8.3;
- Взаимодействие активных металлов с водой:
Задание 12.4. Составьте уравнения таких реакций для натрия, бария, алюминия, железа, свинца. В каких случаях реакция не идёт? Почему? В случае затруднений см. урок 8.3.
В промышленных масштабах водород получают электролизом воды:
а также при пропускании паров воды через раскалённые железные опилки:
Водород — самый распространённый элемент Вселенной. Он составляет бОльшую часть массы звёзд и участвует в термоядерном синтезе — источнике энергии, которую эти звёзды излучают.
Кислород
Кислород — самый распространённый химический элемент нашей планеты: более половины атомов Земной коры приходится на кислород. Вещество кислород О2 составляет около 1/5 нашей атмосферы, а химический элемент кислород — 8/9 гидросферы (Мирового океана).
В Периодической системе Менделеева кислород имеет порядковый номер 8 и находится в VI группе второго периода. Поэтому строение атома кислорода следующее:
Имея на внешнем уровне 6 электронов, кислород является типичным неметаллом, т. е. присоединяет два электрона до завершения внешнего уровня:
Поэтому кислород в своих соединениях проявляет валентность II и степень окисления –2 (за исключением пероксидов).
Принимая электроны, атом кислорода проявляет свойства окислителя. Это свойство кислорода исключительно важно: процессы окисления происходят при дыхании, обмене веществ; процессы окисления происходят при горении простых и сложных веществ.
Горение — окисление простых и сложных веществ, которое сопровождается выделением света и теплоты. В атмосфере кислорода горят или окисляются почти все металлы и неметаллы. При этом образуются оксиды:
При горении в кислороде сложных веществ образуются оксиды химических элементов, входящих в состав исходного вещества. Только азот и галогены выделяются в виде простых веществ:
Вторая из этих реакций используется как источник тепла и энергии в быту и промышленности, так как метан CH4 входит в состав природного газа.
Кислород позволяет интенсифицировать многие промышленные и биологические процессы. В больших количествах кислород получают из воздуха, а также электролизом воды (как и водород). В небольших количествах его можно получить разложением сложных веществ:
Задание 12.5. Расставьте коэффициенты в приведенных здесь уравнениях реакций.
Воду нельзя ничем заменить — этим она отличается практически от всех других веществ, которые встречаются на нашей планете. Воду может заменить только сама вода. Без воды нет жизни: ведь жизнь на Земле возникла тогда, когда на ней появилась вода. Жизнь зародилась в воде, поскольку она является естественным универсальным растворителем. Она растворяет, а значит, измельчает все необходимые питательные вещества и обеспечивает ими клетки живых организмов. А в результате измельчения резко возрастает скорость химических и биохимических реакций. Более того, без предварительного растворения невозможно протекание 99,5 % (199 из каждых 200) реакций! (См. также урок 5.1.)
Известно, что взрослый человек в сутки должен получать 2,5–3 л воды, столько же выводится из организма: т. е. в организме человека существует водный баланс. Если он нарушается, человек может просто погибнуть. Например, потеря человеком всего 1–2 % воды вызывает жажду, а 5 % — повышает температуру тела вследствие нарушения терморегуляции: возникает сердцебиение, возникают галлюцинации. При потере 10 % и более воды в организме возникают такие изменения, которые уже могут быть необратимы. Человек погибнет от обезвоживания.
Вода — уникальное вещество. Её температура кипения должна составлять –80 °C (!), однако равна +100 °C. Почему? Потому что между полярными молекулами воды образуются водородные связи:
Поэтому и лёд, и снег — рыхлые, занимают больший объём, чем жидкая вода. В результате лёд поднимается на поверхность воды и предохраняет обитателей водоёмов от вымерзания. Свежевыпавший снег содержит много воздуха и является прекрасным теплоизолятором. Если снег покрыл землю толстым слоем, то и животные и растения спасены от самых суровых морозов.
Кроме того, вода имеет высокую теплоёмкость и является своеобразным аккумулятором тепла. Поэтому на побережьях морей и океанов климат мягкий, а хорошо политые растения меньше страдают от заморозков, чем сухие.
Без воды в принципе невозможен гидролиз, химическая реакция, которая обязательно сопровождает усвоение белков, жиров и углеводов, которые являются обязательными компонентами нашей пищи. В результате гидролиза эти сложные органические вещества распадаются до низкомолекулярных веществ, которые, собственно, и усваиваются живым организмом (подробнее см. уроки 25–27). Процессы гидролиза были нами рассмотрены в уроке 6. Вода реагирует со многими металлами и неметаллами, оксидами, солями.
Задание 12.6. Составьте уравнения реакций:
- натрий + вода →
- хлор + вода →
- оксид кальция + вода →
- оксид серы (IV) + вода →
- хлорид цинка + вода →
- силикат натрия + вода →
Изменяется ли при этом реакция среды (рН)?
Вода является продуктом многих реакций. Например, в реакции нейтрализации и во многих ОВР обязательно образуется вода.
Задание 12.7. Составьте уравнения таких реакций.
Выводы
Водород — самый распространённый химический элемент во Вселенной, а кислород — самый распространённый химический элемент на Земле. Эти вещества проявляют противоположные свойства: водород — восстановитель, а кислород — окислитель. Поэтому они легко реагируют друг с другом, образуя самое удивительное и самое распространённое на Земле вещество — воду.
Источник