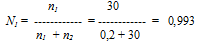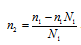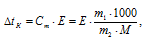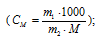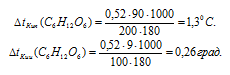- Вычисление понижения давления газа при указанной температуре
- При 293 K давление насыщенного пара над водой равно 17,53 мм рт. ст.
- При 293 К давление насыщенного пара над водой равно 2, 34 кПа?
- В газометре над водой находится 7, 4 л кислорода при 23 °С и давлении 104, 1 кПа?
- 1. Рассчитайте молярную массу эквивалента сульфата аммония и азотной кислоты?
- При 25 градусов давление паров воды равно 23?
- Сколько воды надо прибавить к 5 л раствора сахара С12Н22O11, чтобы понизить его осмотическое давление с 10, 13•10 ^ 5 до 1, 013•10 ^ 5 Па?
- В 500 г?
- Сроччно?
- Сколько молекул воды содержится в 1см3 её паров при 25 градусах и давлении 3171 Па?
- В газометре над водой находится О2 объемом 7, 4 дм3 при 296 К и давлении 104, 1 кПа (781 мм рт?
- Сколько граммов глюкозы С6Н12О6 следует растворить в 150 г?
- Каково давление пара раствора, содержащего 0, 2 моль сахара в 450 гр?
Вычисление понижения давления газа при указанной температуре
Задача 475
При 315 К давление насыщенного пара над водой равно 8,2 кПа (61,5 мм рт. ст.). На сколько понизится давление пара при указанной температуре, если в 540 г воды растворить 36 г глюкозы С6Н12О6?
Решение:
M(С6Н12О6) = 180,г/моль, М(Н2О) – 18,г/моль.
Для расчета по формуле P1 = N1P0 нужно вычислить мольную долю растворителя N1. Мольная масса воды равна 18,г/моль, мольная масса глюкозы — 180 г/моль. Количество воды и сахарозы соответственно равны:
Находим мольную долю воды:
Р1= 0,993 . 8,2 = 8,14 кПа.
Понижение давления пара находим по формуле:

Ответ: 0,06кПа.
Задача 476.
При 293 К давление насыщенного пара над водой равно 2,34 кПа (17,53 мм рт. ст.). Сколько граммов глицерина С3Н5(ОН)3 надо растворить в 180 г воды, чтобы понизить давление пара на 133,3 Па (1 мм рт. ст.)?
Решение:
M[С3Н5(ОН)3] = 92г/моль, М(Н2О) = 18,г/моль.
Из формулы: 
Р1 — Р0 — 
Из формулы P1 = N1P0 находим мольную долю растворителя N1, получим:
Из уравнения 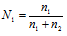
где n1 – число молей растворителя, n2 – число молей растворенного вещества получим выражение для расчета числа молей растворённого вещества глицерина, получим:
Количество воды равно: n1 = 18/18 = 10 моль;
Находим количество глицерина: 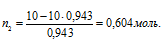
Находим массу глицерина из формулы n2 = m/M, где m – масса вещества; М – мольная масса вещества.
Тогда m = n2M =0,604 . 92 = 55,6г.
Ответ: 55,6г.
Задача 477.
На сколько градусов повысится температура кипения воды, если в 100 г воды растворить 9 г глюкозы С6Н12О6?Решение:
М(С6Н12О6) = 180г/моль. Для расчетов используем уравнение:
где СМ — моляльная концентрация, рассчитаем по уравнению:
где m1 — масса растворённого вещества; m2 — масса растворителя; М – молярная масса растворённого вещества; Е – эбуллиоскопическая константа (для воды Е = 0,52); 
Находим повышение температуры кипения растворов глюкозы:
Ответ: на 0,26 град.
Задача 478.
При какой приблизительно температуре будет кипеть 50%-ный (по массе) раствор сахарозы C12H22О11?
Решение:
M( С12Н22О11 ) = 342г/моль.
При пересчете на 1000 г Н2О содержание сахарозы в растворе равно 500 г. Поскольку мольная масса сахарозы составляет 342 г/моль, то моляльность раствора рассчитаем по уравнению:
где m1 — масса растворённого вещества; m2 — масса растворителя; М – молярная масса растворённого вещества; Е – эбуллиоскопическая константа (для воды Е = 0,52); 
Находим повышение температуры кипения растворов сахарозы:
СМ = (500 . 1000)/(1000 . 342) = 1,46 моля на 1000 г Н2О.
По формуле 

Источник
При 293 K давление насыщенного пара над водой равно 17,53 мм рт. ст.
| 🎓 Заказ №: 22179 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
При 293 K давление насыщенного пара над водой равно 17,53 мм рт. ст. Сколько граммов глицерина C3H8O3 надо растворить в 180 г воды, чтобы понизить давление пара на 12 мм рт. ст.?
Решение: Согласно закону Рауля, относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного вещества 1 2 1 0 n n n P P где: P0 давление насыщенного пара над водой; P относительное понижение давления насыщенного пара; n1 количество растворенного вещества, моль; n2 количество растворителя, моль. Молярная масса воды равна 18 г/моль Находим количество вещества воды
Научись сам решать задачи изучив химию на этой странице:
|
Услуги:
|
Готовые задачи по химии которые сегодня купили:





















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Источник
При 293 К давление насыщенного пара над водой равно 2, 34 кПа?
Химия | 10 — 11 классы
При 293 К давление насыщенного пара над водой равно 2, 34 кПа.
Сколько граммов глицерина C3H5(OH)3 надо растворить в 180 г воды, чтобы понизить давление пара на 133, 3 Па?
По закону Рауля :
p / p0 = N(C3H2(OH)3)
Доля глицерина в растворе N = 133.
057 n(H2O) = m / M = 180 / 18 = 10 моль n(глиц.
) = 0, 057 * 10 / 0, 943 = 0, 604 моль m(глицерина) = M * n = 92 * 0.
В газометре над водой находится 7, 4 л кислорода при 23 °С и давлении 104, 1 кПа?
В газометре над водой находится 7, 4 л кислорода при 23 °С и давлении 104, 1 кПа.
Давление насыщенного водяного пара при 23 °С равно 21 мм рт.
Ст. Какой объем займет находящийся в газометре кислород при нормальных условиях?
1. Рассчитайте молярную массу эквивалента сульфата аммония и азотной кислоты?
1. Рассчитайте молярную массу эквивалента сульфата аммония и азотной кислоты.
2. Как называется способ выражения состава раствора, когда находится отношение массы растворенного вещества к общей массе раствора?
3. Вычислите массу воды и растворяемого вещества, которые потребуются для приготовления 1 литра 8% — ного раствора дихромата калия (ρ = 1, 0554 г / мл).
4. Вычислите молярную концентрацию 12% — ного раствора азотной кислоты (ρ = 1, 066 г / мл).
5. Вычислите давление пара над раствором, содержащим 22 г глицерина C3H5(OH)3 в 120 г воды, если давление пара над чистой водой при данной температуре составляет 101, 3 кПа.
При 25 градусов давление паров воды равно 23?
При 25 градусов давление паров воды равно 23.
Чему равно давление паров воды над растворомсодержащим 6 где мочевины в 180 где воды.
Сколько воды надо прибавить к 5 л раствора сахара С12Н22O11, чтобы понизить его осмотическое давление с 10, 13•10 ^ 5 до 1, 013•10 ^ 5 Па?
Сколько воды надо прибавить к 5 л раствора сахара С12Н22O11, чтобы понизить его осмотическое давление с 10, 13•10 ^ 5 до 1, 013•10 ^ 5 Па.
В 500 г?
Воды растворили 80 л.
HCL, измеренного при 27(градусах)C и давлении 110 кПа.
Вычислить массовую долю HCL в полученном растворе.
Сроччно?
Давление пара водного раствора неэлектролита при 80 градусах цельсия равно 33310Па.
Какое количество воды приходиться на 1 моль растворенного вещества?
Давление пара воды при 80 градусах равно 47375 Па?
Прошу полное решение срочно).
Сколько молекул воды содержится в 1см3 её паров при 25 градусах и давлении 3171 Па?
Сколько молекул воды содержится в 1см3 её паров при 25 градусах и давлении 3171 Па.
В газометре над водой находится О2 объемом 7, 4 дм3 при 296 К и давлении 104, 1 кПа (781 мм рт?
В газометре над водой находится О2 объемом 7, 4 дм3 при 296 К и давлении 104, 1 кПа (781 мм рт.
Давление на — сыщенного водяного пара при этой температуре равно 2, 8 кПа (21 мм рт.
У. ) займет находящий в газо — метре кислород?
Сколько граммов глюкозы С6Н12О6 следует растворить в 150 г?
Сколько граммов глюкозы С6Н12О6 следует растворить в 150 г.
Воды Н2О, чтобы температура кристаллизации раствора понизилась на 0, 465 °С.
Криоскопическая постоянная воды равна 1, 86 (градус ∙ кг) / моль.
Каково давление пара раствора, содержащего 0, 2 моль сахара в 450 гр?
Каково давление пара раствора, содержащего 0, 2 моль сахара в 450 гр.
Вы находитесь на странице вопроса При 293 К давление насыщенного пара над водой равно 2, 34 кПа? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 10 — 11 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
Источник