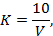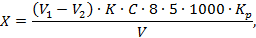- Очистка воды от органики (перманганатная окисляемость)
- Очистка воды от органики из колодца
- Готовые решения, предлагаемые к установке:
- Очистка воды от органики из скважины
- 1 ОБЛАСТЬ ПРИМЕНЕНИЯ
- 2 НОРМАТИВНЫЕ ССЫЛКИ
- 3 ПРИПИСАННЫЕ ХАРАКТЕРИСТИКИ ПОКАЗАТЕЛЕЙ ТОЧНОСТИ ИЗМЕРЕНИЙ
- 4 МЕТОД ИЗМЕРЕНИЙ
- 5 СРЕДСТВА ИЗМЕРЕНИЙ. ВСПОМОГАТЕЛЬНЫЕ УСТРОЙСТВА. РЕАКТИВЫ И МАТЕРИАЛЫ
- 5.1 Средства измерений, вспомогательное оборудование, лабораторная посуда
- 5.2 Реактивы и материалы
- 6 УСЛОВИЯ БЕЗОПАСНОГО ПРОВЕДЕНИЯ РАБОТ
- 7 ТРЕБОВАНИЯ К КВАЛИФИКАЦИИ ОПЕРАТОРА
- 8 УСЛОВИЯ ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
- 9 ОТБОР И ХРАНЕНИЕ ПРОБ
- 10 ПОДГОТОВКА К ВЫПОЛНЕНИЮ ИЗМЕРЕНИЙ
- 10.1 Подготовка дистиллированной воды
- 10.2 Подготовка лабораторной посуды для титрования
- 10.3 Приготовление растворов
- 10.4 Установление поправочного коэффициента к раствору перманганата калия
- 11 ВЫПОЛНЕНИЕ ИЗМЕРЕНИЙ
- 12 ОБРАБОТКА РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
- 13 ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Окисляемость — это величина, показывающая общее содержание в воде органических веществ, окисляемых одним из сильных химических окислителей. Этот показатель отражает общую концентрацию органики в воде. Природа органических веществ может быть разнообразной: гуминовые и фульвокислоты почв, либо сложная органика растений, метаболиты бактерий, а так же химические продукты антропогенного воздействия на окружающую среду.
Перманганатная окисляемость выражается в миллиграммах кислорода, затраченного на окисление таких веществ, содержащихся в 1 литре (дм 3 ) воды.
В практике водоочистки для природных малозагрязненных вод определяют перманганатную окисляемость, а в более загрязненных водах — как правило, бихроматную окисляемость (ХПК — «химическое потребление кислорода»).
Величина окисляемости природных вод может варьироваться в широких пределах от долей миллиграммов до десятков миллиграммов О2 на литр воды. Поверхностные воды имеют более высокую окисляемость по сравнению с подземными. Это понятно — органика из почвы и растительного опада легче попадает в поверхностные воды, чем в грунтовые, чаще всего ограниченные глинистыми водоупорами. Вода равнинных рек как правило имеет окисляемость 5-12 мг О2 /дм 3 , рек с болотным питанием — десятки миллиграммов на 1 дм 3 . Подземные воды имеют в среднем окисляемость на уровне от сотых до десятых долей миллиграма О2 /дм 3 . Хотя подземные воды в районах нефтегазовых месторождений, и торфянников могут иметь очень высокую окисляемость.
Согласно СанПиН 2.1.4.1175-02 «Гигиенические требования к качеству воды нецентрализованного водоснабжения. Санитарная охрана источников» ПДК питьевой воды по перманганатной окисляемости составляет 5,0 мг/дм 3 .
Источник
Очистка воды от органики (перманганатная окисляемость)
Содержание органики в воде отражает показатель перманганатная окисляемость . Если концентрация ПМО в воде превышает 5 мг/л, то это означает, что необходима очистка воды от органики.
Органические вещества по своей сути посторонние в составе воды. Они имеют различное происхождение и пути поступления. Чаще всего в воде они представлены растворёнными кислотами из торфяных почв. Об этом можно судить по интенсивности цвета воды от желтоватого до бурого. Появление органики в воде возможно и в результате жизнедеятельности живых организмов и растений, а так же процессов их разложения.
Чтобы получить бесплатный расчет водоочистной системы (с ценами)
(3-4 варианта, которые гарантированно очистят вашу воду ) :
- Пришлите результаты анализа воды на электронную почту info@kr-company.ru с пояснением, в каких объёмах нужна очищенная вода;
- Или позвоните по телефону 8 (800) 222 80 97
- ЛибоЗакажите анализ воды в нашей аккредитованной лаборатории.
Органические вещества могут быть не только вредными или неприятными, но и опасными для здоровья. Они нарушают работу эндокринной системы. К тому же эти примеси могут содержать различные болезнетворные бактерии и вирусы, а так же токсичные вещества — диоксины. Отравление диоксинами приводит к тому, что подавляется иммунитет и нарушается нормальный процесс деления клеток. А значит органические загрязнения могут значительно способствовать возникновению онкологических заболеваний.

Однако негативное влияние высокого уровня перманганатной окисляемости обуславливается не только этим. Зачастую органика мешает протеканию процессов очистки воды от других примесей. Например, она связывает на молекулярном уровне растворённые вещества, такие как железо и марганец. К тому же для окисления органические продукты первыми потребляют кислород из воды, тем самым для окисления железа или марганца его уже практически не остаётся. Повышенное значение показателя перманганатной окисляемости воде из скважины указывает на присутствие органики.
Вещества органического происхождения не дают долгое время окисляться двухвалентному железу и марганцу. Это опасно тем, что из растворённых форм они переходят в нерастворённую, уже пройдя систему очистки воды . Таким образом тяжёлые металлы могут выпадать в осадок как в бытовой технике, так и в организме человека.
Очистка воды от органики из колодца
Способы очистки воды от органики зависят от её концентрации в воде. Норматив содержания таких примесей – 5 мг/л.
В колодце присутствие органических загрязнений часто бывает превышено. Особенно в жаркое летнее время. Их накоплению способствует наличие кислот в почве.
Другой способ попадания органических веществ в колодец – стоки поверхностных вод или окружающие грунты. Наиболее благоприятной средой для размножения микроводорослей и бактерий обычно становятся верхние слои воды в колодце. Попадание мелкого мусора, насекомых, листьев и пыльцы растений – всё это так же служит источником органических веществ в воде. Разлагаясь, они увеличивают потребление кислорода и значение перманганатной окисляемости.
Выведение органики из воды способствует более активному удалению из неё других примесей. В этом случае для колодезной воды используют фильтры комплексной очистки. Специально подобранная фильтрующая среда удаляет растворённые и взвешенные органические вещества при значениях ПМО до 20 мг-О2/л. Регенерация фильтров производится солевым раствором.
При значениях окисляемости более 20 мг-О2/л в исходную воду необходимо дозировать раствор коагулянта. Этот процесс способствует выведению органических загрязнений из воды тем, что связывает их молекулы между собой и они слипаются в крупные хлопья. Концентрация и объём коагулирующего раствора подбирается индивидуально по значениям ПМО.
Если по каким-то причинам обслуживание фильтра комплексной очистки затруднительно, компания «Комплексные решения» предлагает вариант очистки воды с использованием накопительных баков. Ручная или автоматическая дозация коагулянта способствует быстрому слипанию органики в хлопья и выпадению их в осадок. Вместе с этим из воды устраняются излишки связанного с органикой железа и марганца. Далее из накопительного бака вода подаётся насосной станцией на промывную Титановую мембрану. Органические вещества в виде хлопьев задерживаются на её поверхности и сбрасываются в канализацию при обратной промывке.
Готовые решения, предлагаемые к установке:
Очистка воды от органики из скважины
Наличие органики в скважинах – редкое явление, так как там слишком мало кислорода. В то же время, в скважинах, глубина которых не превышает 10 метров – это вполне возможно. Особенность этих источников такова, что поступление органических веществ в воду перекрывается водоупорными пластами глин. Однако состав залегающих грунтовых слоёв может быть разнообразным. Для неглубоких скважин характерно поступление органики с водой из гумусовых почв. С осадками и стоками органические вещества также могут попадать в неё с поверхности земли. Глубокие скважины в этом отношении наиболее защищены. Единственной проблемой здесь может быть нарушение структуры залегания грунтов вследствие вмешательства человека или природного фактора. В этом случае следы органических соединений могут означать поступление из вышележащих слоёв, либо соседних, где производится сброс хозяйственно-бытовых отходов.
Очистить воду от органики можно с помощью фильтров комплексной очистки, а так же дозацией коагулянта.
Источник
1 ОБЛАСТЬ ПРИМЕНЕНИЯ
Настоящий нормативный документ устанавливает титриметрическую методику определения перманганатной окисляемости (перманганатного индекса) в диапазоне от 0,25 до 100 мг/дм 3 в расчете на атомарный кислород.
Методика предназначена для анализа проб питьевых (в том числе расфасованных в емкости), природных (в том числе поверхностных и подземных источников водоснабжения) и сточных вод (в том числе очищенных и ливневых). Методика может быть использована для анализа проб воды бассейнов и аквапарков, а также воды горячего водоснабжения.
Методика применима для вод с содержанием хлорид-ионов менее 300 мг/дм 3 .
Перманганатная окисляемость — количество кислорода, потребляемое при химическом окислении содержащихся в воде органических и неорганических веществ под действием раствора перманганата калия при нагревании в кислой среде. Поскольку окисляемые неорганические вещества, как правило, в воде присутствуют в незначительных количествах, то принято считать, что перманганатная окисляемость отражает общее содержание в воде органических веществ.
В определенной степени на значение перманганатного индекса могут влиять железо (II), сероводород, нитриты. Если лаборатории необходимо определять по настоящей методике содержание только органических веществ, то необходимо учитывать при расчете окончательного результата содержание восстанавливающих веществ. В этом случае железо (II), сероводород, нитриты определяют отдельно, а результат, пересчитанный на окисляемость, вычитают из найденного значения перманганатной окисляемости. При пересчете исходят из соотношений: 1 мг сероводорода потребляет 0,47 мг атомарного кислорода, 1 мг нитритов — 0,35 мг, 1 мг железа (II) — 0,14 мг.
Обычно в питьевых и природных водах восстановители присутствуют в незначительных количествах и их влиянием на результат определения органических веществ можно пренебречь.
Примечание — Наличие железа (II) и сероводорода в пробе при значениях перманганатного индекса до 2 мг/дм 3 в наибольшей степени может оказать влияние на результат анализа. Такой состав пробы наиболее характерен для подземных вод.
Блок схема проведения анализа приведена в Приложении 1.
2 НОРМАТИВНЫЕ ССЫЛКИ
ГОСТ Р ИСО 5725-6-2002. Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб
ГОСТ Р 51593-2000 Вода питьевая. Отбор проб
ГОСТ Р 52501-2005 Вода для лабораторного анализа. Технические условия
ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 12.0.004-90 Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
ГОСТ 22180-76 Реактивы. Кислота щавелевая. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 27384-2002 Вода. Нормы погрешностей измерений показателей состава и свойств
ГОСТ 28311-89 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
ГОСТ 29169-91 Посуда лабораторная стеклянная. Пипетки с одной отметкой
ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 29251-91 Посуда лабораторная стеклянная. Бюретки. Часть 1. Общие требования
3 ПРИПИСАННЫЕ ХАРАКТЕРИСТИКИ ПОКАЗАТЕЛЕЙ ТОЧНОСТИ ИЗМЕРЕНИЙ
Настоящая методика обеспечивает получение результатов анализа с погрешностями, не превышающими значений, приведенных в таблице 1. Приписанные значения погрешности измерений не превышают нормы погрешности, установленные ГОСТ 27384.
Диапазон измерений, мг/дм 3
Показатель повторяемости (стандартное отклонение повторяемости), σ r , %
Показатель воспроизводимости (стандартное отклонение воспроизводимости) σ R , %
Показатель точности (границы относительной погрешности при Р = 0,95), ±δ,%
от 0,25 до 2,0 вкл.
св. 2 до 100 вкл.
Примечание — Показатель точности измерений соответствует расширенной неопределенности при коэффициенте охвата k = 2
4 МЕТОД ИЗМЕРЕНИЙ
Метод основан на окислении органических и неорганических веществ, присутствующих в пробе воды, известным количеством перманганата калия в сернокислой среде при кипячении в течение 10 минут. Не вошедший в реакцию перманганат калия восстанавливают щавелевой кислотой. Избыток щавелевой кислоты оттитровывают раствором перманганата калия.
Для получения достоверных и сравнимых между собой результатов необходимо строго придерживаться условий проведения анализа.
5 СРЕДСТВА ИЗМЕРЕНИЙ. ВСПОМОГАТЕЛЬНЫЕ УСТРОЙСТВА. РЕАКТИВЫ И МАТЕРИАЛЫ
5.1 Средства измерений, вспомогательное оборудование, лабораторная посуда
5.1.1 Бюретка вместимостью 25 см 3 по ГОСТ 29251,2 класса точности.
Примечание — Допускается использовать цифровые бюретки, например, фирмы BRAND, Hirshman и др.
5.1.2 Весы лабораторные с максимальной нагрузкой 210 г высокого класса точности по ГОСТ Р 53228.
5.1.3 Воронки стеклянные d = 5 см по ГОСТ 25336.
5.1.4 Государственный стандартный образец (далее ГСО) перманганатной окисляемости воды с погрешностью аттестованного значения при доверительной вероятности Р = 0,95 не более 1 %.
5.1.5 Дистиллятор или установка любого типа для получения воды дистиллированной по ГОСТ 6709 или воды для лабораторного анализа степени чистоты 2 по ГОСТ Р 52501 (далее — вода дистиллированная).
5.1.6 Колбы конические вместимостью 250 см 3 по ГОСТ 25336.
5.1.7 Колбы мерные вместимостью 1000 см 3 по ГОСТ 1770, 2 класса точности.
5.1.8 Пипетки вместимостью 5; 10; 15; 100 см 3 по ГОСТ 29227, 2 класса точности.
5.1.9 Пипетки с одной меткой вместимостью 100 см 3 по ГОСТ 29169, 2 класса точности.
5.1.10 Стеклянные шарики или капилляры.
5.1.11 Установка для перегонки дистиллированной воды, состоящая из перегонной колбы, холодильника и приемной колбы (для дополнительной очистки воды).
5.1.12 Холодильник бытовой любого типа, обеспечивающий хранение проб при температуре от 2 °С до 10 °С.
5.1.13 Цилиндры мерные вместимостью 100 см 3 по ГОСТ 1770, 2 класса точности.
5.1.14 Часы песочные на 10 мин или таймер.
5.1.15 Электрическая плитка с регулятором температуры, обеспечивающая быстрое достижение температуры в колбах до 96 — 98 °С с последующим ее поддержанием до окончания кипячения по ГОСТ 14919.
5.1.16 Дозаторы медицинские лабораторные настольные (устанавливаемые на сосуд) или ручные, одноканальные с фиксированным или варьируемым объёмом дозирования по ГОСТ 28311.
Допускается использование средств измерения, вспомогательного оборудования, лабораторной посуды с аналогичными или лучшими метрологическими и техническими характеристиками.
5.2 Реактивы и материалы
5.2.1 Вода дистиллированная по ГОСТ 6709 или для лабораторного анализа по ГОСТ Р 52501 (2-ой степени чистоты).
5.2.2 Перманганат калия, стандарт-титр, С (1/5 KMnO4) (0,1 н, что соответствует 0,02 моль/дм 3 ) по ТУ 6-09-2540.
5.2.3 Серная кислота, х.ч. по ГОСТ 4204.
5.2.4 Щавелевая кислота, ч.д.а. по ГОСТ 22180 или стандарт-титр, С (1/2C2H2O4∙2H2O) (0,1 н, что соответствует 0,05 моль/дм 3 ) по ТУ 6-09-2540.
Допускается использование реактивов более высокой квалификации, а также материалов с аналогичными или лучшими характеристиками.
6 УСЛОВИЯ БЕЗОПАСНОГО ПРОВЕДЕНИЯ РАБОТ
6.1 При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
6.2 При работе с оборудованием необходимо соблюдать правила электробезопасности по ГОСТ Р 12.1.019.
6.3 Обучение работающих безопасности труда должно быть организовано в соответствии с ГОСТ 12.0.004.
6.4 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
7 ТРЕБОВАНИЯ К КВАЛИФИКАЦИИ ОПЕРАТОРА
К выполнению измерений и обработке их результатов допускаются лица, имеющие квалификацию техника-химика или лаборанта-химика и обученные методике.
8 УСЛОВИЯ ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
от 20 °С до 28 °С;
относительная влажность воздуха не более
напряжение в электросети
9 ОТБОР И ХРАНЕНИЕ ПРОБ
9.1 Отбор проб осуществляют в соответствии с ГОСТ Р 51592 и ГОСТ Р 51593. Пробы отбирают в емкости из стекла. Требуемый объем пробы не менее 0,2 дм 3 . Анализ следует проводить как можно быстрее.
9.2 Если проба не может быть проанализирована сразу же после отбора, то допускается её хранение в течение 24 часов при температуре (2 — 10) °С. В случае более длительного хранения (но не больше двух суток) пробу консервируют в лаборатории немедленно после доставки раствором серной кислоты (1:3), исходя из расчета 5 см 3 на 1 дм 3 пробы.
9.3 При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указывается:
— место, дата и время отбора;
— должность, фамилия сотрудника, отбирающего пробу.
10 ПОДГОТОВКА К ВЫПОЛНЕНИЮ ИЗМЕРЕНИЙ
10.1 Подготовка дистиллированной воды
Перед использованием воду проверяют на отсутствие восстановителей. При холостом определении (см. п. 11) расход раствора перманганата калия на титрование не должен превышать 0,5 см 3 , в противном случае следует провести процедуру очистки или использовать воду с меньшим содержанием органических соединений.
Для очистки от восстановителей к 1 дм 3 дистиллированной воды добавляют 10 см 3 серной кислоты (1:15) и небольшой избыток (до образования розового цвета) основного раствора перманганата калия, а затем перегоняют. Первую порцию дистиллята объемом 100 см 3 отбрасывают. Перегнанную дистиллированную воду хранят в стеклянной бутыли со стеклянной пробкой.
Подготовленную дистиллированную воду используют для приготовления растворов реактивов и для разбавления проб.
10.2 Подготовка лабораторной посуды для титрования
Конические колбы, применяемые для титрования, используют только для определения перманганатной окисляемости. Новые колбы очищают путем кипячения с подкисленным раствором перманганата калия. Для этого в коническую колбу приливают 100 см 3 дистиллированной воды, 5 см 3 раствора серной кислоты (1:3) и 20 см 3 раствора перманганата калия (0,002 моль/дм 3 ) и кипятят в течение 10 мин. Чистоту посуды проверяют холостым определением (п. 11).
10.3 Приготовление растворов
При приготовлении растворов серной кислоты необходимо соблюдать осторожность. Растворы готовят в вытяжном шкафу, добавляя серную кислоту к дистиллированной воде. Растворы всех реактивов хранят в стеклянных емкостях.
10.3.1 Раствор серной кислоты (1:3)
Прибавляют при перемешивании к 3 объемам дистиллированной воды 1 объем серной кислоты. После охлаждения раствора (приблизительно до 40 °С) к нему прибавляют по каплям раствор перманганата калия (0,002 моль/дм 3 ) до слабо-розовой окраски. Срок хранения раствора — 6 месяцев при комнатной температуре.
10.3.2 Раствор серной кислоты (1:15)
К 15 объемам дистиллированной воды при перемешивании добавляют 1 объем серной кислоты. После охлаждения раствора (приблизительно до 40 °С) к нему прибавляют по каплям раствор перманганата калия (0,002 моль/дм 3 ) до слабо-розовой окраски. Срок хранения раствора — 6 месяцев при комнатной температуре.
10.3.3 Основной раствор щавелевой кислоты с концентрацией 0,05 моль/дм 3
Растворяют (6,30 ± 0,01) г щавелевой кислоты в растворе серной кислоты (1:15) и доводят объем раствора до 1 дм 3 этим же раствором кислоты. При приготовлении основного раствора из стандарт-титра содержимое ампулы количественно переносят в мерную колбу вместимостью 1 дм 3 и доводят объем раствора до метки раствором серной кислоты (1:15). Срок хранения раствора в темном месте — 6 месяцев при температуре от 2 °С до 10 °С.
10.3.4 Раствор щавелевой кислоты концентрацией 0,005 моль/дм 3
В мерную колбу вместимостью 1 дм 3 пипеткой с одной меткой наливают 100 см 3 раствора щавелевой кислоты (0,05 моль/дм 3 ). Объём доводят до метки раствором серной кислоты (1:15) и перемешивают. Срок хранения раствора — 2 недели при температуре от 2 °С до 10 °С.
10.3.5 Основной раствор перманганата калия концентрацией 0,02 моль/дм 3
При приготовлении основного раствора из стандарт-титра содержимое ампулы количественно переносят в мерную колбу вместимостью 1 дм 3 и доводят объем раствора до метки дистиллированной водой. Основной раствор используют через 2 недели после приготовления. При этом колбу помещают в темное место и в течение 2 недель ежедневно перемешивают. Раствор стабилен в течение 6 месяцев со дня приготовления при хранении в темном месте при температуре от 2 °С до 10 °С.
10.3.6 Раствор перманганата калия концентрацией 0,002 моль/дм 3
В мерную колбу вместимостью 1 дм 3 пипеткой с одной меткой наливают 100 см 3 раствора перманганата калия с концентрацией 0,02 моль/дм 3 . Объём раствора доводят до метки дистиллированной водой и перемешивают. Хранят в склянке из темного стекла. Пригодность раствора проверяют по значению поправочного коэффициента, который устанавливают каждый раз перед использованием раствора (п. 10.4.).
10.4 Установление поправочного коэффициента к раствору перманганата калия
В коническую колбу наливают 100 см 3 дистиллированной воды, прибавляют 10 см 3 раствора щавелевой кислоты (0,005 моль/дм 3 ) и 5 см 3 раствора серной кислоты (1:3). Смесь нагревают до кипения и титруют раствором перманганата калия (0,002 моль/дм 3 ) до слабо-розовой окраски. Поправочный коэффициент (K) для приведения концентрации раствора перманганата калия точно к 0,002 моль/дм 3 рассчитывают по формуле с точностью до третьего знака
10 — объем раствора щавелевой кислоты (0,005 моль/дм 3 ), см 3 ;
V — объем раствора перманганата калия (0,002 моль/дм 3 ), см 3 .
Если поправочный коэффициент (K) раствора отличается от 1,00 больше чем на ±0,05, то раствор укрепляют, разбавляют или готовят заново. Для укрепления раствора добавляют раствор перманганата калия с концентрацией 0,02 моль/дм 3 .
11 ВЫПОЛНЕНИЕ ИЗМЕРЕНИЙ
В колбу помещают 100 см 3 (или меньший её объём, разбавленный дистиллированной водой до 100 см 3 ) хорошо перемешанной пробы, несколько капилляров или стеклянных шариков, приливают 5 см 3 разбавленной серной кислоты (1:3) и 10 см 3 раствора перманганата калия (0,002 моль/дм 3 ). Смесь нагревают так, чтобы она закипела не позднее чем через 5 минут, и кипятят (10 ± 1) мин, закрыв маленькой конической воронкой для уменьшения испарения. Если в процессе кипячения содержимое колбы потеряет розовую окраску или побуреет, то определение повторяют, разбавив исследуемую воду. К горячему раствору немедленно прибавляют 10 см 3 раствора щавелевой кислоты (0,005 моль/дм 3 ). Обесцвеченную горячую смесь сразу титруют раствором перманганата калия (0,002 моль/дм 3 ) до слабо-розового окрашивания. Если при титровании пробы расходуется более 7 см 3 раствора перманганата калия, то пробу разбавляют и повторяют определение.
Если при анализе предварительно разбавленной пробы на титрование расходуется менее 2 см 3 раствора перманганата калия, то определение повторяют с менее разбавленной или неразбавленной пробой.
Одновременно с каждой серией проб проводят холостое определение, используя 100 см 3 дистиллированной воды, которую анализируют так же, как пробу воды. Расход раствора перманганата калия при холостом определении не должен превышать 0,5 см 3 . В противном случае проводят дополнительную очистку используемой дистиллированной воды и посуды (п. 10.1 и 10.2).
12 ОБРАБОТКА РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Значение перманганатной окисляемости, выраженное в расчете на атомарный кислород в мг/дм 3 , определяют по формуле:
V1 — объем раствора перманганата калия, израсходованного на титрование исследуемой пробы, см 3 ;
V2 — объем раствора перманганата калия, израсходованного на титрование холостой пробы, см 3 ;
K — поправочный коэффициент к раствору перманганата калия;
С — концентрация раствора перманганата калия, равная 0,002 моль/дм 3 ;
V — объем пробы, взятой для анализа, см 3 ;
Kр — коэффициент разбавления пробы;
8 — атомная масса кислорода;
5 — стехиометрический коэффициент.
Если поправочный коэффициент (K) к раствору перманганата калия имеет значение от 0,995 до 1,005, то при вычислении результатов его можно не учитывать.
13 ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Результаты количественного анализа в протоколе анализа представляют в следующем виде
δ — значение показателя точности (см. табл. 1).
Результаты измерений округляют с точностью:
Источник