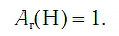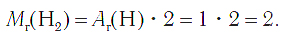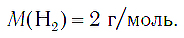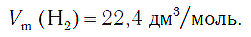- Тест с ответами на тему: “Предмет химии”
- Что изучает наука химия? а) Это наука о веществах в) Это наука о превращении веществ с) Это наука о свойствах веществ d) Это наука о веществах, их свойствах и превращениях.
- 1) Какие из перечисленных веществ являются простыми, а какие сложными: вода, кальцинированная сода, водород, красный фосфор, алмаз, медь, графит, поваренная соль, белый фосфор, озон, аммиак, мышьяк, воздух? 2) Сравните Э.О., радиус атома и металлические свойства для: а) халькогенов; б) P, S, Cl; в) N, O, F; г) щелочных металлов. 3) Определите тип связи в а) углекислом газе; б) аммиаке; в) озоне; г) хлоре.
- Про соду
- Урок 21. Водород — самый лёгкий газ
- Водород как химический элемент
- Водород как простое вещество
- История открытия водорода
- Физические свойства водорода
Тест с ответами на тему: “Предмет химии”
1. Определенный вид атома – это:
а) физическое тело
б) вещество
в) химический элемент +
г) молекула
2. Какое из веществ состоит из молекул:
а) водород
б) алмаз
в) песок
г) вода +
3. Что собой представляют молекулы кислорода:
а) простое вещество +
б) физическое тело
в) сложное вещество
г) химический элемент
4. Вещество – это то, из чего состоят:
а) физические тела +
б) молекулы
в) атомы
г) газы
5. К каким свойствам относят пластичность, твердость:
а) физические свойства +
б) химические свойства
в) сложные вещества
г) физические тела
6. Наука которая изучает вещества, их свойства и превращения – это:
а) физика
б) математика
в) биология
г) химия +
7. Чем являются вода, углекислый газ:
а) атомы
б) физические тела
в) сложные вещества +
г) простые вещества
8. Чем являются вода, углекислый газ, сода, медь:
а) атомы
б) вещества +
в) химические элементы
г) физические тела
9. Чем являются ручка, стол, тарелка, кирпич:
а) химический элемент
б) молекула
в) вещество
г) физическое тело +
10. Из чего состоят молекулы благородных газов:
а) одного атома +
б) множества атомов
в) двух атомов
г) простых веществ
11.Что является веществом:
а) золотая монета
б) поваренная соль +
в) капля воды
г) железная скрепка
12. Физическое явление – это:
а) Скисание молока
б) Горение магния
в) Горение лучины
г) Образование инея +
13. Химическое явление – это:
а) Испарение воды
б) Гниение мусора +
в) Вытягивание алюминиевой проволоки
г) Растворение сахара в воде
14. Элемент 3-го периода II группы главной подгруппы (IIАгруппы) Периодической системы химических элементов Д.И.Менделеева:
а) Магний +
б) Алюминий
в) Кальций
г) Бериллий
15. Химический элемент, названный в честь России:
а) Полоний
б) Европий
в) Рутений +
г) Рений
16.Что означает запись 2Н:
а) 2 атома водорода +
б) одну молекулу водорода
в) две молекулы водорода
г) атом водорода
17. Верны ли суждения о правилах работы с лабораторным оборудованием?
А. Мерный цилиндр используют для измерения объёма жидкостей.
Б. Для прекращения горения спиртовки необходимо накрыть фитиль колпачком.
а) Верно только А
б) Верно только Б
в) Верны оба суждения +
г) Оба суждения неверны
18. Какую группу веществ относят к простым веществам:
а) Кислород, воздух, вода, молоко
б) Медь, водород, железо, кислород +
в) Водород, алюминий, азот, вода
г) Вода, серебро, углекислый газ, алюминий
19. Какую группу веществ относят к сложным веществам:
а) Крахмал, сахар, этиловый спирт, углекислый газ +
б) Кислород, крахмал, гелий, сахар
в) Железо, алюминий, медь, аргон
г) Сера, этиловый спирт, угарный газ, метан
20. Простое вещество – это:
а) Мельчайшая химически неделимая частица
б) Мельчайшая частица вещества, сохраняющая его химические свойства
в) Вещество, состоящее из атомов одного химического элемента +
г) Вещество, состоящее из атомов разных химических элементов
21. Определенный вид атома – это:
а) физическое тело
б) вещество
в) химический элемент +
г) молекула
22. Электронейтральная частица, которые состоят из положительно заряженного ядра и отрицательно заряженных электронов:
а) Молекула
б) Ион
в) Атом +
г) Химический элемент
23. Электронейтральные частицы вещества, которые определяют его химические свойства:
а) Молекулы +
б) Ионы
в) Атомы
г) Химические элементы
24. Какие вещества, которые имеют одинаковый качественный состав:
а) SO2, CO2
б) Na2O, N2O
в) CH4, C6H6 +
г) CrO3, SO3
25. Сложное вещество – это:
а) Серое олово
б) Красный фосфор
в) Графит
г) Поваренная соль +
26. Какие вещества, которые имеют разный количественный состав:
а) Na2O, K2O
б) H2S, H2SO3
в) NHO2, PH3
г) HNO2, HNO3 +
27. Простое вещество – это:
а) Вода
б) Сода
в) Водород +
г) Углекислый газ
28. Частицы, находящиеся в ядре атома – это:
а) Только протоны
б) Только электроны
в) Протоны и нейтроны +
г) Протоны и электроны
29. Заряд ядра атома – это:
а) Нуль
б) Число протонов в ядре +
в) Число нейтронов в ядре
г) Сумма протонов и нейтронов в ядре
30. Порядковый номер элемента – это:
а) Число электронов на внешнем слое атома
б) Число нейтронов в ядре атома
в) Сумма протонов и нейтронов в ядре атома
г) Число электронов в атоме +
Источник
Что изучает наука химия?
а) Это наука о веществах в) Это наука о превращении веществ с) Это наука о свойствах веществ d) Это наука о веществах, их свойствах и превращениях.
Что такое простое вещество?
а) Вещество, образованное химическими элементами в) Вещество, образованное атомами химических элементов с) Вещество, образованное атомами одного химического элемента
d) Вещество, образованное атомами разных химических элементов.
3. В каком ряду расположены только вещества
а) Поваренная соль, сахар, свеча в) Вода, железо, сера с) Медь, гвоздь, кислород d) Кирпич, пищевая сода, керамический стакан.
4. Верны ли следующие суждения? А) Вещество — это то, из чего состоит физическое тело.
В) Химический элемент — это определенный вид атомов.
а) Верно только А в) Верно только В с) Верны оба суждения d) Оба суждения неверны.
5. Тело: а) Графит в) Полиэтилен с) Свинец d) Пробирка.
6. Вещество: а) Медная проволока в) Медная монета с) Медная пластина d) Медь
7. Простое вещество: — — — — — а) Водород в) Углекислый газ с) Сахар d) Поваренная соль
8. Сложное вещество: а) Фосфор в) Крахмал с) Сера d) Медь.
9. Говорят о водороде, как о простом веществе:
а) Водород – самый легкий газ в) Порядковый номер водорода в Периодической таблице — 1
с) Водород входит в состав воды d) Водород входит в состав кислоты
10. Говорят о меди как о химическом элементе
а) Медь не реагирует с соляной кислотой в) Медь окисляется при нагревании
с) Медная проволока d) Медь входит в состав медного купороса
11. Установите , в каком словосочетании имеется в виду элемент, а в каком –простое вещество. Ответ дайте в виде последовательности цифр, соответствующих буквам по алфавиту:
1. Элемент 2. Простое вещество
А) водород горит на воздухе Б) кислород входит в состав углекислого газа
В) кислород малорастворим в воде Г) углерод входит в состав угарного газа
Д) водород самый легкий газ
12. Выберите из предложенных групп, группу сложных веществ.
а) Водород, озон, гелий в) угарный газ, метан, вода с) кислород, сера d) азот, алмаз, графит.
13. Определите молекулярную массу ортофосфорной кислоты (H3PO4) :
а) 160 в) 92 с) 98 106
14. Символ химического элемента магния: а) Mn в) Mo с) Mg d) Md
15. Физическим природным явление следует считать: а) Образование глюкозы в зеленом растении в) Лесной пожар с) Высыхание луж d) Процесс высыхания растения
16. Индивидуальным веществом является:
а) Морская вода в) Сладкий чай с) Поваренная соль d) Воздух
17. О химическом элементе, а не о простом веществе идет речь
а) Азот является частью воздуха в) Взрывчатое вещество тротил содержит азот с) Формула азота N2 d) Жидкий азот иногда используется для замораживания продуктов.
18. Высшую и низшую валентность сера проявляет в соединениях соответственно
а) SO3 ZnS в) SO2 H2S с) SO3 SO2 d) H2S SO3
19. Сумма коэффициентов в уравнении реакции CO+O2=CO2: а) 3 в) 4 с) 5 d) 6
20. Взаимодействие серной кислоты с оксидом меди относится к реакции
а) Разложения в) Соединения с) Замещения d) Обмена
21. Массовая доля натрия в его оксиде равна приблизительно: а) 37 в) 59 с) 63 d) 74
22. Масса цинка, расходуемого для получения 6 моль водорода, при взаимодействии с соляной кислотой Zn+2HCl=ZnCl2+H2 : — — — — — — — — — а) 65 в) 130 с) 390 d) 260
23. Найти массу оксида фосфора, полученного при взаимодействии 3, 1 г. Фосфора с кислородом.
а) 12, 5 в) 10 с) 7, 1 d) 23, 6
24. Найти массу пяти моль кислорода: — — — — — — — — а) 123, 6 в) 160, 5 с) 220 d) 160
25. Найти массовые отношения элементов по формуле серной кислоты.
а) 1:16:32 в) 2:32:1 с) 1:45:16 d) 2:3:5
Источник
1) Какие из перечисленных веществ являются простыми, а какие
сложными: вода, кальцинированная сода, водород, красный фосфор, алмаз, медь, графит, поваренная соль, белый фосфор, озон, аммиак, мышьяк, воздух?
2) Сравните Э.О., радиус атома и металлические свойства для: а) халькогенов; б) P, S, Cl; в) N, O, F; г) щелочных металлов.
3) Определите тип связи в а) углекислом газе; б) аммиаке; в) озоне; г) хлоре.
Если речь о гидратации ЭТИЛЕНА, тогда: C2H4 (M=28 г/моль) + H2O (+T, +H2SO4) = C2H5OH (M=46 г/моль); найдем кол-во в-ва C2H4: 1/28=0.0357 Ммоль, из кот-го пол-ся 0.0357*46=1.6422 т C2H5OH; соот-но из 1.6422 т C2H5OH, чья м.д. в р-ре сос-т 0.96, пол-ся 1.6422/0.96=1.710625 т 96% р-ра спирта.
кроме этих изомеров с изменение углеродного скилета можно построить ещё не один изомер
СН3-О-(СН2)4-СН3 — метилпентиловый эфир
СН3-СН2-О-(СН2)3-СН3 — этилбутиловый эфир
СН3-(СН2)2-О-(СН2)2-СН3 — дипропиловый эфир
ZnCl2+2HOH=Zn(OH)2+2HCl
Zn2+ + 2Cl- + 2HOH=Zn(OH)2 + 2H+ + 2Cl-
Zn2+ + 2HOH=Zn(OH)2 + 2H+
Хлор гораздо более сильный неметалл, поэтому среда раствора ZnCl2 кислая
Источник
Про соду
Сода – это соль. Парадоксально? Ничуть. Сода пищевая , она же сода питьевая, она же натрий двууглекислый NaНCO3 – вещество, относящееся к классу солей. Все соли твердые и построены из ионов, а не из молекул. Современное название соды – гидрокарбонат натрия , оно указывает на то, из каких ионов пищевая сода состоит: это ион натрия и гидрокарбонат-ион.
Представьте, что у банок на кухонной полке отклеились этикетки, и мы не знаем, где поваренная соль, а где сода. Как их отличить друг от друга? Оба вещества – белые порошки, оба растворяются в воде. Кто сказал – на вкус? Увы: вкус у соды тоже соленый. Чтобы ощутить различие, надо быть опытным дегустатором. Соль в кубических кристалликах? Если она мелкая, вы не заметите форму кристаллов.
Ответ простой: эти вещества по-разному ведут себя при нагревании. Соль можно долго греть без последствий (правда, при температуре 801 градус Цельсия она расплавится), а сода выше 60 градусов начинает разлагаться на карбонат натрия, углекислый газ и воду. Только как это увидеть? Ведь, когда мы греем, вода выделяется в виде пара, и ее вместе с углекислым газом не видно, а карбонат натрия – такое же белое твердое вещество, как и гидрокарбонат.
Но выделяющиеся пузырьки газа хорошо видны, если высыпать соду в горячую воду. И не только видны, но и слышны: газ сильно шипит. Это часто происходит, когда мы готовим полоскание для горла.
Да, сода – простое и дешевое средство, употребляемое при ангинах и прочих воспалениях горла, а также десен и зубов. Раствор соды имеет слабощелочную среду – как раз в достаточной степени, чтобы подавлять активность бактерий, но не настолько, чтобы создавать дискомфорт для слизистой оболочки ротовой полости.
Где еще применяется сода? Все видели и, вероятно, не раз проделывали настоящую химическую реакцию – гашение соды уксусом. Кислота, содержащаяся в уксусе, вытесняет из соды углекислый газ, который шипит и пузырится. Гашеную соду добавляют в тесто, чтобы пузырьки углекислого газа разрыхляли его и делали пышным. А если тесто само по себе кислое (например, замешивается на кислом молоке), то уксус можно и не добавлять.
Почему мы уточняли, что говорим о пищевой или питьевой соде? Потому что содами называют очень разные вещества. Тот карбонат натрия Na2CO3, который получается при нагревании пищевой соды – тоже сода, но другая, кальцинированная . Она называется так не потому, что в ней есть кальций (его как раз нет, в чем можно убедиться, посмотрев на формулу), а потому, что для ее получения пищевую соду прокаливают (а по-латыни этот процесс – «calcinatio»).
В природе карбонат натрия тоже встречается, однако минерал имеет немного другой состав: Na2CO3*10H2O. Это кристаллическая сода, причем в ее кристаллах связаны молекулы воды. Другое название этого минерала – натрит. Но не следует думать, будто кристаллическая сода – единственная, которая образует кристаллы. Кристаллы пищевой соды вполне возможно вырастить даже на кухне .
И на закуску – самая загадочная из сод, каустическая . Почему загадочная? Потому что она вообще не сода в полном смысле слова, то есть не карбонат. Каустическая сода или каустик – историческое название гидроксида натрия NaOH. Это едкая щёлочь, такой «содой» горло не прополоскать – заработаете химический ожог. В одном из выпусков мы обязательно расскажем про гидроксид натрия.
Если вам было интересно – ставьте плюсик. Пишите в комментариях, о чем еще рассказать.
Источник
Урок 21. Водород — самый лёгкий газ
В уроке 21 «Водород — самый лёгкий газ» из курса «Химия для чайников» рассмотрим водород как простое вещество и химический элемент; узнаем об истории открытия водорода и о его физических свойствах.
Название водорода происходит от латинского слова Hydrohenium, что означает «воду родящий». Химический символ (знак) Н — это первая буква латинского названия. И действительно, атомы водорода входят в состав молекулы воды Н2О.
Атомы водорода образуют двухатомные молекулы простого вещества водорода, формула которого Н2. Рассмотрим, что имеют в виду, когда говорят о химическом элементе водороде.
Водород как химический элемент
Атом водорода самый легкий, самый простой по строению и один из самых маленьких по размерам. Относительная атомная масса водорода равна:
Сравните ее с относительной атомной массой кислорода и убедитесь, что атомы водорода во много раз легче.
Атомы водорода соединяются с атомами других химических элементов, образуя сложные вещества. Как химический элемент водород входит в состав воды, кислот, природного газа, нефти, глюкозы и многих других веществ. В растительных и животных организмах, включая и человеческий, химический элемент водород содержится главным образом в составе воды и самых разнообразных органических веществ.
Водород как простое вещество
Молекулы водорода образованы двумя атомами химического элемента водорода. Формула его Н2. Относительная молекулярная масса простого вещества водорода равна:
Следовательно, молярная масса водорода равна:
Молярный объем водорода, как кислорода и других газов при нормальных условиях, равен:
В виде простого вещества водород встречается на Земле лишь в небольшом количестве в вулканических и некоторых других природных газах. Молекулы водорода Н2 обнаружены в верхних слоях земной атмосферы. В Солнечной системе простое вещество водород входит в состав атмосферы планет — Юпитера, Сатурна, Урана.
На заметку: Недавние исследования Юпитера, самой большой планеты Солнечной системы, позволили ученым высказать предположение, что под водородной атмосферой этой планеты находится океан жидкого водорода. Глубина этого океана — десятки тысяч километров. Ядро планеты составляет оболочка, состоящая из твердого водорода.
История открытия водорода
Еще в XVI в. Парацельсом было замечено, что при действии кислот на железо и другие металлы выделяется газ. Первоначально его назвали «горючим воздухом». Спустя примерно 100 лет горение водорода на воздухе описал Р. Бойль и этот газ научились собирать. Во второй половине XVIII в. английский ученый Г. Кавендиш подробно исследовал свойства «горючего воздуха». Он установил, что этот газ при сгорании на воздухе образует воду. Г. Кавендиша считают первооткрывателем водорода (1766).
Вывод о том, что «горючий воздух» представляет собой простое вещество, был сделан в 1784 г. французским химиком А. Лавуазье. Он и дал этому веществу латинское название, которое происходило от греческих слов «хюдор» — вода и «геннао» — рождаю. В те годы под элементами подразумевали простые вещества, которые нельзя далее разложить на составные части. Поэтому у химического элемента водорода такое же название, как и у простого вещества Н2.
Физические свойства водорода
Водород при нормальных условиях находится в газообразном состоянии. Это бесцветный газ, у которого нет запаха и вкуса.
Молекула водорода самая легкая из молекул всех веществ. Поэтому газообразный водород по плотности значительно уступает воздуху и кислороду — он в 14,5 раза легче воздуха и в 16 раз легче кислорода. В этом легко убедиться на опыте.
Если наполнить три одинаковых резиновых шарика водородом, углекислым газом и кислородом, крепко завязать их ниткой и выпустить из рук одновременно, то они поведут себя по-разному (рис. 94). Шарик с водородом быстро поднимется к потолку, а шарики с углекислым газом и кислородом опустятся на пол. Быстрее окажется на полу шарик с
углекислым газом.
На заметку: Поскольку водород, как мы знаем, в 14,5 раза легче воздуха, им заполняли воздушные шары и дирижабли. Первыми поднялись на воздушном шаре французские физики Ф. Робер и Ж. Шарль (1783). В августе 1887 г. полет на воздушном шаре, наполненном водородом, с научной целью совершил Д. И. Менделеев.
Из-за своей малой массы и размеров молекулы водорода способны проникать через стенки сосуда, в котором содержится этот газ. Убедимся в этом на примере того же шарика с водородом. Даже если тщательно завязать его ниткой, спустя некоторое время шарик «сдуется». При повышенной температуре и давлении водород способен проникать и через стенки металлических сосудов.
На заметку: Некоторые металлы при повышенной температуре поглощают водород, впитывая его, как губка воду. Например, в образце металла палладия объемом 1 дм 3 растворяется водород объемом свыше 800 дм 3 . При нагревании насыщенного водородом палладия этот газ легко выделяется обратно. Палладий и некоторые другие металлы могут служить как бы аккумуляторами водорода.
При нормальных условиях растворимость водорода в воде меньше, чем кислорода, — 0,0016 г водорода на 1 дм 3 воды. Поскольку водород малорастворим, в лаборатории его собирают методом вытеснения воды или воздуха.
У водорода самые низкие после благородного газа гелия температуры кипения (−252,8 °С) и плавления (−259,2 °С).
Краткие выводы урока:
- Водород — наиболее распространенный элемент во Вселенной.
- Простое вещество водород Н2 — самый легкий газ, у которого нет запаха, цвета, вкуса.
- Водород мало растворяется в воде, его можно собирать методом вытеснения воды и воздуха.
Надеюсь урок 21 «Водород — самый лёгкий газ» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Источник