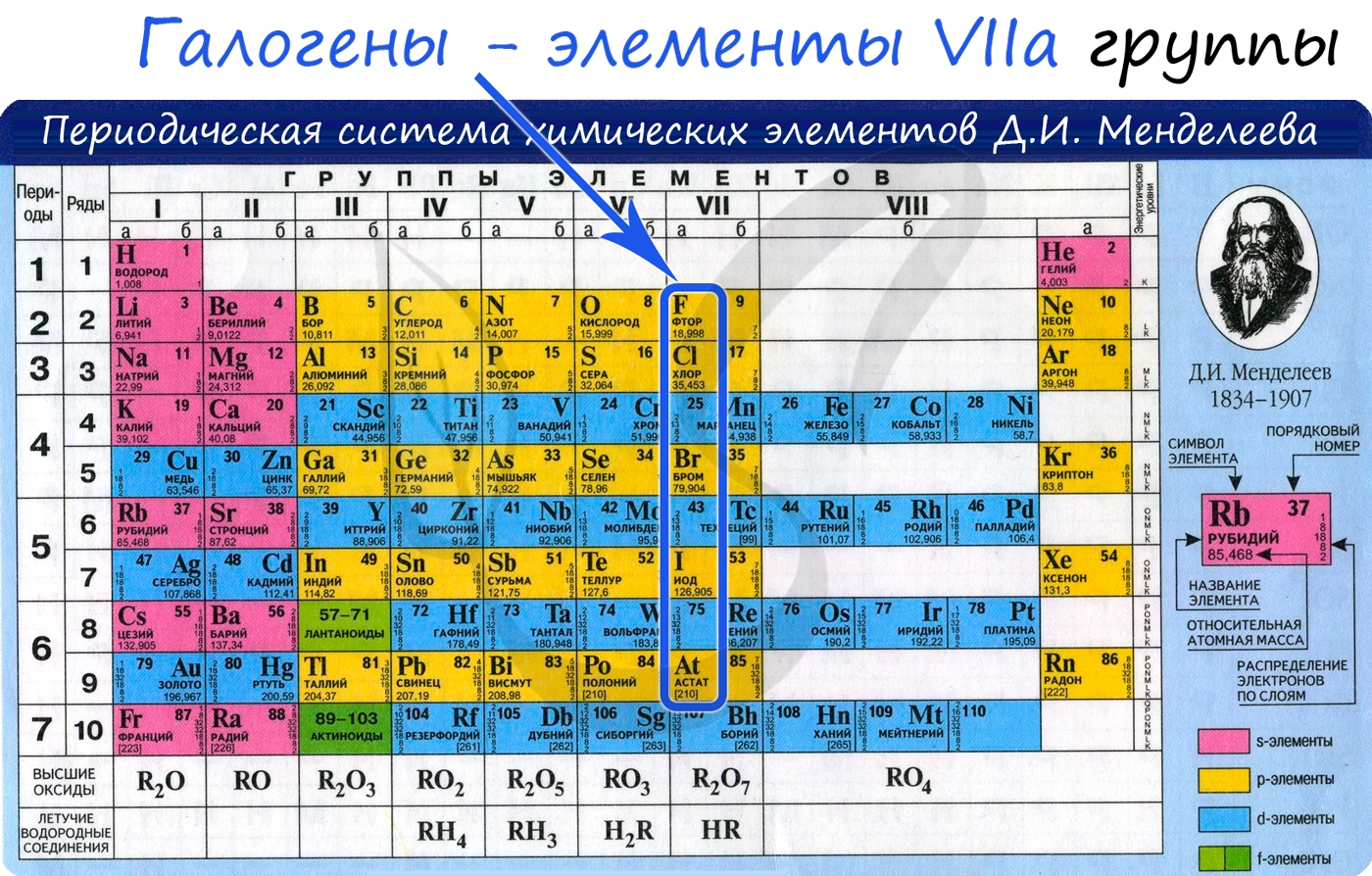
Галогены
Галогены (греч. hals — соль + genes — рождающий) — химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.
Общая характеристика элементов VIIa группы
От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 5 :
- F — 2s 2 2p 5
- Cl — 3s 2 3p 5
- Br — 4s 2 4p 5
- I — 5s 2 5p 5
- At — 6s 2 6p 5
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов в возбужденном состоянии.
Природные соединения
- NaCl — галит (каменная соль)
- CaF2 — флюорит, плавиковый шпат
- NaCl*KCl — сильвинит
- 3Ca3(PO4)2*CaF2 — фторапатит
- MgCl2*6H2O — бишофит
- KCl*MgCl2*6H2O — карналлит
Простые вещества — F2, Cl2, Br2, I2
Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают электролизом водного раствора хлорида натрия.
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте — HF — был впервые получен фтор.
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.
В лабораторных условиях галогены могут быть получены следующими реакциями.
- Реакции с металлами
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере фтора самовоспламеняются.
Реакции с неметаллами
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.
F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность 😉
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром — F — )
Br2 + I2 → IBr3 (бром более электроотрицателен, чем йод — Br — )
Реакции с водой
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
Хлор реагирует с водой обратимо, образуя хлорную воду — смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.
Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами — только при нагревании.
Реакции с щелочами
Cl2 + NaOH → NaCl + NaClO + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Галогеноводороды
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF — фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl — хлороводород (газ), соляная кислота (жидкость)
- HBr — бромоводород, бромоводородная кислота
- HI — йодоводород, йодоводородная кислота
- HAt — астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI — газы, хорошо растворимые в воде.
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
HF — является слабой кислотой, HCl, HBr, HI — сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
KOH + HCl → KCl + H2O (реакция нейтрализации)
Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.
В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с плавиковой кислотой.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Что такое фтор в воде
Фтор (F, Fluorum) относится к наиболее распространенным природным элементам. Изредка встречается в свободном виде. Это электроотрицательное вещество легко вступает во взаимодействие со всеми элементами в любой температурной среде. В природе чаще всего соединяется с кальцием, легко растворяется, поэтому почти всегда и повсеместно в воде есть фтор. Его насыщенность достигает 100 мг на 1 л. Питьевая вода с содержанием фтора может быть одинаково полезной и вредной.
Фтор в воде — что это
Fluorum — это газ светло-желтоватого цвета с едким характерным запахом и ярко выраженными токсичными свойствами. Его соли и кислоты используют для уничтожения насекомых, грызунов, мелких хищников. Фтор в воде — это различные соединения, фториды. В зависимости от того, с какими веществами произошла реакция, образуются фториды этих элементов: с серебром — фторид серебра; с натрием — фторид натрия.
Fluorum, как природный элемент, является частью земной коры, присутствует в пластах грунта и водоносных слоях. Наличие фтора в питьевой воде обусловлено тем, что фториды образуются во многих геологических образованиях с активными минеральными веществами. Базальт, сланец, топаз, биотит постепенно размываются подземными водными потоками. Из локальных водоисточников — артезианских скважин и абиссинских колодцев — поступает питьевая вода с фтором. Такую жидкость нужно очищать от его избытка перед использованием.
Процент соединений фтора в воде зависит от состава и кислотности почвы, пористости породы, из которой вымываются фториды, глубины залегания подземных водоисточников.
В крупных промышленных целях fluorum добывают из плавикового шпата (флюорита, CaF2). В нем содержание F почти 50 %. Залежи расположены в нашей республике, в США, Мексике, соседнем Казахстане. Флюорит (фторид кальция) представляет собой бесцветные кристаллы, не растворяющиеся в водной среде. Вода, в которой содержание фтора представлено нерастворимыми соединениями CaF2, практически безопасна: фториды кальция хорошо улавливаются фильтрами.
Флюорит — это мягкий, хрупкий, прозрачный минерал, повсеместно используется в оптической промышленности для изготовления линз, стекол, приборов оптики. Применяется в астрономической, микроскопической, инфракрасной, голографической, медицинской сфере.
Что представляет собой вода с содержанием фтора
Присутствующие ионы фтора в воде могут быть абсолютно безопасны и смертельно опасны. В микроскопических дозах фторид-ионы F(-) оказывают терапевтическое действие, а в больших концентрациях способны убить. В обычном тюбике зубной пасты количество фторидов таково, что может погубить маленького ребенка, если он съест пасту. Доза 2-3 грамма фторида натрия является смертельной для взрослого человека.
Вода с ионами фтора по степени токсичности гораздо опаснее свинца. Во многих странах водные растворы специально фторируют, так как данный микроэлемент необходим для формирования и нормального развития зубной и костной ткани организма. Самый популярный способ фторирования — добавление фторида натрия. Это самый дорогой реагент, который используют в коммунальных хозяйствах для обогащения водопроводной питьевой воды фтором F(-).
При фторировании важны:
- строгое соблюдение технологии,
- точная дозировка,
- регулярные поступления на объекты водоподготовки фторсодержащего сырья.
Из-за сильной токсичности химического элемента признано опасным избыточно-высокое содержание фтора в воде в количестве выше установленных норм. Многие страны — Китай, Япония, Индия, Израиль — не только отказались, но и ввели запрет на фторирование воды, применяемой для питья.
Норма фтора в воде
Из-за ядовитости газа содержание фтора в питьевой воде строго стандартизовано. В 1994 по нормам ВОЗ г. установлено предельно допустимое значение, которое не следует превышать: ПДК на фтор в воде равен 0,5 мг/л. В России ПДК фтора для воды устанавливает ГОСТ 2874-90.
Нормируемое присутствие фторидов — количество фтора в питьевой воде — зависит от местности и от климата. Там, где стоит круглогодичная жара, где люди пьют много жидкости, рекомендован показатель 0,5 мг/л. На северных территориях установлена норма не выше 1 миллиграмма. На средней полосе в районах с умеренным климатом рекомендуется придерживаться показателя 0,7 мг/л.
Не везде требования соблюдаются. Почти третья часть населения Земли пьёт жидкость, в которой концентрация фтора в воде выше 1,5 мг/л. Обязательно нужно проверять точный состав элементов и соединений в водном растворе и удалять избыток фтора в водопроводной или артезианской воде.
В индийских, южноамериканских и кенийских водах наблюдается опасное превышение фторидов — на литр приходится 25 мг. Во многих юго-западных районах Украины отмечается чрезвычайно низкое содержание F(-). В российских подземных залежах содержание фтора в воде повышено, намного больше 1,5 мг/л. В Подмосковье, на Урале доходит до 4,4 мл/л. В водоемах Казахстана и Азербайджана величина критическая, до 11 мл/г.
В поверхностных водоисточниках концентрация намного меньше, до 0,3 мг/л. В особо опасных районах насыщенность водных растворов ионами F(-) может превышать 65 мг/литр. Морские солёные воды менее опасны, в них присутствие фторидов невысоко, всего 1,1-1,4 мг.
Для местности с пониженным содержанием фторидов (ниже оптимального содержания фтора в воде) здравоохранение рекомендует их искусственно добавлять — фторировать водный раствор перед употреблением. Фториды добавляют в небольших количествах: в микрограммах либо даже в нанограммах.
Показаниями для фторирования служат:
- низкий ПДК воды по фтору,
- отсутствие региональных программ по фторированию пищевых продуктов,
- медицинские показатели — большой процент в данном районе заболеваний кариесом.
Для местностей, где ионы F(-) присутствуют в избытке, нужно выбирать способы, как понизить содержание фтора в воде.
Помимо того, что за ПДК по фтору в воде обязаны следить коммунальные службы, отвечающие за водоснабжение, каждый человек может самостоятельно проверять состав воды и очищать её от всех вредных веществ перед употреблением.
Как определить содержание фтора в воде
В домашних условиях это сделать нельзя. Если в воде есть фтор в виде отрицательно заряженных ионов F(-), обычными органолептическими методами его невозможно обнаружить. Он не меняет вкус, цвет, запах. Можно выполнить проверку с помощью экспресс-тестов, но они дадут большую погрешность.
Лучше заказать определение фтора в воде в сертифицированной лаборатории, которая числится в общем реестре благонадежных организаций. Сотрудники проведут сложную экспертизу и выдадут точные показания — сообщат, что содержание фтора в питьевой воде в норме, завышено или занижено.
Определение массовой концентрации фторидов проводится разными методиками:
- Фотометрическим способом — F(-) способны образовать растворимый в воде тройной комплекс синевато-сиреневого цвета, в его состав входят 3 элемента: фторид, лантан, ализарин-комплексон.
- Потенциометрическим методом — измерение концентрации F(-) с использованием фторселективного электрода на фоне цитратного раствора соли лимонной кислоты с pH = 6.
F(-) легко вступает во взаимодействие со стеклом. Желая установить количественную норму содержания фтора в питьевой воде, необходимо налить пробу в пластиковую посуду, плотно закупорить, очень быстро доставить в лабораторию. Соединения фтора легколетучи, они могут испариться, результаты окажутся неверными.
Влияние фтора в воде на организм человека
Безвредно для организма лишь нормативное содержание фтора в воде. Как избыток, так и недостаток одинаково вредны. Фтор находится во многих пищевых продуктах — в говяжьей печени, орехах, чае, морепродуктах. Более 60 % фторидов поступает в организм из воды. Для нормального функционирования организму достаточно 1-3 мг в сутки, беременным женщинам не более 4 мг.
Избыток фтора в воде негативно влияет на организм — наблюдаются:
- Нарушения щитовидки, нервных импульсов;
- Сердечнососудистые заболевания;
- Воспаления носоглотки, пищеварительного тракта;
- Поражение органов слуха;
- Снижение иммунитета.
Вред от фтора в воде выражается особым заболеванием — флюорозом, при котором наступают изменения костной ткани скелета. Из воды фториды разносятся по всему организму, их большая часть оседает на зубах и костях. На начальной стадии воспаляются челюсти, разрушается зубная эмаль, изменяется цвет зубов. Затем фториды накапливаются в костях, их деформируют. Повышенный уровень фтора в воде вызывает бесплодие и другие неприятные заболевания — остеопороз, рак, болезнь Альцгеймера.
Влияние на организм низкого содержания фтора в питьевой воде выражается тем, что у населения начинаются проблемы с зубами: развивается кариес. Поэтому промышленность выпускает специальные фторовые зубные пасты для защиты от кариеса.
Как очищать воду от фтора
Службы, обеспечивающие бесперебойную подачу водных растворов в промышленных масштабах, и владельцы локальных источников водоподачи должны знать, сколько фтора содержится в воде.
Им предстоит решить две задачи:
Как понизить фтор в воде при его чрезмерном присутствии, как вывести излишки фтора из воды.
Обеспечить оптимальное содержание фтора в питьевой воде при недостатке фторидов.
Нехватка ионов F(-) вызывает проблемы в организме, а переизбыток провоцирует их накапливание в недопустимых размерах, когда фториды начинают действовать как яд. Важно получить профессиональную помощь при выборе способов нормирования фтора в питьевой воде, подходящих очистки воды в загородных домах или для промышленного оборудования.
Подробно о том, как избавиться от фтора в воде, читайте в специальной статье об удалении фторидов из водных растворов.
Источник