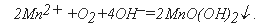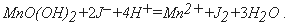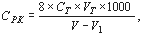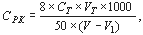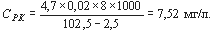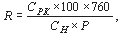- Растворимость некоторых газов в воде (аргона, метана, этилена, этанола, углекислого газа, диоксида углерода, хлорина, водорода, сероводорода , гелия, азота, аммиака, кислорода, диоксида серы).
- Экология СПРАВОЧНИК
- Информация
- Кислород растворимость
- Растворимость кислорода воде таблица
- Оборудование и реактивы
- Отбор пробы
- Проведение анализа
- Вычисление результатов анализа
- Контроль точности измерений
Растворимость некоторых газов в воде (аргона, метана, этилена, этанола, углекислого газа, диоксида углерода, хлорина, водорода, сероводорода , гелия, азота, аммиака, кислорода, диоксида серы).
Растворимость некоторых газов в воде (аргона, метана, этилена, этанола, углекислого газа, диоксида углерода, хлорина, водорода, сероводорода , гелия, азота, аммиака, кислорода, диоксида серы).
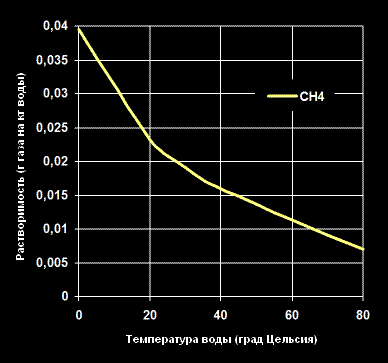
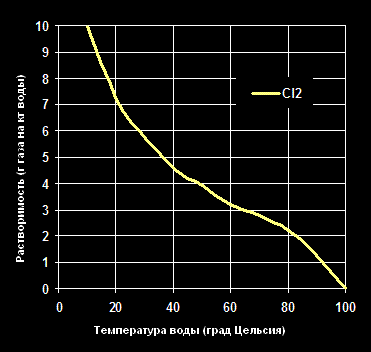
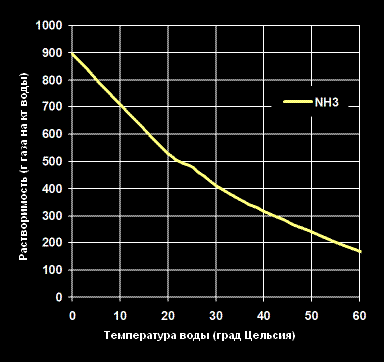
Зависимость растворимости в воде при давлении в одну атмосферу (101.325 кПа) и разных значениях температур показана на графиках ниже:
Растворимость Аргона -Ar- в воде (г газа на кг воды).
Растворимость Метана -CH4— в воде (г газа на кг воды).
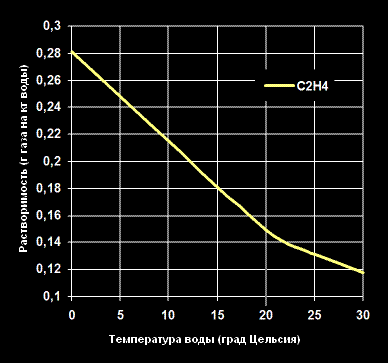
Растворимость Этилена -C2H4— в воде (г газа на кг воды).
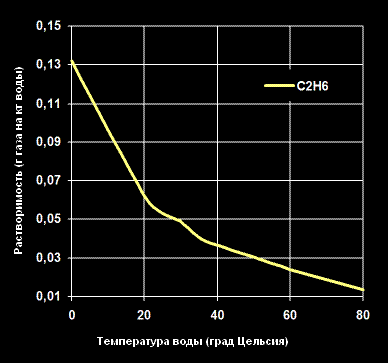
Растворимость Этанола -C2H6— в воде (г газа на кг воды).
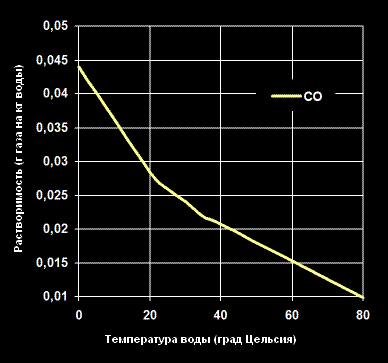
Растворимость Монооксида углерода (Углекислого газа) -CO- в воде (г газа на кг воды).
Растворимость Диоксида углерода -CO2— в воде (г газа на кг воды).
Растворимость Хлорина -Cl2— в воде (г газа на кг воды).
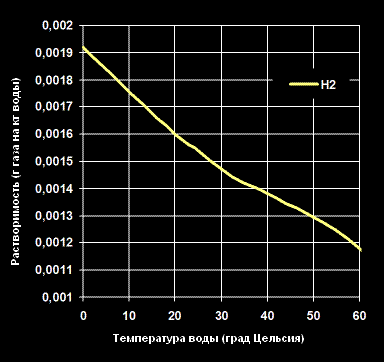
Растворимость Водорода -H2— в воде (г газа на кг воды).
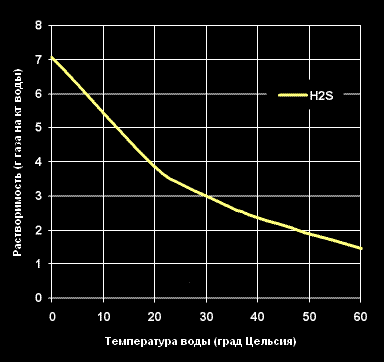
Растворимость Сероводорода -H2S- в воде (г газа на кг воды).
Растворимость Гелия -He- в воде (г газа на кг воды).
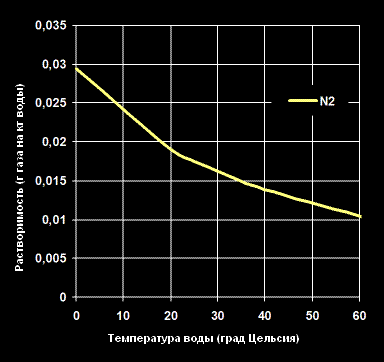
Растворимость Азота -N2— в воде (г газа на кг воды).
Растворимость Аммиака -NH3— в воде (г газа на кг воды).
Растворимость Кислорода -O2— в воде (г газа на кг воды).
Растворимость Диоксида серы -SO2— в воде (г газа на кг воды).
Источник
Экология СПРАВОЧНИК
Информация
Кислород растворимость
Кислород, как и другие газы, может растворяться в воде лишь до определенного, насыщающего воду количества, которое зависит от температуры и давления. Чем выше температура, тем растворимость кислорода меньше. При давлении более высоком, чем парциальное давление содержащегося в воде кислорода, растворимость кислорода будет больше. В табл. 37 приведена растворимость кислорода в дистиллированной воде при различных температурах и давлении 760 мм рт. ст.[ . ]
Растворенный кислород. Растворимые в воде газы определяются при характеристике воды на коррозийные свойства по отношению к металлу и бетону, а также в воде, используемой в паросиловом хозяйстве. Кислород попадает в воду из воздуха, а также может образоваться в результате жизнедеятельности зеленых растений, населяющих близкие к поверхности слои воды. Растворимость чистого кислорода, выделяемого зелеными растениями, в пять раз больше, чем растворимость кислорода из воздуха, в котором содержание этого газа составляет лишь 21%, так как растворимость кислорода в воде обусловливается его парциальным давлением.[ . ]
Общеизвестно, что кислород труднорастворим в жидкости. Вместе с тем в литературе приводится сравнительно мало сведений о кинетике растворения технического кислорода в условиях конкретного инженерного оформления этого процесса. Проведенный выше анализ выявил количественные показатели растворения кислорода для приближенной оценки кинетики процесса в условиях барботажной аэрации. При рассмотрении вопроса сделаны некоторые допущения, основным из которых является принятие постоянного дефицита кислорода. Растворимость технического кислорода в воде С7-1 приведена в табл. 6.[ . ]
В водных местообитаниях количество кислорода, двуокиси углерода и других атмосферных газов, растворенных в воде и потому доступных организмам, сильно варьирует во времени и в пространстве, чего в наземных местообитаниях не бывает. В озерах и в водоемах с высоким содержанием органических веществ кислород является лимитирующим фактором первостепенной важности. Хотя кислород лучше растворяется в воде, чем азот, даже в самом благоприятном случае в воде содержится значительно меньше кислорода, чем в атмосферном воздухе. Так, если на долю кислорода в воздухе приходится 21% (по объему), т. е. в 1 л воздуха содержится 210 см3 кислорода, то в воде содержание кислорода не превышает 10 см3 на 1 л. Температура воды и количество растворенных солей сильно влияют на способность воды удерживать кислород: растворимость кислорода повышается с понижением температуры и снижается с повышением солености. Запас кислорода в воде пополняется главным образом из двух источников: путем диффузии из воздуха и благодаря фотосинтезу водных растений. Кислород диффундирует в воду очень медленно; диффузии способствует ветер и движение воды; важнейшим фактором, обеспечивающим фотосинтетическую продукцию кислорода, является свет, проникающий в толщу воды. Таким образом, содержание кислорода в водной среде сильно меняется в зависимости от времени суток, времени года и местоположения.[ . ]
В воде чистых водоемов содержится растворенный кислород. Растворимость, а следовательно, его концентрация зависят от температуры воды. Растворенный кислород расходуется на окисление органических веществ, попадающих в водоем, в том числе вносимых загрязнениями сточных вод при спуске их в водоем.[ . ]
Заморы — массовая гибель водных обитателей из-за нехватки растворенного кислорода. Растворимость кислорода сильно уменьшается при загрязнении и нагревании воды.[ . ]
Азот попадает в природные воды при поглощении его из воздуха, восстановлении соединений азота денитрифицирующими бактериями, а также разложении органических остатков. Несмотря на меньшую, по сравнению с кислородом, растворимость азота содержание последнего в природных водах большее благодаря более высокому парциальному давлению его в воздухе.[ . ]
Скорость выделения или поглощения газов зависит от величины поверхности соприкосновения среды обитания микроорганизмов с атмосферой и возрастает при перемешивании. Эта закономерность важна для регулирования роста микроорганизмов и снабжения их кислородом. Растворимость кислорода в воде при 760 мм рт. ст. изменяется в зависимости от температуры. В 1 л йоды при 25 °С растворяется 8,3; при 30 °С 7,5; при 35 °С 7,0; при 40 °С 6,5; при 45 °С 6,0 мг кислорода. Недостаток кислорода замедляет процессы биохимического окисления загрязнений сточных вод.[ . ]
Вторая группа специфических гумусовых веществ — фульвокислоты — изучена значительно слабее. Согласно исследованиям И. В. Тюрина, они являются высокомолекулярными оксикарбоновыми кислотами, содержащими азот. От гуминовых кислот отличаются светлой окраской, меньшим количеством углерода и большим содержанием кислорода, растворимостью в воде и минеральных кислотах и более значительной способностью к кислотному гидролизу.[ . ]
Чрезвычайно распыленный по горным породам марганец вымывается водой, попадая в подземные воды, а также в реки, по которым сотнями тысяч тонн ежегодно выносится в океан. Между тем содержание марганца в морской воде очень мало (10-7—10-6%), тогда как ил глубоких мест океана содержит значительно большее его количество (до 0,3%). Обусловлено это постоянно протекающим медленным окислением (за счет растворенного в воде кислорода) растворимых соединений двухвалентного марганца до практически нерастворимого гидрата двуокиси МпОг-хНгО, который и осаждается на дно. В отдельных местах океанского дна обнаружены камнеподобные образования («конкреции»), содержащие иногда до 45% марганца.[ . ]
Источник
Растворимость кислорода воде таблица
Кислород постоянно присутствует в растворенном виде в поверхностных водах. Содержание растворенного кислорода (РК) в воде характеризует кислородный режим водоема и имеет важнейшее значение для оценки его экологического и санитарного состояния. Кислород должен содержаться в воде в достаточном количестве, обеспечивая условия для дыхания гидробионтов. Он также необходим для самоочищения водоемов, т.к. участвует в процессах окисления органических и других примесей, разложения отмерших организмов. Снижение концентрации РК свидетельствует об изменении биологических процессов в водоеме, о загрязнении водоема биохимически интенсивно окисляющимися веществами (в первую очередь органическими). Потребление кислорода обусловлено также химическими процессами окисления содержащихся в воде примесей, а также дыханием водных организмов.
Поступление кислорода в водоем происходит путем растворения его при контакте с воздухом (абсорбции), а также в результате фотосинтеза водными растениями, т.е. в результате физико-химических и биохимических процессов. Кислород также поступает в водные объекты с дождевыми и снеговыми водами. Поэтому существует много причин, вызывающих повышение или снижение концентрации в воде растворенного кислорода.
Растворенный в воде кислород находится в виде гидратированных молекул О2. Содержание РК зависит от температуры, атмосферного давления, степени турбулизации воды, количества осадков, минерализации воды др. При каждом значении температуры существует равновесная концентрация кислорода, которую можно определить по специальным справочным таблицам, составленным для нормального атмосферного давления. Степень насыщения воды кислородом, соответствующая равновесной концентрации, принимается равной 100%. Растворимость кислорода возрастает с уменьшением температуры и минерализации и с увеличением атмосферного давления.
В поверхностных водах содержание растворенного кислорода может колебаться от 0 до 14 мг/л и подвержено значительным сезонным и суточным колебаниям. В эвтрофированных и сильно загрязненных органическими соединениями водных объектах может иметь место значительный дефицит кислорода. Уменьшение концентрации РК до 2 мг/л вызывает массовую гибель рыб и других гидробионтов.
В воде водоемов в любой период года до 12 часов дня концентрация РК должна быть не менее 4 мг/л. ПДК растворенного в воде кислорода для рыбохозяйственных водоемов установлена 6 мг/л (для ценных пород рыбы) либо 4 мг/л (для остальных пород).
Растворенный кислород является весьма неустойчивым компонентом химического состава вод. При его определении особо тщательно следует проводить отбор проб: необходимо избегать контакта воды с воздухом до фиксации кислорода (связывания его в нерастворимое соединение).
Контроль содержания кислорода в воде – чрезвычайно важная проблема, в решении которой заинтересованы практически все отрасли народного хозяйства, включая черную и цветную металлургию, химическую промышленность, сельское хозяйство, медицину, биологию, рыбную и пищевую промышленность, службы охраны окружающей среды. Содержание РК определяют как в незагрязненных природных водах, так и в сточных водах после очистки. Процессы очистки сточных вод всегда сопровождаются контролем содержания кислорода. Определение РК является частью анализа при определении другого важнейшего показателя качества воды – биохимического потребления кислорода (БПК).
Определение концентрации РК в воде проводится методом йодометрического титрования – методом Винклера, широко используемым и общепринятым при санитарно-химическом и экологическом контроле*. Метод определения концентрации РК основан на способности гидроксида марганца (II) окисляться в щелочной среде до гидроксида марганца (IV), количественно связывая при этом кислород. В кислой среде гидроксид марганца (IV) снова переходит в двухвалентное состояние, окисляя при этом эквивалентное связанному кислороду количество йода. Выделившийся йод оттитровывают раствором тиосульфата натрия в присутствии крахмала в качестве индикатора.
Определение РК проводится в несколько этапов. Сначала в анализируемую воду добавляют соль Мn (II), который в щелочной среде реагирует с растворенным кислородом с образованием нерастворимого дегидратированного гидроксида Мn (IV) по уравнению:
Таким образом производится фиксация, т.е. количественное связывание, кислорода в пробе. Фиксация РК, являющегося неустойчивым компонентом в составе воды, должна быть проведена сразу после отбора пробы.
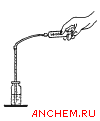
Далее к пробе добавляют раствор сильной кислоты (как правило, соляной или серной) для растворения осадка и раствор йодида калия, в результате чего протекает химическая реакция с образованием свободного йода по уравнению:
Затем свободный йод титруют раствором тиосульфата натрия в присутствии крахмала, который добавляют для лучшего определения момента окончания титрования. Реакции описываются уравнениями:
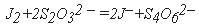
J2 + крахмал —» синее окрашивание
О завершении титрования судят по исчезновению синей окраски (обесцвечиванию) раствора в точке эквивалентности. Количество раствора тиосульфата натрия, израсходованное на титрование, пропорционально концентрации растворенного кислорода.
В ходе анализа воды определяют концентрацию РК (в мг/л) и степень насыщения им воды (в %) по отношению к равновесному содержанию при данных температуре и атмосферном давлении.
В сточных и загрязненных поверхностных водах могут присутствовать компоненты, оказывающие мешающее влияние и искажающие результаты определения РК методом Винклера. К таким компонентам относятся следующие загрязняющие вещества.
1. Взвешенные и окрашенные вещества. Они могут помешать определению, адсорбируя йод на своей поверхности или химически взаимодействуя с ним. При наличии в анализируемой воде взвешенных веществ их отделяют отстаиванием (не фильтрованием!) либо осветлением при добавлении раствора алюмокалиевых квасцов и аммиака.
2. Биологически активные взвешенные вещества (например, активный ил биохимических очистных сооружений). Пробы сточных вод, содержащие плохо оседающие взвешенные вещества, которые могут вызвать снижение концентрации кислорода вследствие продолжающейся жизнедеятельности микроорганизмов, необходимо осветлять также прибавлением раствора алюмокалиевых квасцов при одновременном добавлении токсичного для микроорганизмов вещества (растворов сульфаминовой кислоты, хлорида ртути или сульфата меди) сразу после отбора пробы.
3. Восстановители, реагирующие с выделенным йодом в кислой среде (сульфиты, тиосульфаты, сульфиды). Для устранения влияния восстановителей используют метод Росса, основанный на добавках к пробам растворов гипохлорита натрия NaOCl, хлорной извести CaOCl2 и роданида калия KNCS.
4. Окислители, выделяющие йод из йодида калия (активный хлор, нитриты, катионы железа (III) и др.). Влияние железа (III) устраняется добавлением раствора фторида калия.
Влияние нитритов, которые часто встречаются в природных и сточных водах, устраняют добавлением раствора сульфаниловой кислоты, обычно предусмотренного в измерительных комплектах производства ЗАО «Крисмас+».
Процесс определения РК проводится в кислородных калиброванных склянках из комплекта и включает:
– специальную обработку пробы для устранения мешающего влияния примесей (выполняется при необходимости, преимущественно при анализе сточных вод);
– фиксацию кислорода, проводимую немедленно после заполнения кислородной склянки;
– титрование, которое может быть проведено через некоторое время (но не более суток).
При выполнении анализа несколько раз повторяются следующие операции.
 | 1. Наполнение мерных пипеток растворами проводят с помощью медицинского шприца с соединительной трубкой (а не ртом!). 2. Перенос раствора в наполненной пипетке проводят (при необходимости), герметично зажав ее верхнее отверстие пальцем. Раствор не должен скапывать с пипетки! |
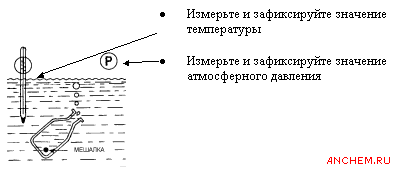
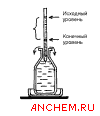 | 3. Погружение пипетки с раствором в кислородную склянку осуществляют на глубину 2–3 см, как показано на рисунке, и по мере выливания раствора поднимают вверх. Излишек жидкости из склянки стекает через край на подставленную чашку Петри. |
 | 4. После введения раствора склянку быстро закрывают пробкой, слегка наклонив ее. Излишек жидкости стекает через край. В склянке не должно остаться пузырьков воздуха. Склянка не должна оставаться открытой. |
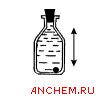 | 5. Содержимое склянки перемешивают помещенной внутрь склянки мешалкой, удерживая склянку рукой. |
Оборудование и реактивы
Барометр любого типа; груша резиновая или медицинский шприц; колба коническая вместимостью 250–300 мл; склянка кислородная калиброванная (100–200 мл) с пробкой; мешалка (стеклянные шарик, палочка и т.п.) известного объема; пипетки мерные на 1 мл и 10 мл; термометр с ценой деления не более 0,5°С; поддон.
Раствор соли марганца; раствор серной кислоты (1:2); раствор тиосульфата натрия (0,02 моль/л экв.); раствор крахмала (0,5%); раствор йодида калия щелочной.
Если в лаборатории имеются приборы для измерения содержания растворенного в воде кислорода (оксиметры), их с успехом можно использовать для выполнения анализов в полевых условиях.
Приготовление растворов см. приложение 3.
Отбор пробы
Отбор проб на содержание РК имеет ряд особенностей.
Для отбора проб на РК в общем случае (ГОСТ 17.1.5.05) используют батометр, к крану которого прикреплена резиновая трубка длиной 20–25 см. Для отбора проб воды из поверхностных горизонтов используют эмалированную либо стеклянную посуду. Если отбирается общая проба воды для анализов по разным компонентам, то проба для определения РК должна быть первой, взятой для дальнейшей обработки.
Водой из отобранной пробы ополаскивают 2–3 раза чистые калиброванные склянки из состава комплекта или (если требуется специальная подготовка проб, например отстаивание) стеклянные бутыли.
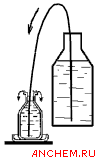
Отбор пробы для измерения концентрации РК непосредственно на водоеме выполняют следующим образом.
Примечания. 1. В склянке не должно остаться пузырьков воздуха.
2. Анализируйте пробу, по возможности, скорее.
Проведение анализа
А. Фиксация кислорода в пробе
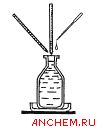 | 1. Введите в склянку разными пипетками 1 мл раствора соли марганца, затем 1 мл раствора йодида калия и 1–2 капли раствора сульфаминовой кислоты**, после чего закройте склянку пробкой. 2. Перемешайте содержимое склянки с помощью имеющейся внутри мешалки, держа склянку в руке. Дайте отстояться образующемуся осадку не менее 10 мин. |
Примечание. Склянку с фиксированной пробой можно хранить в затемненном месте не более 1 суток .
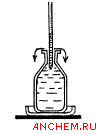 | 3. Введите в склянку пипеткой 2 мл раствора серной кислоты, погружая пипетку до осадка (не взмучивать!) и постепенно поднимая ее вверх по мере опорожнения. 4. Склянку закройте пробкой и содержимое перемешайте до растворения осадка. |
 | 5. Содержимое склянки полностью перенесите в коническую колбу на 250 мл. Примечание. Определение концентрации РК в воде можно выполнять путем титрования части пробы. При этом в колбу на 100 мл цилиндром переносят 50,0 мл пробы с растворенным осадком***. Дальнейшие операции проводят, как описано ниже, для обработки полной пробы. |
 | 6. В бюретку (пипетку), закрепленную в штативе из состава комплекта, наберите 10 мл раствора тиосульфата и титруйте пробу до слабо желтой окраски. Затем добавьте пипеткой 1 мл раствора крахмала (раствор в колбе синеет) и продолжайте титрование до полного обесцвечивания раствора. |
 | 7. Определите общий объем раствора тиосульфата, израсходованный на титрование (как до, так и после добавления раствора крахмала). |
При наличии в анализируемой воде мешающих примесей (взвешенных и окрашенных веществ, восстановителей, железа в концентрациях более 1 мг/л) выполняют специальную обработку пробы (подробно описано в паспорте на комплект «Растворенный кислород»). Далее пробой заполняют кислородную склянку, выполняют фиксацию и титрование, как описано выше.
Вычисление результатов анализа
В случае титрования всего количества раствора в кислородной склянке массовую концентрацию РК в анализируемой пробе воды (СРК) в мг/л рассчитайте по формуле:
где:
8 – эквивалентная масса атомарного кислорода;
CТ – концентрация титрованного стандартного раствора тиосульфата, моль/л экв.;
VТ – общий объем раствора тиосульфата, израсходованного на титрование (до и после добавления раствора крахмала), мл;
V – внутренний объем калиброванной кислородной склянки с закрытой пробкой (определяется заранее для каждой склянки отдельно), мл;
V1 – суммарный объем растворов хлорида марганца и йодида калия, добавленных в склянку при фиксации РК, а также мешалки, мл (рассчитывается как V1=1+1+0,5=2,5 мл);
1000 – коэффициент пересчета единиц измерения из г/л в мг/л.
Примечание. Принимается, что потери растворенного кислорода в фиксированной форме при сливе излишков жидкости из склянки и при выполнении других операций много меньше результата измерений (пренебрежимо малы).
В случае титрования части пробы (50,0 мл) в кислородной склянке, массовую концентрацию РК в анализируемой пробе воды (СРК в мг/л) рассчитывают по формуле:
Пример расчета концентрации растворенного кислорода в воде.
При общем объеме раствора тиосульфата, израсходованного на титрование, равном 4,7 мл, концентрации раствора тиосульфата 0,02 ммоль/л экв. и объеме кислородной склянки 102,5 мл содержание растворенного кислорода рассчитывается как:
Для определения степени насыщения воды кислородом по табл. 13 определите величину концентрации насыщенного раствора кислорода в воде (СН, мг/л), исходя из температуры воды, зафиксированной в момент отбора пробы.
Далее рассчитайте степень насыщения воды кислородом (R) в % с учетом фактической величины атмосферного давления по формуле:
где:
100 – коэффициент пересчета единиц измерения из мг/л в %;
760 – нормальное атмосферное давление, мм рт. ст.;
СН – величина концентрации насыщенного раствора кислорода для условий отбора, определенная по табл. 13.
Р – фактическая величина атмосферного давления в момент отбора пробы.
Примечание. При отсутствии данных об атмосферном давлении в момент отбора допускается его принимать равным нормальному (т.е. 760 мм рт. ст.).
Зависимость равновесной концентрации кислорода в воде от температуры
(атмосферное давление – 760 мм рт. ст.)
| Температура | Равновесная концентрация растворенного кислорода (в мг/л) при изменении температуры на десятые доли °С (Сн) | |||||||||
| °С | 0 | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 |
| 0 | 14,65 | 14,61 | 14,57 | 14,53 | 14,49 | 14,45 | 14,41 | 14,37 | 14,33 | 14,29 |
| 1 | 14,25 | 14,21 | 14,17 | 14,13 | 14,09 | 14,05 | 14,02 | 13,98 | 13.94 | 13,90 |
| 2 | 13,86 | 13,82 | 13,79 | 13,75 | 13,71 | 13,68 | 13,64 | 13,60 | 13,56 | 13,53 |
| 3 | 13,49 | 13,46 | 13,42 | 13,38 | 13,35 | 13,31 | 13,28 | 13,24 | 13,20 | 13,17 |
| 4 | 13,13 | 13,10 | 13,06 | 13,03 | 13,00 | 12,96 | 12,93 | 12,89 | 12,86 | 12,82 |
| 5 | 12,79 | 12,76 | 12,72 | 12,69 | 12,66 | 12,52 | 12,59 | 12,56 | 12,53 | 12,49 |
| 6 | 12,46 | 12,43 | 12,40 | 12,36 | 12,33 | 12,30 | 12,27 | 12,24 | 12,21 | 12,18 |
| 7 | 12,14 | 12,11 | 12,08 | 12,05 | 12,02 | 11,99 | 11,96 | 11,93 | 11,90 | 11,87 |
| 8 | 11,84 | 11,81 | 11,78 | 11,75 | 11,72 | 11,70 | 11,67 | 11,64 | 11,61 | 11,58 |
| 9 | 11,55 | 11,52 | 11,49 | 11,47 | 11,44 | 11,41 | 11,38 | 11,35 | 11,33 | 11,30 |
| 10 | 11,27 | 11,24 | 11,22 | 11,19 | 11,16 | 11,14 | 11,11 | 11,08 | 11,06 | 11,03 |
| 11 | 11,00 | 10,98 | 10,95 | 10,93 | 10,90 | 10,87 | 10,85 | 11,82 | 10,80 | 10,77 |
| 12 | 10,75 | 10,72 | 10,70 | 10,67 | 10,65 | 10,62 | 10,60 | 10,57 | 10,55 | 10,52 |
| 13 | 10,50 | 10,48 | 10,45 | 10,43 | 10,40 | 10,38 | 10,36 | 10,33 | 10,31 | 10,28 |
| 14 | 10,26 | 10,24 | 10,22 | 10,19 | 10,17 | 10,15 | 10,12 | 10,10 | 10,08 | 10,06 |
| 15 | 10,03 | 10,01 | 9,99 | 9,97 | 9,95 | 9,92 | 9,90 | 9,88 | 9,86 | 9,84 |
| 16 | 9,82 | 9,79 | 9,77 | 9,75 | 9,73 | 9,71 | 9,69 | 9,67 | 9,65 | 9,63 |
| 17 | 9,61 | 9,58 | 9,56 | 9,54 | 9,52 | 9,50 | 9,48 | 9,46 | 9,44 | 9,42 |
| 18 | 9,40 | 9,38 | 9,36 | 9,34 | 9,32 | 9,30 | 9,29 | 9,27 | 9,25 | 9,23 |
| 19 | 9,21 | 9,19 | 9,17 | 9,15 | 9,13 | 9,12 | 9,10 | 9,08 | 9,06 | 9,04 |
| 20 | 9,02 | 9,00 | 8,98 | 8,97 | 8,95 | 8,93 | 8,91 | 9,90 | 8,88 | 8,86 |
| 21 | 8,84 | 8,82 | 8,81 | 8,79 | 8,77 | 8,75 | 8,74 | 8,72 | 8,70 | 8,68 |
| 22 | 8,67 | 8,65 | 8,63 | 8,62 | 8,60 | 8,58 | 8,56 | 8,55 | 8,53 | 8,52 |
| 23 | 8,50 | 8,48 | 8,46 | 8,45 | 8,43 | 8,42 | 8,40 | 8,38 | 8,37 | 8,35 |
| 24 | 8,33 | 8,32 | 8,30 | 8,29 | 8,27 | 8,25 | 8,24 | 8,22 | 8,21 | 8,19 |
| 25 | 8,18 | 8,16 | 8,14 | 8,13 | 8,11 | 8,11 | 8,08 | 8,07 | 8,05 | 8,04 |
| 26 | 8,02 | 8,01 | 7,99 | 7,98 | 7,96 | 7,95 | 7,93 | 7,92 | 7,90 | 7,89 |
| 27 | 7,87 | 7,86 | 7,84 | 7,83 | 7,81 | 7,80 | 7,78 | 7,77 | 7,75 | 7,74 |
| 28 | 7,72 | 7,71 | 7,69 | 7,68 | 7,66 | 7,65 | 7,64 | 7,62 | 7,61 | 7,59 |
| 29 | 7,58 | 7,56 | 7,55 | 7,54 | 7,52 | 7,51 | 7,49 | 7,48 | 7,47 | 7,45 |
| 30 | 7,44 | 7,42 | 7,41 | 7,40 | 7,38 | 7,37 | 7,35 | 7,34 | 7,32 | 7,31 |
Пример расчета степени насыщения воды кислородом.
При значениях СРК=7,52 мг/л, СН=9,82 мг/л, Р=735 мм рт. ст. и температуре воды в момент отбора 16°С степень насыщения составляет:
Контроль точности измерений
При выполнении измерений концентрации РК в воде контроль точности необходимо проводить по поверенному (образцовому) оксиметру.
* Например, РД 52.24.419, ИСО 5813 и др.
** Если вода не содержит нитритов или их содержание менее 0,05 мг/л, раствор сульфаминовой кислоты можно не добавлять. Однако концентрация нитритов, как правило, неизвестна, поэтому мы рекомендуем добавлять сульфаминовую кислоту при каждом анализе.
*** В данном случае из одной фиксированной пробы можно получить несколько параллельных результатов измерений, однако это приводит к некоторому снижению точности анализа.
Источник