- Органическая химия
- FONT_SIZE
- SCREEN
- Статьи
- Видеоуроки
- Определение воды по К. Фишеру
- Теория титрования по Фишеру
- Получение реактива Фишера
- Типы титрования по Фишеру и рекомендации
- Метод Карла Фишера простыми словами
- Варианты реализации метода Карла Фишера
- Безмембранные электроды для метода Карла Фишера
- Ограничения при использовании безмембранных ячеек
- Реактив фишера с водой
Органическая химия
Взгляд из лаборатории
FONT_SIZE
SCREEN
- WIDE_SCREEN
- FULL_SCREEN
- NARROW_SCREEN
Статьи

Видеоуроки

Определение воды по К. Фишеру

Вода – это превосходный растворитель. Нетоксичный и дешевый. Однако лишь немногие органические реакции способны протекать в водной среде. Более того, вода способна оказывать разрушающее действие на многие органические соединения, приводить к побочным реакциям в химических процессах. Т.о. необходимо точное определение воды в используемых реагентах и/или растворителях.
Теория титрования по Фишеру
Для определения содержания воды в органических соединениях следовало подобрать такую реакцию, в которую вступает лишь растворенная вода, а сам метод может быть использован для широкого класса соединений.
Эту задачу удалось решить в 1935 году немецкому химику Карлу Фишеру (см. лит.). Фундаментальный принцип «определения воды по Фишеру» основан на реакции Бунзена между йодом, диоксидом серы и водой. К. Фишер обнаружил, что использование избытка диоксида серы, метанола в качестве растворителя и пиридина как основания (для буферизации раствора) можно использовать для определения воды в неполярных растворителях.
Титрование представляет собой трехстадийный процесс:
На первой стадии вода реагирует с диоксидом серы, в результате чего I2 восстанавливается до I — (реакция 1). Выделяющейся триоксид серы образует с пиридином комплекс (реакция 2), который в присутствии метанола (или другого спирта) превращается в стабильный пиридиновый комплекс (реакция 3). Таким образом, для титрования каждого эквивалента воды затрачивается один эквивалент йода.
В качестве спирта обычно используется метанол, реже диэтиленгликоль.
В качестве основания – пиридин, но чаще имидазол или первичные амины.
Получение реактива Фишера
Типы титрования по Фишеру и рекомендации
Волюметрическое титрование (от 100 ppm до 100% воды)
1) К образцу в подходящем для титрования растворителе (или без растворителя если вещество жидкое) из бюретки добавляют титрант, содержащий все необходимые компоненты реактива Фишера.
2) К образцу растворенному в среде содержащей основание, диоксид серы и спирт из бюретки добавляют титрант, содержащий только йод и спирт.
Кулонометрическое титрование (от 1 ppm до 5% воды)
В данном титровании йод генерируется электрохимически in situ в течение титрования, а содержание воды определяется как общее количество тока, прошедшее через кулонометрическую ячейку. В данном случае результат титрования определяется микропроцессором прибора и выводится на экран.
Внимание!
1. Реагент Фишера неустойчив к действию света и влаги. Его стандартизация должна проводиться перед каждым использованием.
2. Рабочий интервал pH для определения воды по Фишеру между 5 и 8, в противном случае высоко кислотные или основные соединения рекомендуется буферизовать.
3. Плохо растворимые в метаноле соединения (например, жиры, углеводороды) следует растворять в высших спиртах или хлороформе, возможны также добавки формамида (для полярных веществ).
4. Следует избегать титрования веществ, которые способны реагировать с компонентами реактива Фишера (например, альдегиды и кетоны, сильные кислоты и основания, окислители и восстановители, соединения, реагирующие с компонентами реактива Фишера с образованием воды).
Источник
Метод Карла Фишера простыми словами
Метод Карла Фишера служит для определения содержания воды (влаги) в различных образцах с помощью титрования. Схему реакции и историю открытия метода Вы найдете в Интернете. Мы здесь кратко изложим его специфику в виде шпаргалки.
Реакция (точнее три реакции), открытая в 1935 году Карлом Фишером, на вид не простая, но именно она была положена в основу определения содержания воды в образцах методом титрования, поскольку идеально подходила под эту технику.
Основное, что нужно понять это то, что здесь вода – не растворитель, как это обычно бывает, а реагент. Для простоты можно себе представить, что йод взаимодействует с водой в определенном стехиометрическом соотношении, а обеспечивается это наличием соответствующего растворителя
Варианты реализации метода Карла Фишера
Существует два варианта реализации данного метода в лаборатории:
- волюметрический
- кулонометрический
Первый вариант – это классическое (иначе волюметрическое) титрование, когда Вы этот йод добавляете к раствору из бюретки до достижения точки эквивалентности, т.е пока не оттитруете всю содержащуюся воду. У данного варианта есть ограничение по пределу обнаружения. Оно связано с минимальным размером порции добавляемого титранта, т.е размером капли жидкости. Таким образом этот вариант применим для определения не очень низких концентраций воды, от 0,2% и выше.
Для определения же влаги в концентрации менее 0,2% и практически до 0,0005% существует второй вариант этого титрования – кулонометрический. Он состоит в том, что йод не добавляется порциями, а генерируется электролизом на соответствующем электроде, также погруженном в исследуемый раствор. Генерируется он по реакции 2I — — 2ē -> I2 0 . Для этого йодид (соль йодида калия) также добавляется в раствор. В кулонометрическом варианте количество йода, израсходованное до достижения точки эквивалентности прямо пропорционально количеству электричества, пошедшего на его генерирование, оно может быть очень малым и соответственно связать мизерное количество воды. Электроды для генерирования йода (иначе их называют ячейками) бывают двух модификаций: электроды мембранные и безмембранные, и у каждой есть свои нюансы использования. Первые титраторы по методу Карла Фишера выпускались с электродами с мембраной, однако позднее появились безмембранные версии. Остановимся коротко на их преимуществах.

Безмембранные электроды для метода Карла Фишера
Производство первых безмембранных ячеек для кулонометров Фишера было начато в 1989 г. По сравнению с мембранными ячейками они имеют следующие основные преимущества:
- исключаются проблемы с загрязнением или засорением мембраны;
- существенно облегчается очистка ячеек;
- достигается меньшее значение дрейфа.
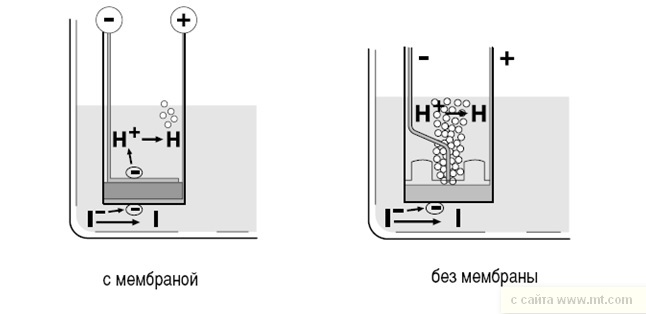
Вначале мембрана представляла собой часть генерирующего электрода. Ее назначение — не пропускать выделившийся йод к катоду, где он может снова восстановиться до йодида (вместо того чтобы вступить в реакцию с водой).
Подобный процесс невозможен в современной модификации безмембранного электрода. Катод имеет меньшие размеры и конструкцию, затрудняющую доступ йода, так что йод успевает прореагировать с водой раньше, чем достигает катода.
Водород, выделяющийся на катоде, формирует на его поверхности газовую пленку. Она практически исключает возможность проникновения йода к катоду и восстановления его до йодида. Этот эффект дополнительно усиливается за счет придания катоду специальной формы.
Тем не менее, незначительная часть йода все-таки может достигать катода. Образующуюся вследствие этого ошибку можно минимизировать путем увеличения объема образца.
На практике ячейки с мембранами имеет смысл использовать только при измерении образцов с очень низким содержанием воды (
Ограничения при использовании безмембранных ячеек
Ячейки без мембран не подходят для измерения легко восстанавливающихся образцов.
Образующийся в ходе реакции водород выделяется на катоде. Он является очень сильным восстановителем, особенно для нитросоединений, например, нитробензола.
R-NO2 + 6 H → R-NH2 + 2 H2O
Другие легко восстанавливающиеся вещества, такие как ненасыщенные жирные кислоты и т.п, также могут восстанавливаться на катоде с образованием воды.
Область применения безмембранных ячеек
Безмембранные ячейки идеально подходят для определения содержания воды в следующих
- углеводороды; — хлорированные углеводороды;
- спирты; — фенолы (в большинстве случаев);
- простые и сложные эфиры;
- кетоны (со специальным реагентом); — ацетамид;
- эфирные масла и эссенции; — пищевые масла.
- минеральные масла;
Ячейки с мембранами необходимо использовать в следующих случаях:
- при измерении образцов с очень низким содержанием воды (
- при необходимости получения очень точных результатов;
- при измерении нитросоединений;
- ненасыщенных углеводородов (в особенности легко восстанавливающихся).
Преимущества использования безмембранных электродов
- используется только один реагент Фишера
- наборы для автоматической смены реагентов, выпускаемые такими производителями, как Mettler Toledo и Metrohm, на все 100% работают только с безмембранными электродами.
Определение точки эквивалентности
Что касается определения точки эквивалентности, то для этих целей используется поляризованный электрод. На два контакта этого электрода постоянно подается напряжение для поддержания заданного тока поляризации. После достижения точки эквивалентности, т.е когда в системе появится йод, которому не с чем связаться, проводимость раствора увеличится и соответственно напряжение для поддержания того же тока резко упадет. По этой точке и проводят расчет количества оттитрованной воды.
С точки зрения практической реализации метода Карла Фишера сложность состоит в том, что в любом лабораторном аппарате всегда присутствует влага из воздуха и более того, необходимо учесть, что даже в процессе титрования или ожидания какое-то количество влаги будет поступать в систему извне. Для того, чтобы это учесть и затем скорректировать результат анализа прибор, на котором выполняется титрование по Фишеру должен уметь постоянно оттитровывать влагу, поступающую извне (это называется дрейфом), т.е титровать, находясь в режиме ожидания.
Определения содержания воды методом Карла Фишера на современных титраторах производится с высокой точностью и не требует от оператора специальной подготовки.
Ограничения использования метода Карла Фишера
Метод Карла Фишера может использоваться для широкого спектра образцов однако у него есть и ограничения, обусловленные возможным взаимодействием образца или входящих в его состав компонентов с реагентом Карла Фишера. В таких случаях может возникать ошибка определения. Если образец или его компоненты взаимодействует с йодом то ошибка будет в сторону завышения. Если же в результате окисления йодсодержащих компонентов реагента Карла Фишера формируется йод, то будет ошибка в сторону занижения результатов.
В данной таблице приведены соединения и материалы, которые могут быть оттитрованы методом Карла Фишера напрямую, вещества, которые могут титроваться только после специальной обработки и в последней группе те соединения, для которых данный метод не подходит вовсе.
Однако даже для последней группы соединений есть возможность применить непрямой метод титрования по Карлу Фишеру, а именно выпаривание воды из образца с выдуванием в ячейку с последующим титрованием. Для реализации такого подхода производители предлагают специальные печки. Нужно понимать, что если Ваш образец хорошо отдает воду при нагревании, то анализ с использованием печи будет самым оптимальным: сама титровальная ячейка будет всегда чистой и при этом у Вас будет существенная экономия на реагентах!
Вещества, которые могут быть оттитрованы прямым добавлением в ячейку титрования
Органические соединения:
- Углеводороды (насыщенные, непредельные соединения)
- Спирты, многоатомные спирты, фенолы, эфиры
- Кетоны: диизопропилкетон и др.)
- Альдегиды: формальдегид, трихлоруксусный альдегид (хлораль) и др.)
- Органические кислоты, аминокислоты
- Кислотные ангидриды
- Эфиры, лактоны, эфиры неорганических кислот
- Амины
- Белки, Амиды, Анилиды
- Нитрилы, Цианогидрины, производные циановой кислоты
- Нитросоединения, Оксимы, Гидроксимовые кислоты
- Тиоцианат, Тиоэфирах, Thioesters
- Галогенированные углеводороды, Галогенированные ацилы
- Сахара, органические соли и их гидраты
Неорганические соединения:
- Неорганические соли и их гидраты
- Неорганические кислоты
- Хелатные комплексы
- Удобрения
- Карбонат кальция
- Поливольфраматы
Соединения, которые могут быть оттитрованы только после специальной обработки
Источник
Реактив фишера с водой
Как было сказано выше, волюметрическое титрование сводится к добавлению йодсодержащего титранта. Для протекания реакции йода с водой также необходимы спирт (или аналог) и органическое основание, которые могут содержаться как в титранте, так и в реактиве для титровальной ячейки.
В зависимости от состава реактивы Фишера бывают однокомпонентные и двухкомпонентные.
Однокомпонентный реактив Фишера (титрант) содержит в себе все реагирующие вещества: йод, имидазол, спирт, двуокись серы. В этом случае в титровальной ячейки необходима лишь среда для протекания реакции: спирт, хлороформ и др.
В Двухкомпонентных реактивах Фишера — взаимодействующие вещества распределение между титрантом и растворителем. Первый реактив (титрант) — это спиртовой раствор йода, а второй (растворитель) — это спиртовой раствор SO2 с имидазолом или пиридином.
Наибольшее распространение получили реактивы Honeywell, под торговой маркой Hydranal и Merck торговая марка Aquastar. Также на рынке представлены отечественные реактивы Карла Фишера достойного качества.
Однокомпонентные реактивы Фишера не устойчивы и за год хранения в запечатанной бутыли титр может измениться на 0,5 мг. Двухкомпонентные реактивы Фишера устойчивы при хранении и дают большую скорость титрования из-за избыточного содержания SO2 в растворителе.
Титранты Карла Фишера выпускаются с титром 1, 2 и 5 мг воды на 1 мл титранта.
С течением времени концентрация титранта может меняться, так как входящий в его состав йод не устойчив под воздействием света, титрант поглощает влагу из атмосферы и реагирует на изменение температуры. Согласно ИСО 760 повышение температуры на 1 °C приводит к уменьшению концентрации йода на 0,1%.
GLP рекомендует выполнять стандартизацию титранта каждые 4 часа в процессе работы, но при отсутствии изменений температуры и влажности в течении дня достаточно стандартизовать титрант каждый день перед началом работ. Для этого используют стандартные растворы воды или дигидрат тартрата натрия.
Если в качестве стандарта используется дигидрат тартрата натрия, то после внесения порошка в титровальную ячейку необходимо дождаться его полного растворения, обычно это занимает 2−3 минуты (раствор станет прозрачным). В противном случае при титровании мутного раствора будут получены неправильные результаты.
Источник