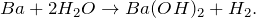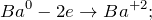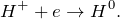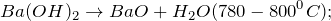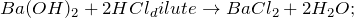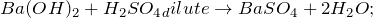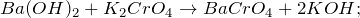- Барий: способы получения и химические свойства
- Способ получения
- Качественная реакция
- Химические свойства
- Реакция бария с водой
- Реакция взаимодействия бария с водой.
- Уравнение реакции взаимодействия бария с водой:
- Мировая экономика
- Справочники
- Востребованные технологии
- Поиск технологий
- О чём данный сайт?
- О Второй индустриализации
- Ba + H2O = ? уравнение реакции
- Гидрид бария: способы получения и химические свойства
- Способ получения
- Химические свойства
- 2.2.2. Химические свойства металлов IIA группы.
- Взаимодействие с простыми веществами
- с кислородом
- с галогенами
- с неметаллами IV–VI групп
- с водородом
- Взаимодействие со сложными веществами
- с водой
- c кислотами-неокислителями
- c кислотами-окислителями
- − разбавленной азотной кислотой
- − концентрированной азотной кислотой
- − концентрированной серной кислотой
- с щелочами
- с оксидами
Барий: способы получения и химические свойства
Барий Ba — щелочноземельный металл. Серебристо-белый, ковкий, пластичный. На воздухе покрывается темной оксидно-нитридной пленкой. Реакционноспособный. Сильный восстановитель;
Относительная молекулярная масса Mr = 137,327; относительная плотность для твердого и жидкого состояния d = 3,6; tпл = 727º C; tкип = 1860º C.
Способ получения
1. В результате взаимодействия оксида бария и кремния при 1200º С образуются силикат бария и барий:
3BaO + Si = BaSiO3 + 2Ba
2. Оксид бария взаимодействует с алюминием при 1100 — 1200º С образуя барий и алюминат бария:
4BaO + 2Al = 3Ba + Ba(AlO2)2
3. В результате разложения гидрида бария при температуре выше 675º С образуется барий и водород:
Качественная реакция
Барий окрашивает пламя газовой горелки в желто — зеленый цвет.
Химические свойства
1. Барий вступает в реакцию с простыми веществами :
1.1. Барий взаимодействует с азотом при 200 — 460º С образуя нитрид бария:
1.2. Барий сгорает в кислороде (воздухе) при температуре выше 800º С, то на выходе будет образовываться оксид бария:
2Ba + O2 = 2BaO
1.3. Барий активно реагирует при температуре 100 — 150º С с хлором, бромом, йодом и фтором . При этом образуются соответствующие соли :
1.4. С водородом барий реагирует при температуре 150 — 300º C с образованием гидрида бария:
1.6. Барий взаимодействует с серой при 150º С и образует сульфид бария:
Ba + S = BaS
1.7. Барий взаимодействует с углеродом (графитом) при 500º С и образует карбид бария:
Ba + 2C = BaC2
2. Барий активно взаимодействует со сложными веществами:
2.1. Барий при комнатной температуре реагирует с водой . Взаимодействие бария с водой приводит к образованию гидроксида бария и газа водорода:
2.2. Барий взаимодействует с кислотами:
2.2.1. Барий реагирует с разбавленной соляной кислотой, при этом образуются хлорид бария и водород :
Ba + 2HCl = BaCl2 + H2 ↑
2.2.2. Реагируя с разбавленной азотной кислотой барий образует нитрат бария, оксид азота (I) и воду:
если азотную кислоту еще больше разбавить, то образуются нитрат бария, нитрат аммония и вода:
2.2.3. Барий вступает во взаимодействие с сероводородной кислотой при температуре выше 350 с образованием сульфида бария и водорода:
Ba + H2S = BaS + H2
2.3. Барий вступает в реакцию с газом аммиаком при 600 — 650º С. В результате данной реакции образуется нитрид бария и гидрид бария:
если аммиак будет жидким, то в результате реакции в присутствии катализатора платины образуется амид бария и водород:
2.4. Барий взаимодействует с оксидами :
Барий реагирует с углекислым газом при комнатной температуре с образованием карбоната бария и углерода:
2Ba + 3CO2 = 2BaCO3 + C
Источник
Реакция бария с водой
Реакция взаимодействия бария с водой.
Уравнение реакции взаимодействия бария с водой:
Реакция бария с водой протекает при обычных условиях.
В результате реакции бария с водой образуются гидроксид бария и водород .
Примечание: © Фото https://www.pexels.com, https://pixabay.com

Мировая экономика
Справочники
Востребованные технологии
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (106 485)
- Экономика Второй индустриализации России (102 475)
- Программа искусственного интеллекта ЭЛИС (27 492)
- Метан, получение, свойства, химические реакции (23 735)
- Этилен (этен), получение, свойства, химические реакции (22 821)
- Природный газ, свойства, химический состав, добыча и применение (21 169)
- Крахмал, свойства, получение и применение (20 575)
- Целлюлоза, свойства, получение и применение (19 426)
- Пропилен (пропен), получение, свойства, химические реакции (19 106)
- Прямоугольный треугольник, свойства, признаки и формулы (18 729)
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник
Ba + H2O = ? уравнение реакции
Здесь есть кто-нибудь, кто хорошо разбирается в химии? Мне нужна помощь: взаимодействует ли барий с водой (Ba + H2O = ?) и, что при этом получается. Укажите основные физические и химические свойства полученного соединения. Заранее, большое спасибо!
В результате взаимодействия бария с водой (Ba + H2O = ?) происходит образование гидроксида бария и выделение газа водорода. Молекулярное уравнение реакции имеет вид:
Данная реакция относится к окислительно-восстановительным, поскольку химические элементы барий и водород изменяют свои степени окисления. Схемы электронного баланса выглядят следующим образом:
Гидроксид бария (едкий барит) представляет собой кристаллы белого цвета, которые плавятся без разложения, но при дальнейшем нагревании разлагаются. Хорошо растворяется в воде, образует сильнощелочной раствор. Проявляет основные свойства, реагирует с кислотами. Вступает в реакции обмена.
Помимо вышеуказанной реакции гидроксид бария получают путем растворения оксида бария в воде (1) или при горячей воды на сульфид бария (2):
Источник
Гидрид бария: способы получения и химические свойства
Гидрид бария BaH2 — неорганическое бинарное соединение щелочноземельного металла бария и водорода. Белый, плавится без разложения в атмосфере H2, при дальнейшем нагревании разлагается. Сильный восстановитель.
Относительная молекулярная масса Mr = 42,09 относительная плотность для тв. и ж. состояния d = 1,9; tпл ≈ 1000º C.
Способ получения
1. Гидрид бария получают реакцией взаимодействия бария и водорода при 150 — 300º C:
Химические свойства
1. Гидрид бария реагирует с простыми веществами :
1.1. При взаимодействии с кислородом при температуре 150 — 200º C гидрид бария образует оксид бария и воду:
1.2. При температуре 400 — 450º C г идрид бария взаимодействует с азотом , образуя нитрид бария и водород:
2. Гидрид бария взаимодействует со сложными веществами :
2.1. При взаимодействии с водой гидрид бария образует гидроксид бария и газ водород:
2.2. Гидрид бария вступает в реакцию с кислотами :
2.2.1. С разбавленной хлороводородной кислотой гидрид бария реагирует с образованием хлорида бария и газа водорода:
2.3. Гидрид бария вступает во взаимодействие с солями :
2.3.1. В результате реакции между гидридом бария и хлоратом калия при 350 — 400º С образуется хлорид калия, оксид бария и вода:
3BaH2 + 2KClO3 = 2KCl + 3BaO + 3H2O
3. Гидрид бария разлагается при температуре выше 675º C, с образованием бария и водорода:
Источник
2.2.2. Химические свойства металлов IIA группы.
IIA группа содержит только металлы – Be (бериллий), Mg (магний), Ca (кальций), Sr (стронций), Ba (барий) и Ra (радий). Химические свойства первого представителя этой группы — бериллия — наиболее сильно отличаются от химических свойств остальных элементов данной группы. Его химические свойства во многом даже более схожи с алюминием, чем с остальными металлами IIA группы (так называемое «диагональное сходство»). Магний же по химическим свойствами тоже заметно отличается от Ca, Sr, Ba и Ra, но все же имеет с ними намного больше сходных химических свойств, чем с бериллием. В связи со значительным сходством химических свойств кальция, стронция, бария и радия их объединяют в одно семейство, называемое щелочноземельными металлами.
Все элементы IIA группы относятся к s-элементам, т.е. содержат все свои валентные электроны на s-подуровне. Таким образом, электронная конфигурация внешнего электронного слоя всех химических элементов данной группы имеет вид ns 2 , где n – номер периода, в котором находится элемент.
Вследствие особенностей электронного строения металлов IIA группы, данные элементы, помимо нуля, способны иметь только одну единственную степень окисления, равную +2. Простые вещества, образованные элементами IIA группы, при участии в любых химических реакциях способны только окисляться, т.е. отдавать электроны:
Ме 0 – 2e — → Ме +2
Кальций, стронций, барий и радий обладают крайне высокой химической активностью. Простые вещества, образованные ими, являются очень сильными восстановителями. Также сильным восстановителем является магний. Восстановительная активность металлов подчиняется общим закономерностям периодического закона Д.И. Менделеева и увеличивается вниз по подгруппе.
Взаимодействие с простыми веществами
с кислородом
Без нагревания бериллий и магний не реагируют ни с кислородом воздуха, ни с чистым кислородом ввиду того, что покрыты тонкими защитными пленками, состоящими соответственно из оксидов BeO и MgO. Их хранение не требует каких-либо особых способов защиты от воздуха и влаги, в отличие от щелочноземельных металлов, которые хранят под слоем инертной по отношению к ним жидкости, чаще всего керосина.
Be, Mg, Ca, Sr при горении в кислороде образуют оксиды состава MeO, а Ba – смесь оксида бария (BaO) и пероксида бария (BaO2):
Следует отметить, что при горении щелочноземельных металлов и магния на воздухе побочно протекает также реакция этих металлов с азотом воздуха, в результате которой, помимо соединений металлов с кислородом, образуются также нитриды c общей формулой Me3N2.
с галогенами
Бериллий реагирует с галогенами только при высоких температурах, а остальные металлы IIA группы — уже при комнатной температуре:
с неметаллами IV–VI групп
Все металлы IIA группы реагируют при нагревании со всеми неметаллами IV–VI групп, но в зависимости от положения металла в группе, а также активности неметаллов требуется различная степень нагрева. Поскольку бериллий является среди всех металлов IIA группы наиболее химически инертным, при проведении его реакций с неметаллами требуется существенно большая температура.
Следует отметить, что при реакции металлов с углеродом могут образовываться карбиды разной природы. Различают карбиды, относящиеся к метанидам и условно считающимися производными метана, в котором все атомы водорода замещены на металл. Они так же, как и метан, содержат углерод в степени окисления -4, и при их гидролизе или взаимодействии с кислотами-неокислителями одним из продуктов является метан. Также существует другой тип карбидов – ацетилениды, которые содержат ион C2 2- , фактически являющийся фрагментом молекулы ацетилена. Карбиды типа ацетиленидов при гидролизе или взаимодействии с кислотами-неокислителями образуют ацетилен как один из продуктов реакции. То, какой тип карбида – метанид или ацетиленид — получится при взаимодействии того или иного металла с углеродом, зависит от размера катиона металла. С ионами металлов, обладающих малым значением радиуса, образуются, как правило, метаниды, с ионами более крупного размера – ацетилениды. В случае металлов второй группы метанид получается при взаимодействии бериллия с углеродом:
Остальные металлы II А группы образуют с углеродом ацетилениды:
С кремнием металлы IIA группы образуют силициды — соединения вида Me2Si, с азотом – нитриды (Me3N2), фосфором – фосфиды (Me3P2):
с водородом
Все щелочноземельные металлы реагируют при нагревании с водородом. Для того чтобы магний прореагировал с водородом, одного нагрева, как в случае со щелочноземельными металлами, недостаточно, требуется, помимо высокой температуры, также и повышенное давление водорода. Бериллий не реагирует с водородом ни при каких условиях.
Взаимодействие со сложными веществами
с водой
Все щелочноземельные металлы активно реагируют с водой с образованием щелочей (растворимых гидроксидов металлов) и водорода. Магний реагирует с водой лишь при кипячении вследствие того, что при нагревании в воде растворяется защитная оксидная пленка MgO. В случае бериллия защитная оксидная пленка очень стойкая: с ним вода не реагирует ни при кипячении, ни даже при температуре красного каления:
c кислотами-неокислителями
Все металлы главной подгруппы II группы реагируют с кислотами-неокислителями, поскольку находятся в ряду активности левее водорода. При этом образуются соль соответствующей кислоты и водород. Примеры реакций:
c кислотами-окислителями
− разбавленной азотной кислотой
С разбавленной азотной кислотой реагируют все металлы IIA группы. При этом продуктами восстановления вместо водорода (как в случае кислот-неокислителей) являются оксиды азота, преимущественно оксид азота (I) (N2O), а в случае сильно разбавленной азотной кислоты – нитрат аммония (NH4NO3):
− концентрированной азотной кислотой
Концентрированная азотная кислота при обычной (или низкой) температуре пассивирует бериллий, т.е. в реакцию с ним не вступает. При кипячении реакция возможна и протекает преимущественно в соответствии с уравнением:
Магний и щелочноземельные металлы реагируют с концентрированной азотной кислотой с образованием большого спектра различных продуктов восстановления азота.
− концентрированной серной кислотой
Бериллий пассивируется концентрированной серной кислотой, т.е. не реагирует с ней в обычных условиях, однако реакция протекает при кипячении и приводит к образованию сульфата бериллия, диоксида серы и воды:
Барий также пассивируется концентрированной серной кислотой вследствие образования нерастворимого сульфата бария, но реагирует с ней при нагревании, сульфат бария растворяется при нагревании в концентрированной серной кислоте благодаря его превращению в гидросульфат бария.
Остальные металлы главной IIA группы реагируют с концентрированной серной кислотой при любых условиях, в том числе на холоду. Восстановление серы происходит преимущественно до сероводорода:
с щелочами
Магний и щелочноземельные металлы со щелочами не взаимодействуют, а бериллий легко реагирует как растворами щелочей, так и с безводными щелочами при сплавлении. При этом при осуществлении реакции в водном растворе в реакции участвует также и вода, а продуктами являются тетрагидроксобериллаты щелочных или щелочноземельных металлов и газообразный водород:
При осуществлении реакции с твердой щелочью при сплавлении образуются бериллаты щелочных или щелочноземельных металлов и водород
с оксидами
Щелочноземельные металлы, а также магний могут восстанавливать менее активные металлы и некоторые неметаллы из их оксидов при нагревании, например:
Метод восстановления металлов из их оксидов магнием называют магниетермией.
Источник