- Галогены
- Химические свойства фтора
- Фтор в воде опасен, так как создает 3 проблемы
- Фтор в воде наносит вред вашему здоровью
- Что такое фтор?
- Фтор в воде
- Почему мы пьем фтор в первую очередь?
- Опасности фтора в воде
- Удаление фтора из воды
- Обеспечение безопасности детей
- Факторы фтора: ОСТАНОВИТЕ Вред своего здоровья
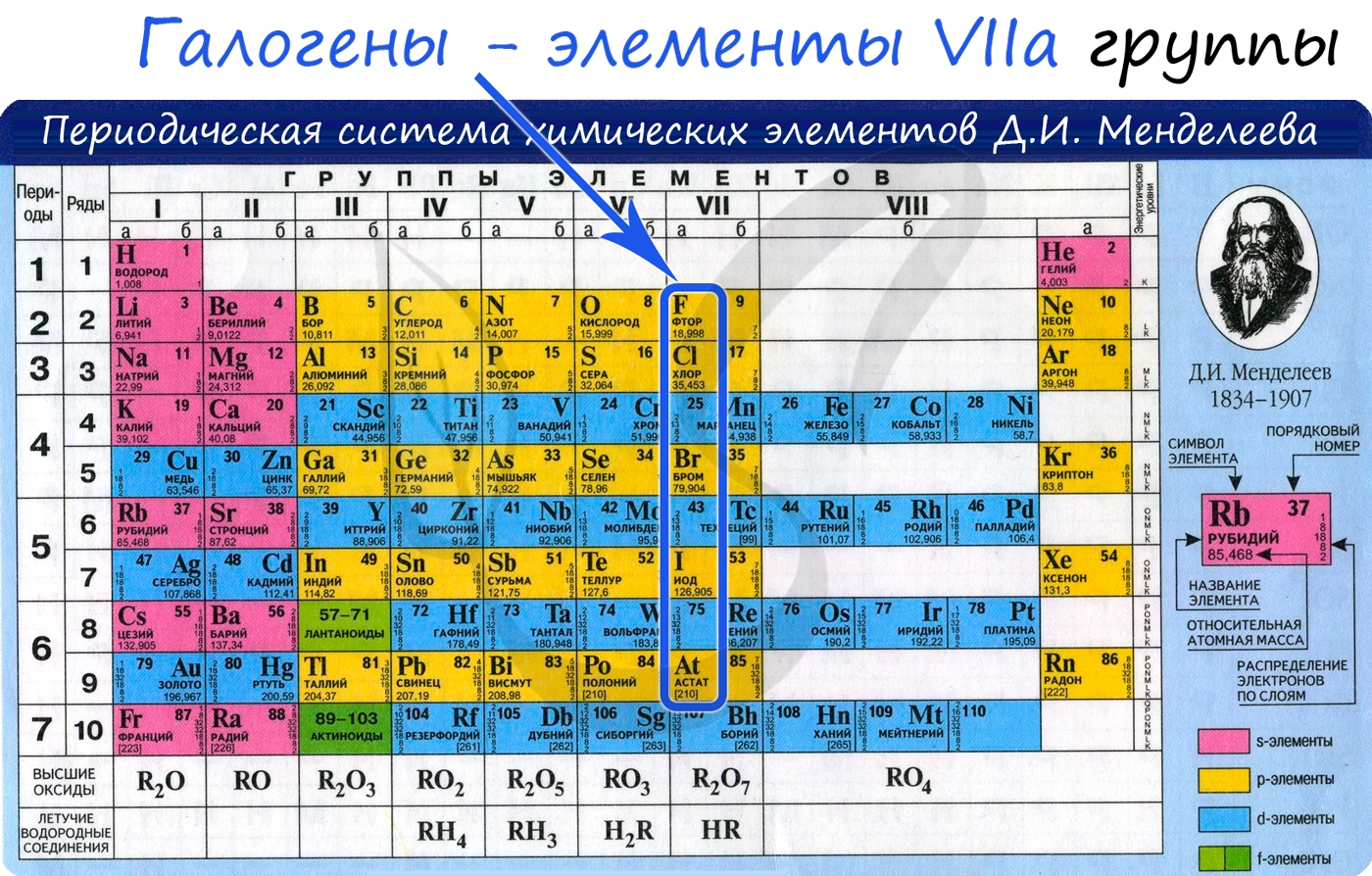
Галогены
Галогены (греч. hals — соль + genes — рождающий) — химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.
Общая характеристика элементов VIIa группы
От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 5 :
- F — 2s 2 2p 5
- Cl — 3s 2 3p 5
- Br — 4s 2 4p 5
- I — 5s 2 5p 5
- At — 6s 2 6p 5
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов в возбужденном состоянии.
Природные соединения
- NaCl — галит (каменная соль)
- CaF2 — флюорит, плавиковый шпат
- NaCl*KCl — сильвинит
- 3Ca3(PO4)2*CaF2 — фторапатит
- MgCl2*6H2O — бишофит
- KCl*MgCl2*6H2O — карналлит
Простые вещества — F2, Cl2, Br2, I2
Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают электролизом водного раствора хлорида натрия.
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте — HF — был впервые получен фтор.
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.
В лабораторных условиях галогены могут быть получены следующими реакциями.
- Реакции с металлами
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере фтора самовоспламеняются.
Реакции с неметаллами
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.
F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность 😉
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром — F — )
Br2 + I2 → IBr3 (бром более электроотрицателен, чем йод — Br — )
Реакции с водой
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
Хлор реагирует с водой обратимо, образуя хлорную воду — смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.
Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами — только при нагревании.
Реакции с щелочами
Cl2 + NaOH → NaCl + NaClO + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Галогеноводороды
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF — фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl — хлороводород (газ), соляная кислота (жидкость)
- HBr — бромоводород, бромоводородная кислота
- HI — йодоводород, йодоводородная кислота
- HAt — астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI — газы, хорошо растворимые в воде.
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
HF — является слабой кислотой, HCl, HBr, HI — сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
KOH + HCl → KCl + H2O (реакция нейтрализации)
Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.
В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с плавиковой кислотой.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Химические свойства фтора
Большая энергия связей между атомом фтора и атомами других элементов является следствием большой электроотрицательности фтора и маленьким размером его атома. Благодаря малой энергии связи молекула фтора легко диссоциирует на атомы и энергия активации реакций со фтором обычно не велика, поэтому процессы с участием фтора протекают очень быстро.
Для фтора характерно:
1. Отсутствие положительных степеней окисления в соединениях с другими элементами.
2. Чрезвычайно низкая энергия активации реакций.
3. Большое выделение энергии при переходе молекулы фтора в анионы F – .
4. Стремление максимально использовать валентные электроны партнеров. Именно в соединениях со фтором реализуются высшие степени окисления многих элементов: BiF5, SF6, IF7, OsF7, CuF3 и др.
Итак, фтор – сильнейший окислитель. По образному выражению академика А. Е. Ферсмана его можно назвать “всесъедающим”.
Щелочные металлы, свинец, железо и большинство порошков других металлов загораются в атмосфере фтора при комнатной температуре. На некоторые металлы (алюминий, железо, никель, медь, цинк, марганец, магний) фтор на холоде не действует из-за образования поверхностной пленки фторидов, защищающей металл от дальнейшего взаимодействия. Поэтому сплавы этих металлов или никеля используют для хранения фтора. Однако при нагревании фтор реагирует со всеми металлами, в т.ч. с золотом и платиной.
Со многими неметаллами (водород, йод, бром, сера, фосфор, мышьяк, сурьма, углерод, кремний, бор) фтор взаимодействует на холоде; реакции протекают со взрывом или с образованием пламени.
С серой, фосфором и сурьмой фтор взаимодействует даже при температуре жидкого воздуха (-190 °C):
С водородом фтор взаимодействует уже при температуре -252 °C
Криптон взаимодействует с фтором под действием электрического разряда, а ксенон горит в атмосфере фтора ярким пламенем.
С кислородом фтор реагирует при низких тепературах в электрических разрядах с образованием эндотермических фторидов кислорода. O2 + F2 = O2F2, -190 °C, электрич. разряд.
При нагревании с фтором реагирует хлор с образованием ClF и ClF3. Бром и йод при взаимодействии с фтором образуют следующие соединения: BrF, BrF3, BrF5, IF, IF3, IF5, IF7.
При нагревании фтор вступает в реакцию и с азотом:
Непосредственно фтор не реагирует только с углеродом (в виде алмаза), гелием, неоном и аргоном.
В реакциях с фтором в роли восстановителей выступают такие вещества как азотная и серная кислоты:
Под действием фтора разлагается вода:
0 °C: H2O(тв) + F2 = HF + HOF (фтороксигенат водорода)
В атмосфере фтора горят такие стойкие вещества, как стекло (в виде ваты), асбест, кварц:
Катализатором этой реакции является вода. С совершенно сухим кварцем или стеклом фтор не взаимодействует.
Источник
Фтор в воде опасен, так как создает 3 проблемы
Фтор в воде наносит вред вашему здоровью
Вы абсолютно не можете пропустить то, о чем мы собираемся поделиться фтор в воде!
У вас есть пятна и пятна на зубах
Когда-либо иметь проблемы со сном ночью
Есть несколько лишних фунтов вокруг вашей середины
Причиной может быть вода из TAP…
Читайте дальше, чтобы узнать, как фтор в воде наносит вред вашему здоровью и зубам, и что вы можете сделать сегодня, чтобы обезопасить себя.
Что такое фтор?
Фтор является минералом в ваших зубах и костях. Это найдено естественно в:
Он также синтезируется и добавляется в питьевую воду, зубную пасту, жидкость для полоскания рта и другие химические продукты.
Когда речь идет о вашем здоровье, фтор в основном используется для «улучшения» здоровья зубов, поскольку считается, что он укрепляет эмаль зубов.
Тем не менее, страшная правда в том, что большая часть водоснабжения в США все еще фторируется. Кроме того, вы получаете дополнительное воздействие зубной пасты и других стоматологических продуктов, а это означает, что вы, скорее всего, перегружены Фторидом!
Почему это важно? Потому что это становится Сильно токсичен для вашего тела!
Давайте подробнее рассмотрим, что вам нужно знать о фтористом растворе в воде и о том, как он потенциально наносит вред вашему здоровью.
Фтор в воде
Фтор был добавлен в воду вскоре после Второй мировой войны в попытке улучшить Стоматологическая помощьОднако фторирование продолжается и по сей день.
Как и в случае с большинством новых идей в области здравоохранения, было много волнений и внимание было сосредоточено только на преимуществах фтора. Риски регулярного потребления этого получают мало внимания.
В настоящее время существует множество информации и исследований, которые показывают опасные побочные эффекты использования фторида, одним из которых является его негативное влияние на ваше общее состояние здоровья и благополучия.
Одним из главных вредных эффектов фтора является то, что он препятствует нормальной работе вашей шишковидной железы. Он расположен в центре вашего мозга и отвечает за выработку мелатонина, который регулирует ваш цикл сна.
Когда фтор ослабляет вашу шишковидную железу, это может привести к множеству проблем, таких как:
- Раннее старение
- Проблемы со сном
- Увеличение веса.
Есть очень мало исследований, которые показывают какую-либо значительную пользу от питьевой воды, содержащей фтор. Это удивительно, учитывая потенциальные риски потребления слишком много фтора из-за подачи фторированной воды. Основной риск — отравление фтором.
Некоторые исследования даже показали, что в городах, которые не добавляли фтор в свою питьевую воду, было меньше полостей по сравнению с городами, которые это делали. Всемирная организация здравоохранения обнаружила, что, хотя только 3% западноевропейских стран фторируют свою воду, у них такая же частота зубных полостей, что и у областей, в которых их нет.
Это и многие другие исследования с аналогичными результатами должны заставить вас задуматься…
Почему мы пьем фтор в первую очередь?
Мы должны напомнить себе, что сам фтор является токсичным веществом, Так почему же мы преднамеренно подвергаем себя воздействию этих токсинов через нашу систему водоснабжения?
Опасности фтора в воде
Пятна, пятна, пятнышки, вмятины и повреждения зубов.
Флюороз зубов показатели росли в течение многих лет и теперь достигли новаторских уровней. Информация, полученная в результате опроса Центры по контролю и профилактике заболеваний показал, что:
- 41% американских подростков имеют некоторую форму флюороза.
- Это увеличение 400% по сравнению с 60 лет назад.
- Стоматологические кабинеты продолжают настаивать на лечении фтором, не информируя родителей о потенциальных рисках должным образом
- Стоматологи не в состоянии должным образом объяснить, как измерять и контролировать количество фтора, потребляемого их ребенком.
Фтор, фтор ВЕЗДЕ!
Итак, что вы можете сделать, чтобы защитить себя и свою семью? Далее, давайте более подробно рассмотрим шаги, которые вы можете предпринять СЕГОДНЯ, чтобы уменьшить воздействие фтора.
Удаление фтора из воды
Если у вас есть фторид в воде (будь то дома или на работе), и ваши попытки подать прошение в город о прекращении фторирования воды не увенчались успехом, вы можете предпринять шаги, чтобы удалить его. Вот несколько вариантов на выбор:
- Найти другой источник: Вы можете получить питьевую воду из альтернативного источника. Хорошим началом будет поиск воды, обработанной обратным осмосом или дистиллированной. Лучше всего выбрать щелочную или дистиллированную воду и ИЗБЕГАТЬ водопроводной воды. Быстрый поиск услуг доставки воды в вашем регионе предоставит варианты.
- Фильтруйте свою собственную воду: Вы также можете фильтровать свою воду, чтобы удалить из нее добавленный фтор. От домашних систем фильтрации до кувшинов для фильтрации воды — рынок полон продуктов, которые помогут вам получить более чистую питьевую воду. Опять же, быстрый поиск устройств для фильтрации воды предоставит вам решение.
Несмотря на то, что крайне важно иметь фильтрованную питьевую воду для себя, есть еще более особые соображения, когда у вас есть маленькие дети.
Обеспечение безопасности детей
Использование воды без содержания фтора особенно важно для нас в детских смесях и детском питании, когда это возможно.
При использовании водопроводной воды дети, находящиеся на искусственном вскармливании, подвергаются более высокому риску. Несмотря на то, что риск может быть небольшим, если в воде есть фтор, использование фильтрованной воды в детских смесях — простой способ защитите своего ребенка от флюороза зубов.
Одно исследование показало, что кормление детей смесью подвергает их воздействию фтора в 200 раз больше, чем детей, находящихся на грудном вскармливании. Педиатр д-р Иоланда Уайт сообщила следующее:
«Я диагностирую флюороз зубов в среднем 5 раз в день, но фтор влияет не только на зубы. Это может потенциально повлиять на мозг и нервную систему, почки, кости и другие ткани у маленьких детей во время их критических стадий развития органов ».
Теперь, когда у вас есть более чистая и безопасная питьевая вода, следующий шаг в защите вашего здоровья и зубов от чрезмерного воздействия фтора на использование более здоровых стоматологических продуктов.
Факторы фтора: ОСТАНОВИТЕ Вред своего здоровья
Если вы все еще немного скептически относитесь к тому, нужно ли вам избегать фторида, вот 3 тревожных факта о фториде:
- Многие развитые страны НЕ фторируют свою воду: Потребление воды с фтором в США выше, чем во всем мире, вместе взятом!
- Фтор является единственным лекарственным средством, добавляемым в общественную воду: Поскольку его добавляют в воду для предотвращения кариеса (болезни), Управление по санитарному надзору за качеством пищевых продуктов и медикаментов считает его лекарством.
- Фтор НЕ является необходимым питательным веществом: Нужно ли говорить больше?
Источник