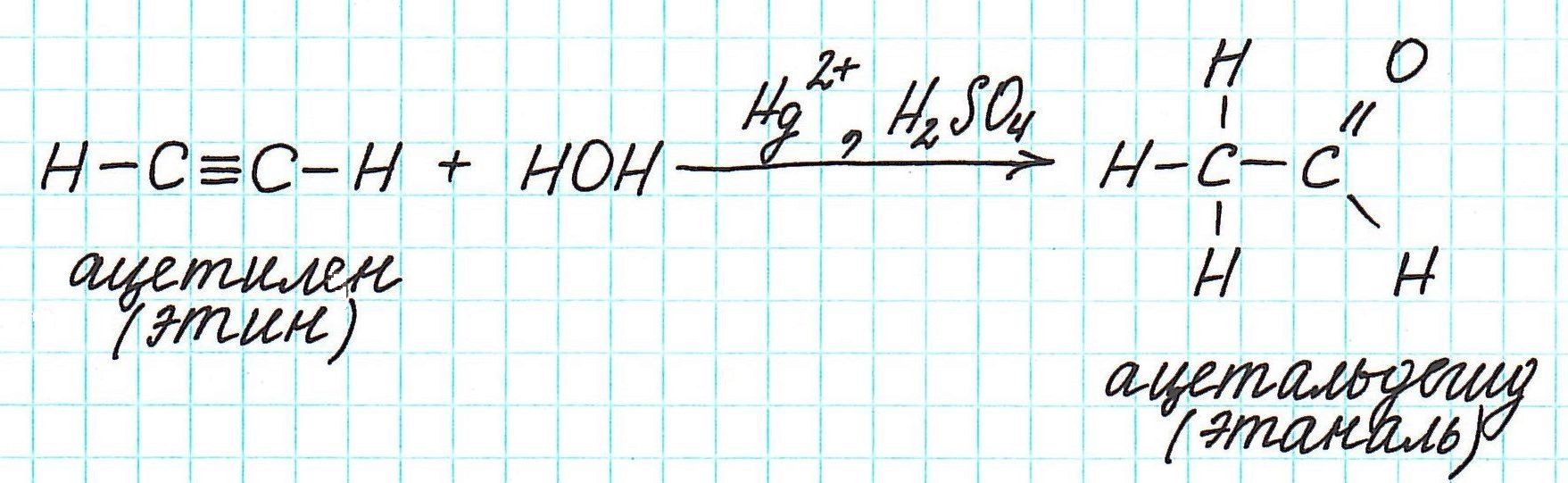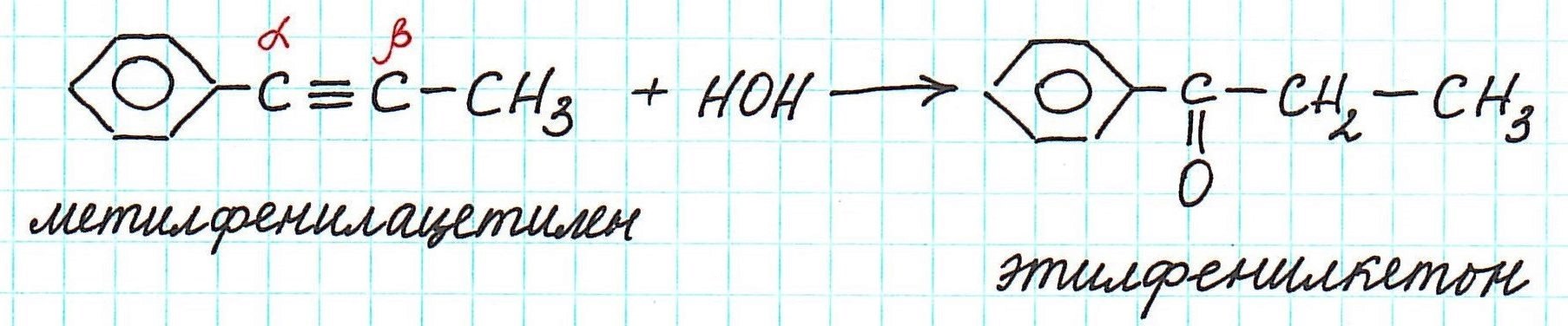- Реакция кучерова это взаимодействие с водой
- РЕАКЦИЯ КУЧЕРОВА
- Механизм реакции Кучерова для ацетилена
- Механизм реакции Кучерова для гомологов ацетилена
- Алкины
- Чем знаменит Кучеров? Реакция гидратации алкинов
- Краткая характеристика алкинов
- Химические свойства
- Механизм
- Галогенирование и гидрогалогенирование
- Заключение
Реакция кучерова это взаимодействие с водой
Реакция Кучерова (гидратация алкинов) – гидратация ацетилена с образованием ацетальдегида и гомологов ацетилена с образованием кетонов в присутствии солей ртути в качестве катализатора.
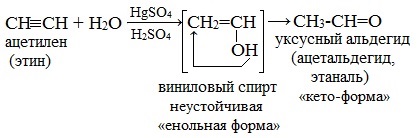
Реакция гидратации ацетилена (присоединение воды) была открыта в 1881 г. русским ученым М.Г. Кучеровым, который пытался получить непредельный спирт (виниловый), а затем его полимеризовать. Вместо ожидаемого спирта Кучеров выделил легкокипящую жидкость с характерным запахом – уксусный альдегид.
Реакция идет в присутствии солей ртути (обычно HgSO4) в серной кислоте и идет через образование неустойчивого непредельного спирта (енола), который изомеризуется в уксусный альдегид (в случае ацетилена):
На первой стадии образуются енолы (соединения, в молекулах которых гидроксогруппы соединены с атомом углерода при двойной связи).
Т.к. образующийся на промежуточном этапе виниловый спирт неустойчив, то происходит перегруппировка в термодинамически белее стабильную изомерную структуру – уксусный альдегид. Эта перегруппировка получила название перегруппировка Эльтекова-Эрленмейера.
Реакция имеет большое практическое значение, т. к. уксусный альдегид применяется в технике для получения уксусной кислоты и этилового спирта.
При гидратации гомологов ацетилена образуются кетоны, т.к. присоединение воды по тройной связи происходит в соответствии с правилом Марковникова, и группа -ОН оказывается не у концевого, а у центрального углеродного атома:
Источник
РЕАКЦИЯ КУЧЕРОВА
Реакция Кучерова для ацетилена (1881 г) стала основой промышленного получения уксусного альдегида как исходного сырья в синтезе многих органических соединений.
Кучеров Михаил Григорьевич (1850 – 1911) – российский химик-органик, внесший значительный вклад в развитие органического синтеза.
Взаимодействие ацетилена с водой (гидратация) приводит к образованию уксусного альдегида (ацетальдегида):
Обязательным условием протекания реакции является присутствие в качестве катализатора раствора (5%) соли ртути (II) в сернокислой (10%) среде. Катализаторами могут быть также соли Au + , Cu + , Ag + и Ru 3+ . Однако доказана лучшая эффективность солей Hg 2+ (чаще HgSO4).
Механизм реакции Кучерова для ацетилена
Несмотря на кажущуюся простоту процесса, механизм его до сих пор не совсем ясен.
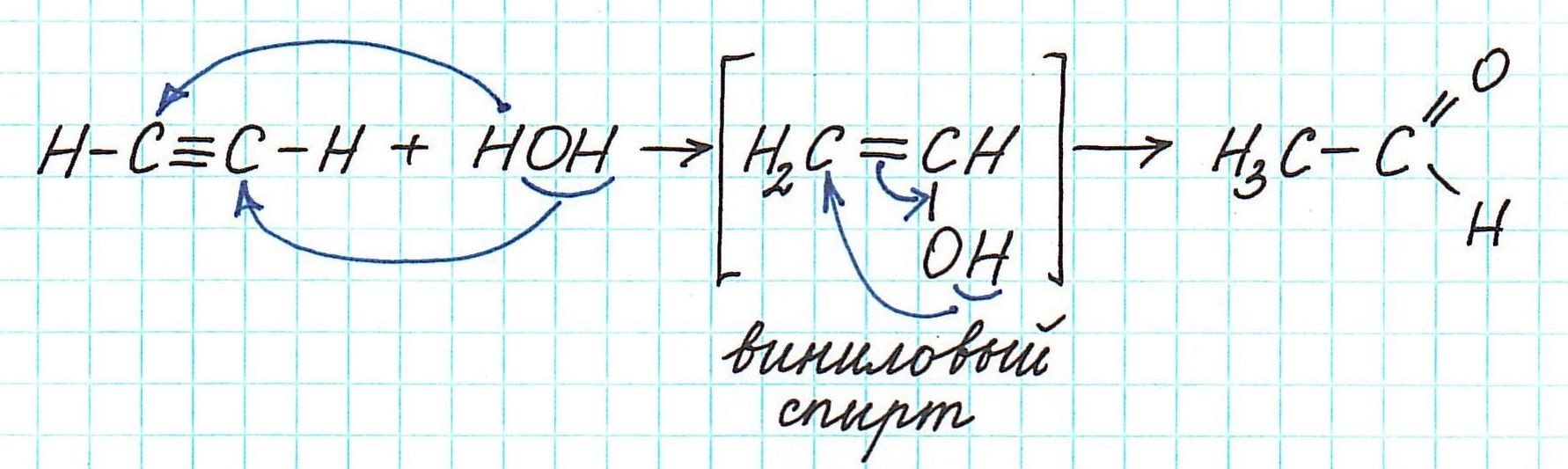
Однако достоверно известно, что одной из промежуточных стадий является образование неустойчивых непредельных спиртов (енолей). Их молекулы содержат гидроксильную группу –ОН у атома углерода с двойной связью.
Например, реакция Кучерова для ацетилена проходит следующим образом:
Механизм реакции Кучерова для гомологов ацетилена
При гидратации гомологов ацетилена образуются не альдегиды, а кетоны . Причем присоединение воды происходит по правилу Марковникова:
Алкины ряда R ̶ C≡CH при гидратации всегда образуют метилкетоны: R ̶ C(O) ̶ CH3. Реакция получения ацетона (диметилкетона) как раз является таким примером.
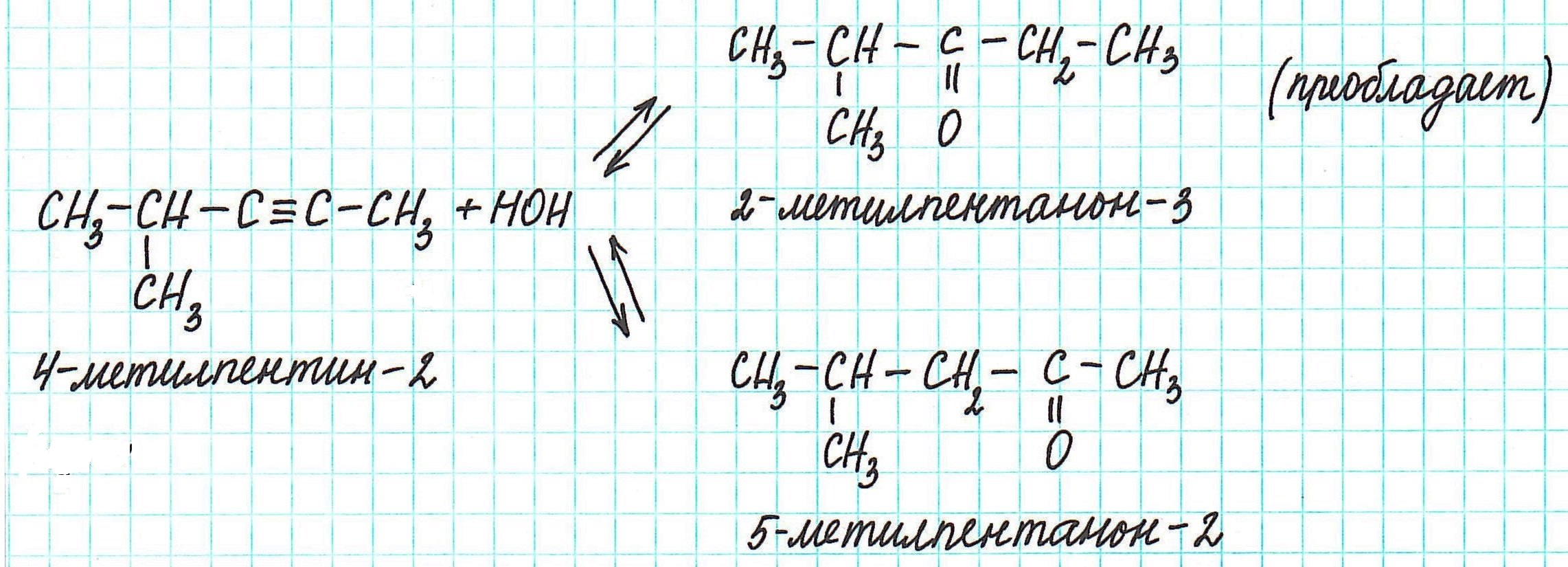
Алкины ряда R1 ̶ C≡C ̶ R2 при гидратации в зависимости от строения R1 и R2 могут давать смесь кетонов с явным преобладанием одного из них:
Как определить, какой кетон будет преобладать?
Молекула 4-метилпентина-2 содержит третичный атом углерода. Ближний к нему атом углерода с тройной связью находится в α-положении к нему, следующий – в β-положении. Образование карбонильной группы, характерной для кетонов, происходит в основном у углерода в α-положении.
Еще пример:
Итак, реакция Кучерова для ацетилена приводит к образованию ацетальдегида; реакция Кучерова для гомологов ацетилена приводит к образованию кетонов.
Источник
Алкины
Алкины — непредельные (ненасыщенные) углеводороды, имеющие в молекуле одну тройную связь С≡С. Каждая такая связь содержит одну сигма-связь (σ-связь) и две пи-связи (π-связи).
Алкины также называют ацетиленовыми углеводородами. Первый член гомологического ряда — этин — CH≡CH (ацетилен). Общая формула их гомологического ряда — CnH2n-2.
Номенклатура и изомерия алкинов
Названия алкинов формируются путем добавления суффикса «ин» к названию алкана с соответствующим числом: этин, пропин, бутин и т.д.
При составлении названия алкина важно учесть, что главная цепь атомов углерода должна обязательно содержать тройную связь. Нумерация атомов углерода в ней начинается с того края, к которому ближе тройная связь. В конце названия указывают атом углерода у которых начинается тройная связь.
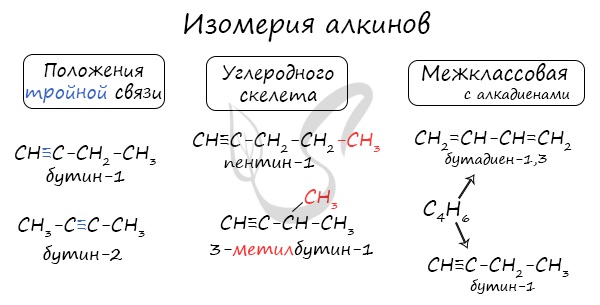
Для алкинов характерна изомерия углеродного скелета, положения тройной связи, межклассовая изомерия с алкадиенами.
Пространственная геометрическая изомерия для них невозможна, ввиду того, что каждый атом углерода, прилежащий к тройной связи, соединен только с одним единственным заместителем.
Некоторые данные, касающиеся алкинов, надо выучить:
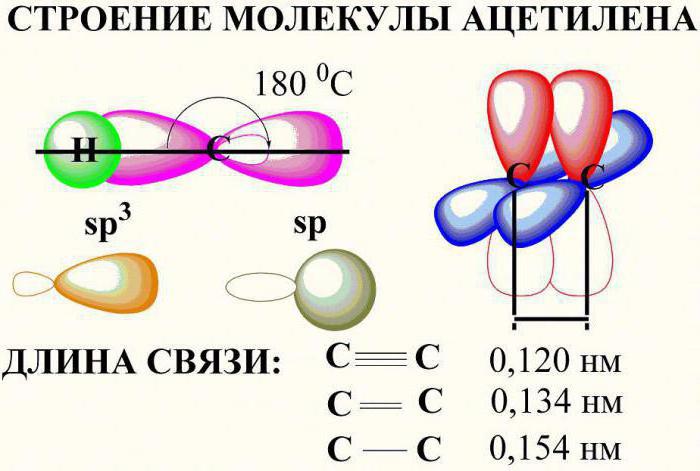
- В молекулах алкинов присутствуют тройные связи, длина которых составляет 0,121 нм
- Тип гибридизации атомов углерода — sp
- Валентный угол (между химическими связями) составляет 180°
Получение алкинов
Ацетилен получают несколькими способами:
- Пиролиз метана
При нагревании метана до 1200-1500 °C происходит димеризация молекул метана, в ходе чего отщепляется водород.
Осуществляется напрямую, из простых веществ. Протекает на вольтовой (электрической) дуге, в атмосфере водорода.
2C + H2 → (t, вольтова дуга) CH≡CH
Разложение карбида кальция
В результате разложения карбида кальция образуется ацетилен и гидроксид кальция II.
Получение гомологов ацетилена возможно в реакциях дегидрогалогенирования дигалогеналканов, в которых атомы галогена расположены у одного атома углерода или у двух соседних атомов.
Химические свойства алкинов
Алкины — ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны.
Водород присоединяется к атомам углерода, образующим тройную связь. Пи-связи (π-связи) рвутся, остается единичная сигма-связь (σ-связь).
CH≡C-CH3 + H2 → (t, Ni) CH2=CH-CH3 (в реакции участвует 1 моль водорода)
CH≡CH + 2H2 → (t, Ni) CH3-CH3 (в реакции участвует 2 моль водорода)
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу.
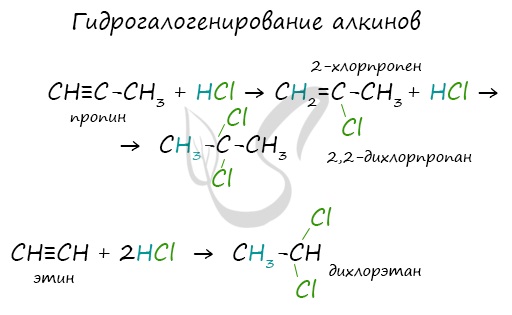
Алкины вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена — к наименее гидрированному атому углерода.
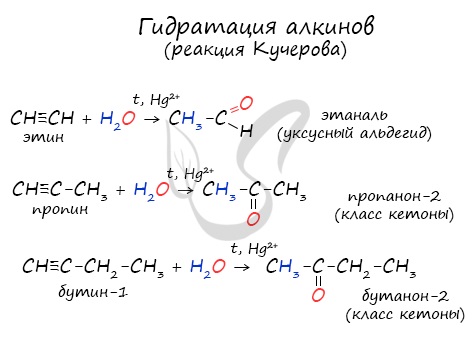
Реакцией Кучерова называют гидратацию ацетиленовых соединений с образованием карбонильных соединений. Открыта русским химиком М.Г. Кучеровым в 1881 году. Катализатор — соли ртути Hg 2+ .
Только в реакции с ацетиленом образуется уксусный альдегид. Во всех остальных реакциях (с гомологами ацетилена) образуются кетоны.
При горении алкины, как и все органические соединения, сгорают с образование углекислого газа и воды — полное окисление.
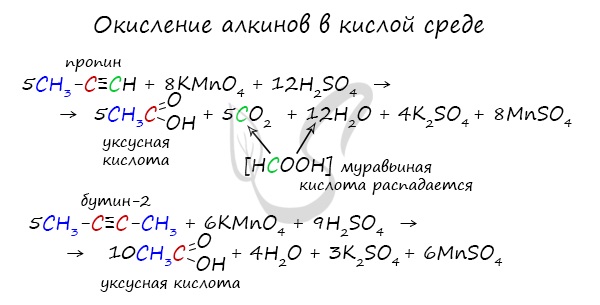
Сильные окислители (особенно в подкисленной среде) способны разрывать молекулы алкинов в самом слабом месте — в месте тройной связи.
Так, при окислении пропина, образуется уксусная кислота и муравьиная кислота, окисляющаяся до угольной кислоты, которая распадается на углекислый газ и воду.
Данная реакция протекает при пропускании ацетилена над активированным углем при t = 400°C. В результате образуется ароматический углеводород — бензол.
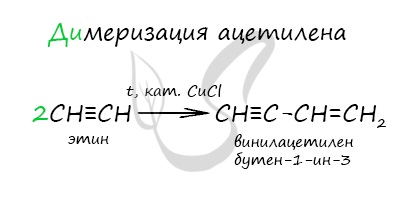
Димеризация ацетилена происходит при наличии катализатора — солей меди I. В результате реакции две молекулы ацетилена соединяются, образуя винилацетилен.
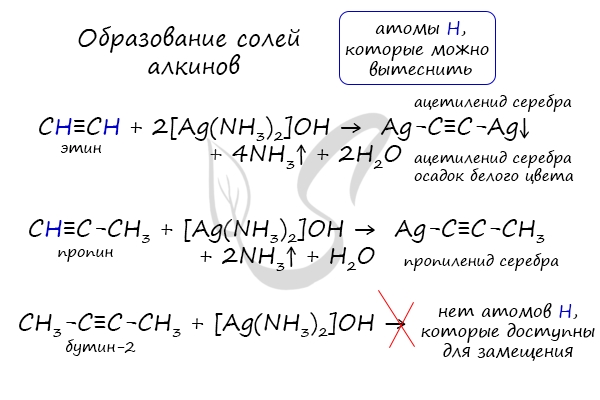
В случае если тройная связь прилежит к краевому атому углерода, то имеющийся у данного атома водород может быть замещен атомом металла. Если тройная связь спрятана внутри молекулы, то образование солей невозможно.
Реакция аммиачного раствора серебра и ацетилена — качественная реакция, в ходе которой выпадает осадок ацетиленида серебра.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Чем знаменит Кучеров? Реакция гидратации алкинов
Михаил Кучеров, реакция которого стала основой получения карбонильных соединений из углеводородов ряда алкинов, является русским ученым, внесшим вклад в развитие органической химии. Рассмотрим особенности самого химического процесса, а также основные условия протекания данного взаимодействия.
Краткая характеристика алкинов
Уравнение реакции Кучерова связано с химическими свойствами веществ, которые имеют в своей молекуле тройную связь. Представители данного класса органических веществ имеют общую формулу CnH2n-2. Углеродные атомы при кратной связи находятся в sp-гибридном состоянии, угол составляет 180 градусов.
По физическим свойства алкины схожи с алкенами и алканами. Первые представители этого гомологического ряда являются газообразными веществами, малорастворимыми в воде. Алкины растворяются в органических неполярных растворителях.
Для получения представителей данного класса используют реакцию взаимодействия дигалогенпроизводных алканов со спиртовым раствором щелочи.
Так как ацетилен является востребованным сырьем в современной химической промышленности, его получают путем высокотемпературного крекинга метана. В лабораторных условиях этин образуется при взаимодействии карбида кальция с водой. Реакция протекает при обычных условиях.
Химические свойства
Что представляет собой реакция Кучерова? Формула ацетилена С2Н2. Газ вступает в реакцию с водой по следующей схеме:
В качестве продукта реакции выступает альдегид – этаналь. Какой используется катализатор в реакции Кучерова? В качестве вещества, способствующего ускорению химического процесса, выступает соль двухвалентной ртути.
Какую роль внес в изучение свойств непредельных углеводородов А. М. Кучеров? Реакция гидратации, рассмотренная ученым, протекает по механизму электрофильного присоединения. В отличие от алкенов, которые имеют двойную связь, процесс происходит медленнее. Причина в особенностях строение алкинов. Тройная связь предполагает более компактное расположение p-электронной плотности, чем в этиленовых углеводородах, поэтому реакционная способность у всех представителей ряда ацетилена существенно снижена.
Механизм
Мы уже отметили, что катализатор в реакции Кучерова – соли двухвалентной ртути. Данный процесс является двухстадийным, рассмотрим каждый этап по отдельности. Сначала при взаимодействии алкина с водой образуется непредельный одноатомный спирт, это отмечал и Кучеров. Реакция продолжается, и ее продуктом является карбонильное соединение.
Только для ацетилена, являющегося первым представителем ряда, характерно образование альдегида. Для остальных алкинов данный процесс характеризуется образованием кетонов. Какой еще катализатор брал для данного процесса Кучеров? Реакция проводилась при разных условиях, но оптимальным вариантом оказались именно соли ртути (сульфат и хлорид).
Открыта данная реакция была в конце девятнадцатого века, своим названием она обязана ученому, который впервые осуществил подобное превращение. Например, при каталитической гидратации пропина образуется ацетон (пропаналь).
Галогенирование и гидрогалогенирование
Помимо гидратации, ацетиленовые углеводороды также вступают в реакцию присоединения с представителями седьмой группы главной подгруппы (галогенами). Механизм протекания данного процесса аналогичен алкенам, но реакция осуществляется в две стадии.
Ацетилен и его гомологи обесцвечивают бромную и йодную воду, проявляя типичные для ненасыщенных СхНу свойства.
Взаимодействие с галогеноводородом осуществляется в два этапа. Сначала происходит разрушение одной двойной связи, в итоге образуется непредельное галогенозамещенное соединение. На второй стадии присоединение происходит по правилу Марковникова.
Заключение
Реакция гидратации, механизм которой сумел объяснить русский ученый Кучеров, стала основой для промышленного производства карбонильных соединений.
Ацетон, образуемый при взаимодействии пропина с водой, является отличным растворителем, поэтому востребован в разных отраслях современной промышленности.
Этаналь используют для производства уксусной кислоты, производства синтетических тканей и полимерных материалов.
Источник