- Нитроглицерин
- Содержание
- Получение
- Физико-химические свойства
- Применение
- В фармакологии
- Во взрывотехнике
- В литературе и кино
- Нитроглицерин — Nitroglycerin
- СОДЕРЖАНИЕ
- История
- Темпы производства в военное время
- Нестабильность и десенсибилизация
- Детонация
- Производство
- Использование как взрывчатого вещества и метательного заряда
- Медицинское использование
- Промышленное воздействие
Нитроглицерин
| Нитроглицерин | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Нитроглицерин |
| Химическая формула | CHONO2(CH2ONO2)2 |
| Физические свойства | |
| Молярная масса | 227.0865 г/моль |
| Плотность | 1.595 г/см³ |
| Термические свойства | |
| Температура плавления | 13 °C |
| Классификация | |
| SMILES | C(C(CO[N+](=O)O |
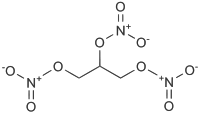
Нитроглицерин (глицеринтринитрат, тринитроглицерин, тринитрин, НГЦ) — сложный эфир глицерина и азотной кислоты. Исторически сложившееся название «нитроглицерин» с точки зрения современной номенклатуры является несколько некорректным, поскольку нитроглицерин является нитроэфиром, а не «классическим» нитросоединением. Широко известен благодаря своим взрывчатым (и в некоторой степени лекарственным) свойствам. Химическая формула O2NOCH2CH(ONO2)CH2ONO2. Впервые синтезирован итальянским химиком Асканьо Собреро в 1847 году, первоначально был назван «пироглицерин» (итал. pyroglycerina ).
Согласно номенклатуре IUPAC именуется 1,2,3-тринитроксипропан.
Содержание
Получение
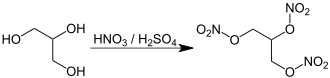
В лаборатории получают этерификацией глицерина смесью концентрированной азотной и серной кислот. Кислоты и глицерин должны быть очищены от примесей. Для этерификации предварительно при постоянном перемешивании и охлаждении смешивают кислоты, изготавливая таким образом нитрующую смесь, и добавляют по каплям глицерин при постоянном охлаждении колбы льдом и контроле температуры.
Описание реакции: 2H2SO4 + HNO3 ↔ H2SO4 · H2O + NO2 HSO4 Реакция равновесна с сильным смещением равновесия влево.
Затем реакционную смесь кислот и глицерина выдерживают непродолжительное время, при охлаждении льдом. Жидкость расслаивается на два слоя. Нитроглицерин легче нитрующей смеси и всплывает в виде мутного слоя.
Нитроглицерин отделяют от нитрующей смеси, и промывают содовым раствором до полной нейтрализации кислот. В промышленности получают непрерывным нитрованием глицерина нитрующей смесью в специальных инжекторах. В связи с возможной опасностью взрыва, НГЦ не хранят, а сразу перерабатывают в бездымный порох или взрывчатые вещества. Подробное описание лабораторного получения нитроглицерина, техника безопасности при работе с ним и занимательные эксперименты приведены в статье Нитроглицерин (Химия и Химики № 6 2011) На настоящий момент это наиболее подробная и достоверная информация о нитроглицерине в сети.
Физико-химические свойства
Сложный эфир глицерина и азотной кислоты. Прозрачная вязкая нелетучая жидкость (как масло), склонная к переохлаждению. Смешивается с органическими растворителями, почти нерастворим в воде [1] (0.13 % при 20 °C, 0,2 % при 50 °C, 0,35 % при 80 °C, по другим данным [источник не указан 1317 дней] 1,8 % при 20 °C и 2,5 % при 50 °C). При нагревании с водой до 80 °C гидролизуется. Быстро разлагается щёлочами.
Токсичен, всасывается через кожу, вызывает головную боль. Очень чувствителен к удару, трению, высоким температурам, резкому нагреву и т. п. Чувствительность к удару для груза 2 кг — 4 см (гремучая ртуть — 2 см, тротил — 100 см). Весьма опасен в обращении. При осторожном поджигании в малых количествах неустойчиво горит синим пламенем. Температура кристаллизации 13,5 °C (стабильная модификация, лабильная кристаллизуется при 2,8 °C). Кристаллизуется со значительным увеличением чувствительности к трению. При нагревании до 50 °C начинает медленно разлагаться и становится ещё более взрывоопасным. Температура вспышки около 200 °C. Теплота взрыва 6,535 МДж/кг. Температура взрыва 4110 °C. Несмотря на высокую чувствительность, восприимчивость к детонации довольно низка — для полного взрыва необходим капсюль-детонатор № 8. Скорость детонации 7650 м/с. 8000-8200 м/c — в стальной трубе диаметром 35 мм, инициирован с помощью детонатора № 8. В обычных условиях жидкий НГЦ часто детонирует в низкоскоростном режиме 1100—2000 м/с. Плотность 1,595 г/см³, в твёрдом виде — 1,735 г/см³. Твёрдый нитроглицерин менее чувствителен к удару, но более к трению, поэтому очень опасен. Объем продуктов взрыва 715 л/кг. Фугасность и бризантность сильно зависят от способа инициирования, при использовании слабого детонатора мощность сравнительно невелика. Фугасность в песке — 390 мл, в воде — 590 мл (кристаллического несколько выше), работоспособность (фугасность) в свинцовой бомбе 550 см³. Применяется как компонент некоторых жидких ВВ, динамитов и главным образом бездымных порохов (пластификатор — нитроцеллюлоза). Кроме того, в малых концентрациях применяется в медицине.
Применение
Я пью его в мельчайших дозах,
На сахар капаю раствор,
А он способен бросить в воздух
Любую из ближайших гор.
Он, растворенный в желатине
И превращенный в динамит,
В далекой золотой долине,
Взрывая скалы, загремит.
И содрогнулся шнур бикфордов,
Сработал капсюля запал,
И он разламывает твердый,
Несокрушимый минерал.
Сердечной боли он – причина,
И он один лекарство мне –
Так разъяснила медицина
В холодной горной стороне.
В фармакологии
Нитроглицерин относится к категории веществ, называемых вазодилататорами — средствам, понижающим кровяное давление, расслабляет гладкую мускулатуру кровеносных сосудов, бронхов, желчных и мочевых путей, желудочно-кишечного тракта. Основное применение имеет при стенокардии, главным образом для купирования острых приступов спазмов коронарных сосудов. Для предупреждения приступов он мало пригоден из-за кратковременности действия. Иногда применяется при эмболии центральной артерии сетчатки, а также функциональных холицистопатиях.
Применяется в виде таблеток по 0,5 мг для помещения под язык; а также в 1 % спиртовом растворе.
Во взрывотехнике
Нитроглицерин широко применялся во взрывотехнике. В чистом виде он очень неустойчив и опасен. После открытия Собреро нитроглицерина, в 1853 г. русский химик Зинин предложил использовать его в технических целях. Спустя 10 лет инженер Петрушевский первым начал производить его в больших количествах, под его руководством нитроглицерин был применён в горном деле в 1867 г. Альфред Нобель в 1863 г. изобрёл инжектор-смеситель для производства нитроглицерина и капсюль-детонатор, а в 1867 г. — динамит, получаемый смешением нитроглицерина с кизельгуром (диатомитом, инфузорной землёй).
В литературе и кино
Герои приключенческого романа «Таинственный остров» (1874) Жюль Верна использует нитроглицерин для подрыва гранитной скалы. Автор подробно описывает процесс получения нитроглицерина из природных веществ, обнаруженных на острове (хотя Жюль Верн намеренно опустил один из важных этапов синтеза). Писатель характеризует это вещество следующим образом [3] :
Действительно, это был нитроглицерин — ужасное вещество, обладающее в десять раз большей взрывчатой силой, чем порох, и причинившее уже так много несчастий. Правда, с тех пор как нитроглицерин научились превращать в динамит, смешивая его с каким-нибудь пористым веществом — например, глиной или сахаром, способным удержать опасную жидкость, им можно пользоваться с меньшим риском. Но в то время, когда колонисты действовали на острове Линкольна, динамит ещё не был известен.
Основная часть сюжета фильма «Плата за страх» (1953) заключается в процессе перевозки нитроглицерина на грузовиках.
В романе Чака Паланика «Бойцовский клуб» (1996) и одноимённом фильме (1999) главный герой получает нитроглицерин путём плавления мыла и добавления глицерина в азотную кислоту.
Возьмите одну часть 98%-ной дымящей азотной кислоты, и смешайте с тремя частями концентрированной серной кислоты. Делать это надо на ледяной бане. Затем добавляйте глицерин по капле из глазной пипетки. Вы получили нитроглицерин.
В фильме «Вертикальный предел» (2000) есть эпизод с самопроизвольной детонацией жидкого нитроглицерина от прямого воздействия солнечных лучей.
В сериале Побег сезон 2 серия 9 в ботаническом саду находят ящик с ампулами нитроглицерина, который спрятал Майкл Скофилд.
В фильме «Легенда Зорро» (2005) главный злодей демонстрирует нитроглицерин заказчикам, также финальная сцена фильма происходит в поезде, перевозящем нитроглицерин.
В многосерийном фильме «Террористка Иванова» Полина Иванова хочет отомстить следователю за смерть мужа, взорвав отделение милиции при помощи нитроглицерина.
В фильме Серджио Леоне «За пригоршню динамита» один из главных персонажей — ирландский террорист (исполняемый Кобурном) обвешан динамитными шашками и бутылями нитроглицерина. В начале фильма он демонстрирует взрывчатые свойства последнего, капая каплю на камень.
Источник
Нитроглицерин — Nitroglycerin
- 55-63-0
Y
- ЧЕБИ: 28787
Y
- ChEMBL730
Y
- 4354
Y
- DB00727
Y
- D00515
Y
- G59M7S0WS3
Y
- Тетрагональные в C1, C2 и C3
- Тригональные плоские в N7, N8 и N9
- Тетраэдр в C1, C2 и C3
- Двугранный в N7, N8 и N9




 Y проверить ( что есть ?)
Y проверить ( что есть ?)  Y
Y  N
NНитроглицерин ( НГ ), также известная как нитроглицерин , trinitroglycerin ( ПНП ), нитро , глицерил тринитрат ( GTN ), или 1,2,3-trinitroxypropane , представляет собой плотная, бесцветная маслянистая, взрывчатая жидкость обычно получают путь нитрования глицерина с белым дымящая азотная кислота в условиях, подходящих для образования эфира азотной кислоты . Химически это вещество представляет собой органическое нитратное соединение, а не нитросоединение , но традиционное название сохраняется. Изобретенный в 1847 году Асканио Собреро , нитроглицерин с тех пор используется в качестве активного ингредиента при производстве взрывчатых веществ , а именно динамита , и поэтому он используется в строительстве , сносе и горнодобывающей промышленности. С 1880-х годов он использовался военными в качестве активного ингредиента и желатинизатора для нитроцеллюлозы в некоторых твердых ракетах, таких как кордит и баллистит . Он является основным компонентом бездымных порохов двойного действия, используемых в перезарядных устройствах . Сотни комбинаций пороха в сочетании с нитроцеллюлозой используются в перезарядных устройствах для винтовок, пистолетов и дробовиков.
Нитроглицерин уже более 130 лет используется в медицине как мощное сосудорасширяющее средство (расширение сосудистой системы) для лечения сердечных заболеваний, таких как стенокардия и хроническая сердечная недостаточность . Хотя ранее было известно, что эти положительные эффекты связаны с превращением нитроглицерина в оксид азота , сильнодействующее венодилататор, ферментом для этого преобразования было обнаружено митохондриальная альдегиддегидрогеназа ( ALDH2 ) только в 2002 году. Нитроглицерин доступен в сублингвальных таблетках и спреях. , мази и пластыри.
СОДЕРЖАНИЕ
История
Нитроглицерин был первым произведенным взрывчатым веществом, которое было сильнее черного пороха . Он был впервые синтезирован итальянским химиком Асканио Собреро в 1847 году под руководством Теофиля-Жюля Пелуза в Туринском университете . Собреро первоначально назвал свое открытие пироглицерином и решительно предостерегал от его использования в качестве взрывчатого вещества.
Позднее нитроглицерин был принят в качестве коммерчески полезного взрывчатого вещества Альфредом Нобелем , который экспериментировал с более безопасными способами обращения с опасным соединением после того, как его младший брат Эмиль Оскар Нобель и несколько заводских рабочих были убиты в результате взрыва на оружейном заводе Nobels в 1864 году в 1864 году. Хеленеборг , Швеция.
Год спустя Нобель основал Alfred Nobel and Company в Германии и построил изолированную фабрику на холмах Крюммель в Гестхахте недалеко от Гамбурга . Этот бизнес экспортировал жидкую комбинацию нитроглицерина и пороха под названием «Blasting Oil», но это было крайне нестабильно и с трудом справлялось, о чем свидетельствуют многочисленные катастрофы. Дважды разрушались здания фабрики Крюммеля.
В апреле 1866 года три ящика нитроглицерина были отправлены в Калифорнию для Центрально-Тихоокеанской железной дороги , которая планировала провести эксперименты с ним в качестве взрывчатого вещества, чтобы ускорить строительство туннеля на высшем уровне длиной 1659 футов (506 м) через горы Сьерра-Невада. . Один из ящиков взорвался, в результате чего был разрушен офис компании Wells Fargo в Сан-Франциско и погибли 15 человек. Это привело к полному запрету на провоз жидкого нитроглицерина в Калифорнии. Таким образом, производство нитроглицерина на месте потребовалось для бурения и взрывных работ в твердых породах, необходимых для завершения строительства Первой трансконтинентальной железной дороги в Северной Америке .
В июне 1869 года два однотонных фургона, груженных нитроглицерином, в то время известный как Powder-Oil, взорвались на дороге в деревне Cwm-y-glo в Северном Уэльсе . Взрыв привел к гибели шести человек, множеству ранений и значительному ущербу для села. От двух лошадей не было обнаружено никаких следов. Правительство Великобритании было настолько встревожено нанесенным ущербом и тем, что могло произойти в городе (эти две тонны были частью более крупного груза, доставляемого из Германии через Ливерпуль), что вскоре они приняли Закон о нитроглицерине 1869 года. Жидкий нитроглицерин был Также широко запрещен в других странах, и эти юридические ограничения привели к тому, что Альфред Нобель и его компания разработали динамит в 1867 году. Это было сделано путем смешивания нитроглицерина с диатомитовой землей (« Кизельгур » на немецком языке), найденной на холмах Крюммеля . Подобные смеси, такие как «дуалин» (1867 г.), «литофрактер» (1869 г.) и « гелигнит » (1875 г.), были образованы путем смешивания нитроглицерина с другими инертными абсорбентами, и многие комбинации были опробованы другими компаниями в попытках обойти. Защищенные патенты Нобеля на динамит.
Смеси динамита, содержащие нитроцеллюлозу , повышающую вязкость смеси, широко известны как «желатины».
После открытия, что амилнитрит помогает облегчить боль в груди, врач Уильям Мюррелл экспериментировал с использованием нитроглицерина для облегчения стенокардии и снижения артериального давления . Он начал лечить своих пациентов небольшими разбавленными дозами нитроглицерина в 1878 году, и это лечение вскоре стало широко использоваться после того, как Мюррелл опубликовал свои результаты в журнале The Lancet в 1879 году. За несколько месяцев до своей смерти в 1896 году Альфреду Нобелю прописали нитроглицерин. из-за этого сердечного заболевания, написав другу: «Разве это не ирония судьбы, что мне прописали нитроглицерин для внутреннего приема! Они называют это Тринитрин, чтобы не напугать химика и общественность». Медицинское учреждение также использовало название «тринитрат глицерина» по той же причине.
Темпы производства в военное время
Нитроглицерин в больших количествах производился во время Первой и Второй мировых войн для использования в качестве топлива в военных целях и в военно-инженерных работах. Во время Первой мировой войны завод HM Factory в Гретне , крупнейший завод по производству топлива в Великобритании, производил около 800 тонн кордита RDB в неделю. Это количество требовало не менее 336 тонн нитроглицерина в неделю (при условии отсутствия производственных потерь). У Королевского военно-морского флота была собственная фабрика на Кордитовой фабрике Королевского флота, Холтон-Хит , в Дорсете , Англия. Большой завод по производству кордита был также построен в Канаде во время Первой мировой войны. Завод по производству кордита Canadian Explosives Limited в Нобеле, Онтарио , был спроектирован для производства 1 500 000 фунтов (680 т) кордита в месяц, что требует около 286 тонн нитроглицерина в месяц.
Нестабильность и десенсибилизация
В неразбавленном виде нитроглицерин представляет собой контактное взрывчатое вещество , которое при физическом шоке может взорваться. Если он не был должным образом очищен во время производства, он может со временем разложиться до еще более нестабильных форм. Это делает нитроглицерин очень опасным для транспортировки или использования. В неразбавленном виде это одно из самых мощных взрывчатых веществ в мире, сопоставимое с недавно разработанными гексогеном и тэном .
В начале своей истории было обнаружено, что жидкий нитроглицерин « десенсибилизируется » путем его замораживания при температуре ниже 45–55 ° F (от 7 до 13 ° C) в зависимости от его чистоты. Его чувствительность к ударам в замороженном состоянии несколько непредсказуема: «Он более нечувствителен к ударам молниеносной крышки или винтовочного ядра в таком состоянии, но, с другой стороны, он более склонен к взрыву при разрыве, раздавливании, утрамбовывании. так далее.» Замороженный нитроглицерин намного менее энергетичен, чем жидкий, поэтому перед употреблением его необходимо разморозить. Размораживание может вызвать повышенную чувствительность, особенно если присутствуют загрязнения или слишком быстрое нагревание. Динитрат этиленгликоля или другой полинитрат может быть добавлен, чтобы снизить плавление и тем самым избежать необходимости оттаивания замороженного взрывчатого вещества.
Химически «десенсибилизировать» нитроглицерин можно до такой степени, что он может считаться примерно таким же «безопасным», как современные взрывчатые вещества , например, путем добавления этанола , ацетона или динитротолуола . Нитроглицерин, возможно, придется экстрагировать из десенсибилизатора, чтобы восстановить его эффективность перед использованием, например, путем добавления воды для удаления этанола, используемого в качестве десенсибилизатора.
Детонация
Нитроглицерин и любые разбавители, безусловно, могут загореться (сжечь). Взрывная сила нитроглицерина происходит от детонации : энергия от начального разложения вызывает сильную волну давления, которая взрывает окружающее топливо. Это самоподдерживающаяся ударная волна, которая распространяется через взрывоопасную среду со скоростью, в 30 раз превышающей скорость звука, как вызванное почти мгновенным давлением разложение топлива на раскаленный добела газ. При детонации нитроглицерина образуются газы, которые занимают более чем в 1200 раз исходный объем при обычной комнатной температуре и давлении. Выделяющееся тепло поднимает температуру примерно до 5000 ° C (9000 ° F). Это полностью отличается от дефлаграции , которая зависит исключительно от доступного топлива, независимо от давления или удара. Разложение приводит к гораздо более высокому отношению энергии к количеству выделяемых молей газа по сравнению с другими взрывчатыми веществами, что делает его одним из самых горячих взрывчатых веществ .
Производство
Нитроглицерин можно получить путем кислотно-катализируемого нитрования глицерина (глицерина).
В процессе промышленного производства глицерин часто реагирует со смесью концентрированной серной кислоты и концентрированной азотной кислоты примерно 1: 1 . Это может быть получено путем смешивания белой дымящей азотной кислоты — довольно дорогой чистой азотной кислоты, в которой удалены оксиды азота, в отличие от красной дымящей азотной кислоты , которая содержит оксиды азота, — и концентрированной серной кислоты . Чаще всего эту смесь получают более дешевым методом смешивания дымящей серной кислоты , также известной как олеум — серной кислоты, содержащей избыток триоксида серы, — и азеотропной азотной кислоты (состоящей примерно из 70% азотной кислоты , остальное — вода).
Серная кислота производит протонированную азотные кислоту видов, которые атакованы глицерин «с нуклеофильным кислородом атомами. Нитро группа , таким образом , добавляют в качестве сложного эфира С-О-NO 2 и вода выпускается. Это отличается от реакции электрофильного ароматического замещения, в которой ионы нитрония являются электрофилами .
Добавление глицерина приводит к экзотермической реакции (т. Е. Выделению тепла), как обычно при смешанном кислотном нитровании. Если смесь становится слишком горячей, это приводит к неуправляемой реакции, состоянию ускоренного нитрования, сопровождающемуся деструктивным окислением органических материалов горячей азотной кислотой и выделением ядовитого газообразного диоксида азота с высоким риском взрыва. Таким образом, смесь глицерина медленно добавляют в реакционный сосуд, содержащий смешанную кислоту (а не кислоту по отношению к глицерину). Нитратор охлаждают холодной водой или какой-либо другой охлаждающей смесью и на протяжении всего добавления глицерина поддерживают при температуре около 22 ° C (72 ° F), намного ниже которой этерификация происходит слишком медленно, чтобы ее можно было использовать. Емкость нитратора, часто сделанная из железа или свинца и обычно перемешиваемая сжатым воздухом , имеет в основании аварийный люк, который нависает над большим бассейном с очень холодной водой и в который может быть помещена вся реакционная смесь (называемая загрузкой). сброшены, чтобы предотвратить взрыв, процесс, называемый утоплением. Если температура заряда превышает 30 ° C (86 ° F) (фактическое значение зависит от страны) или в вентиляционном отверстии нитратора появляются коричневые пары, то он немедленно тонет.
Использование как взрывчатого вещества и метательного заряда
Основное применение нитроглицерина по тоннажу — это взрывчатые вещества, такие как динамит, и топливо.
Нитроглицерин — маслянистая жидкость, которая может взорваться при воздействии тепла, удара или пламени.
Альфред Нобель разработал использование нитроглицерина в качестве взрывчатого вещества путем смешивания нитроглицерина с инертными абсорбентами , в частности « кизельгуром » или диатомитовой землей . Он назвал этот взрывной динамит и запатентовал его в 1867 году. Он был поставлен готовым к использованию в виде палочек, индивидуально завернутых в промасленную водонепроницаемую бумагу. Динамит и аналогичные взрывчатые вещества широко использовались для задач гражданского строительства , например, при бурении автомобильных и железнодорожных туннелей , для добычи полезных ископаемых , для очистки сельскохозяйственных угодий от пней, при разработке карьеров и при демонтажных работах . Точно так же военные инженеры использовали динамит при строительных и демонтажных работах.
Нитроглицерин также использовался в качестве ингредиента военного топлива для использования в огнестрельном оружии .
Нитроглицерин использовался в сочетании с гидроразрывом пласта , процессом, используемым для извлечения нефти и газа из сланцевых пластов. Этот метод включает вытеснение и детонацию нитроглицерина в естественных или гидравлически индуцированных системах трещин или вытеснение и детонацию нитроглицерина в гидравлически индуцированных трещинах с последующими выстрелами из ствола скважины с использованием гранулированного TNT .
Нитроглицерин имеет преимущество перед некоторыми другими взрывчатыми веществами в том, что при детонации он практически не производит видимого дыма. Следовательно, он полезен в качестве ингредиента в составе различных видов бездымного пороха .
Его чувствительность ограничила применимость нитроглицерина в качестве военной взрывчатки, а менее чувствительные взрывчатые вещества, такие как тротил , гексоген и октоген , в значительной степени заменили его в боеприпасах. Он остается важным в военной инженерии, и саперы по- прежнему используют динамит.
Затем Альфред Нобель разработал баллистит , объединив нитроглицерин и пушистый хлопок . Он запатентовал его в 1887 году. Баллистит был принят на вооружение правительствами ряда европейских стран в качестве военного топлива. Италия была первой, кто его принял. Британское правительство и правительства Содружества взяли на вооружение кордит , который был разработан сэром Фредериком Абелем и сэром Джеймсом Дьюаром из Соединенного Королевства в 1889 году. Первоначальный кордит Mk I состоял из 58% нитроглицерина, 37% хлопка и 5,0% вазелина. . И баллистит, и кордит изготавливались в виде «шнуров».
Бездымные порохи изначально были разработаны с использованием нитроцеллюлозы в качестве единственного взрывчатого ингредиента. Поэтому они были известны как одноосновное топливо. Также был разработан ряд бездымных порохов, содержащих как нитроцеллюлозу, так и нитроглицерин, известных как топливо с двойным основанием. Изначально бездымные порохи поставлялись только для использования в военных целях, но вскоре они были разработаны и для гражданского использования и были быстро приняты на вооружение в спорте. Некоторые из них известны как спортивные порошки. Тройное топливо содержит нитроцеллюлозу, нитроглицерин и нитрогуанидин , но зарезервировано в основном для боеприпасов чрезвычайно большого калибра, таких как те, которые используются в танковых пушках и военно-морской артиллерии . Взрывной желатин, также известный как гелигнит , был изобретен Нобелем в 1875 году с использованием нитроглицерина, древесной массы и нитрата натрия или калия . Это было раннее дешевое гибкое взрывное устройство.
Медицинское использование
Нитроглицерин относится к группе препаратов, называемых нитратами, в которую входят многие другие нитраты, такие как динитрат изосорбида (Isordil) и мононитрат изосорбида (Imdur, Ismo, Monoket). Все эти агенты оказывают свое действие, превращаясь в оксид азота в организме митохондриальной альдегиддегидрогеназой ( ALDH2 ), а оксид азота является мощным природным вазодилататором.
В медицине нитроглицерин используется при стенокардии , болезненном симптоме ишемической болезни сердца, вызванной недостаточным притоком крови и кислорода к сердцу, и как сильнодействующее гипотензивное средство. Нитроглицерин корректирует дисбаланс между потоком кислорода и крови к сердцу и потребностями сердца в энергии. В малых дозах нитроглицерин расширяет вены больше, чем артерии, тем самым уменьшая преднагрузку (объем крови в сердце после наполнения); это считается его основным механизмом действия. Снижая предварительную нагрузку, сердце перекачивает меньше крови, что снижает потребность в кислороде, поскольку сердцу не приходится работать так тяжело. Кроме того, меньшая преднагрузка снижает трансмуральное давление желудочков (давление, оказываемое на стенки сердца), что снижает компрессию сердечных артерий, позволяя большему количеству крови проходить через сердце. В более высоких дозах он также расширяет артерии, тем самым уменьшая постнагрузку (снижая давление, против которого должно работать сердце). Улучшенное соотношение потребности миокарда в кислороде и его поступлении приводит к следующим терапевтическим эффектам во время приступов стенокардии: уменьшение боли в груди, снижение артериального давления , учащение пульса и ортостатическая гипотензия . Пациенты, страдающие стенокардией при выполнении определенных физических нагрузок, часто могут предотвратить симптомы, приняв нитроглицерин за 5-10 минут до активности. Передозировка может вызвать метгемоглобинемию .
Нитроглицерин выпускается в виде таблеток, мази, раствора для внутривенного введения , трансдермальных пластырей или спреев, вводимых сублингвально . Некоторые формы нитроглицерина сохраняются в организме намного дольше, чем другие. Было показано, что постоянное воздействие нитратов приводит к тому, что организм перестает нормально реагировать на это лекарство. Специалисты рекомендуют снимать пластыри на ночь, позволяя организму через несколько часов восстановить свою чувствительность к нитратам. Препараты нитроглицерина короткого действия можно использовать несколько раз в день с меньшим риском развития толерантности. Впервые нитроглицерин был использован Уильямом Мюрреллом для лечения приступов стенокардии в 1878 году, и в том же году было опубликовано открытие.
Промышленное воздействие
Редкое воздействие высоких доз нитроглицерина может вызвать сильную головную боль, известную как « головная боль » или «удар головой». Эти головные боли могут быть достаточно серьезными, чтобы вывести из строя некоторых людей; однако у людей развиваются толерантность и зависимость от нитроглицерина после длительного воздействия. Хотя это случается редко, синдром отмены может быть фатальным. Симптомы отмены включают боль в груди и другие проблемы с сердцем. Эти симптомы можно облегчить при повторном контакте с нитроглицерином или другими подходящими органическими нитратами.
Для рабочих на предприятиях по производству нитроглицерина (NTG) последствия отмены иногда включают «воскресные сердечные приступы» у тех, кто регулярно подвергается воздействию нитроглицерина на рабочем месте, что приводит к развитию толерантности к венодилатирующим эффектам. В выходные рабочие теряют толерантность, и когда они снова подвергаются воздействию в понедельник, резкое расширение сосудов вызывает учащенное сердцебиение , головокружение и головную боль. Это называется «болезнью понедельника».
Люди могут подвергаться воздействию нитроглицерина на рабочем месте при вдыхании, абсорбции через кожу, проглатывании или попадании в глаза. Управление по охране труда и здоровья установило законный предел ( допустимый предел воздействия ) для воздействия нитроглицерина на рабочем месте, равный 0,2 ppm (2 мг / м 3 ) воздействия на кожу в течение 8-часового рабочего дня. Национальный институт профессиональной безопасности и здоровье установил рекомендуемый предел экспозиции 0,1 мг / м 3 воздействия на кожу в течение 8-часового рабочего дня. При уровне 75 мг / м 3 нитроглицерин немедленно опасен для жизни и здоровья .
Источник