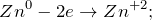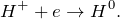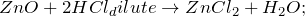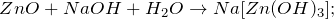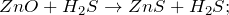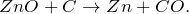- Цинк — общая характеристика элемента, химические свойства цинка и его соединений
- Форум химиков
- реакция цинка с водой
- реакция цинка с водой
- Re: реакция цинка с водой
- Re: реакция цинка с водой
- Реакция цинка с водой что происходит
- Zn + H2O = ? уравнение реакции
- Реакция цинка с водой
- Реакция взаимодействия цинка с водой.
- Уравнение реакции взаимодействия цинка с водой:
- Мировая экономика
- Справочники
- Востребованные технологии
- Поиск технологий
- О чём данный сайт?
- О Второй индустриализации
Цинк — общая характеристика элемента, химические свойства цинка и его соединений

В четвертом периоде цинк является последним d-элементом, его валентные электроны 3d 10 4s 2 . В образовании химических связей участвуют только электроны внешнего энергетического уровня, поскольку конфигурация d 10 является очень устойчивой. В соединениях для цинка характерна степень окисления +2.
Цинк – химически активный металл, обладает выраженными восстановительными свойствами, по активности уступает щелочно-земельным металлам. Проявляет амфотерные свойства.
Взаимодействие цинка с неметаллами
При сильном нагревании на воздухе сгорает ярким голубоватым пламенем с образованием оксида цинка:
2Zn + O2 → 2ZnO.
При поджигании энергично реагирует с серой:
Zn + S → ZnS.
С галогенами реагирует при обычных условиях в присутствии паров воды в качестве катализатора:
Zn + Cl2 → ZnCl2.
При действии паров фосфора на цинк образуются фосфиды:
Zn + 2P → ZnP2 или 3Zn + 2P → Zn3P2.
С водородом, азотом, бором, кремнием, углеродом цинк не взаимодействует.
Взаимодействие цинка с водой
Реагирует с парами воды при температуре красного каления с образованием оксида цинка и водорода:
Zn + H2O → ZnO + H2.
Взаимодействие цинка с кислотами
В электрохимическом ряду напряжений металлов цинк находится до водорода и вытесняет его из неокисляющих кислот:
Zn + 2HCl → ZnCl2 + H2;
Zn + H2SO4 → ZnSO4 + H2.
Взаимодействует с разбавленной азотной кислотой, образуя нитрат цинка и нитрат аммония:
4Zn + 10HNO3 → 4Zn(NO3)2 + NH4NO3 + 3H2O.
Реагирует с концентрированными серной и азотной кислотами с образованием соли цинка и продуктов восстановления кислот:
Zn + 2H2SO4 → ZnSO4 + SO2 + 2H2O;
Zn + 4HNO3 → Zn(NO3)2 + 2NO2 + 2H2O
Взаимодействие цинка со щелочами
Реагирует с растворами щелочей с образованием гидроксокомплексов:
Zn + 2NaOH + 2H2O → Na2[Zn(OH)4] + H2
при сплавлении образует цинкаты:
Zn + 2KOH → K2ZnO2 + H2.
Взаимодействие с аммиаком
С газообразным аммиаком при 550–600°С образует нитрид цинка:
3Zn + 2NH3 → Zn3N2 + 3H2;
растворяется в водном растворе аммиака, образуя гидроксид тетраамминцинка:
Zn + 4NH3 + 2H2O → [Zn(NH3)4](OH)2 + H2.
Взаимодействие цинка с оксидами и солями
Цинк вытесняет металлы, стоящие в ряду напряжения правее него, из растворов солей и оксидов:
Zn + CuSO4 → Cu + ZnSO4;
Zn + CuO → Cu + ZnO.
Оксид цинка (II) ZnO – белые кристаллы, при нагревании приобретают желтую окраску. Плотность 5,7 г/см 3 , температура возгонки 1800°С. При температуре выше 1000°С восстанавливается до металлического цинка углеродом, угарным газом и водородом:
ZnO + C → Zn + CO;
ZnO + CO → Zn + CO2;
ZnO + H2 → Zn + H2O.
С водой не взаимодействует. Проявляет амфотерные свойства, реагирует с растворами кислот и щелочей:
ZnO + 2HCl → ZnCl2 + H2O;
ZnO + 2NaOH + H2O → Na2[Zn(OH)4].
При сплавлении с оксидами металлов образует цинкаты:
ZnO + CoO → CoZnO2.
При взаимодействии с оксидами неметаллов образует соли, где является катионом:
2ZnO + SiO2 → Zn2SiO4,
ZnO + B2O3 → Zn(BO2)2.
Гидроксид цинка (II) Zn(OH)2 – бесцветное кристаллическое или аморфное вещество. Плотность 3,05 г/см 3 , при температуре выше 125°С разлагается:
Zn(OH)2 → ZnO + H2O.
Гидроксид цинка проявляет амфотерные свойства, легко растворяется в кислотах и щелочах:
Zn(OH)2 + H2SO4 → ZnSO4 + 2H2O;
Zn(OH)2 + 2NaOH → Na2[Zn(OH)4];
также легко растворяется в водном растворе аммиака с образованием гидроксида тетраамминцинка:
Zn(OH)2 + 4NH3 → [Zn(NH3)4](OH)2.
Получается в виде осадка белого цвета при взаимодействии солей цинка со щелочами:
ZnCl2 + 2NaOH → Zn(OH)2 + 2NaCl.
Источник
Форум химиков
реакция цинка с водой
реакция цинка с водой
Сообщение Achilles777 » Пн авг 14, 2006 9:47 am
Кто может подробно в деталях описать, что происходит, когда под открытым небом, т.е. под воздействием всех естественных природных факторов, вода соприкасается с цинком и по какой причине в этом месте погибают бактерии?
Re: реакция цинка с водой
Сообщение pepelac-driver » Пн авг 14, 2006 10:10 am
Achilles777 писал(а): Всем привет!
Кто может подробно в деталях описать, что происходит, когда под открытым небом, т.е. под воздействием всех естественных природных факторов, вода соприкасается с цинком и по какой причине в этом месте погибают бактерии?
Вкратце:
Z2n + O2 = 2ZnO
Zn + 2 H2O = Zn(OH)2 + H2
Zn(OH)2 + CO2 = ZnCO3 + H2O
Фокус в том, что соединения цинка достаточно ядовиты. Но при этом, данные карбонаты и гидроксиды неплохо растворимы, создавая повышенные концентрации металла, губительные для биоты.
Re: реакция цинка с водой
Сообщение Achilles777 » Пн авг 14, 2006 11:18 am
Achilles777 писал(а): Всем привет!
Кто может подробно в деталях описать, что происходит, когда под открытым небом, т.е. под воздействием всех естественных природных факторов, вода соприкасается с цинком и по какой причине в этом месте погибают бактерии?
Вкратце:
Z2n + O2 = 2ZnO
Zn + 2 H2O = Zn(OH)2 + H2
Zn(OH)2 + CO2 = ZnCO3 + H2O
Фокус в том, что соединения цинка достаточно ядовиты. Но при этом, данные карбонаты и гидроксиды неплохо растворимы, создавая повышенные концентрации металла, губительные для биоты.
Источник
Реакция цинка с водой что происходит
Цинк – химически активный металл, обладает выраженными восстановительными свойствами, по активности уступает щелочно-земельным металлам. Проявляет амфотерные свойства.
- Взаимодействие с неметаллами
При сильном нагревании на воздухе сгорает ярким голубоватым пламенем с образованием оксида цинка:
При поджигании энергично реагирует с серой:
С галогенами реагирует при обычных условиях в присутствии паров воды в качестве катализатора:
При действии паров фосфора на цинк образуются фосфиды:
С водородом, азотом, бором, кремнием, углеродом цинк не взаимодействует.
Взаимодействие с водой
Реагирует с парами воды при температуре красного каления с образованием оксида цинка и водорода:
Взаимодействие с кислотами
В электрохимическом ряду напряжений металлов цинк находится до водорода и вытесняет его из неокисляющих кислот:
Взаимодействует с разбавленной азотной кислотой, образуя нитрат цинка и нитрат аммония:
Реагирует с концентрированными серной и азотной кислотами с образованием соли цинка и продуктов восстановления кислот:
Взаимодействие со щелочами
Реагирует с растворами щелочей с образованием гидроксокомплексов:
при сплавлении образует цинкаты:
Взаимодействие с аммиаком
С газообразным аммиаком при 550–600°С образует нитрид цинка:
растворяется в водном растворе аммиака, образуя гидроксид тетраамминцинка:
Взаимодействие с оксидами и солями
Цинк вытесняет металлы, стоящие в ряду напряжения правее него, из растворов солей и оксидов:
Источник
Zn + H2O = ? уравнение реакции
Закончите уравнение реакции Zn + H2O = ? Расставьте стехиометрические коэффициенты. Запишите молекулярное уравнение реакции. Охарактеризуйте полученное соединение: приведите его основные физические и химические свойства. Каким образом его можно получить в лаборатории? А в промышленности?
В результате взаимодействия цинка с водой (Zn + H2O = ?) происходит образование оксида цинка и воды. Молекулярное уравнение реакции имеет вид:
Данная реакция относится к окислительно-восстановительным, поскольку химические элементы цинк и водород изменяют свои степени окисления. Схемы электронного баланса выглядят следующим образом:
Оксид цинка представляет собой термически устойчивые кристаллы белого цвета (иногда с желтоватым оттенком), которые при сильном прокаливании возгоняются и разлагаются, однако плавятся только под избыточным давлением кислорода. Не реагирует с водой, не восстанавливается водородом. Проявляет амфотерные свойства; реагирует с кислотами, щелочами, кислотными и основными оксидами. Восстанавливается коксом.
Основной промышленный способ получения оксида цинка – из природных минералов.
Источник
Реакция цинка с водой
Реакция взаимодействия цинка с водой.
Уравнение реакции взаимодействия цинка с водой:
Цинк и вода взаимодействуют друг с другом.
Zn + H2O → ZnO + H2 (t = 600-800 °C).
При обычных условиях цинк с водой практически не реагирует. Только раскаленный до красна цинк может вступать в реакцию с водяным паром при температуре 600-800 о С.
Реакция цинка с водой протекает при условии: при температуре 600-800 °C.
В результате реакции цинка с водой образуются оксид цинка и водород .
Однако в присутствии кислорода или во влажном воздухе цинк медленно окисляется .
Реакция цинка, воды и кислорода протекает при обычных условиях: при комнатной температуре.
В результате реакции цинка, воды и кислорода образуется гидроксид цинка .
Примечание: © Фото https://www.pexels.com, https://pixabay.com

Мировая экономика
Справочники
Востребованные технологии
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (106 485)
- Экономика Второй индустриализации России (102 475)
- Программа искусственного интеллекта ЭЛИС (27 492)
- Метан, получение, свойства, химические реакции (23 735)
- Этилен (этен), получение, свойства, химические реакции (22 821)
- Природный газ, свойства, химический состав, добыча и применение (21 169)
- Крахмал, свойства, получение и применение (20 575)
- Целлюлоза, свойства, получение и применение (19 426)
- Пропилен (пропен), получение, свойства, химические реакции (19 107)
- Прямоугольный треугольник, свойства, признаки и формулы (18 729)
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник