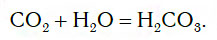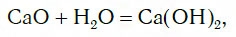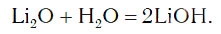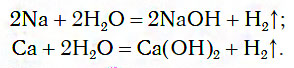- Какие металлы реагируют с водой?
- Все химические реакции, которые необходимы для успешной сдачи ОГЭ
- Правило 1.1. Взаимодействие простых веществ (металлов и неметаллов) с водой
- Правило 1.2. Взаимодействие оксидов с водой
- Активированная вода
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
- ОПТИМАЛЬНЫЙ ОВП ОРГАНИЗМА ЧЕЛОВЕКА
- ПОЛЬЗА УПОТРЕБЛЕНИЯ АКТИВИРОВАННОЙ ВОДЫ ДЛЯ ЗДОРОВЬЯ
- ВРЕДНОСТЬ АКТИВИРОВАННОЙ ВОДЫ
- СПОСОБЫ АКТИВАЦИИ ВОДЫ
- Урок 28. Химические свойства воды
- Взаимодействие с оксидами неметаллов
- Взаимодействие с оксидами металлов
- Взаимодействие с металлами
Какие металлы реагируют с водой?
Прежде всего следует запомнить, что металлы делят в целом на три группы:
1) Активные металлы: к таким металлам относятся все щелочные металлы, щелочноземельные металлы, а также магний и алюминий.
2) Металлы средней активности: к таковым относят металлы, расположенные между алюминием и водородом в ряду активности.
3) Малоактивные металлы: металлы, расположенные в ряду активности правее водорода.
В первую очередь нужно запомнить, что малоактивные металлы (т.е. те, что расположены после водорода) с водой не реагируют ни при каких условиях.
Щелочные и щелочноземельные металлы реагируют с водой при любых условиях (даже при обычной температуре и на холоде), при этом реакция сопровождается выделением водорода и образованием гидроксида металла. Например:
Магний из-за того, что покрыт защитной оксидной пленкой, реагирует с водой только при кипячении. При нагревании в воде оксидная пленка, состоящая из MgO, разрушается и находящийся под ней магний начинает реагировать с водой. При этом реакция также сопровождается выделением водорода и образованием гидроксида металла, который, однако, в случае магния нерастворим:
Алюминий так же, как и магний, покрыт защитной оксидной пленкой, однако в этом случае кипячением ее разрушить нельзя. Для ее снятия требуются либо механическая чистка (каким-либо абразивом), либо ее химическое разрушение щелочью, растворами солей ртути или солей аммония:
Металлы средней активности реагируют с водой лишь тогда, когда она находится в состоянии перегретого водяного пара. Сам металл при этом должен быть нагрет до температуры красного каления (около 600-800 о С). В отличие от активных металлов, металлы средней активности при реакции с водой вместо гидроксидов образуют оксиды металлов. Продуктом восстановления и в этом случае является водород:
Fe + H2O = FeO + H2 (в зависимости от степени нагрева)
Источник
Все химические реакции, которые необходимы для успешной сдачи ОГЭ
Правило 1.1. Взаимодействие простых веществ (металлов и неметаллов) с водой
1) Щелочные (Li-Fr) и щелочноземельные (Ca-Ra) металлы взаимодействуют с водой при комнатной температуре с образованием щелочи (растворимого основания) и выделением водорода. Например:
2) Магний также взаимодействует с водой, но при сильном нагревании и с образованием нерастворимого гидроксида:
3) Алюминий реагирует с водой, но только если убрать оксидную пленку:
4) Металлы, находящиеся в ряду активности от Zn (включительно) до Pb (включительно), взаимодействуют с парами воды (т.е. при температуре выше 100°С), при этом образуются оксиды соответствующих металлов и водород:
5) Металлы, стоящие в ряду активности правее водорода, с водой не взаимодействуют даже при нагревании.
Cu + H2O → реакция не идет.
6) Из неметаллов с водой реагируют галогены, C и Si при высоких температурах:
Правило 1.2. Взаимодействие оксидов с водой
1) Основные оксиды щелочных и щелочноземельных металлов реагируют с водой при комнатной температуре с образованием соответствующих щелочей:
2) Амфотерные оксиды не реагируют с водой и не растворяются в ней.
ZnO + H2O → реакция не идет.
3) Кислотные оксиды взаимодействуют с водой с образованием соответствующих кислот: P2O5 + 3H2O → 2H3PO4
Только в случае NO2 образуются две кислоты:
2NO2 + H2O → HNO2 + HNO3 и, как следствие, при взаимодействии с щелочами образуются две соли (нитраты и нитриты соответствующего металла):
SiO2 + H2O → реакция не идет.
Источник
Активированная вода
Активированная вода – это вода, имеющая биокаталитический заряд, а точнее избыток заряженных частиц, электронов. Такая вода имеет более активные биофизические и биологические показатели. Биологическая активность воды является одним из важных и полезных показателей для любого организма.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Основными процессами, обеспечивающими жизнедеятельность любого организма, являются окислительно-восстановительные реакции, т.е. химические реакции, связанные с передачей или присоединением электронов.
Дыхание, теплообмен, пищеварение, метаболизм — все это сопровождается множественными реакциями, в которых происходит процесс отдачи и приема электронов. В результате происходит выделение энергии, поддерживающей жизнедеятельность и восстановление клеток. Можно сказать, что реакции, протекающие в жидкой среде, зависят от активности электронов, иначе, окислительно-восстановительный потенциал (ОВП) этой среды.

Вода имеет собственный окислительно-восстановительный потенциал (ОВП), то есть вода заряженная отрицательными или положительными частицами — ионами. Чем больше количество отрицательно заряженных электронов (-), тем выше количество антиоксидантных свойств, за счёт высокого содержания в ней свободных (валентных) электронов, которые нейтрализуют свободные радикалы.
И наоборот, чем выше показатель положительно заряженных ионов (+), тем больше в такой воде находиться свободных радикалов, то есть молекул с не достающим электроном на орбите, которые отнимают электроны у здоровых клеток и тканей, окисляя каждое соединение. ОВП воды значительно отражается на работе клеток организма. При высоком (-) ОВП клетки организма регенерируют (восстанавливаются), а при высоком (+) ОВП клетки организма стареют (разрушаются).
ОПТИМАЛЬНЫЙ ОВП ОРГАНИЗМА ЧЕЛОВЕКА
Любая жидкость, в том числе и вода, может принимать как отрицательные показатели, так и положительные. ОВП воды и любой другой жидкости может принимать разные значения: как положительные, так и отрицательные.
Но внутренняя среда человека по своим биологическим показателям всегда является активной, поэтому имеет отрицательные значения, которые обычно находятся в пределах от -70мВ до -200мВ (милливольт). Если ОВП организма стремится к 0 т.е. повышается выше -70…-50мВ, то у человека возникают различные заболевания.

ОВП простой воды находиться в диапазоне выше 0 и находиться в диапазоне от +100мВ до +400мВ. Такие показатели практически у всех типов воды: водопроводная во всех странах мира, бутилированная в стеклянных и пластиковых бутылках, которая очищается в установках обратного осмоса и большинства разнообразных водоочистительных систем.
Обычная вода с показателями «+ОВП» >0 (вода с недостатком отрицательных электронов), после попадания в организм, начинает отбирать необходимые электроны у клеток и тканей, которые состоят из жидкости. Как результат – биологическая составляющая организма человека (клеточная мембрана, органоиды клетки, нуклеиновая кислота и др.) разрушается из-за окисления. В этом причина старения организма, износа органов и потери их функций, снижения иммунитета.
Негативные процессы могут быть замедлены, если в организм с питьем и пищей поступает активированная вода, обладающая свойствами внутренней среды организма, т.е. обладающая защитными восстановительными свойствами.
ПОЛЬЗА УПОТРЕБЛЕНИЯ АКТИВИРОВАННОЙ ВОДЫ ДЛЯ ЗДОРОВЬЯ
При употреблении активированной воды, где ОВП соответствует ОВП внутренней среды человека, исчезает необходимость растраты большого количества биологической энергии, требуемой для изменения активности электронов воды.
Итогом потребления является хорошая ассимиляция воды и сохранение организмом дополнительной энергии. Так же энергетические затраты происходят при метаболизме, поэтому любое увеличение энергии активирует обмен веществ, что приносит большую пользу для организма.

Активированная вода, насыщенная отрицательно заряженными ионами и электронами, активно стимулирует перенос кислорода и электронов из внешней среды к клеткам и тканям, что нормализует метаболический и окислительно-восстановительные процессы. Это способствует восстановлению электрического потенциала клеточных мембран и повышению кислородной насыщенности эритроцитов и плазмы крови. А так как кровь и лимфа имеет небольшой отрицательный заряд, который наш организм всеми силами поддерживает на определенном уровне, то прием активированной воды благотворно влияет на здоровье.
За последнее десятилетие было проведено более 400 клинических исследований японскими и американскими учеными. Исследования доказали, что активированная вода насыщенная газообразным водородом предотвращает образование свободных радикалов и прерывает цепную реакцию окисления организма.
В ряде исследований было обнаружено, что активированная вода, обогащенная молекулярным водородом, является не только мощным антиоксидантом, но и многофункциональным антиокислителем. С одной стороны, вода сама обладает антиоксидантными свойствами, а с другой стороны — значительно усиливает действие ферментных и неферментных антиоксидантов: СОД, флавоноидов,каталазы, квертецина и витамина С.

ВРЕДНОСТЬ АКТИВИРОВАННОЙ ВОДЫ
У активированной воды есть и обратная сторона. Воду с высокими отрицательными показателями ОВП (от -400мВ до -800мВ) не рекомендуется пить в больших количествах и на постоянной основе. Это связанно с большим содержанием в воде отрицательно заряженных ионов, которые могут нарушить баланс окислительно-восстановительных реакций в организме, что может привести к заболеваниям.
Сейчас рекламируют множество приборов для активации воды, которые способны сделать воду с высокими показателями ОВП более -400мВ и рН более 10, но относительно недавно стало известно о негативных последствиях потребления воды с высокими показателями. Такую воду можно потреблять только в небольшом количестве и только при сильном окислительном стрессе организма.
Природой установлено, что жидкость в живом организме имеет слабощелочную среду рН от 7,2 до 7,5 и окислительно-восстановительный потенциал в диапазоне от -70мВ до -200мВ, в связи с чем, любое сильное превышение этих показателей в отрицательную или положительную сторону, начинает нарушать баланс организма, что приводит к нагрузке на организм.
Японские ученые рекомендуют потреблять воду на постоянной основе со слабощелочными показателями и ОВП с небольшими отрицательными значениями.
СПОСОБЫ АКТИВАЦИИ ВОДЫ
Активированная вода встречается в природе в горных источниках, однако существует возможность получить активированную воду искусственным путем в домашних условиях, при помощи различных активаторов воды. Каждый способ имеет разное активирующее воздействие, поэтому в одних методах вода будет иметь очень сильную биокаталитическую активность, а другие не значительную.
Методы получения активированной воды дома:
- Влияние на воду магнитным полем. Поток воды проходит через магнитное поле, которое перпендикулярно самой струе воды.
- Сталкивание воды с электронами. Проводится при помощи электронно-лучевой трубки.
- Облучение воды ультрафиолетовым светом. В результате фотоэффекта на поверхности воды отделяются электроны.
- Минералы или микроэлементы, которые имеют собственные информационные и энергетические поля. Активируют воду только те минералы, которые при взаимодействии с водой образуют отрицательно заряженные ионы. Показатели могут быть различными в зависимости от минерала.
- Химическая реакция. Самый эффективный и естественный способ активации воды можно получить при помощи магния. Реакция магния с водой образует молекулярный водород и гидроксид магния, в результате чего высвобождаются электроны. Например водородные таблетки «Шипучий магний Drink HRW» позволяют получить сверх высокие концентрации водорода до 8 мг/л и окислительно-восстановительный потенциал до — 550 мВ.
- Кавитация воды. Воду активируют при помощи ультразвуковой обработки.
- Электролиз воды. Активация происходит путем пропускания через воду электрического тока при помощи двух электродов. На одном электроде образуется катодная вода ОВП 0. Катодная и анодная вода активно применяется в медицине и биологии.
Здесь приведены только некоторые методы активации и энергетизации воды. Существуют и другие методы повышения биологической активности воды – как природные, естественные, так и искусственные, техногенные, экспериментальные, но они более трудоемкие и сложные.
В нашем магазине Вы можете купить товары, которые могут сделать активированную, щелочную, водородную и живую воду для любых задач.
Источник
Урок 28. Химические свойства воды
В уроке 28 «Химические свойства воды» из курса «Химия для чайников» узнаем о взаимодействии воды с различными веществами.
При обычных условиях вода является достаточно активным веществом по отношению к другим веществам. Это означает, что со многими из них она вступает в химические реакции.
Взаимодействие с оксидами неметаллов
Если струю газообразного оксида углерода(IV) CO2 (углекислого газа) направить в воду, то часть его растворится в ней (рис. 109).
При этом в растворе протекает химическая реакция соединения, в результате которой образуется новое вещество — угольная кислота H2CO3:
На заметку: Собирая углекислый газ над водой, Дж. Пристли обнаружил, что часть газа растворяется в воде и придает ей приятный терпкий вкус. По сути дела, Пристли впервые получил напиток типа газированной, или содовой, воды.
Реакция соединения происходит также, если к воде прибавить твердый оксид фосфора(V) P2O5. При этом протекает химическая реакция с образованием фосфорной кислоты H3PO4 (рис. 110):
Испытаем растворы, полученные при взаимодействии CO2 и P2O5 с водой, индикатором метиловым оранжевым. Для этого прибавим по 1—2 капли раствора индикатора к полученным растворам. Цвет индикатора изменится с оранжевого на красный, что говорит о присутствии кислот в растворах. Значит, при взаимодействии CO2 и P2O5 с водой действительно образовались кислоты H2CO3 и H3PO4.
Оксиды, подобные CO2 и P2O5, которые при взаимодействии с водой образуют кислоты, относят к кислотным оксидам.
Кислотные оксиды — это оксиды, которым соответствуют кислоты.
Некоторые из кислотных оксидов и соответствующих им кислот приведены в таблице 11. Обратите внимание, что это оксиды элементов неметаллов. Как правило, оксиды неметаллов являются кислотными оксидами.
Взаимодействие с оксидами металлов
С оксидами металлов вода реагирует иначе, чем с оксидами неметаллов.
Исследуем взаимодействие оксида кальция CaO с водой. Для этого поместим в стакан с водой небольшое количество CaO и тщательно перемешаем. При этом протекает химическая реакция:
в результате которой образуется новое вещество Ca(OH)2, относящееся к классу оснований. Таким же образом реагируют с водой оксиды лития, натрия. При этом также образуются основания, например:
Подробнее с основаниями вы познакомитесь в следующем уроке. Оксиды металлов, которым соответствуют основания, называют основными оксидами.
Основные оксиды — это оксиды, которым соответствуют основания.
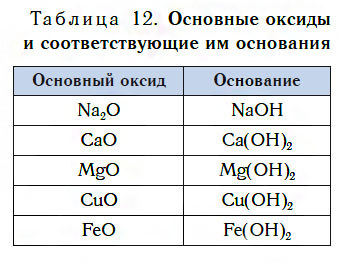
В таблице 12 приведены формулы некоторых основных оксидов и соответствующих им оснований. Заметьте, что, в отличие от кислотных оксидов, в состав основных оксидов входят атомы металлов. Большинство оксидов металлов — это основные оксиды.
Несмотря на то что каждому основному оксиду соответствует основание, не все основные оксиды взаимодействуют с водой, подобно CaO, образуя основания.
Взаимодействие с металлами
При обычных условиях активные металлы (K, Na, Ca, Ba и др.) бурно реагируют с водой:
В этих реакциях выделяется водород и образуются растворимые в воде основания.
Как химически активное вещество вода вступает в реакции со многими другими веществами, но об этом вы узнаете при дальнейшем изучении химии.
Краткие выводы урока:
- Вода — химически активное вещество. Она вступает в реакции с кислотными и основными оксидами, активными металлами.
- При взаимодействии воды с большинством кислотных оксидов образуются соответствующие кислоты.
- Некоторые основные оксиды при реакции с водой образуют растворимые основания.
- При обычных условиях вода реагирует с наиболее активными металлами. При этом образуются растворимые основания и водород.
Надеюсь урок 28 «Химические свойства воды» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Источник