- помогите сделать химию
- 1. Смесью веществ в отличие от индиви¬дуального вещества является: А. Водопроводная вода. Б. Углекислый газ. В. Медь. 2. Ряд формул, в котором все вещест¬ва — оксиды: A. ZnO, ZnCl2, H20. Б. S03, MgO, CuO. B.КОН, К20, MgO. 3. Азот проявляет наибольшую степень окисления в соединении с формулой: A. NH3. Б. N02. В. N205. 4. Общая формула основания выражена условной записью: A. М(ОН)х Б. ЭХНу. B. НхКО, где М — металл, Э—элемент, КО — кислотный остаток. 5. Число формул кислот в следующем списке: H2C03, Fe(OH)2, NaOH, H2Si03, Ba(OH)2, Cu(OH)2, CaO, S02 — равно: А.1. Б. 2. В. 3. Г. 4. Выпишите формулы кислот 6. Формула сульфата железа (II): A. FeS. Б. Fe2(S04)3. В. FeS04. 7. Установите соответствие, дайте названия веществам: Формула соединения: l.Na20. 2. MgS04. 3. NaOH. 4. НС1. 5. С02. 6. H3P04. Класс соединений: А. Оксиды. Б. Основания. В. Кислоты. Г.Соли.
- Ответы к заданиям по химии 8 класс 6 работ (Часть 3)
- Вводный контроль по химии 8 класс УМК Рудзитис Г. Е., Фельдман Ф. Г.
- Просмотр содержимого документа «Вводный контроль по химии 8 класс УМК Рудзитис Г. Е., Фельдман Ф. Г.»
- Тест для 8 класса «Чистые вещества и смеси».
- Дистанционное обучение как современный формат преподавания
- Современные педтехнологии в деятельности учителя
- Современные образовательные технологии в преподавании химии с учетом ФГОС
- Оставьте свой комментарий
- Подарочные сертификаты
помогите сделать химию
1 (2 балла). Смесью веществ в отличие от индивидуального вещества является:
A. Водопроводная вода. Б. Углекислый газ. B. Медь.
2 (2 балла). Ряд формул, в котором все вещества — оксиды:
A. ZnO, ZnCl2, H2O.
Б. SO3, MgO, CuO.
B. КОН, К2О, MgO.
3 (2 балла). Азот проявляет наибольшую степень окисления в соединении с формулой:
A. NH3. Б. NO2. B. N2O5.
4 (2 балла). Общая формула основания выражена условной записью:
A. М(ОН)хБ. ЭхНу B. НхКО,
где М — металл, Э — элемент, КО — кислотный остаток.
5 (2 балла). Общая формула основания выражена условной записью:
A. М(ОН)хБ. ЭхНу B. НхКО
6 (2 балла). Массовая доля серы в серной кислоте H2SO4 равна:
А. 2,04%. Б. 65,31%. В. 32,65%.
7 (2 балла). В 80 г воды растворили 20 г соли. Массовая доля соли в полученном растворе равна:
А. 20%. Б. 25%. В. 40%.
8 (2 балла). Формула сульфата железа (II): A.FeS. Б. Fe2(SO4)3. В. FeSO4.
9 (2 балла). Формула кислоты, в которой заряд иона кислотного остатка равен 2-:
А. НСl. Б. H2SO4. В. Н3РО4.
10 (2 балла). Щелочью является вещество с формулой:
A. Fe(OH)2. Б. КОН. В. Сu(ОН)2.
11. (6 баллов). Установите соответствие.
Формула соединения:
l. Na2O. 2.MgSO4. 3.NaOH. 4. НСl. 5. CO2. 6. H3PO4.
Класс соединений:
А. Оксиды. Б. Основания. В. Кислоты. Г. Соли.
ЧАСТЬ Б. Задания со свободным ответом
12 (4 балла). Соотнесите.
Формула соединения:
1. HNO3. 2.А12О3. 3. Са(ОН)2. 4. CaSO4. 5.СаО. 6. Н3РО4. 7.А1(ОН)3. 8. K2SO4.
Название вещества:
A. Оксид кальция. Б. Азотная кислота. B. Гидроксид алюминия. Г. Сульфат калия.
13 (6 баллов). Для гидроксидов (кислоты или основания) напишите формулы соответствующих им оксидов:
А. Н2СО3. Б. Mg(OH)2. В. А1(0Н)3.
14 (8 баллов). Составьте химические формулы соединений:
A. Оксид калия.
Б. Соляная кислота.
B. Фосфат кальция.
Г Гидроксид бария.
15. (6 баллов) Рассчитайте объем кислорода, полученного из 200л воздуха, если известно, что объемная доля кислорода в воздухе составляет 21%.
Источник
1. Смесью веществ в отличие от индиви¬дуального вещества является: А. Водопроводная вода. Б. Углекислый газ. В. Медь. 2. Ряд формул, в котором все вещест¬ва — оксиды: A. ZnO, ZnCl2, H20. Б. S03, MgO, CuO. B.КОН, К20, MgO. 3. Азот проявляет наибольшую степень окисления в соединении с формулой: A. NH3. Б. N02. В. N205. 4. Общая формула основания выражена условной записью: A. М(ОН)х Б. ЭХНу. B. НхКО, где М — металл, Э—элемент, КО — кислотный остаток. 5. Число формул кислот в следующем списке: H2C03, Fe(OH)2, NaOH, H2Si03, Ba(OH)2, Cu(OH)2, CaO, S02 — равно: А.1. Б. 2. В. 3. Г. 4. Выпишите формулы кислот 6. Формула сульфата железа (II): A. FeS. Б. Fe2(S04)3. В. FeS04. 7. Установите соответствие, дайте названия веществам: Формула соединения: l.Na20. 2. MgS04. 3. NaOH. 4. НС1. 5. С02. 6. H3P04. Класс соединений: А. Оксиды. Б. Основания. В. Кислоты. Г.Соли.
Смесью веществ является: А.Водопроводная вода
Ряд формул, в котором все оксиды Б.SO3, MgO,CuO
Азот проявляет наибольшую степень окисления с: В. N2O5
Формула основания: M(OH)
Число формул кислот: Б. 2
Формула сульфата железа(ii): Б. Fe2(SO4)3
7) A — Na2O, CO2
Б — NaOH
В — HC1, H3PO4
Г — MgSO4
Xг 10% 11,2л
Ca(OH)₂ + CO₂ = CaCO₃ + H₂O
M(Ca(OH)₂) = 74 г/моль
Vm(CO₂) = 22,4 л/моль
Y / 74 = 11,2 / 22,4 Y = ( 74 * 11,2 ) / 22,4 = 37 г — масса чистого гидроксида кальция
Х — 100%
37 — 10% Х = (37 * 100 ) / 10 = 370 г — масса всего раствора гидроксида кальция
Ответ:
1-й ряд — лишняя медь (Cu), так как все металлы главных подгрупп и лишь она побочной
2-й ряд лишнее железо (Fe). Все тяжелые металлы, кроме него
3 -й ряд — лишний хлорид свинца (PbCl2). Все кислоты и лишь одна соль
Ba +H2O= Ba(OH)2 +H2
2K + 2H2O = 2 KOH + H2
Если с галогенами. то кислоты вида НГ.
Чем ниже галоген в группе. тем сильнее кислота.
HI — самая сильная
HBr — менее сильная. но всё равно сильная
HCl — слабее первых двух. но всё равно сильная
HF — самая слабая. И вообще слабая кислота.
Есть ещё H₂S — сероводородная кислота.
Она очень слабая.
Сила кислот зависит от лёгкости отщепления протона (катиона водорода Н⁺).
Чем легче он отщепляется, тем кислота сильнее.
Источник
Ответы к заданиям по химии 8 класс 6 работ (Часть 3)
Контрольная работа № 3
Соединения химических элементов
ВАРИАНТ-1
Часть 1
А1. Смесью веществ в отличие от чистого вещества является:
1) алюминий 3) магний
2) водопроводная вода 4) углекислый газ
А2. Ряд формул, в котором все вещества – оксиды:
1) SO3, MgO, CuO 3) ZnO, ZnCl2, H2O
2) KOH, K2O, MgO 4) H2SO4, Al2O3, HCl
А3. Азот проявляет наибольшую степень окисления в соединении с формулой:
1) NO2 3) NH3
2) NO 4) N2O5
А4. Формула сульфата железа (III):
1) FeS 3) Fe2 (SO4)3
2) FeSO4 4) Fe2(SO3)3
А5. В 80г воды растворили 20г соли. Массовая доля соли в полученном растворе равна:
1) 40% 3) 50%
2) 25% 4) 20%
А6. Верны ли следующие высказывания?
А. В состав оснований входит ион металла.
Б. В состав оснований входит кислотный остаток.
1) верно только А 3) верно только Б
2) верны оба суждения 4)оба суждения не верны
Часть 2
В1. Установите соответствие между названием вещества и формулой соединения:
Название вещества: Формула соединения:
А) Оксид алюминия 1) Al(OH)3
Б) Серная кислота 2) Al2 (SO4)3
В) Гидроксид алюминия 3) AlО
Г) Сульфат алюминия 4) Al2O3
5) H2SO4
6) H2SO3
А Б В Г
В2. К кислотам относятся:
1) H2CO3 3) H2SiO3 5) HCl
2) Fe(OH)2 4) Hg(NO3)2 6) SO2
В3. Массовая доля (%) кислорода в серной кислоте равна ______. (Запишите число с точностью до десятых).
Часть 3
C1. Рассчитайте объем кислорода, полученного из 200л воздуха, если известно, что объемная доля кислорода в воздухе составляет 21%?
Контрольная работа № 3
Соединения химических элементов
ВАРИАНТ-2
Часть 1
А1. Чистое вещество в отличие от смеси — это:
1) морская вода 3) кислород
2) воздух 4) молоко
А2.Ряд формул, в котором все вещества – основания:
1) СuOH, CuCl2, NaOH 3) Ca(OH)2, Mg(OH)2, MgOHCl
2) K2O, HCl, Ca(OH)2 4) KOH, Ba(OH)2, Cu(OH)2
A3.Углерод проявляет наименьшую степень окисления в соединении с формулой:
1) СаСО3 3) СO2
2) СH4 4) СO
А4.Формула хлорида меди (II):
1) CuCl 3) CuCl2
2) Cu(NO3)2 4) CuSO4
А5. В 180г воды растворили 20г хлорида натрия. Массовая доля соли в полученном растворе равна:
1) 15% 3) 30%
2) 20% 4) 10%
А6. Верны ли следующие высказывания?
А. В состав кислот входит ион водорода.
Б. В состав кислот входит кислотный остаток.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
Часть 2
В1. Установите соответствие между названием вещества и формулой соединения:
Название вещества: Формула соединения:
А) Оксид магния 1) MnCl2
Б) Соляная кислота 2) Mg(OH)2
В) Гидроксид магния 3) HF
Г) Хлорид магния 4) HCl
5) MgCl2
6) MgO
А Б В Г
В2. К солям относятся:
1) H2CO3 3) Ba(OH)2 5)Na2S
2) KNO3 4) SO2 6) CaCO3
B3. Массовая доля (%) кислорода в оксиде алюминия равна ______.(Запишите число с точностью до десятых).
Часть 3
.
C1. Рассчитайте объём воздуха, необходимого для получения 39л азота, если известно, что объёмная доля азота в воздухе составляет 78%?
Контрольная работа № 3
Соединения химических элементов
ВАРИАНТ-3
Часть 1
А1. Смесью веществ не является:
1) речная вода 3) воздух
2) дистиллированная вода 4) почва
A2. Ряд формул, в котором все вещества – кислоты:
1) HCl, CaCl2, H2SO4 3) HNO3, H2SO3 , H3PO4
2) NaOH, H2CO3, H2S 4) CaO, Na2CO3, H2S
A3.Cера проявляет наибольшую степень окисления в соединении с формулой:
1) H2 S 3) Na 2S
2) SO2 4) SO3
A4. Формуласульфитахрома (III):
1) Cr2S3 3) CrSO4
2) Cr2(SO4)3 4) Cr2(SO3)3
A5. В 120г воды растворили 30г соли. Массовая доля соли в полученном растворе равна:
1) 20% 3) 30%
2) 25% 4) 10%
А6. Верны ли следующие высказывания?
А. В состав солей входит ион металла.
Б. В состав солей входит кислотный остаток.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
Часть 2
В1. Установите соответствие между названием вещества и формулой соединения:
Название вещества: Формула соединения:
А) Оксид меди (II) 1) Cu2O
Б) Нитрат меди (II) 2) HNO3
В) Азотная кислота 3) Cu(OH)2
Г) Гидроксид меди (II) 4) Cu(NO3)2
5) H3PO4
6) CuO
А Б В Г
В2. К оксидам относятся:
1) NaOH 3) BaSO4 5) SO2
2) MgO 4) K2O 6) OF2
B3. Массовая доля (%) кислорода в азотной кислоте равна ______. (Запишите число с точностью до десятых).
Часть 3
C1. Рассчитайте объём газа метана СН4, полученного из 500л природного газа, если известно, что объёмная доля метана в природном газе составляет 95%?
Контрольная работа № 3
Соединения химических элементов
ВАРИАНТ-4
Часть 1
A1.Смесью веществ, в отличие от чистого вещества, является:
1) алюминий 3) азот
2) воздух 4) золото
А2.Ряд формул, в котором все вещества – соли:
1) NaCl, BaSO4, KNO3 3) MgSO3, CaO, AlCl3
2) CaSO4 ,Na2CO3 , H2CO3 4) ZnS, CaI2, Al2O3
A3. Фосфор проявляет наименьшую степень окисления в соединении с формулой:
1) Р2O5 3) РН3
2) Р2O3 4) Н3РО4
А4. Формула нитрата железа (II):
1) Fe(NO3)2 3) Fe(NO3)3
2) Fe3N2 4) Fe(NO2)2
А5. В 450г воды растворили 50г соли. Массовая доля соли в полученном растворе равна:
1) 9% 3) 14%
2)10% 4) 11%
А6. Верны ли следующие высказывания?
А. Оксиды состоят из двух элементов.
Б. Степень окисления кислорода в оксидах +2.
1) верно только А 3) верно только Б
2) верны оба суждения 4) оба суждения не верны
Часть 2
В1. Установите соответствие между названием вещества и формулой соединения:
Название вещества: Формула соединения:
А) Сернистая кислота 1) H2SO4
Б) Гидроксид бария 2) BaSO3
В) Сульфат бария 3) BaO
Г) Оксид бария 4) BaSO4
5) Ва(OH)2
6) H2 SO3
А Б В Г
В2. К основаниям относятся:
1) H2SO3 3) MgO 5) K2S
2) NaOH 4) Fe(OH)2 6) Ba(OH)2
B3.Массовая доля (%) углерода в карбонате кальция равна ______.(Запишите число с точностью до десятых).
Часть 3
C1. Рассчитайте объём воздуха, необходимого для получения 50л кислорода, если известно, что объёмная доля кислорода в воздухе составляет 21%?
Источник
Вводный контроль по химии 8 класс УМК Рудзитис Г. Е., Фельдман Ф. Г.

Просмотр содержимого документа
«Вводный контроль по химии 8 класс УМК Рудзитис Г. Е., Фельдман Ф. Г.»
Вводный контроль по химии в 8 классе
2. К химическим явлениям относятся:
А) приготовление пищи Б) падение предмета с высоты
В) горение бумаги
Г) таяние льда
3. Какие из признаков характерны для химических реакций?
А) изменение цвета
Б) растворение вещества в воде
В) образование осадка
Г) электропроводность
4. К чистым веществам относятся
А) соль, растворенная в воде Б) золото
В) минерал кварц Г) сера
5.Укажите, где речь идет о физических явлениях:
Углекислый газ собирается на дне стакана и постепенно вытесняет находившийся в нем воздух;
Углекислый газ и вода в процессе фотосинтеза образуют крахмал;
Углекислый газ вызывает помутнение известковой воды;
«Сухой лед» (твердый углекислый газ) превращается в газ, минуя жидкую фазу.
6. Верны ли следующие суждения о чистых веществах и смесях?
А. Молоко является смесью веществ.
Б. Водопроводная вода является чистым веществом.
1) верно только а 3) верны оба суждения
2) верно только б 4) оба суждения неверны
7. Верны ли следующие суждения о способах разделения смесей?
А. Железные опилки из смеси можно выделить магнитом.
Б. Очистить воду от угольной пыли можно выпариванием.
1) верно только а 3) верны оба суждения
2) верно только б 4) оба суждения неверны
8. К чистым веществам относится:
1) почва 2) алмаз 3) кровь 4) минеральная вода
9. Верны ли следующие суждения о правилах работы в химической лаборатории?
А. Пробирку следует закреплять в лапке штатива около её отверстия.
Б. Сразу после прогревания всей пробирки необходимо нагревать реагирующие вещества.
1) верно только А 2) верно только Б 3) верны оба суждения
4) оба суждения неверны
10.
Вставьте пропущенные слова (из следующего набора: фильтрование, перегонка, отстаивание, упаривание, дистилляция; плотность, температура кипения, температура плавления) в необходимом падеже в предложение.
Сливки и обезжиренное молоко можно отделить друг от друга ……………………………………., так как эти вещества имеют разную ……………………………
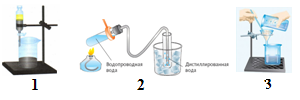
11. . На каком рисунке показано:
а) разделение смеси твердое – жидкое фильтрованием;
б) разделение смеси жидкое – жидкое;
в) освобождение жидкости от растворенных в ней примесей путем дистилляции.
12.Укажите способы разделения следующих веществ:
а) вода и сахар ( );
б) медные и железные опилки ( );
в) подсолнечное масло и вода ( );
г) вода и уксусная кислота ( ).
Источник
Тест для 8 класса «Чистые вещества и смеси».
Самостоятельная работа по теме «Чистые вещества и смеси».
А1. Чистым (индивидуальным) веществом является:
1) стекло 2) речная вода 3) кислород 4) сталь
А2. Неоднородная смесь – это
1) молоко 2) раствор сахара 3) воздух 4) стекло
А3. Химический анализ состава смесей не проводят
геологи при разведке полезных ископаемых
продавцы хозяйственных магазинов
лаборанты химических лабораторий
А4. Смесь медных и железных опилок может быть разделена методом
1) отстаивания 2) фильтрования 3) кристаллизации 4) действия магнита
А5. Для очистки воды от растворённых в ней минеральных солей используют
1) центрифугирование 2) отстаивание 3) дистилляцию 4) фильтрование
А6. Способ разделения неоднородных смесей – это
1) дистилляция 2) выпаривание 3) хроматография 4) отстаивание
А7. Масса хлорида натрия, полученная при выпаривании 100 г 5%-го раствора NaCl
1) 2г 2) 3г 3) 5г 4) 10г
А
А9. Газообразная смесь – это
1) природный газ 2) латунь 3) углекислый газ 4) кислород
А10. Газ, который не входит в состав воздуха
А11. Признак или свойство, на основе которого можно разделить смесь растительного масла с водой: 1) цвет 2) плотность 3) запах 4) агрегатное состояние
А12. Нефтепродуктом является
1) природный газ 2) кокс 3) бензол 4) мазут
А13. Для разделения смеси сахарного песка с водой используют
чашку для выпаривания
воронку с фильтром
Прибор для дистилляции
А14. Масса сахара, необходимая для приготовления 200 г 5%-ного раствора сахара
1) 2г 2) 4г 3) 10 г 4) 20г
А15. Верны ли суждения о способах разделения смесей?
1)верно только А
2)верно только Б
3) верны оба суждения
4) оба суждения неверны
В1. Однородной смесью являются
раствор уксусной кислоты
смесь глины с водой
В2. Установите соответствие между следующими понятиями.
1) раствор сахара в воде
2) железная скрепка
В) чистые вещества
4) дистиллированная вода
9) стеклянный цилиндр
10) медная проволока
С1. Рассчитайте массовую долю соды в растворе, полученном при добавлении 20 г воды к 60 г 20%-ного раствора соды.
Самостоятельная работа по теме «Чистые вещества и смеси».
А1. Смесью является: 1) водопроводная вода 2) углекислый газ 3) кислород 4) азот
А2. Однородная смесь – это: 1) молоко 2) раствор этилового спирта 3) смесь мела с водой 4) нефть
А3. Фильтрованием можно разделить смесь воды и
1) сахарного песка 2) машинного масла 3) бензина 4) почвы
А4. Меньше всего растворённых солей содержит вода
1) морская 2) дождевая 3) дистиллированная 4) колодезная
А5. Водная смесь зубного порошка и поваренной соли может быть разделена
1) выпариванием 2) отстаиванием 3) перегонкой 4) кристаллизацией
А6. Способ разделения однородных смесей
1) выпаривание 2) отстаивание 3) фильтрование 4) действие магнитом
А7. Масса нитрата калия, образующегося при выпаривании 200 г 10%-ного раствора KNO 3
1) 20г 2) 25г 3) 30г 4) 40г
А8. Верны ли суждения о чистых веществах и смесях?
А. Виноградный сок – это чистое вещество.
Б. Раствор сахара в воде является неоднородной смесью.
1)верно только А
2)верно только Б
3) верны оба суждения
4) оба суждения неверны
А9. На рисунке показан способ разделения смеси
м
Раствора мела в воде
Раствора столового уксуса
Воды и растительного масла
А10. К твёрдой смеси относится: 1) природный газ 2) нефть 3) бензин 4) чугун
А11. Газ, который преобладает в воздухе: 1) O 2 2) Ar 3) N 2 4) CO 2
А12. Смесь порошков железа и серы можно разделить с помощью
1) возгонки 2) дистилляции 3) действия магнита 4) фильтрования
А13. Для очистки питьевой воды на водозаборной станции используют
речной песок 2) бумажный фильтр 3) матерчатый фильтр 4) вату
А14. Для разделения смеси подсолнечного масла и воды используют
чашку для выпаривания
прибор для фильтрования
прибор для дистилляции
А15. Масса соли, полученная при выпаривании 300 г её раствора с массовой долей 0,15
1) 15г 2) 20 г 3) 30 г 4) 45 г
В1. Правильные суждения о чистых веществах и смесях.
при растворении мела в воде образуется неоднородная смесь
в однородных смесях частицы компонентов можно обнаружить невооружённым глазом
при растворении в воде поваренной соли образуется неоднородная смесь
смесь воды и сахара можно разделить выпариванием
однородные смеси при хранении самопроизвольно разделяются
В2. Установите соответствие между следующими понятиями.
В) чистые вещества
4) сахарный песок
5) водопроводная вода
С1. К 200 г 15%-ного раствора сахара добавили 15 г сахара. Какова массовая доля сахара в полученном растворе?
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Курс повышения квалификации
Современные образовательные технологии в преподавании химии с учетом ФГОС
Номер материала: ДБ-1101682
Международная дистанционная олимпиада Осень 2021
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
В московском метро появились наклейки для потерявшихся детей
Время чтения: 1 минута
В Госдуме предложили установить предельно допустимые цены за обучение в вузах
Время чтения: 1 минута
В России объявлены нерабочие дни с 30 октября по 7 ноября
Время чтения: 2 минуты
Рособрнадзор оставил за регионами решение о дополнительных школьных каникулах
Время чтения: 1 минута
В школе в Пермском крае произошла стрельба
Время чтения: 1 минута
Рособрнадзор рассчитывает, что экспресс-тесты на ковид в школах помогут избежать удаленки
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Источник