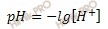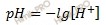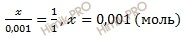- Химик.ПРО – решение задач по химии бесплатно
- Решение задачи
- Урок №8. Диссоциация кислот, оснований и солей
- 1.4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
- Диссоциация кислот
- Диссоциация оснований
- Диссоциация солей
- Соляная кислота это электролит
- Содержание
- Степень диссоциации [ править | править код ]
- Классификация [ править | править код ]
- Использование термина [ править | править код ]
- В естественных науках [ править | править код ]
- В технике [ править | править код ]
- В электрохимии [ править | править код ]
- В источниках тока [ править | править код ]
- Электролитический конденсатор [ править | править код ]
- Активности в электролитах [ править | править код ]
Химик.ПРО – решение задач по химии бесплатно
К какому объёму воды следует добавить 1 миллилитр соляной кислоты (HCl) с молярной концентрацией 0,1 моль/л, чтобы получить раствор с рОН 11?
Решение задачи
Используя формулу, вычислим pH раствора:
Водородный показатель (pH) раствора численно равен отрицательному десятичному логарифму концентрации ионов водорода в этом растворе.
По формуле вычислим концентрацию ионов водорода:
[H + ] = 10 -3 = 0,001 (моль/л).
Соляная кислота вода
По уравнению диссоциации вычислим, молярную концентрацию полученной (после добавления воды) соляной кислоты (HCl), соляная кислота вода:
при диссоциации 1 моль HCl образуется 1 моль ионов H +
при диссоциации х моль HCl образуется 0,001 моль ионов H +
Следовательно, полученный раствор соляной кислоты (HCl) 0,001 моль/л. Соляная кислота вода
Напомню, молярная концентрация – число молей вещества содержащегося в единице объема раствора.
Исходя из выражения закона эквивалентов и учитывая, что количество кислоты при разбавлении сохраняется, справедливо выражение:
С1, С2 – концентрация исходного и полученного раствора соляной кислоты (HCl) соответственно;
V1, V2 – концентрация исходного и полученного раствора соляной кислоты (HCl) соответственно.
Получаем, соляная кислота вода:
V2 (HCl) = 0,1 ⋅ 1 /0,001 = 100 (мл).
V (H2O) = V2 (HCl) — V1 (HCl) = 100 — 1 = 399 (мл).
Источник
Урок №8. Диссоциация кислот, оснований и солей
Диссоциация кислот, оснований и солей в водных растворах
С помощью теории электролитической диссоциации дают определения и описывают свойства кислот, оснований и солей.
Диссоциация кислот
Кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода (H + )
Многоосновные кислоты диссоциируют ступенчато:
Н 3 РО 4 ↔ Н + + Н 2 РО — 4 (первая ступень) – дигидроортофосфат ион
Н 2 РО — 4 ↔ Н + + НРO 2- 4 (вторая ступень) – гидроортофосфат ион
НРО 2- 4 ↔ Н + + PО З- 4 (третья ступень) – ортофосфат ион
Диссоциация многоосновной кислоты протекает главным образом по первой ступени, в меньшей степени по второй и лишь в незначительной степени — по третьей.
Диссоциация оснований
Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы (OH — )
Щёлочи – это основания, растворимые в воде (основания щелочных и щелочноземельных металлов) : LiOH, NaОН, КОН, RbОН, СsОН, FrОН и Са(ОН) 2 , Sr(ОН) 2 , Ва(ОН) 2 , Rа(ОН) 2 , а также NН 4 ОН
Примеры уравнений диссоциации щелочей:
NH 4 OH ↔ NH + 4 + OH —
Многокислотные основания диссоциируют ступенчато:
Ba(ОН) 2 → Bа(ОН) + + OH — (первая ступень)
Ba(OH) + ↔ Ba 2+ +OH — (вторая ступень)
Диссоциация амфотерных оснований (амфолитов)
Амфолиты — это электролиты, которые при диссоциации одновременно образуют катионы водорода (H + ) и гидроксид-ионы (OH — )
Диссоциацию амфотерного гидроксида цинка Zn(ОН) 2 можно выразить уравнением:
2ОН — + Zn 2+ + 2Н 2 О ↔ Zn(ОН) 2 + 2Н 2 О ↔ [Zn(ОН) 4 ] 2- + 2Н +
Диссоциация солей
Солями называются электролиты, при диссоциации которых образуются катионы металлов, а также катион аммония (NH + 4 ) и анионы кислотных остатков.
Диссоциация средних солей
Na 3 PO 4 →3Na + + PO 3- 4
Кислые и основные соли диссоциируют ступенчато.
Диссоциация кислых солей
У кислых солей вначале отщепляются ионы металлов, а затем катионы водорода.
KHSO 4 → K + + HSO — 4
HSO — 4 ↔ H + + SO 2- 4
Диссоциация основных солей
У основных солей вначале отщепляются кислотные остатки, а затем гидроксид-ионы.
MgOHCl → MgOH + + Cl —
MgOH + ↔ Mg 2+ + OH —
ЗАДАНИЕ ДЛЯ ЗАКРЕПЛЕНИЯ
Используя таблицу растворимости солей, кислот, оснований напишите уравнения диссоциации следующих веществ: HF, Mg(OH) 2 , CaCl 2 , Zn(NO 3 ) 2 , Ba(OH) 2 , K 2 SO 4 , H 2 SiO 3 , FeI 3 , NiCl 2 , H 3 PO 4 , Ca(OH) 2 , Na 2 CO 3 , Na 3 PO 4 , HNO 3 , KOH, Ba(OH) 2 , H 2 SO 3 , Ca(NO 3 ) 2 , Ca 3 (PO 4 ) 2 , H 2 S, NaOH, HBr
Источник
1.4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
Как известно из курса физики, электрическим током называют упорядоченное движение заряженных частиц. В случае металлов, электропроводность обеспечивается подвижными электронами в кристалле, слабо связанными c ядрами атомов, что позволяет им направленно двигаться под действием разности потенциалов.
Кроме металлов, существуют также вещества растворы или расплавы которых проводят электрический ток. Такие вещества называют электролитами.
Электролиты — вещества, расплавы или водные растворы которых проводят электрический ток.
Но за счет чего обеспечивается электрическая проводимость расплавов и растворов электролитов?
Рассмотрим такое соединение как хлорида натрия. Это вещество характеризуется ионным строением. В узлах его структурной решетки находятся попеременно в шахматном порядке катионы натрия и анионы хлора:
Как можно видеть, заряженные частицы, которые могли бы быть обеспечивать электрическую проводимость присутствуют, но статичны, т.е. неподвижны в узлах решетки. Поэтому, чтобы электрический ток смог протекать через хлорид натрия, нужно еще и обеспечить «подвижность» ионов, из которых он состоит.
Как известно, для одного и того же вещества наиболее подвижны составляющие его частицы в том случае, когда он находится в жидком, а не в твердом агрегатном состоянии. Поэтому для того, чтобы хлорид натрия смог проводить электрический ток, его необходимо расплавить, т.е. превратить в жидкость. В результате сообщения энергии кристаллу хлорида натрия в виде большого количества теплоты частично разрушаются ионные связи Na + Cl − , т.е. происходит диссоциация на свободные подвижные ионы:
Na + Cl − ↔ Na + + Cl −
Однако, добиться диссоциации хлорида натрия можно не только его плавлением, но также и его растворением в воде. Но каким образом, это становится возможным? Ведь для того чтобы произошло разрушение кристаллической решетки требуется сообщить ей энергию, что и происходило при расплавлении. Откуда же берется энергия на разрушение решетки в случае растворения?
При помещении кристалла NaCl в воду его поверхность подвергается «облепливанию» молекулами воды или гидратации, в результате которой, ионам в структурной решетке сообщается энергия, достаточная для выделения из структурной решетки и «отправления в свободное плавание» в «оболочке» из молекул воды:
или более упрощенно:
NaCl ↔ Na + + Cl − (участвующие в гидратации кристалла NaCl и ионов молекулы воды не записываются)
Если энергия, выделяющаяся при гидратации кристалла, меньше энергии кристаллической решетки, то его растворение и диссоциация становятся невозможными. Например, поверхность кристалла сульфата бария, помещенного в водную среду, также покрывается молекулами воды, но выделяющаяся в результате этого энергия недостаточна отрыва ионов Ba 2+ и SO4 2- из кристаллической решетки и, как следствие, становится невозможно его растворение (на самом деле возможно, но в крайне малой степени, т.к. абсолютно нерастворимых веществ не бывает).
Аналогичным образом диссоциация осуществляется также гидроксидами металлов. Например:
Помимо веществ ионного строения, электролитически диссоциировать способны также и некоторые вещества молекулярного строения с ковалентным полярным типом связи, а именно кислоты. Как и в случае ионных соединений, причина образования ионов из электронейтральных молекул кроется в их гидратации. Существование гидратированных ионов энергетически более выгодно, чем существование гидратированных молекул. Например, диссоциация молекулы соляной кислоты выглядит примерно следующим образом:
Гидратация катионов водорода настолько сильна, что можно говорить не просто о катионе водорода, окружённом молекулами воды (как это было с катионами натрия), а о полноценной частице – ионе гидроксония H3O + , содержащей три полноценные ковалентные связи H-О, одна из которых образована по донорно-акцепторному механизму. Таким образом, уравнение диссоциации соляной кислоты правильнее записывать так:
Тем не менее, даже в этом случае, чаще всего, уравнение диссоциации соляной кислоты, впрочем, как и любой другой, записывают, игнорируя явное участие в диссоциации кислот молекул воды.
Диссоциация многоосновных кислот протекает ступенчато, например:
Таким образом, как мы уже выяснили, к электролитам относят: соли, кислоты и основания.
Для описания способности электролитов к электролитической диссоциации используют величину, которая называется степенью диссоциации (α).
Степень диссоциации – отношение числа продиссоциировавших частиц, к общему числу растворенных частиц.
Источник
Диссоциация кислот
При диссоциации кислот роль катионов играют ионы водорода (H + ), других катионов при диссоциации кислот не образуется:
Именно ионы водорода придают кислотам их характерные свойства: кислый вкус, окрашивание индикатора в красный цвет и проч.
Отрицательные ионы (анионы), отщепляемые от молекулы кислоты, составляеют кислотный остаток.
Одной из характеристик диссоциации кислот является их оснОвность — число ионов водорода, содержащихся в молекуле кислоты, которые могут образоываваться при диссоциации:
Процесс отщепления катионов водорода в многоосновных кислотах происходит ступенчато: сначала отщепляется один ион водорода, затем другой (третий).
Ступенчатая диссоциация двухосновной кислоты:
Ступенчатая диссоциация трехосновной кислоты:
При диссоциации многоосновных кислот самая высокая степень диссоциации приходится на первую ступень. Например, при диссоциации фосфорной кислоты степень диссоциации первой ступени равняется 27%; второй — 0,15%; третьей — 0,005%.
Диссоциация оснований
При диссоциации оснований роль анионов играют гидроксид-ионы (ОH — ), других анионов при диссоциации оснований не образуется:
Кислотность основания определяется кол-вом гидроксид-ионов, образующихся при диссоциации одной молекулы основания:
- однокислотные основания — KOH, NaOH;
- двухкислотные основания — Ca(OH)2;
- трехкислотные основания — Al(OH)3.
Многокислотные основания диссоциируют, по аналогии с кислотами, также ступенчато — на каждом этапе отщепляется по одному гидроксид-иону:
Некоторые вещества, в зависимости от условий, могут выступать, как в роли кислот (диссоциировать с отщеплением катионов водорода), так и в роли оснований (диссоциировать с отщеплением гидроксид-ионов). Такие вещества называются амфотерными (см. Кислотно-основные реакции).
Диссоциация Zn(OH)2, как основания:
Диссоциация Zn(OH)2, как кислоты:
Диссоциация солей
Соли диссоциируют в воде на анионы кислотных остатков и катионы металлов (или других соединений).
Классификация диссоциации солей:
- Нормальные (средние) соли получаются полным одновременным замещением всех атомов водорода в кислоте на атомы металла — это сильные электролиты, полностью диссоциируют в воде с образованием катоинов металла и однокислотного остатка: NaNO3, Fe2(SO4)3, K3PO4.
- Кислые соли содержат в своем составе кроме атомов металла и кислотного остатка, еще один (несколько) атомов водорода — диссоциируют ступенчато с образованием катионов металла, анионов кислотного остатка и катиона водорода: NaHCO3, KH2PO4, NaH2PO4.
- Основные соли содержат в своем составе кроме атомов металла и кислотного остатка, еще одну (несколько) гидроксильных групп — диссоциируют с образованием катионов металла, анионов кислотного остатка и гидроксид-иона: (CuOH)2CO3, Mg(OH)Cl.
- Двойные соли получаются одновременным замещением атомов водорода в кислоте на атомы различных металлов: KAl(SO4)2.
- Смешанные соли диссоциируют на катионы металла и анионы нескольких кислотных остатков: CaClBr.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Источник
Соляная кислота это электролит
Содержание
Электроли́т — вещество, которое проводит электрический ток вследствие диссоциации на ионы, что происходит в растворах и расплавах, или движения ионов в кристаллических решётках твёрдых электролитов. Примерами электролитов могут служить кислоты, соли и основания и некоторые кристаллы (например, иодид серебра, диоксид циркония). Электролиты — проводники второго рода, вещества, электропроводность которых обусловлена подвижностью положительно или отрицательно заряженных ионов.
Степень диссоциации [ править | править код ]
Процесс распада молекул в растворе или расплаве электролита на ионы называется электролитической диссоциацией. Одновременно в электролите протекают процессы ассоциации ионов в молекулы. При неизменных внешних условиях (температура, концентрация и др.) устанавливается динамическое равновесие между распадами и ассоциациями. Поэтому в электролитах диссоциирована определённая доля молекул вещества. Для количественной характеристики электролитической диссоциации было введено понятие степени диссоциации [1] .
Классификация [ править | править код ]
Исходя из степени диссоциации все электролиты делятся на две группы:
- Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты (сильные кислоты, такие как HCl, HBr, HI, HNO3, H2SO4).
- Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот (слабые кислоты, такие как HF), основания p- , d- и f-элементов.
Между этими двумя группами чёткой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом — слабого.
Использование термина [ править | править код ]
В естественных науках [ править | править код ]
Термин электролит широко используется в биологии и медицине. Чаще всего подразумевают водный раствор, содержащий те или иные ионы (напр., «всасывание электролитов» в кишечнике).
В технике [ править | править код ]
Слово электролит широко используется в науке и технике, в разных отраслях оно может иметь различающийся смысл.
В электрохимии [ править | править код ]
Многокомпонентный раствор для электроосаждения металлов, а также травления и др. (технический термин, например электролит золочения).
В источниках тока [ править | править код ]
Электролиты являются важной частью химических источников тока: гальванических элементов и аккумуляторов. [2] Электролит участвует в химических реакциях окисления и восстановления с электродами, благодаря чему возникает ЭДС. В источниках тока электролит может находиться в жидком состоянии (обычно это водный раствор) или загущённым до состояния геля.
Электролитический конденсатор [ править | править код ]
В электролитических конденсаторах в качестве одной из обкладок используется электролит. В качестве второй обкладки — металлическая фольга (алюминий) или пористый, спечённый из металлических порошков блок (тантал, ниобий). Диэлектриком в таких конденсаторах служит слой оксида самого металла, формируемый химическими методами на поверхности металлической обкладки.
Конденсаторы данного типа, в отличие от других типов, обладают несколькими отличительными особенностями:
- высокая объёмная и весовая удельная ёмкость;
- требование к полярности подключения в цепях постоянного напряжения. Несоблюдение полярности вызывает бурное вскипание электролита, приводящее к механическому разрушению корпуса конденсатора (взрыву);
- значительные утечки и зависимость электрической ёмкости от температуры;
- ограниченный сверху диапазон рабочих частот (типовые значения сотни кГц — десятки МГц в зависимости от номинальной ёмкости и технологии).
Активности в электролитах [ править | править код ]
Химический потенциал для отдельного i-го иона имеет вид: μ i = μ i 0 + R T l n a i , +RTlna_,> 

Для электролита в целом имеем:
μ e l = ∑ i v i μ i = v + μ M + + v − μ A − = v + ( μ + 0 + R T l n a M + ) + v − ( μ − 0 + R T l n a A − ) = =sum _v_mu _=v_ mu _>+v_ mu _>=v_ (mu _ ^ +RTlna_>)+v_ (mu _ ^ +RTlna_>)=> 
= ( v + μ + 0 + v − μ − 0 ) + R T l n ( a M + v − ⋅ a A − v − ) = μ 0 + R T l n a , mu _ ^ +v_ mu _ ^ )+RTln (a_>^>cdot a_>^>)=mu _ +RTlna,> 


Таким образом, имеем:
a = a + v + ⋅ a − v − . ^>cdot a_ ^>.>
Усредненная активность иона равна:
a ± = [ a + v + ⋅ a − v − ] 1 v + + v − . ^>cdot a_ ^>
ight]^ +v_ >>.>
Для одно-одновалентного электролита v + = v − = 1 =v_ =1> 


Для добавления растворов электролитов принято пользоваться моляльной (m) концентрацией (для разбавленных водных растворов m (в моль/кг) численно близка к с (молярной концентрации, в моль/л)). Значит, a i = γ i m i , 

1. Электролиты — это вещества, растворы или расплавы которых проводят электрический ток.
2. К электролитам относятся щелочи, растворимые соли и кислоты.
3. В водных растворах электролиты распадаются на ионы.
4. Неэлектролиты — вещества, растворы которых не проводят электрический ток.
5. К неэлектролитам относят простые вещества (металлы и неметаллы), оксиды, большинство органических веществ: углеводороды, спирты, альдегиды, углеводы, простые и сложные эфиры и др.
Давайте порассуждаем вместе
1. К электролитам относится
3) хлорид железа (II)
4) оксид железа (III)
Ответ: электролитом является хлорид железа (II) — растворимая соль
2. К электролитам относится
4) уксусная кислота
Ответ: электролитом является уксксная кислота — т.к. это растворимая кислота.
3. К слабым электролитам не относится
3) угольная кислота
4) уксусная кислота
Ответ: соляная кислота не относится к слабым электролитам, это сильный электролит
4. К сильным электролитам не относится
4) серная кислота
Ответ: сероводород — это слабый электролит, не относится к сильным электролитам
5. Сильным электролитом является
2) серная кислота
Ответ: серная кислота — сильный электролит
6. Не является электролитом
3) азотная кислота
Ответ: спирт не является электролитом
7. К электролитам относится
Ответ: Ca (OH)2 — малорастворимое основание, значит относится к электролитам
1.1. Электролитическая диссоциация. Степень диссоциации. Сила электролитов
Согласно теории электролитической диссоциации, соли, кислоты, гидроксиды, растворяясь в воде, полностью или частично распадаются на самостоятельные частицы – ионы.
Процесс распада молекул веществ на ионы под действием полярных молекул растворителя называют электролитической диссоциацией. Вещества, диссоциирующие на ионы в растворах, называют электролитами. В результате раствор приобретает способность проводить электрический ток, т.к. в нем появляются подвижные носители электрического заряда. Согласно этой теории, при растворении в воде электролиты распадаются (диссоциируют) на положительно и отрицательно заряженные ионы. Положительно заряженные ионы называют катионами; к ним относятся, например, ионы водорода и металлов. Отрицательно заряженные ионы называются анионами; к ним принадлежат ионы кислотных остатков и гидроксид-ионы.
Для количественной характеристики процесса диссоциации введено понятие степени диссоциации. Степенью диссоциации электролита (α) называется отношение числа его молекул, распавшихся в данном растворе на ионы ( n ), к общему числу его молекул в растворе ( N ), или
α = 
Степень электролитической диссоциации принято выражать либо в долях единицы, либо в процентах.
Электролиты со степенью диссоциации больше 0,3 (30%) обычно называют сильными, со степенью диссоциации от 0,03 (3%) до 0,3 (30%)—средними, менее 0,03 (3%)—слабыми электролитами. Так, для 0,1 M раствора CH 3 COOH α = 0,013 (или 1,3 %). Следовательно, уксусная кислота является слабым электролитом. Степень диссоциации показывает, какая часть растворенных молекул вещества распалась на ионы. Степень электролитической диссоциации электролита в водных растворах зависит от природы электролита, его концентрации и температуры.
По своей природе электролиты можно условно разделить на две большие группы: сильные и слабые. Сильные электролиты диссоциируют практически полностью (α = 1).
К сильным электролитам относятся:
1) кислоты ( H 2 SO 4 , HCl , HNO 3 , HBr , HI , HClO 4 , H М nO 4 );
2) основания – гидроксиды металлов первой группы главной подгруппы (щелочи) – LiOH , NaOH , KOH , RbOH , CsOH , а также гидроксиды щелочноземельных металлов – Ba ( OH )2 , Ca ( OH )2, Sr ( OH )2;.
3) соли, растворимые в воде (см. таблицу растворимости).
Слабые электролиты диссоциируют на ионы в очень малой степени, в растворах они находятся, в основном в недиссоциированном состоянии (в молекулярной форме). Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами.
К слабым электролитам относятся:
1) неорганические кислоты ( H 2 CO 3 , H 2 S , HNO 2 , H 2 SO 3 , HCN , H 3 PO 4 , H 2 SiO 3 , HCNS , HСlO и др.);
3) гидроксид аммония ( NH 4 OH );
4) большинство органических кислот
(например, уксусная CH3COOH, муравьиная HCOOH);
5) нерастворимые и малорастворимые соли и гидроксиды некоторых металлов (см. таблицу растворимости).
Процесс электролитической диссоциации изображают, пользуясь химическими уравнениями. Например, диссоциация соляной кислоты (НС l ) записывается следующим образом:
Основания диссоциируют с образованием катионов металла и гидроксид-ионов. Например, диссоциация КОН
Многоосновные кислоты, а также основания многовалентных металлов диссоциируют ступенчато. Например,
H2CO3
HCO3 – 
Первое равновесие – диссоциация по первой ступени – характеризуется константой

Для диссоциации по второй ступени:

В случае угольной кислоты константы диссоциации имеют следующие значения: KI = 4,3 × 10 –7 , KII = 5,6 × 10 –11 . Для ступенчатой диссоциации всегда KI>KII>KIII> . , т.к. энергия, которую необходимо затратить для отрыва иона, минимальна при отрыве его от нейтральной молекулы.
Средние (нормальные) соли, растворимые в воде, диссоциируют с образованием положительно заряженных ионов металла и отрицательно заряженных ионов кислотного остатка
Кислые соли (гидросоли) – электролиты, содержащие в анионе водород, способный отщепляться в виде иона водорода Н + . Кислые соли рассматривают как продукт, получающийся из многоосновных кислот, в которых не все атомы водорода замещены на металл. Диссоциация кислых солей происходит по ступеням, например:
KHCO 3 → K + + HCO 3 – (первая ступень)
HCO 3 – 
Однако степень электролитической диссоциации по второй ступени очень мала, поэтому раствор кислой соли содержит лишь незначительное число ионов водорода.
Основные соли (гидроксосоли) – электролиты, содержащие в катионе одну или несколько гидроксо-групп OH – . Основные соли характерны для многовалентных металлов. Основные соли диссоциируют с образованием основных и кислотных остатков. Например:
FeOHCl 2 
FeOH 2+ 
( ZnOH )2 SO 4 
ZnOH + 
Источник