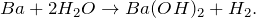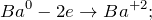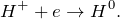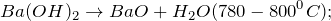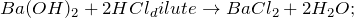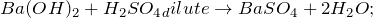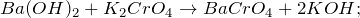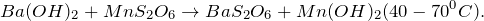- Ba + H2O = ? уравнение реакции
- Барий: способы получения и химические свойства
- Способ получения
- Качественная реакция
- Химические свойства
- Реакция бария с водой
- Реакция взаимодействия бария с водой.
- Уравнение реакции взаимодействия бария с водой:
- Мировая экономика
- Справочники
- Востребованные технологии
- Поиск технологий
- О чём данный сайт?
- О Второй индустриализации
- 1)составьте уравнение реакции бария с водой 2)составьте уравнения реакций BeO и Na2CO3 3)составьте уравнения реакций кислород, оксид углерода 4)составьте уравнения Al(OH)3+NaCl
Ba + H2O = ? уравнение реакции
Здесь есть кто-нибудь, кто хорошо разбирается в химии? Мне нужна помощь: взаимодействует ли барий с водой (Ba + H2O = ?) и, что при этом получается. Укажите основные физические и химические свойства полученного соединения. Заранее, большое спасибо!
В результате взаимодействия бария с водой (Ba + H2O = ?) происходит образование гидроксида бария и выделение газа водорода. Молекулярное уравнение реакции имеет вид:
Данная реакция относится к окислительно-восстановительным, поскольку химические элементы барий и водород изменяют свои степени окисления. Схемы электронного баланса выглядят следующим образом:
Гидроксид бария (едкий барит) представляет собой кристаллы белого цвета, которые плавятся без разложения, но при дальнейшем нагревании разлагаются. Хорошо растворяется в воде, образует сильнощелочной раствор. Проявляет основные свойства, реагирует с кислотами. Вступает в реакции обмена.
Помимо вышеуказанной реакции гидроксид бария получают путем растворения оксида бария в воде (1) или при горячей воды на сульфид бария (2):
Источник
Барий: способы получения и химические свойства
Барий Ba — щелочноземельный металл. Серебристо-белый, ковкий, пластичный. На воздухе покрывается темной оксидно-нитридной пленкой. Реакционноспособный. Сильный восстановитель;
Относительная молекулярная масса Mr = 137,327; относительная плотность для твердого и жидкого состояния d = 3,6; tпл = 727º C; tкип = 1860º C.
Способ получения
1. В результате взаимодействия оксида бария и кремния при 1200º С образуются силикат бария и барий:
3BaO + Si = BaSiO3 + 2Ba
2. Оксид бария взаимодействует с алюминием при 1100 — 1200º С образуя барий и алюминат бария:
4BaO + 2Al = 3Ba + Ba(AlO2)2
3. В результате разложения гидрида бария при температуре выше 675º С образуется барий и водород:
Качественная реакция
Барий окрашивает пламя газовой горелки в желто — зеленый цвет.
Химические свойства
1. Барий вступает в реакцию с простыми веществами :
1.1. Барий взаимодействует с азотом при 200 — 460º С образуя нитрид бария:
1.2. Барий сгорает в кислороде (воздухе) при температуре выше 800º С, то на выходе будет образовываться оксид бария:
2Ba + O2 = 2BaO
1.3. Барий активно реагирует при температуре 100 — 150º С с хлором, бромом, йодом и фтором . При этом образуются соответствующие соли :
1.4. С водородом барий реагирует при температуре 150 — 300º C с образованием гидрида бария:
1.6. Барий взаимодействует с серой при 150º С и образует сульфид бария:
Ba + S = BaS
1.7. Барий взаимодействует с углеродом (графитом) при 500º С и образует карбид бария:
Ba + 2C = BaC2
2. Барий активно взаимодействует со сложными веществами:
2.1. Барий при комнатной температуре реагирует с водой . Взаимодействие бария с водой приводит к образованию гидроксида бария и газа водорода:
2.2. Барий взаимодействует с кислотами:
2.2.1. Барий реагирует с разбавленной соляной кислотой, при этом образуются хлорид бария и водород :
Ba + 2HCl = BaCl2 + H2 ↑
2.2.2. Реагируя с разбавленной азотной кислотой барий образует нитрат бария, оксид азота (I) и воду:
если азотную кислоту еще больше разбавить, то образуются нитрат бария, нитрат аммония и вода:
2.2.3. Барий вступает во взаимодействие с сероводородной кислотой при температуре выше 350 с образованием сульфида бария и водорода:
Ba + H2S = BaS + H2
2.3. Барий вступает в реакцию с газом аммиаком при 600 — 650º С. В результате данной реакции образуется нитрид бария и гидрид бария:
если аммиак будет жидким, то в результате реакции в присутствии катализатора платины образуется амид бария и водород:
2.4. Барий взаимодействует с оксидами :
Барий реагирует с углекислым газом при комнатной температуре с образованием карбоната бария и углерода:
2Ba + 3CO2 = 2BaCO3 + C
Источник
Реакция бария с водой
Реакция взаимодействия бария с водой.
Уравнение реакции взаимодействия бария с водой:
Реакция бария с водой протекает при обычных условиях.
В результате реакции бария с водой образуются гидроксид бария и водород .
Примечание: © Фото https://www.pexels.com, https://pixabay.com

Мировая экономика
Справочники
Востребованные технологии
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (106 487)
- Экономика Второй индустриализации России (102 476)
- Программа искусственного интеллекта ЭЛИС (27 495)
- Метан, получение, свойства, химические реакции (23 751)
- Этилен (этен), получение, свойства, химические реакции (22 849)
- Природный газ, свойства, химический состав, добыча и применение (21 176)
- Крахмал, свойства, получение и применение (20 583)
- Целлюлоза, свойства, получение и применение (19 439)
- Пропилен (пропен), получение, свойства, химические реакции (19 125)
- Прямоугольный треугольник, свойства, признаки и формулы (18 742)
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник
1)составьте уравнение реакции бария с водой
2)составьте уравнения реакций BeO и Na2CO3
3)составьте уравнения реакций
кислород, оксид углерода
4)составьте уравнения
Al(OH)3+NaCl
Дано:
m(C6H14)=43 г
М(С6Н14)=86 г/моль
Найти:
n(C6H14)
n(C6H14) = m(C6H14) / M(C6H14) = 43 / 86 = 0,5 моль
Привет! Сейчас рассчитаем
1. К 400 граммам 10% раствора добавили 90 грамм вещества. Просят узнать концентрацию. Обратим внимание на то, что масса вещества прибавляется и к ранее растворенному веществу, и к массе раствора. Значит, масса раствора 400+90 = 490 грамм. А масса вещества 40+90=130г. Следовательно, массовая доля W = 130:490 = 0,2653 или 26,53%.
2. В 400 грамма 5-ти% раствора содержалось 400*0,05 = 20г вещества. В 150 грамма 30% раствора содержалось 150*0,3 = 45 грамм вещества. Растворы смешали, был получен раствор массой 400+150=550 г. Кол-во растворенного вещества в данном растворе 20+45=65г. Массовая доля W= 65:550 = 0,1181 или 11,81%
3. Тут видимо имеется ввиду раствор массой 4200г, содержащий 500 г ВЕЩЕСТВА, а не воды. Значит, добавили воду (400 г) масса нового раствора 4200+400=4600 г. Массовая доля растворенного вещества 500:4600 = 0,1087 или 10,87%
Источник