Теплофизические свойства воды и водяного пара
Автор: С.Л. Ривкин. .
Тип документа: Справочник .
Год издания: 1980 .

Введение
Часть первая. ИСХОДНЫЕ МАТЕРИАЛЫ ДЛЯ СОСТАВЛЕНИЯ ТАБЛИЦ ТЕПЛОФИЗИЧЕСКИХ СВОЙСТВ ВОДЫ И ВОДЯНОГО ПАРА
Раздел первый. Термодинамические свойства
1-1. Международная система уравнений для точного описания термодинамических свойств воды и водяного пара
1-2. Описание таблиц термодинамических
свойств воды и водяного пара
Раздел второй. Коэффициенты переноса, число Прандтля и поверхностное натяжение
2-1. Динамическая вязкость воды н водяного пара
2-2. Теплопроводность воды и водяного пара
2-3. Число Прандтля для воды и водяного пара
2-4. Поверхностное натяжение воды
Раздел третий. Единицы величин, входящих в таблицы. Соотношения между единицами теплофизических величин
3-1. Единицы величин, входящих в таблицы
3-2. Соотношения между единицами тепло-физических величин
Список литературы
Часть вторая. ТЕПЛОФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ И ВОДЯНОГО ПАРА (таблицы в Международной системе единиц)
Таблица II-I. Термодинамические свойства воды и водяного пара в состоянии насыщения (по температурам)
Таблица II-II. Термодинамические ‘ свойства воды и водяного пара в состоянии насыщения (по давлениям)
Таблица II-III. Термодинамические свойства воды и перегретого пара
Таблица II-IV. Истинная изобарная теплоемкость воды и водяного пара
Таблица II-IV. Динамическая вязкость воды и водяного пара
Таблица II-VI. Теплопроводность воды н водяного пара
Таблица II-VII. Число Прандтля для воды и водяного пара
Таблица II-VIII. Поверхностное натяжение воды, изобарная теплоемкость, теплопроводность, динамическая вязкость, число Прандтля воды и водяного пара в состоянии насыщения
Часть третья. ТЕПЛОФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ И ВОДЯНОГО ПАРА (таблицы, составленные с применением килокалории в качестве единицы теплоты)
Таблица Термодинамические свойства воды и водяного пара в состоянии насыщения (по температурам)
Таблица III-II. Термодинамические свойства воды и водяного пара в состоянии насыщения (по давлениям)
Таблица III-II. Термодинамические свойства воды и перегретого пара
Таблица III-IV. Истинная изобарная теплоемкость воды- и водяного пара
Таблица III-V. Динамическая вязкость воды и водяного пара
Таблица III-VI. Теплопроводность воды и водяного пара
Таблица III-VII. Число Прандтля для воды и водяного пара
Таблица III-VIII. Поверхностное натяжение воды, изобарная теплоемкость, теплопроводность, динамическая вязкость, число Прандтля воды и водяного пара в состоянии насыщения
Приложение 1. Международные скелетные таблицы (1963)
П-1-1. Термодинамические свойства воды и водяного пара на линии насыщения
П-1-2. Удельный объем воды и перегретого водяного пара, см3/г
П-1-3. Удельная энтальпия воды и перегретого водяного пара, Дж/г
Приложение 2. Международная таблица усредненных экспериментальных значений динамической вязкости, мкПа-с, воды и водяного пара (1975)
Приложение 3. Международные таблицы усредненных экспериментальных значений теплопроводности, мВт/(м-К), (1977)
П-3-1. ВоДа и водяной пар в состоянии насыщения
П-3-2. Вода и водяной пар
Приложение 4. Международная таблица усредненных экспериментальных значений поверхностного натяжения воды, Н/м, (1976)
Приложение 5. Изобарная теплоемкость, ккал/(кг-°С), воды при параметрах, близких к критическим.
Источник
Таблица ривкина вода водяной пар
Инженерные расчеты процессов изменения состояния воды и водяного пара и паровых циклов осуществляются по таблицам термодинамических свойств воды и водяного пара [11]. Эти таблицы составлены на основании надежных экспериментальных данных с согласованием результатов экспериментов и расчетных величин в мировом масштабе.
В нашей стране утвержденным стандартом являются таблицы термодинамических свойств воды и водяного пара, составленные М.П.Вукаловичем, С.Л.Ривкиным, А.А.Александровым [11].
Они включают в себя данные по термодинамическим свойствам воды и водяного пара в диапазоне изменений давления от 0,0061 до 1000 бар и температуры от 0 до 1000 0 С.
Таблицы содержат все данные, необходимые для расчетов термодинамических параметров в области жидкости, влажного пара и в области перегретого пара. В таблицах не приведены значения внутренней энергии, для ее расчета используется соотношение u = h — Рv. При расчете внутренней энергии необходимо обратить внимание на соответствие единиц измерения энтальпии h, она в таблицах приведена в кДж/кг, и произведения Рv, при использовании давления в кПа это произведение тоже будет в кДж/кг.
Таблицы построены следующим образом. Первая и вторая таблицы описывают свойства воды и водяного пара в состоянии насыщения, как функции от температуры (1-я таблица) и давления (2-я таблица). Эти две таблицы дают зависимость параметров на линиях x = 0 (вода в состоянии насыщения) и x = 1 (сухой насыщенный пар) от температуры и давления. Нахождение всех параметров ведется по одной величине; в табл. 1 — по температуре, в табл. 2 — по давлению насыщения. Эти определяющие параметры находятся в крайних левых столбцах таблиц. Далее в правых столбцах идут соответствующие Р Н и t Н величины: v’ и v», h’ и h», r=h»-h’, s’ и s», s»-s’. Параметры с одним штрихом относятся к воде в состоянии насыщения, с двумя штрихами — к сухому насыщенному пару. Величины параметров влажного насыщенного пара определяются расчетным путем с использованием степени сухости x. Для облегчения этих расчетов в таблицах даны величины r и s»-s’. Например, определение удельного объема, энтальпии и энтропии влажного пара ведется по формулам:
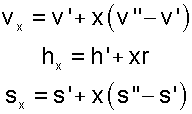 |
Диапазон определяющих параметров этих таблиц: от t=0 0 С до t КР =374,12 0 С и от Р=0,0061 бар до Р КР =221,15 бар, т.е. нижний предел — тройная точка воды, верхний предел — критическая точка воды.
Необходимо отметить, что в качестве определяющего параметра в табл. 1 и 2 можно использовать любой из параметров (v’, v», h’, h», s’, s»), а не только давление и температуру насыщения. Поскольку в инженерной практике Р и t выступают чаще всего в качестве определяющих параметров, их и поместили в левой колонке.
Следующая — третья таблица описывает свойства воды и перегретого пара. Их диапазон от 0 до 1000 0 С (может быть и до 800 0 С) и от 1 кПа до 100 МПа. В качестве определяющих параметров здесь необходимы две величины. В 3-х таблицах это давление — верхняя горизонтальная строка — и температура — левая крайняя колонка. Под строкой давлений дается прямоугольник, в котором приведены все параметры состояния насыщения, соответствующие данному давлению. Это позволяет быстро ориентироваться в фазовом состоянии воды и пара и, не листая таблицы, выполнять необходимые расчеты для различных фазовых состояний воды. Каждому давлению и температуре в 3-х таблицах даны v, h, s в соответствующих вертикальных колонках.
Для наглядной ориентации параметры жидкой фазы и паровой отделены в этих колонках жирными горизонтальными линиями. Выше этих линий находится жидкая фаза воды, ниже — перегретый пар. При давлениях выше критического (22,12 МПа) эти разделительные линии отсутствуют, т.к. при сверхкритических параметрах нет линии видимого фазового перехода жидкости в пар.
В табл. 3 в качестве определяющих, кроме Р и t, может выступать любая пара параметров: Р, t, v, h, s.
При ориентации в фазовых состояниях воды и пара с использованием таблиц необходимо помнить:
1) при Р = const:
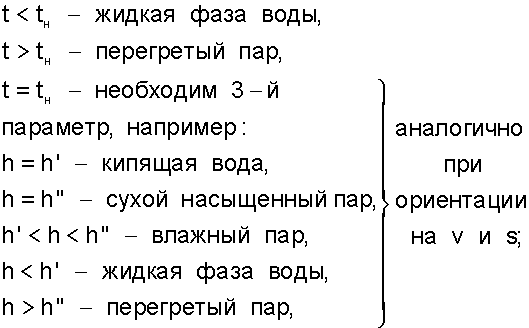 |
2) при t = const:
 |
Некоторые выпуски таблиц включают в себя 2 части: 1-я в системе СИ, где Р — в Па, h — в кДж/кг, и 2-я в системе СГС, где Р — в кгс/см 2 , а h — в ккал/кг.
Источник
Таблица ривкина вода водяной пар
Основные параметры воды и водяного пара
Сначала рассмотрим параметры для воды. Удельный объём воды при 00С и любом давлении равен 


Буквы, обозначающие параметры жидкости, имеют индекс штрих (/), а нижний индекс указывает, что температура воды 00С. Значения параметров воды при других температурах определяют по таблицам Ривкина. В таблицах термодинамических свойств воды у Ривкина имеются три таблицы: таблицы I и II относятся к насыщенному пару. Разница между этими двумя таблицами состоит в том, они построены по разным независимым переменным: таблица I построена по параметру температура, а таблица II ― по параметру давление.
Во втором вертикальном столбце таблицы I стоят значения давления насыщения, то есть того давления, при котором вода при данной температуре начинает превращаться в пар.
Например, для воды при 600С процесс парообразования начнётся, если давление воды будет 0,02 МПа. Для воды при температуре 1250С процесс парообразования начнётся, если давление будет 0,232 МПа.
Во втором столбце таблицы II указаны значения температуры кипения (насыщения), то есть температуры при которой начинается кипение, если вода находится при соответствующем ей давлении, значение которого находится в первом столбце.
Температура сухого насыщенного пара однозначно определяется его давлением и наоборот. Значения параметров такого пара обозначаются двумя штрихами. Буквой r обозначается скрытая теплота парообразования, или теплота фазового перехода, то есть количество тепла, необходимое для превращения воды, нагретой до температуры насыщения при данном давлении, в сухой насыщенный пар.
Когда к жидкости, находящейся в состоянии кипения, подводится при постоянном давлении количество тепла, равное скрытой теплоте парообразования, это не вызывает увеличения температуры. Подведённое количество тепла в этом случае идёт на преодоление сил сцепления между молекулами и на работу расширения.
Обозначим r=d+w, где d называется внутренней теплотой парообразования. Это то количество тепла, которое идёт на преодоление сил сцепления между молекулами жидкости; w ― это работа, производимая при увеличении объёма во время перехода из состояния жидкости в состояние сухого насыщенного пара, и называется внешней теплотой парообразования.
Значение внутренней энергии сухого насыщенного пара можно получить из уравнения u+pv=h. Тогда u//=h//-pv//. Здесь все величины, стоящие в правой части уравнения известны и могут быть взяты из таблиц Ривкина.
Мы уже знаем, что влажный насыщенный пар представляет собой смесь кипящей воды и сухого насыщенного пара. Объём v 1 кг влажного пара состоит из объёма х кг сухого пара и (1-х) кг воды, где х – массовая доля сухого пара, содержащегося во влажном паре; (1-х) ― массовая доля воды во влажном паре. Так как удельный объём сухого пара v//, а удельный объём кипящей воды v/, то удельный объём влажного пара составит: v=v//x+v/(1-x). Величина v/(1-x) часто оказывается очень малой по сравнению с v//x, поэтому для влажного пара приближённо, но достаточно точно для большинства технически важных расчётов можно принять: v=v//x.
Из сказанного видно, что удельный объём влажного пара меньше удельного объёма сухого пара. Внутренняя энергия влажного пара находится по уравнению:
u=h-pv, где все величины относятся к тому состоянию влажного пара, для которого определяется внутренняя энергия u.
Перегретый пар по своим свойствам соответствует идеальному газу в том смысле, что его состояние определяется, если заданы два параметра: давление и температура и сильно отличается от свойств насыщенного пара. Чем выше температура перегретого пара и чем ниже его давление, тем меньше отклоняется перегретый пар от свойств идеального газа. При высоких давлениях и при температурах, близких к состоянию насыщения, перегретый пар будет значительно отклоняться от свойств идеального газа.
Однако удельный объём перегретого пара при заданных давлении и температуры не может быть найден по уравнению идеального газа. Для водяного пара было предложено большое число характеристических уравнений (то есть уравнений состояния). При этом чем точнее какое-либо из них описывает определённые экспериментально свойства водяного пара, тем оно более сложно и менее удобно для расчётов. Поэтому для вычисления удельного объёма и других параметров перегретого пара удобнее всего пользоваться таблицами, составленными по экспериментальным данным с использованием уравнения состояния, например, таблицами по Ривкину.
Количество теплоты, которое подводится к 1 кг сухого насыщенного пара при превращении его в перегретый, называется теплотой перегрева и обозначается qпе. Эту теплоту можно найти их уравнения: qпе=сpm(t-tн), где:
t ― температура перегретого пара;
сpm ― средняя массовая изобарная теплоёмкость перегретого пара.
Теплоёмкость перегретого пара сpm зависит от давления и температуры.
1.4.21. h,s-диаграмма водяного пара
Кроме табличного метода расчётов тепловых процессов, на практике широко применяется графический метод с использованием h,s-диаграммы.
Эта диаграмма впервые была предложена в 1904 году немецким физиком Молье. В настоящее время в системе СИ пользуются диаграммой Вукаловича и Ривкина. Строится диаграмма по данным таблицы термодинамических свойств воды и водяного пара.
Практически h,s-диаграмма вся не изображается. Часть её, соответствующую очень влажному пару, опускают, что даёт возможность выполнить рабочую часть диаграммы в более крупном масштабе. А это повышает точность определения параметров пара и, следовательно, расчёта всех процессов при помощи этой диаграммы.
Повторю основные положения пройденного материала.
Паром называется всякий реальный газ, который в условиях его применения способен переходить в жидкость.
Скрытая теплота парообразования, или теплота фазового перехода ― это количество тепла, необходимое для превращения воды, нагретой до температуры насыщения при данном давлении, в сухой насыщенный пар.
Теплотой перегрева называется количество теплоты, которое подводится к 1 кг сухого насыщенного пара при превращении его в перегретый.
1. Какая температура называется температурой насыщения?
А. Температура, при которой происходит перегрев пара.
В. Температура, при которой жидкость перестаёт испаряться.
С. Температура, при которой происходит кипение жидкости при постоянном давлении.
2. Какую величину следует вычислять по формуле, а не по h,s-диаграмме?
А. Внутреннюю энергию пара. С. Температуру пара.
В. Давление пара. D. Энтальпию пара.
3. Что обозначает на h,s-диаграмме буква х?
А. Энтальпию пара. С. Удельный объём пара.
В. Энтропию пара. D. Степень сухости пара.
4. В какой области р,v-диаграммы находится область насыщенного пара?
A. В области I. В. В области II. С. В области III.
Источник



