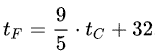- Расчет объема воды разных температур при смешивании
- Калькулятор смешивания воды
- Сколько воды надо смешать для получения нужной температуры
- Калькулятор смеси воды разных температур
- Градус Цельсия °C в Фаренгейта °F
- Градусы жесткости воды: dGH (GH), Clark, fh, usH и другие. Перевод градусов жесткости.
- Что показывают градусы жесткости воды и их перевод друг в друга и в мэкв.
- В настоящее время жесткость воды надо измерять в мэкв, но по традиции в аквариуме жесткость измеряют в градусах, а в разных странах свои собственные градусы жесткости. Эта статья поможет начинающему аквариумисту п ереводить одни градусы в другие и понять зачем они нужны и что же все-таки они означают.
- Сразу перейти к таблице перевода одних градусов другие в другие и в мэкв >>>
- Жесткость воды – это совокупность ее свойств, обусловленных присутствием в ней катионов кальция (Ca 2+ ), магния (Mg 2+ ), и отчасти двухвалентного железа (Fe 2+ ) * . Различают постоянную, временную и общую жесткость.
- НЕМЕЦКИЕ ГРАДУСЫ (dGH):
- ФРАНЦУЗСКИЕ ГРАДУСЫ (fh):
- АМЕРИКАНСКИЕ ГРАДУСЫ (usH):
- АНГЛИЙСКИЕ ГРАДУСЫ (Clark):
Расчет объема воды разных температур при смешивании
Задача определения объема воды разных температур для смешивания и получения необходимой температуры довольно распространена в быту. Особенно она актуальна если в доме есть маленький (грудной) ребенок. Температура смеси для кормления должна быть определенной температуры — как правило это 36-37°C. Получают ее, как правило, смешиванием кипятка (вода при температуре 100°C) и воды, находящейся при комнатной температуре (18-24°C). Как определить сколько воды нужно взять для смешивания?
А если отключили воду и приходится греть ее на плите — как получить нужную температуру для купания малыша? На этот и многие другие вопросы по смешиванию воды (и других жидкостей) разных температур поможет ответить наш калькулятор. Достаточно измерить температуру холодной воды, а зная температуру кипятка и подставив нужный объем воды в калькулятор легко получить нужные пропорции для смешивания.
Калькулятор смешивания воды
Сколько воды надо смешать для получения нужной температуры
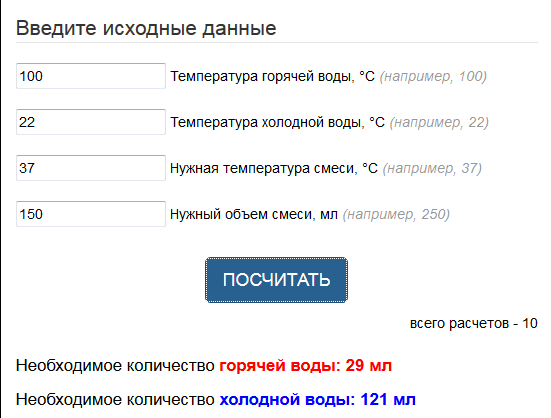
Пример расчета температуры смеси воды
Рассмотрим на простом примере. Вы хотите приготовить 150мл смеси для кормления ребенка, у вас есть кипяток и вода при комнатной температуре (22°C). Нужная температура смеси 37 градусов. Подставив данные в калькулятор мы получим, что для получения такого количества смеси при требуемой температуре нужно смешать 29мл кипятка и 121мл воды при комнатной температуре.
Калькулятор смеси воды разных температур
Еще одна задача на смешивание воды — определение итоговой температуры смеси и ее объема. Для ее решения воспользуйтесь вторым калькулятором ниже — просто введите известные данные и тут же получите результат.
Источник
Градус Цельсия °C в Фаренгейта °F
Онлайн калькулятор для перевода градусов Цельсия в градусы по Фаренгейту и обратно, может перевести градусы Цельсия в Кельвина и наоборот.
Конвертер способен выразить градусы по Цельсию в градусах по Фаренгейту, Кельвину.
Например: температура воздуха 32°C градуса по Цельсию равна 90°F градусов по Фаренгейту.
1 градус Цельсия = 34 градуса по Фаренгейту
Градус Цельсия (обозначение: °C) — широко распространённая единица измерения температуры, применяется в Международной системе единиц (СИ) наряду с кельвином. Используется всеми странами, кроме США, Багамских Островов, Белиза, Каймановых островов и Либерии.
Градус Цельсия назван в честь шведского учёного Андерса Цельсия, предложившего в 1742 году новую шкалу для измерения температуры.
Согласно современному определению, один градус Цельсия равен одному кельвину (K), а ноль шкалы Цельсия установлен таким образом, что температура тройной точки воды равна 0,01 °C. В итоге, шкалы Цельсия и Кельвина сдвинуты на 273,15 единиц: tc = tk — 273,15
Ноль Цельсия — это 32 Фаренгейта, 1 градус Фаренгейта равен 5/9 градуса Цельсия.
Формулы для перевода градусов Цельсия в градусы Фаренгейта и наоборот:
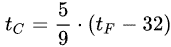
Калькулятор поможет ответить на вопросы:
32 градуса по Фаренгейту сколько по Цельсию = 0 градусов Цельсия
Чему равны 8 градусов Цельсия в Фаренгейтах = 46 градусов Фаренгейта
100 градусов по Цельсию скольку будет по Фаренгейту = 212 градусов по Фаренгейту
Интересный факт:
Самая высокая температура, которую создал человек, составила 4 миллиарда градусов Цельсия, рекорд был поставлен в Естественной Лаборатории Брукхэвена в Нью-Йорке в ионном коллайдере RHIC. Эта температура в 250 раз выше температуры ядра Солнца.
Источник
Градусы жесткости воды: dGH (GH), Clark, fh, usH и другие. Перевод градусов жесткости.
 |
| 1° = 1часть оксида кальция – СаО в 100000 частей воды, или 0.719 частей оксида магния – MgO в 100000 частей воды, или 10 мг СаО в 1 л воды, или 7.194 мг MgO в 1 л воды. dGH (dH) и dKH в настоящее время наиболее часто употребляется в аквариумистике как единица измерения жесткости, причем обозначение dGH – относится к общей жесткости, dKH – к карбонатной; |
ФРАНЦУЗСКИЕ ГРАДУСЫ (fh): | |
| 1° = 1 часть CaCO 3 в 100000 частей воды, или 10 мг CaCO 3 в 1 л воды; | |
АМЕРИКАНСКИЕ ГРАДУСЫ (usH): | |
| 1° = 1 гран (0.0648 г) CaCO 3 в 1 галлоне (американском! 3.785 л) воды. Поделив граммы на литры получаем: 17.12 мг/л СаСО 3 . Однако есть еще одно определение американского градуса: 1 часть CaCO 3 в 1000000 частей воды (в англоязычной литературе выражение концентрации, как 1 часть на 1 000 000 частей называют ppm — part per million (одна часть на миллион), и часто используют. На практике оно идентично 1мг/л) . Таким образом этот 1 американский градус = 1мг CaCO 3 в 1 л воды. Именно эта величина американского градуса принята во всех таблицах с переходными коэффициентами для перевода одних единиц измерения жесткости в другие; (случай странный, ибо люди сведующие в штатовской жизни, такие как например автор известного аквариумного сайта Миклуха (которого я специально об этом спрашивал, а он любезно мне ответил, за что БОЛЬШОЕ СПАСИБО) утверждают, что в США используется именно первый из упомянутых американских градусов) . | |
АНГЛИЙСКИЕ ГРАДУСЫ (Clark): | |
| 1° = 1 гран (0.0648 г) в 1 галлоне (английском! 4.546 л) воды = 14.254 мг/л CaCO3 . | |
Чувствуете как все не просто?! Поэтому приведу таблицу, позволяющую сравнивать и переводить одни градусы жесткости в другие:
| Таблица 1 | |||||
| Наименование единиц | Мг-экв/л | Градус жесткости | |||
| немецкий | французский | американский | английский | ||
| 1 мг-экв/л | 1 | 2.804 | 5.005 | 50.045 | 3.511 |
| 1 немецкий градус dH | 0.3566 | 1 | 1.785 | 17.847 | 1.253 |
| 1 французский градус | 0.1998 | 0.560 | 1 | 10,000 | 0.702 |
| 1 американский градус | 0.0200 | 0.056 | 0.100 | 1 | 0.070 |
| 1 английский градус | 0.2848 | 0.799 | 1.426 | 14.253 | 1 |
Как пользоваться этой таблицей? Допустим, что из лаборатории вы получили результаты анализа аквариумной воды: «Общая жесткость» = 3.25 мг-экв/л. Вам надо перевести эту величину в немецкие градусы. В ячейке, соответствующей пересечению строки мг-экв/л и столбца немецких градусов находим коэффициент, он же множитель, равный 2.804. Теперь надо умножить 3.25 на 2.804. Произведение этих чисел и будет жесткостью в немецких градусах (dHG). Жесткость вашей воды в dGH=9.110. То есть, сравнительно с мг-экв/л, немецкие градусы – более мелкие единицы измерения. Если же вы счастливый обладатель американского теста, и он выдал результат, к примеру, 14 американских градусов (usH), а вам нужны все те же немецкие, то ответ в dGH будет: 14×0.056=0.780. Но это только в том случае, если мы считаем что американский градус равен 1 мг CaCO3 в 1 л воды (так пишут во всей русскоязычной литературе), сами же американцы считают, что их градус жесткости в 17.12 раз больше (см. выше), соответственно, и результат измерения в dGH будет равен 13.35. То есть эти американские градусы довольно близки к немецким.
Пользование разными единицами измерения жесткости без их пересчета (ведь все же они градусы, можно не «заостриться» на том какие они) может привести к существенному искажению данных. Так 14 американских градусов – это всего лишь 0.78 немецких. Поэтому читая сообщения американского коллеги-рыбовода, о том, что его рыбки отнерестились при 14° град. жесткости, не думайте, что им подходит для нереста жесткая вода, эта вода на самом деле очень мягкая. Забавно, что если имелись в виду другие американские градусы, то ошибка будет небольшой, так что и в самом деле, можно не заостряться. В общем, первое что надо сделать – это выяснить в каких единицах представлены результаты.
Как пример путаницы другого рода, связанной с пересчетом содержания кальция в молекулах CaO и CaCO3, приведу фрагмент из очень популярной ныне книги: **
| Единицы жесткости воды, выраженные в миллионных долях (ppm) растворенных солей кальция I) | |||||
| 1 английский градус (Clark) 1 немецкий градус (dH) II) 1 американский градус 1 французский градус (fh) | =14.3 ppm =17.9 ppm =17.1 ppm =10.0 ppm | ||||
1 ppm = 1 миллиграмм на литр
| |||||
Что здесь не так? С Кларком все в порядке – величина 14.3 ppm по сути та же, что приводилась нами ранее на этой страничке, только округленная. А вот 1 немецкий градус какой-то странный: мы знаем, что он равен 10 мг СаО в 1 литре. Авторы книги тоже утверждают, что немецкие градусы показывают содержание СаО, но откуда тогда они взяли цифру 17.9 ppm? Нельзя сказать что эта цифра взята с «потолка», то есть случайная, нет: позанимавшись немного арифметикой я установил, что она соответствует такому количеству СаСО3, какое содержит столько же Са, сколько его в 10 мг СаО! То есть выражает эквивалентное по кальцию количество СаСО3. А сколько же Са в СаО? Посчитаем: молекула СаО имеет массу, выраженную в а.е.м. равную 40.08+16=56.08 (сумма атомных масс кальция и кислорода). Каков вклад кальция в эту массу мы знаем, поэтому можно составить такую пропорцию:
| 40.08 | — | 56.08 |
| Х | — | 10 |
Откуда Х=7.15, таким образом в 1° dGH содержится 7,15 мг кальция .
Теперь определим массу молекулы СаСО3: 40.08+12+3×16(сумма масс кальция, углерода и трех кислородов) = 100.09. Вклад массы кальция составляет 40.08, поэтому можно составить еще одну пропорцию:
| 40.08 | — | 100.08 |
| 7.15 | — | Y |
Здесь Y – это та масса СаСО3 (в мг), в которой кальция содержится 7.15 мг. Y=17.85 (округленно, те самые 17.9). То есть, вопреки сделанному ими самими примечанию, авторы книги представили 1 немецкий градус (10 мг/л СаО) в пересчете на эквивалентное (равноценное) по кальцию количество СаСО3. Совершили ли они в конечном счете ошибку? Конечно! Ведь они указали что эти 17.9 мг/л относятся к СаО. Сколько же в таком случае было бы здесь кальция?
| 40.08 | — | 56.08 |
| Х | — | 17.9 |
Х=12.8 мг. Такое количество кальция к немецкому градусу жесткости не имеет никакого отношения! Как видно из приведенного примера главный недостаток градусов, как единиц измерения жесткости, в том, что они показывают содержание кальция и магния не НЕПОСРЕДСТВЕННО, а в ПЕРЕСЧЕТЕ на окись или на карбонатную соль. Как уже упоминалось раньше – это УСЛОВНЫЕ единицы. На самом деле окись кальция (СаО) в воде существовать не может *** . А СаСО3 – мало растворимое в воде вещество: в стандартных условиях при давлении 1 атм. и температуре 25°С растворяется лишь 6.7 мг/л, что может поднять ее жесткость лишь до 0.24 мг-экв/л, или dGH=0.670. Выходит так, что если аквариумист, горя желанием узнать, сколько же в воде его аквариума присутствует ионов кальция и магния, сделает тест (все покупные тесты измеряют жесткость в градусах), то узнает он вовсе не это, а то сколько там БЫЛО БЫ СаО или СаСО3, если бы массу действительно присутствующих в воде ионов кальция и магния (Ca 2+ и Mg 2+ ) пересчитать на эквивалентное количество этих веществ, которых на самом деле в воде нет!
Приведу еще одну табличку, которая показывает сколько же мг/л ионов кальция и магния (тех, которые на самом деле в воде есть, но не виде условных веществ, а в виде реально растворенных ионов) соответствуют различным единицам (градусам) измерения жесткости.
| Таблица 2 | |||||
| Единица измерения жесткости | Содержание какого вещества отражают | Численное значение 1 единицы | Эквивалентная масса ионов, реально существующих в воде | ||
| Для кальция | Для магния | Са 2+ | Мg 2+ | ||
| Мг-экв/л | Са 2+ и Мg 2+ | 1 мг-экв/л | 1 мг-экв/л | 20.04 | 12.15 |
| Немецкий градус dGH | CaO и MgO | 10 мг/л СаО | 7.19 мг/л MgO | 7.15 мг/л | 4.34 мг/л |
| Французский градус fh | CaCO 3 | 10 мг/л CaCO 3 | 8.425 мг/л MgCO 3 | 4.005 | 2.429 |
| Американский градус usH | CaCO 3 | 1 мг/л CaCO 3 | 0.8425 мг/л MgCO 3 | 0.4005 | 0.2429 |
| Английский градус (Clark) | CaCO 3 | 14.254 мг/л CaCO 3 | 12.008 мг/л MgCO 3 | 5.708 | 3.463 |
В доступной мне литературе в отношении французских, американских и английских градусов я не встретил упоминаний об эквивалентных для этих градусов количествах MgCO3. С другой стороны, без магния-то как?! Поэтому я, по аналогии с немецкими градусами, сделал пересчеты с массы СаСО3 на эквивалентные количества MgCO3 и привел в таблице все соответствующие магниевой жесткости величины.
В общем, очень неудобные единицы измерения эти градусы. От того с ними и вечная путаница. Особенно «обнадеживающе» выглядит второе примечание из приведенного выше фрагмента книги (помеченное II) ), из него следует, что теперь далеко не всегда понятно, какие именно градусы обозначает значок dH, а значит путаница будет расти. И она растёт. Авторы книг по аквариумистике из разных стран ссылаются друг на друга, используя переводы. А некоторые переводчики и редакторы не слишком вникают в суть вопроса. И ведь есть ещё простые типографские опечатки, которые кочуют из издания в издание. Так что подчас не понятно о каких именно градусах на самом деле идёт речь, и те ли это градусы, которые имел в виду автор. В качестве примера приведу табличку из широко известной книги Г. Майланда **** (стр.52).
| Таблица 3 | |||||
| Нем. °dH | Англ. °eH | Франц. °fH | Америк. °usH | СНГ °suH | |
| 1 нем. градус | 1.00 | 1.25 | 1.78 | 17.8 | 7.15 |
| 1 англ. градус | 0.798 | 1.00 | 1.43 | 14,3 | 5.70 |
| 1 франц. градус | 0.560 | 0.702 | 1.00 | 10.0 | 4.0 |
| 1 америк. градус III) | 0.056 | 0.070 | 0.10 | 1.0 | 0.40 |
| 1 рус.градус | 0.14 | 0.111 | 0.078 | 0.0078 | 1.00 |
| III) Данные в ppm (parts per million) при условии, что масса 1 литра воды равна 1 кг. | |||||
Я скопировал эту табличку полностью. В принципе это та же самая таблица, что и приведенная выше таблица 1, только менее точная. В ней почти все правильно, за исключением данных относящихся к неким «Русским градусам» (suH). Судя по крайнему правому столбцу таблицы, они равны 1 мг/л Ca 2+ и тогда весь этот столбец правильный. Множитель 0.14 в нижней строчке тоже правильный. Это легко проверить: мы знаем (табл. 2), что 1° dGH равноценен 7.15 мг Ca 2+ на литр. Если 1° suH действительно равен 0.14 dGH, то в 1° suH кальция содержится 7.15×0.14=1 мг/л. Все сошлось, и значит – все это верно. Но тогда последующие цифры в этой строке никакого разумного объяснения не имеют. Перемножение соответствующих градусам жесткости эквивалентных масс кальция на приведенные коэффициенты 1 мг не дает. Я прикидывал и так и этак, что хотел показать автор, или в чем он ошибся – догадаться не сумел (если вы догадаетесь – напишите пожалуйста). Короче говоря, даже если «Русские градусы» равные 1 мг/л кальция есть, то пользоваться этой таблицей для их перевода в другие единицы все равно нельзя!
В серьёзной науке и технике принято использовать единицы измерения, общие для всех вне зависимости от «страны измерения». Просто для того, чтобы лучше понимать друг друга.
Выражение жесткости в миллиграмм эквивалентах на литр воды (мг-экв/л, иногда пишут еще миллиэквивалент) куда удобнее, чем градусы.
Завершая этот материал, упомяну о парадоксальных результатах, которые можно получить измеряя временную (карбонатную) и общую жесткость. А именно: временная жесткость может оказаться больше общей. Тесты можно переделать заново несколько раз, но «странный результат» будет упорно воспроизводиться – значит дело не в случайной ошибке тестирования. О возможности получения таких результатов упоминает в своей книге и Г.Майланд ***** , но вразумительного объяснения не дает (правда может быть это просто перевод книги невразумительный). А между тем этот ларчик открывается очень просто. О том как – можно прочитать в статье про временную жесткость .
Автор отнюдь не всезнайка, и хотя потратил кучу времени, чтобы разобраться во всех этих градусах, вполне мог где-то допустить ошибки. Если Вы их заметили, пожалуйста напишите нам. Замечания и пожелания будут приняты с благодарностью.
* О.С.Зайцев, «Исследовательский практикум по общей химии», М., издательство МГУ, 1994 г.
Назад к тексту
** М.Бейли, П.Бергесс, «Золотая книга акариумиста», Москва, «Аквариум», 2002 г. (страница 116).
Назад к тексту
*** CaO – негашеная, или жженая известь реагирует с водой с образованием большого количества теплоты: CaO + H 2 O = Ca(OH) 2 + 65 кДж. Этот процесс называется гашением извести, а образующийся продукт называется гашеной известью. Ca(OH) 2 мало растворим в воде. В 1 л растворяется при 20°С всего около 1.56 г. Насыщенный раствор гидроксида кальция называется известковой водой и имеет щелочную реакцию. На воздухе известковая вода быстро становится мутной вследствие поглощения ею диоксида углерода (СО 2 ) и образования нерастворимого карбоната кальция.
Назад к тексту
**** Г.Й.Майланд «Аквариум и его обитатели», БММ АО, Москва 1998 г.
Назад к тексту
Источник