- Неорганические вещества клетки. Вода, соли, их роль в жизнедеятельности клетки.
- Лекция № 1. Введение. Химические элементы клетки. Вода и другие неорганические соединения
- Введение
- Признаки, отличающие живую материю от неживой:
- Уровни организации живой материи:
- Многообразие жизни
- Цитология
- Химические элементы клетки
- Биологическое значение воды:
- Другие неорганические соединения клетки
Неорганические вещества клетки. Вода, соли, их роль в жизнедеятельности клетки.
Большинство химических соединений, которые входят в состав клетки, встречаются только в живой природе. Почти все молекулы за небольшим исключением, встречающиеся в клетке, относятся к соединениям углерода и рассматриваются в курсе органической химии. Однако вода встречается и в живой, и в неживой природе. В среднем почти 70% от массы живых организмов составляет вода. Но содержание воды в клетке может колебаться в зависимости, например, от ее конкретного вида или возраста. Помимо воды в клетках в значительных количествах встречаются некоторые соли, которые важны для осуществления функций живых организмов.
Вода (H2O) представляет собой вещество, которое в физическом и химическом отношении существенно отличается от других растворителей. Жизнь возникла в первичном океане, и в процессе дальнейшего развития природа использовала уникальные свойства воды.
У воды в отличии от других жидкостей необычайно высокие температуры кипения и плавления и высокая удельная теплоемкость. Также отличительными особенностями воды являются большая удельная теплота испарения, плавления и высокое поверхностное натяжение. Вода имеет все эти свойства благодаря тому, что ее молекулы более прочно связаны друг с другом в отличии от молекул других растворителей.
Эти уникальные свойства воды оказывают большое влияние на жизнедеятельность клеток. Например, высокая теплоемкость воды, т.е. способность поглощать тепло при незначительном изменении своей собственной температуры, предохраняет клетки от резких изменений температуры. Высокую теплоту испарения воды живые организмы используют для предохранения от перегрева. Вспомним, что испарение жидкости животными и растениями — это защитная реакция на повышение температуры. Благодаря высокой теплопроводности воды обеспечивается равномерное распределение теплоты по всему организму, а благодаря тому, что вода плохо сжимается, клетки обладают упругостью и могут поддерживать свою форму.
Свои уникальные физические и химические свойства вода получила благодаря особенностям структуры своей молекулы, а точнее, благодаря тому, как именно в молекуле воды располагаются электроны в атомах кислорода и водорода. Два электрона, располагающиеся на внешней электронной орбите атома кислорода в молекуле воды, объединяются с двумя электронами, принадлежащими атомам водорода (у атома водорода на внешней орбите только один электрон). Благодаря этому в молекуле воды образуются две ковалентные связи (между атомом кислорода и двумя атомами водорода). Электроотрицательность * атома кислорода выше, чем у атомов водорода, благодаря чему, электроны притягиваются к нему сильнее. В результате этого на атоме кислорода появляется частично отрицательный заряд, а на атомах водорода — частично положительный. Между более отрицательно заряженными атомами кислорода одних молекул воды и более положительно заряженными атомами водорода других молекул воды образуются так называемые водородные связи, и молекулы воды оказываются связанными между собой.
* Электроотрицательность — это способность атома в молекуле смещать к себе общие электронные пары. Относится к фунадментальным свойствам атома и выражается в количественных характеристиках.
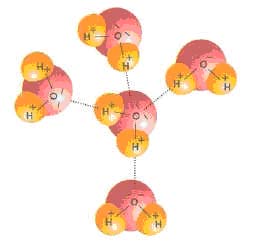
5 молекул воды с водородными связями между ними
На рисунке изображены молекулы воды. Ковалентные связи связывают атомы кислорода и водорода внутри каждой молекулы (сплошные линии), а водородные связи образуются между соседними молекулами (пунктирные линии).
Водородные связи примерно в 20 раз более слабые, чем ковалентные. Поэтому они легко образуются и разрываются. Даже при температуре кипения (100°С) взамодействие между молекулами воды остается достаточно сильным. Именно водородные связи обеспечивают структурированность воды и объясняют такие ее свойства, как высокие температуры кипения и плавления, а также высокую теплоемкость.
Другое важное свойство молекулы воды — ее дипольность. В молекуле воды, как отмечалось ранее, атомы кислорода имеют небольшой отрицательный заряд, а атомы водорода — положительный. Т.к. угол между связями H-O-H составляет 104.5°, получается, что отрицательный заряд в молекуле воды сосредотачивается на одной стороне, а положительный — на другой. Благодаря дипольности молекулы воды имеют способность к ориентации в электрическом поле. Это свойство объясняет, что вода является уникальным растворителем. Если в молекулах веществ присутствуют заряженные группы атомов, они, вступая в электростатическое взаимодействие с молекулами воды, растворяются в ней. Такие вещества с заряженными или полярными группами, растворяющиеся в воде, называются гидрофильными.
Растворение NaCl в воде.
Способность воды растворять кристалл NaCl зависит от электростатического притяжения между полярными молекулами воды и заряженными ионами натрия и хлора.
К гидрофильным соединениям, которые в большом количестве есть в клетках, относятся соли, некоторые низкомолекулярные органические соединения (органические кислоты, аминокислоты, простые сахара), а также полимеры: некоторые полисахариды, белки, нуклеиновые кислоты. Однако существует ряд веществ, почти не имеющих заряженных атомов, и, поэтому, не растворяющихся в воде. Такие вещества называются гидрофобными. К ним, например, относятся липиды (жиры). Гидрофобные вещества не взаимодействуют с водой, но могут взаимодействовать друг с другом. Поэтому они хорошо растворяются в некоторых органических растворителях, как, например, хлороформ. Липиды, относящиеся к гидрофобным соединениям, формируют двумерные структуры (биологические мембраны), практически непроницаемые для воды.
По сравнению с другими растворителями вода может растворить больше химических веществ, благодаря своей полярности. Жизнедеятельность клетки невозможна без многочисленных химических реакций, которые осуществляются в ее водной среде, где растворены различные химические вещества. Также вода растворяет и продукты реакций. Затем в растворенном виде они выводятся из клеток и многоклеточных организмов. За счет перемещения воды в организмах животных и растений осуществляется обмен различными веществами между тканями. Еще одним важным свойством воды является то, что, как химическое соединение, вода вступает во многие химические реакции, которые протекают в клетке. Такие реакции называют реакциями гидролиза. В свою очередь, молекулы воды сами образуются в результате многих реакций в клетках живых организмов.
Т.к. масса атома водорода мала, а атом кислорода в молекуле воды удерживает его единственный электрон, протон (ядро атома водорода, лишенное электрона) способен отрываться от молекулы воды. В результате этого из молекулы воды образуются гидроксильный ион (ОН — ) и протон (Н + ).
H2O H + + OH —
Данный процесс называют диссоциацией воды. Гидроксильные ионы и протоны, которые образуются при диссоциации воды, являются, в свою очередь, участниками многих важных реакций в живых организмах.
В жизнедеятельности клетки также очень важны соли, растворенные в воде. Главным образом соли представлены катионами калия (К + ), натрия (Na + ), магния (Mg 2+ ), кальция (Ca 2+ ) и других металлов, а также анионами соляной (Cl — ), угольной (НСО3 — ) и фосфорных кислот (Н2РО4 — , НРО4 2- ).
Многие катионы характеризуются неравномерным распределением между клеткой и окружающей ее средой. Например, для цитоплазмы характерна более высокая концентрация К + , чем для окружающей клетку среды, между тем, в той же цитоплазме концентрация Na + и Са 2+ будет ниже, чем снаружи клетки. В качестве внешней среды по по отношению к клетке может выступать не только природная среда, например, океан, но и жидкости внутри живого организма, такие как кровь или тканевая жидкость, близкие по своему ионному составу к морской воде. В процессе жизнедеятельности неравномерное распределение катионов между клетками и окружающей их средой постоянно поддерживается, на это затрачивается значительная часть энергии в клетках. Такая неравномерная концентрация ионов между клетками и окружающей их средой необходима для многих процессов жизнедеятельности, к примеру, для передачи возбуждения по нервным и мышечным клеткам или сокращения мышц. Когда клетка умирает, концентрация катионов внутри нее и снаружи быстро становится одинаковой.
Кислотность цитоплазмы клетки в процессе жизнедеятельности практически нейтральная (т.е. значение концентрации ионов водорода (рН) в цитоплазме находится в диапазоне 6,5-7,5). Это происходит несмотря на то, что в процессе жизнедеятельности в клетке образуются и щелочи, и кислоты. Важную роль в поддержании нейтральной кислотности играют анионы слабых кислот (НСО3 — , НРО4 2- ), содержащиеся в клетке. Анионы слабых кислот нейтрализуют внутриклеточную среду, связывая протоны кислот и гидроксильные ионы щелочей.
Необходимо отметить, что анионы слабых кислот вступают в химические реакции, происходящие в клетке. Например, для синтеза АТФ, одного из важных соединений для клетки, необходимы анионы фосфорной кислоты. О синтезе АТФ я расскажу более подробно позднее. Неорганические вещества в живых организмах содержатся не только в растворенном, но и в твердом состоянии. В качестве примера можно привести кости, где преобладает фосфат кальция и в меньшем количестве фосфат магния. В раковинах моллюсков преобладает карбонат кальция.
Источник
Лекция № 1. Введение. Химические элементы клетки. Вода и другие неорганические соединения
Введение
Биология — наука о жизни. Важнейшая задача биологии — изучение многообразия, строения, жизнедеятельности, индивидуального развития и эволюции живых организмов, их взаимоотношений со средой обитания.
Живые организмы имеют ряд особенностей, отличающих их от неживой природы. По отдельности каждое из отличий достаточно условно, поэтому их следует рассматривать в комплексе.
Признаки, отличающие живую материю от неживой:
- способность к размножению и передаче наследственной информации следующему поколению;
- обмен веществ и энергии;
- возбудимость;
- адаптированность к конкретным условиям обитания;
- строительный материал — биополимеры (важнейшие из них — белки и нуклеиновые кислоты);
- специализация от молекул до органов и высокая степень их организации;
- рост;
- старение;
- смерть.
Уровни организации живой материи:
- молекулярный,
- клеточный,
- тканевой,
- органный,
- организменный,
- популяционно-видовой,
- биогеоценотический,
- биосферный.
Многообразие жизни
Живые организмы, имеющие клеточное строение, подразделяются на две группы: 1) прокариоты (отсутствует структурно оформленное ядро), 2) эукариоты (имеется структурно оформленное ядро). К прокариотам относятся бактерии, к эукариотам — растения, животные, грибы. Кроме выше перечисленных, существует группа организмов, не имеющих клеточного строения, — вирусы, которые могут размножаться, только паразитируя или в прокариотических, или в эукариотических клетках.
Первыми на нашей планете появились безъядерные клетки. Большинством ученых принимается, что ядерные организмы появились в результате симбиоза древних архебактерий с синезелеными водорослями и бактериями-окислителями (теория симбиогенеза).
Цитология
Цитология — наука о клетке. Изучает строение и функции клеток одноклеточных и многоклеточных организмов. Клетка является элементарной единицей строения, функционирования, роста и развития всех живых существ. Поэтому процессы и закономерности, характерные для цитологии, лежат в основе процессов, изучаемых многими другими науками (анатомия, генетика, эмбриология, биохимия и др.).
Химические элементы клетки
Химический элемент — определенный вид атомов с одинаковым положительным зарядом ядра. В клетках обнаружено около 80 химических элементов. Их можно разделить на четыре группы:
1 группа — углерод, водород, кислород, азот (98% от содержимого клетки),
2 группа — калий, натрий, кальций, магний, сера, фосфор, хлор, железо (1,9%),
3 группа — цинк, медь, фтор, йод, кобальт, молибден и др. (меньше 0,01%),
4 группа — золото, уран, радий и др. (меньше 0,00001%).
Элементы первой и второй групп в большинстве пособий называют макроэлементами, элементы третьей группы — микроэлементами, элементы четвертой группы — ультрамикроэлементами. Для макро- и микроэлементов выяснены процессы и функции, в которых они участвуют. Для большинства ультрамикроэлементов биологическая роль не выявлена.
| Химический элемент | Вещества, в которых химический элемент содержится | Процессы, в которых химический элемент участвует |
|---|---|---|
| Углерод, водород, кислород, азот | Белки, нуклеиновые кислоты, липиды, углеводы и др. органические вещества | Синтез органических веществ и весь комплекс функций, осуществляемых этими органическими веществами |
| Калий, натрий | Na + и K + | Обеспечивание функции мембран, в частности, поддержание электрического потенциала клеточной мембраны, работы Na + /Ka + -насоса, проведение нервных импульсов, анионный, катионный и осмотический балансы |
| Кальций | Са +2 | Участие в процессе свертывания крови |
| Фосфат кальция, карбонат кальция | Костная ткань, зубная эмаль, раковины моллюсков | |
| Пектат кальция | Формирование срединной пластинки и клеточной стенки у растений | |
| Магний | Хлорофилл | Фотосинтез |
| Сера | Белки | Формирование пространственной структуры белка за счет образования дисульфидных мостиков |
| Фосфор | Нуклеиновые кислоты, АТФ | Синтез нуклеиновых кислот |
| Хлор | Cl — | Поддержание электрического потенциала клеточной мембраны, работы Na + /Ka + -насоса, проведение нервных импульсов, анионный, катионный и осмотический балансы |
| HCl | Активизация пищеварительных ферментов желудочного сока | |
| Железо | Гемоглобин | Транспорт кислорода |
| Цитохромы | Перенос электронов при фотосинтезе и дыхании | |
| Марганец | Декарбоксилазы, дегидрогеназы | Окисление жирных кислот, участие в процессах дыхания и фотосинтеза |
| Медь | Гемоцианин | Транспорт кислорода у некоторых беспозвоночных |
| Тирозиназа | Образование меланина | |
| Кобальт | Витамин В12 | Формирование эритроцитов |
| Цинк | Алькогольдегидрогеназа | Анаэробное дыхание у растений |
| Карбоангидраза | Транспорт СО2 у позвоночных | |
| Фтор | Фторид кальция | Костная ткань, зубная эмаль |
| Йод | Тироксин | Регуляция основного обмена |
| Молибден | Нитрогеназа | Фиксация азота |
Атомы химических элементов в живых организмах образуют неорганические (вода, соли) и органические соединения (белки, нуклеиновые кислоты, липиды, углеводы). На атомном уровне различий между живой и неживой материей нет, различия появятся на следующих, более высоких, уровнях организации живой материи.
Вода — самое распространенное неорганическое соединение. Содержание воды составляет от 10% (зубная эмаль) до 90% массы клетки (развивающийся эмбрион). Без воды жизнь невозможна, биологическое значение воды определяется ее химическими и физическими свойствами.
Молекула воды имеет угловую форму: атомы водорода по отношению к кислороду образуют угол, равный 104,5°. Та часть молекулы, где находится водород, заряжена положительно, часть, где находится кислород, — отрицательно, в связи с этим молекула воды является диполем. Между диполями воды образуются водородные связи. Физические свойства воды: прозрачна, максимальная плотность — при 4 °С, высокая теплоемкость, практически не сжимается; чистая вода плохо проводит тепло и электричество, замерзает при 0 °С, кипит при 100 °С и т.д. Химические свойства воды: хороший растворитель, образует гидраты, вступает в реакции гидролитического разложения, взаимодействует со многими оксидами и т.д. По отношению к способности растворяться в воде различают: гидрофильные вещества — хорошо растворимые, гидрофобные вещества — практически нерастворимые в воде.
Биологическое значение воды:
- является основой внутренней и внутриклеточной среды,
- обеспечивает поддержание пространственной структуры,
- обеспечивает транспорт веществ,
- гидратирует полярные молекулы,
- служит растворителем и средой для диффузии,
- участвует в реакциях фотосинтеза и гидролиза,
- способствует охлаждению организма,
- является средой обитания для многих организмов,
- способствует миграциям и распространению семян, плодов, личиночных стадий,
- является средой, в которой происходит оплодотворение,
- у растений обеспечивает транспирацию и прорастание семян,
- способствует равномерному распределению тепла в организме и мн. др.
Купить проверочные работы
по биологии


Другие неорганические соединения клетки
Другие неорганические соединения представлены в основном солями, которые могут содержаться или в растворенном виде (диссоциированными на катионы и анионы), или твердом. Важное значение для жизнедеятельности клетки имеют катионы K + , Na + , Ca 2+ , Mg 2+ (см. таблицу выше) и анионы HPO4 2— , Cl — , HCO3 — , обеспечивающие буферные свойства клетки. Буферность — способность поддерживать рН на определенном уровне (рН — десятичный логарифм величины, обратной концентрации водородных ионов). Величина рН, равная 7,0, соответствует нейтральному, ниже 7,0 — кислому, выше 7,0 — щелочному раствору. Для клеток и тканей характерна слабощелочная среда. За поддержание этой слабощелочной реакции отвечают фосфатная (1) и бикарбонатная (2) буферные системы:
| Низкий рН | ⇔ | Высокий рН | (1) |
| НРО4 2— + Н + | Н2РО4 — | ||
| Гидрофосфат | Дигидрофосфат | ||
| Низкий рН | ⇔ | Высокий рН | (2) |
| НCО3 — + Н + | Н2CО3 | ||
| Гидрокарбонат | Угольная кислота |
В твердом нерастворенном состоянии находятся в костной ткани, в раковинах моллюсков карбонаты и фосфаты кальция и магния, в зубной эмали — фторид кальция и т.д.
Перейти к лекции №2 «Строение и функции углеводов и липидов»
Смотреть оглавление (лекции №1-25)
Источник