- Архимедова сила: что это такое и как действует
- «Эврика!» Открытие закона Архимеда
- Формула силы Архимеда
- Как действует сила Архимеда
- Сила Архимеда в жидкости: почему корабли не тонут
- Сила Архимеда в газах: почему летают дирижабли
- Когда сила Архимеда не работает
- Интересное по рубрике
- Найдите необходимую статью по тегам
- Подпишитесь на нашу рассылку
- Мы в инстаграм
- Рекомендуем прочитать
- Реальный опыт семейного обучения
- Основные агрегатные состояния вещества
- Агрегатные состояния вещества
- Твердое состояние
- Жидкое состояние
- Газообразное состояние
- Фазовые переходы: изменение агрегатных состояний вещества
- График фазовых переходов
- Решение задач по фазовым переходам
- Сублимация и десублимация
- Влажность воздуха: испарение и конденсация
- Как влажность влияет на человека
Архимедова сила: что это такое и как действует
Рассказываем, почему железные корабли не тонут, а воздушные шары летают, что такое «эврика» и при чём здесь Дональд Дак.
Гениальный учёный Архимед, живший в древнегреческих Сиракузах в III веке до нашей эры, прославился среди современников как создатель оборонительных машин, способных перевернуть боевой корабль. Другое его изобретение, «Архимедов винт», по сей день остаётся важнейшей деталью гигантских буровых установок и кухонных мясорубок. Мир обязан Архимеду революционными открытиями в области оптики, математики и механики.
Его личность окутана легендами, порой весьма забавными. С одной из них мы и начнём нашу статью.
«Эврика!» Открытие закона Архимеда
Однажды царь Сиракуз Гиерон II обратился к Архимеду с просьбой установить, действительно ли его корона выполнена из чистого золота, как утверждал ювелир. Правитель подозревал, что мастер прикарманил часть драгоценного металла и частично заменил его серебром.
В те времена не существовало способов определить химический состав металлического сплава. Задача поставила учёного в тупик. Размышляя над ней, он отправился в баню и лёг в ванну, до краёв наполненную водой. Когда часть воды вылилась наружу, на Архимеда снизошло озарение. Такое, что учёный голышом выскочил на улицу и закричал «Эврика!», что по-древнегречески означает «Нашёл!».
Он предположил, что вес вытесненной воды был равен весу его тела, и оказался прав. Явившись к царю, он попросил принести золотой слиток, равный по весу короне, и опустить оба предмета в наполненные до краёв резервуары с водой. Корона вытеснила больше воды, чем слиток. При одной и той же массе объём короны оказался больше, чем объём слитка, а значит, она обладала меньшей плотностью, чем золото. Выходит, царь правильно подозревал своего ювелира.
Так был открыт принцип, который теперь мы называем законом Архимеда:
На тело, погружённое в жидкость или газ, действует выталкивающая сила, равная весу жидкости или газа в объёме погружённой части тела.
Эта выталкивающая сила и называется силой Архимеда.
Формула силы Архимеда
На любой объект, погружённый в воду, действует выталкивающая сила, равная весу вытесненной им жидкости. Таким образом, вес объекта, погружённого в воду, будет отличаться от его веса в воздухе в меньшую сторону. Разница будет равна весу вытесненной воды.
Чем больше плотность среды — тем меньше вес. Именно поэтому погрузившись в воду, мы можем легко поднять другого человека.
Выталкивающая сила зависит от трёх факторов:
- плотности жидкости или газа (p);
- ускорения свободного падения (g);
- объёма погружённой части тела (V).
Сопоставив эти данные, получаем формулу:
Как действует сила Архимеда
Поскольку сила Архимеда, действующая на тело, зависит от объёма его погружённой части и плотности среды, в которой оно находится, можно рассчитать, как поведёт себя то или иное тело в определённой жидкости или газе.
Если плотность тела меньше плотности жидкости или газа — оно будет плавать на поверхности.
Если плотности тела и жидкости или газа равны — тело будет находиться в безразличном равновесии в толще жидкости или газа.
Если плотность тела больше, чем плотность жидкости или газа, — оно уйдёт на дно.
Сила Архимеда в жидкости: почему корабли не тонут
Корпус корабля заполнен воздухом, поэтому общая плотность судна оказывается меньше плотности воды, и сила Архимеда выталкивает его на поверхность. Но если корабль получит пробоину и пространство внутри заполнится водой, то общая плотность судна увеличится, и оно утонет.
В подводных лодках существуют специальные резервуары, заполняемые водой или сжатым воздухом в зависимости от того, нужно ли уйти на глубину или подняться ближе к поверхности. Тот же самый принцип используют рыбы, наполняя воздухом специальный орган — плавательный пузырь.
На тело, плотно прилегающее ко дну, выталкивающая сила не действует. Это учитывают при подъёме затонувших кораблей. Сначала судно слегка приподнимают, позволяя воде проникнуть под него. Тогда давление воды начинает действовать на корабль снизу.
Но чтобы поднять корабль на поверхность, необходимо уменьшить его плотность. Разумеется, воздух в получившем пробоину корпусе не удержится. Поэтому его заполняют каким-нибудь лёгким веществом, например, шариками пенополистирола.
Примечательно, что эта идея впервые пришла в голову не учёным, а авторам диснеевского комикса, в котором Дональд Дак таким образом поднимает со дна яхту Скруджа Макдака. Датский инженер Карл Кройер (Karl Krøyer), впервые применивший метод на практике, по собственному признанию вдохновлялся «Утиными историями».
Сила Архимеда в газах: почему летают дирижабли
В воздухе архимедова сила действует так же, как в жидкости. Но поскольку плотность воздуха обычно намного меньше, чем плотность окружённых им предметов, выталкивающая сила оказывается ничтожно мала.
Впрочем, есть исключения. Воздушный шарик, наполненный гелием, стремится вверх именно потому, что плотность гелия ниже, чем плотность воздуха. А если наполнить шар обычным воздухом — он упадёт на землю. Плотность воздуха в нём будет такая же, как у воздуха снаружи, но более высокая плотность резины обеспечит падение шарика.
Этот принцип используется в аэростатах — воздушные шары и дирижабли наполняют гелием или горячим воздухом (чем горячее воздух, тем ниже его плотность), чтобы подняться, и снижают концентрацию гелия (или температуру воздуха), чтобы спуститься. На них действует та же выталкивающая сила, что и на подводные лодки. Именно поэтому перемещения на аэростатах называют воздухоплаванием.
Учите физику вместе с домашней онлайн-школой «Фоксфорда»! По промокоду PHYSICS72021 вы получите бесплатный доступ к курсу физики 7 класса, в котором изучается архимедова сила.
Когда сила Архимеда не работает
- Если тело плотно прилегает к поверхности. Если между телом и поверхностью нет жидкости или газа — нет и выталкивающей силы. Именно поэтому подводным лодкам нельзя ложиться на илистое дно — мощности их двигателей не хватит, чтобы преодолеть давление толщи воды сверху.
- В невесомости. Наличие веса у жидкости или газа — обязательное условие для возникновения архимедовой силы. В состоянии невесомости горячий воздух не поднимается, а холодный не опускается. Поэтому на МКС создают принудительную конвекцию воздуха с помощью вентиляторов.
- В растворах и смесях. Если в воду налить спирт, на него не будет действовать сила Архимеда, хотя плотность спирта меньше плотности воды. Поскольку связь между молекулами спирта слабее, чем связь молекул воды, он растворится в воде, и образуется новая жидкость — водный раствор спирта.
У нас вы сможете учиться в удобном темпе, делать упор на любимые предметы и общаться со сверстниками по всему миру.

Интересное по рубрике
Найдите необходимую статью по тегам
Подпишитесь на нашу рассылку
Мы в инстаграм
Домашняя онлайн-школа
Помогаем ученикам 5–11 классов получать качественные знания в любой точке мира, совмещать учёбу со спортом и творчеством

Рекомендуем прочитать
Реальный опыт семейного обучения
Звонок по России бесплатный
Пишите нам письма
Посмотреть на карте
Если вы не нашли ответ на свой вопрос на нашем сайте, включая раздел «Вопросы и ответы», закажите обратный звонок. Мы скоро свяжемся с вами.
Источник
Основные агрегатные состояния вещества
О чем эта статья:
Агрегатные состояния вещества
Чтобы разобраться с тем, какими бывают агрегатные состояния, предлагаю по ходу чтения статьи заполнять таблицу.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
Лед, вода и водяной пар — это все три агрегатных состояния одного вещества. Лед — твердое состояние, вода — жидкая, пар — газообразное. Для каждого вещества существует три состояния.
Твердое состояние
Его очень легко представить — это любой предмет, который мы встречаем в жизни. В этом состоянии тело сохраняет форму и объем. Расстояние между молекулами, приблизительно равно размеру самих молекул, которые, в свою очередь, расположены очень структурированно.
Такая структура называется кристаллической решеткой — из-за четкой структуры молекулам сложно двигаться, и они просто колеблются около своих положений.
Заполняем нашу табличку
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
Жидкое состояние
В этом состоянии сохраняется объем, но не сохраняется форма. Например, если перелить молоко из кувшина в стакан, то молоко, имевшее форму кувшина, примет форму стакана. Кстати, в корове у молока тоже была другая форма.

Расстояние между молекулами в жидком состоянии чуть больше, чем в твердом, но все равно невелико. При этом частицы не собраны в кристаллическую решетку, а расположены хаотично. Молекулы почти не двигаются, но при нагревании жидкости делают это более охотно.
Вспомните, что происходит, если залить чайный пакетик холодной водой — он почти не заваривается. А вот если налить кипяточку — чай точно будет готов.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
Газообразное состояние
В жизни мы встречаем газообразное состояние вещества, когда чувствуем запахи. Запах очень легко распространяется, потому что газ не имеет ни формы, ни объема (он занимает весь предоставленный ему объем), состоит из хаотично движущихся молекул, расстояние между которыми больше, чем размеры молекул.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
занимают предоставленный объем
больше размеров молекул
хаотичное и непрерывное
С агрегатными состояниями разобрались, ура! Но до сих пор неясно, каким образом у каждого вещества их целых три, и как одно переходит в другое. Для этого узнаем, что такое фазовые переходы.
Фазовые переходы: изменение агрегатных состояний вещества
При изменении внешних условий (например, если внутренняя энергия тела увеличивается или уменьшается в результате нагревания или охлаждения) могут происходить фазовые переходы — изменения агрегатных состояний вещества.
Фазовые переходы интересны тем, что все живое не Земле существует лишь благодаря тому, что вода умеет превращаться в лед или пар. С кристаллизацией, плавлением, парообразованием и конденсацией связаны многие процессы металлургии и микроэлектроники.
На схеме — названия всех фазовых переходов:

Переход из твердого состояния в жидкое — плавление;
Переход из жидкого состояния в твердое — кристаллизация;
Переход из газообразного состояния в жидкое — конденсация;
Переход из жидкого состояния в газообразное — парообразование;
Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
График фазовых переходов
Если взять процесс превращения льда в воду, воды — в пар, и обратные действия, то мы получим очень информативный график.
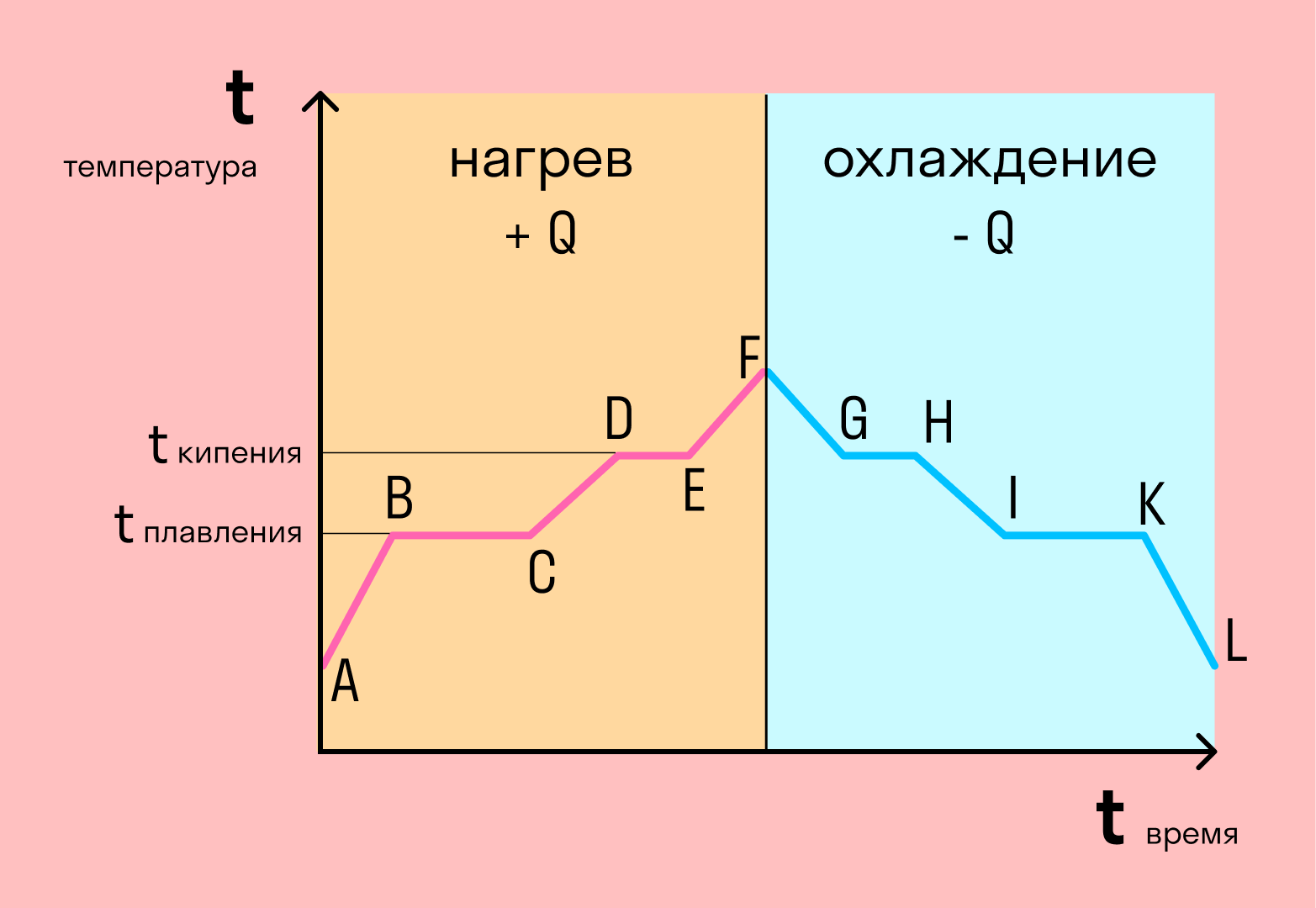
Разбираемся по шагам. Сначала взяли лед, конечно, при отрицательной температуре, потому что при нуле лед начинает плавиться. Нагрели лед до температуры плавления (до 0 градусов).
- AB — нагревание льда
После того, как лед нагрелся до температуры плавления, он начинает плавиться. Плавление происходит при постоянной температуре тем дольше длится, чем больше масса плавящегося вещества. Еще этот процесс зависит от свойств самого вещества, но об этом немного позже.
- BC — плавление льда
Расправившись вещество уже в жидком состоянии снова начинает нагреваться, и температура увеличивается, пока не достигает температуры кипения. В данном случае нагревается вода — это значит, что ее температура кипения равна 100 градусам Цельсия.
- CD — нагревание воды
При 100 градусах вода кипит, пока не выкипит целиком. В данном случае процесс аналогично плавлению происходит при постоянной температуре. Данный процесс нельзя путать с испарением, потому что парообразование происходит при конкретной температуре, а испарение — при любой.
- DE — кипение (парообразование) воды
Далее полученный пар нагревается, но путем нагревания невозможно дойти до другого фазового перехода — можно пойти только обратно.
- EF — нагревание пара
Первый шаг в обратную сторону — охлаждение до температуры кипения.
- FG — охлаждение пара
Дойдя до температуры кипения (в данном случае 100 градусов), пар начинает переходить в жидкое состояние. Этот процесс также происходит при постоянной температуре.
- GH — конденсация пара
Сконденсировавшись, вода охлаждается, пока не начнет замерзать.
- HI — охлаждение воды
Кристаллизуется (замерзает) вода при той же температуре, что и плавится лед — 0 градусов. Кристаллизация также происходит при постоянной температуре.
- IK — кристаллизация воды
После кристаллизации лед охлаждается.
- KL — охлаждение льда
С нагреванием и охлаждением все совсем просто — мы либо передаем теплоту телу (веществу), и оно идет на увеличение температуры, либо тело отдает тепло и охлаждается.
В остальных процессах температура не меняется. Это связано с тем, что количество теплоты не всегда зависит от температуры. Формулы для всех процессов выглядят так:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
m — масса [кг]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Плавление
Кристаллизация
Q — количество теплоты [Дж]
λ — удельная теплота плавления вещества [Дж/кг]
m — масса [кг]
Парообразование
Конденсация
Q — количество теплоты [Дж]
L — удельная теплота парообразования вещества [Дж/кг]
m — масса [кг]
Решение задач по фазовым переходам
С теорией разобрались — а теперь давайте практиковаться!
Задачка раз. Температура медного образца массой 100 г повысилась с 20 °С до 60 °С. Какое количество теплоты получил образец? Удельную теплоёмкость меди считать равной 380 Дж/(кг умножить на °С)
Сначала нужно перевести массу в килограммы:
Берем формулу количества теплоты для нагревания вещества:
Q = 380 * 0,1*(60-20) = 1520 Дж
Ответ: образец получил 1520 Дж
Задачка два. Какое количество теплоты необходимо для плавления 2,5 т стали, взятой при температуре плавления? Удельная теплота плавления стали λ=80кДж/кг. Теплопотерями пренебречь.
Сначала нужно перевести массу в килограммы и удельную теплоту в Дж/кг:
80 кДж/кг = 80000 Дж/кг
Берем формулу количества теплоты для плавления вещества:
Q = 80000*2500 = 200 000 000 Дж = 200 МДж
Ответ: для плавления 2,5 т стали необходимо 200 МДж теплоты.
Сублимация и десублимация
Мы уже рассказали про такие процессы, как сублимация и десублимация.
- Переход из твердого состояния в газообразное, минуя жидкое — сублимация (возгонка);
- Переход из газообразного состояния в твердое, минуя жидкое — десублимация.



.png)


















