- Почему вода испаряется?
- Почему вода испаряется при комнатной температуре?
- Итак . почему это происходит?
- Химические свойства молекул воды
- Температура и молекулярная энергия
- Влажность
- Испарение при комнатной температуре
- Испарение
- Испарение: что это за процесс
- Испарение на уровне молекул
- Интенсивность испарения
- Насыщенный пар
- Испарение в жизни
- Испарение в организме человека и животных
- Испарение у растений
- Испарение в природе и окружающей среде
- Испарение в промышленности и быту
Почему вода испаряется?
Все знают, что если развесить выстиранное белье, то оно высохнет. И так же очевидно, что мокрый тротуар после дождя обязательно станет сухим.
Испарение — это процесс, при котором жидкость постепенно переходит в воздух в форме пара или газа. Все жидкости испаряются с разной скоростью. Спирт, аммиак и керосин испаряются быстрей воды.
Есть две силы, воздействующие на молекулы, из которых состоят все вещества. Первая — это сцепление, которое удерживает их между собой. Другая — тепловое движение молекул, которое заставляет их разлетаться в разные стороны. Когда эти две силы уравновешены, мы имеем жидкость.
На поверхности жидкости ее молекулы находятся в движении. Эти молекулы, которые движутся быстрей соседних, находящихся внизу, могут улетать в воздух, преодолевая силы сцепления. Это и является испарением.
Когда жидкость подогрета, испарение происходит быстрей. Так происходит потому, что в теплой жидкости скорость движения молекул больше, больше молекул имеет шанс покинуть жидкость. В закрытом сосуде испарение отсутствует. Так случается потому, что количество молекул в паре достигает определенного уровня. Тогда количество молекул, покидающих жидкость, будет равно количеству молекул, вернувшихся в нее. Когда это происходит, мы можем сказать, что пар достиг точки насыщения.
Когда воздух над жидкостью движется, скорость испарения увеличивается. Чем больше поверхность испаряющейся жидкости, тем быстрее происходит испарение. Вода в круглой сковородке испарится быстрей, чем в высоком кувшине.
Куда исчезает вода, когда она высыхает?
Выглянув на улицу или посмотрев на дорогу, вы увидели там воду. Один час яркого солнечного света — и вода исчезает! Или, например, вывешенное на веревке белье высыхает к концу дня. Куда исчезает вода?
Мы говорим, что вода испаряется. Но что это значит? Испарение — это процесс, при котором жидкость на воздухе быстро становится газом или паром. Многие жидкости испаряются очень быстро, гораздо быстрее, чем вода. Это относится к алкоголю, бензину, нашатырному спирту. Некоторые жидкости, например ртуть, испаряются очень медленно.
Из-за чего происходит испарение? Чтобы понять это, надо кое-что представлять о природе материи. Насколько мы знаем, каждое вещество состоит из молекул. Две силы оказывают воздействие на эти молекулы. Одна из них — сцепление, которое притягивает их друг к другу. Другая — это тепловое движение отдельных молекул, которое заставляет их разлетаться.
Если сила сцепления выше, вещество остается в твердом состоянии. Если же тепловое движение настолько сильно, что оно превосходит сцепление, то вещество становится или является газом. Если две силы примерло уравновешены, то тогда мы имеем жидкость.
Вода, конечно, является жидкостью. Но на поверхности жидкости есть молекулы, которые движутся настолько быстро, что преодолевают силу сцепления и улетают в пространство. Процесс вылета молекул и называется испарением.
Почему вода испаряется быстрее, когда она находится на солнце или нагревается? Чем выше температура, тем интенсивнее тепловое движение в жидкости. Это значит, что все большее количество молекул набирает достаточную скорость, чтобы улететь. Когда улетают самые быстрые молекулы, скорость оставшихся молекул в среднем замедляется. Почему остающаяся жидкость охлаждается за счет испарения.
Так что, когда вода высыхает, это означает, что она превратилась в газ или пар и стала частью воздуха.
Источник
Почему вода испаряется при комнатной температуре?
В школе нас учили, что когда вода закипает, она меняет фазу с жидкости на пар. Чтобы вызвать это изменение, требуется высокая температура, называемая точкой кипения. Для воды эта точка составляет 100 °C. Однако вспомните, что во время дождя лужи испаряются после прояснения неба, особенно когда выходит солнце. При испарении фаза воды также переходит из жидкой в парообразную, и это происходит при температурах, далеко не равных 100 °C.
Итак . почему это происходит?
Ответ кроется в физических и химических свойствах молекул воды и связей, образующихся между этими молекулами (межмолекулярных связей).
Химические свойства молекул воды
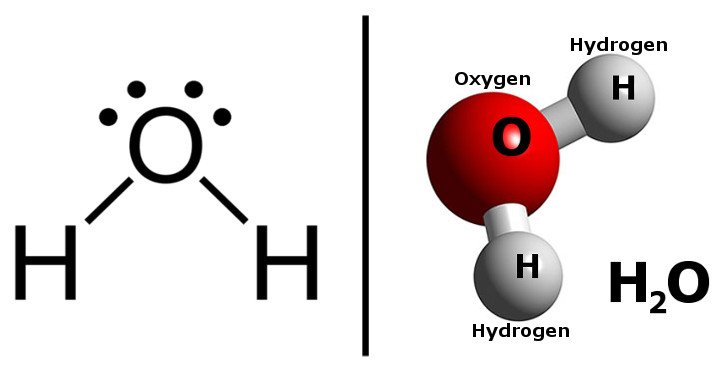
Молекула воды состоит из двух атомов водорода, соединенных с одним атомом кислорода. Связи между атомами O и H образуются за счет обмена электронами. Эти связи называются ковалентными. Каждый элемент стремится достичь энергетически наименьшего состояния (т.е. наиболее стабильного состояния), теряя или приобретая электроны, чтобы достичь ближайшей конфигурации благородного газа.
Кислород содержит шесть электронов во внешней оболочке и нуждается в двух электронах, чтобы завершить октет и войти в конфигурацию благородного газа — неона. Водород имеет один электрон в своей внешней оболочке и, получив один электрон, может достичь конфигурации благородного газа гелия. Таким образом, один атом кислорода делится двумя электронами, а два атома водорода — одним электроном, образуя одну молекулу воды, т.е. H2O.
Молекула воды имеет слегка изогнутую форму благодаря электронам на атоме кислорода. Это способствует образованию межмолекулярной водородной связи.
Кислород имеет высокую склонность притягивать к себе электроны. Это свойство называется электроотрицательностью. Из-за высокой электроотрицательности электроны проводят больше времени вблизи O, и на O образуется частичный отрицательный заряд. Аналогично, на H образуется частичный положительный заряд. Геометрия молекулы воды такова, что происходит разделение положительных (вблизи двух атомов H) и отрицательных зарядов (на O).
Когда две молекулы воды находятся рядом друг с другом, частично отрицательный O одной молекулы имеет тенденцию притягивать частично положительный атом H другой молекулы, что приводит к слабой связи, называемой водородной связью. Эта связь существует между двумя разными молекулами (межмолекулярная связь). Поскольку водородная связь слабая, для ее разрыва требуется меньше энергии, поэтому вода остается жидкостью при комнатной температуре.
Температура и молекулярная энергия
Температура — это мера средней кинетической энергии, которой обладает молекула. Чем выше температура, тем больше средняя энергия, и тем легче молекулам преодолеть межмолекулярное притяжение и двигаться более свободно. Для того чтобы жидкость перешла в парообразное состояние, необходимо преодолеть две силы.
Первая — это межмолекулярное притяжение близлежащих молекул, называемое когезионными силами. Вторая — нисходящее давление, оказываемое атмосферой. Когда жидкость меняет фазу на пар, ее молекулы приобретают достаточную кинетическую энергию, чтобы преодолеть все межмолекулярные силы, а также преодолеть нисходящее давление, оказываемое окружающей атмосферой.
Влажность
Количество водяного пара, присутствующего в атмосфере, называется влажностью. При любой заданной температуре атмосфера может удерживать только фиксированное количество водяного пара. Чем выше температура, тем большее количество водяного пара присутствует в атмосфере. Концентрация водяного пара в атмосфере имеет верхний предел, за которым водяной пар не может удерживаться.
При испарении, в отличие от кипения, только некоторые молекулы на поверхности обладают достаточной энергией для перехода в парообразную фазу.
Испарение при комнатной температуре
Предположим, что вода налита на стол тонким слоем. Молекулы расположены слоями. Молекулы в самом верхнем слое испытывают межмолекулярные силы притяжения только снизу и с боков, тогда как молекулы в объеме жидкости испытывают межмолекулярное притяжение со всех сторон. Таким образом, молекулы наверху испытывают меньшие суммарные межмолекулярные силы, чем молекулы внутри объема. Поскольку эти межмолекулярные силы (водородные связи) слабы, когда верхний слой подвергается воздействию солнечного света, некоторые молекулы получают достаточно кинетической энергии, чтобы уйти в атмосферу при комнатной температуре.
Более того, чем ниже влажность, тем легче испаряется жидкость. По мере испарения концентрация водяного пара в атмосфере увеличивается. За критическим порогом атмосфера больше не может удерживать водяной пар. Это называется состоянием насыщения. Если состояние насыщения не достигнуто, испарение продолжается.
Таким образом, сочетание влажности и высокой молекулярной энергии делает возможным испарение некоторых молекул на поверхности даже при низких температурах!
Источник
Испарение
О чем эта статья:
Испарение: что это за процесс
Процесс перехода из жидкого состояния в газообразное называется парообразованием. У этого процесса есть две разновидности: испарение и кипение.
Например, мы заварили себе горячий чай. Над чашкой мы точно увидим пар, так как вода только что поучаствовала в процессе кипения.
Подождите-ка, мы ведь только что сказали, что кипение и испарение — разные вещи. Это действительно так, при этом эти два процесса могут происходить параллельно.
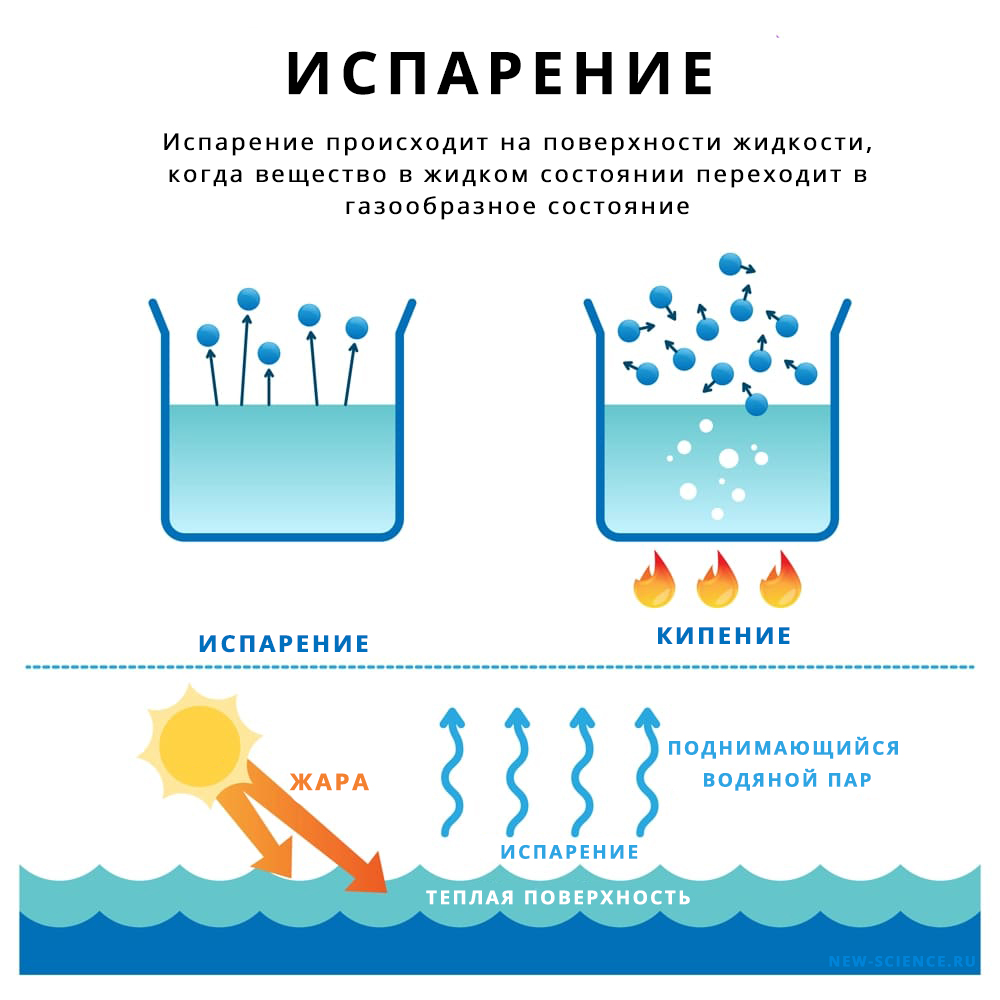
- Испарение — это превращение или переход жидкости в газ (пар) со свободной поверхности жидкости. Если поверхность жидкости открыта и с нее начинается переход вещества из жидкого состояния в газообразное, это будет называться испарением.
- Кипение — процесс интенсивного парообразования, который происходит в жидкости при определенной температуре.
Испарение может происходить и без кипения, просто тогда оно не будет для нас заметно. Например, вода в озере испаряется, хотя мы этого и не замечаем. Кипение по сути своей — это интенсивное испарение, которое вызвали внешними условиями — доведя вещество до температуры кипения.
Физика объясняет испарение тем, что жидкость обычно несколько холоднее окружающего воздуха — из-за разницы температур происходит испарение. Как будто бы это фазовый переход, о котором мы говорим в статье об агрегатных состояниях .
Если нет каких-то внешних воздействий, испарение жидкостей происходит крайне медленно. Молекулы покидают жидкость из-за явления диффузии.
Интересно то, что направление тепловых потоков при испарении может идти в разной последовательности и комбинациях:
- из глубины жидкости к поверхности, а затем в воздух;
- только из жидкости к поверхности;
- к поверхности из воды и газовой среды одновременно;
- к площади поверхности только от воздуха.
Подытожим, чтобы не запутаться: в чем главная разница между испарением и кипением:
| Испарение | Кипение |
| При любой температуре, с поверхности жидкости | При определенной температуре, во всем объеме жидкости |
Испарение на уровне молекул
Давайте вспомним об особенностях разных агрегатных состояний вещества.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
занимают предоставленный объем
больше размеров молекул
хаотичное и непрерывное
Из этой таблицы видно, что молекулы в жидкостях находятся близко друг другу, но хаотично, то есть не имеют кристаллической решетки, как в твердых телах. Эти молекулы движутся (причем, чем выше температура, тем быстрее движутся) и в ходе движения сталкиваются. Столкновения меняют направление и скорость движения — из-за этого молекулы иногда быстро устремляются к поверхности жидкости и вылетают из нее. Это и есть испарение.
В предыдущем абзаце мы не случайно заметили, что молекулы движутся быстрее при увеличении температуры — ведь из-за этого испарение идет интенсивнее. В этом случае происходит охлаждение: нагретую жидкость уже покинули все самые быстрые молекулы и температура самой жидкости понижается.
Интенсивность испарения
Интенсивностью испарения называют количество воды, которое испаряется с поверхности площадью 1 см2 за одну секунду.
Интенсивность испарения зависит от следующих факторов:
- Температура поверхности. Чем выше температура, тем больше испарение. После дождя в Санкт-Петербурге улицы долгое время остаются влажными, а вот в Таиланде даже в сезон дождей все высыхает быстро — из-за высокой температуры. Но это только если в сезон дождей дождь умудрился прекратиться 🙂
- Ветер. Чем больше скорость ветра, тем больше испарение. Фен для волос работает на этом принципе — по сути, он создает портативный ветер, который помогает высушить ваши волосы.
- Дефицит влажности. Интенсивность испарения будет выше там, где больше дефицит влажности. Вряд ли многие из нас были Сахаре, но что это такое представляют все. В любой пустыне колоссально низкая влажность — из-за этого испарение идет интенсивнее.
- Давление. Чем больше давление, тем меньше испарение. Мы уже выяснили, что не смотря на разницу между кипением и испарением, эти два процесса между собой связаны. Таким образом, температура кипения воды на вершине Эвереста равна 69 градусам Цельсия. В то время, как в нашей повседневной жизни она равна 100. Это возвращает нас к первому фактору — температуре.
Скорость испарения — количество жидкости, которая испаряется со свободной поверхности в единицу времени.
Интенсивность испарения — количество жидкости, которая испаряется с единицы площади поверхности в единицу времени.
По сути, это два очень близких друг к другу понятия, поэтому разница будет лишь в величинах и единицах измерения, а суть процесса отражают обе формулировки.
Насыщенный пар
Процесс испарения напрямую связан с круговоротом воды в природе. Вода, испаряясь, превращается в водяной пар и поднимается вверх, где происходит конденсация пара, образуются облака, и вода возвращается на землю в виде осадков.
Вследствие конденсации водяного пара, который живет в воздухе, образуются облака и туман. По этой же причине холодное стекло запотевает, соприкасаясь с теплым воздухом.
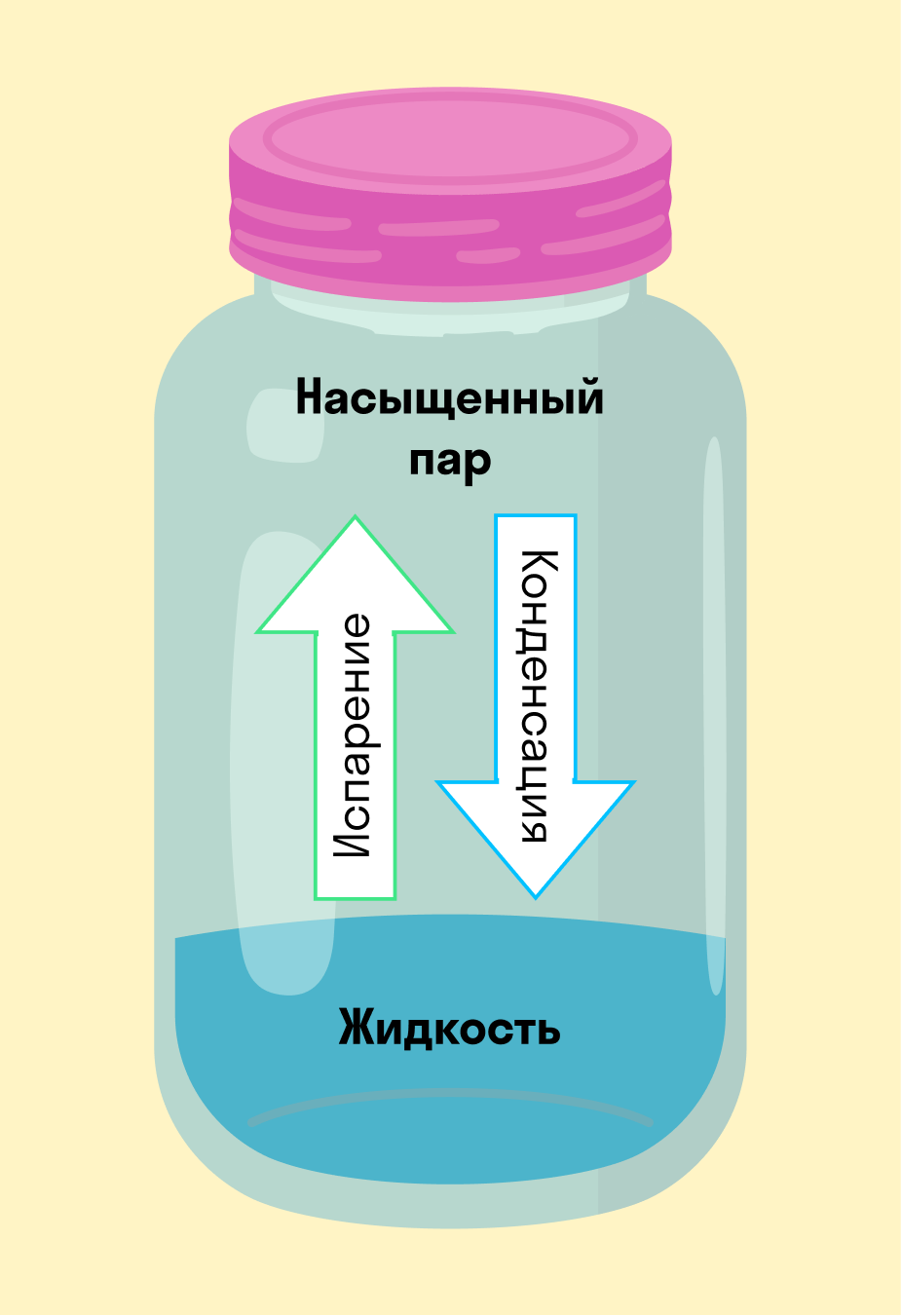
На рисунке — процессы испарения и конденсации в плотно закрытом сосуде, когда жидкость и пар находятся в динамическом равновесии. Это значит, что одновременно конденсируется и испаряется одинаковое количество вещества.
Влажность воздуха говорит нам о том, сколько в воздухе содержится водяного пара. Но бесконечное количество пара в воздух не запихнешь. Поэтому, во-первых, его там очень мало, а во-вторых, при избыточном количестве водяного пара происходит конденсация — это когда образуется роса.
Допустим, зимой при температуре -20 градусов в 1 литре воздуха содержится 1 миллиграмм пара. Относительная влажность в таком случае равна 100% — испарения не будет, больше пара в этот воздух уже не запихнешь.
Но если мы тот же воздух поместим в помещение с температурой +20 градусов, то в него может испариться уже до 17 миллиграмм пара. Значит его влажность будет равна 1/17 = 6%. Человеку комфортнее всего находиться при значении влажности 40-50%.
Испарение в жизни
И действительно: чего в этой жизни только не испаряется — мы встречаемся с этим каждый день. Давайте узнаем, зачем этот процесс вообще нужен, и как люди научились извлекать из него пользу.
Испарение в организме человека и животных
Выше мы разбирали вопрос, почему если облиться теплой водой, нам все равно станет холодно. По этому же принципу работает ощущение холода после того, как мы вспотели — в какой-то момент нам становится холодно.
Само потоотделение — важный процесс терморегуляции организма. Если мы достигаем высокой температуры (из-за внешних воздействий или же из-за болезни), то организм стремится себя охладить, чтобы не умереть из-за превращения белков в нашем организме в яичницу.
Пот выделяется через поры кожи, а затем испаряется — все это позволяет нашему организму быстро избавиться от лишней энергии, охладить тело и нормализовать температуру.
При высокой влажности холод и тепло воспринимаются более чувствительно. Это связано с потливостью человека при высокой температуре. Такой механизм помогает нам бороться с жарой и «скинуть» избыточное тепло, но при высокой влажности пот не может испариться.
При низкой влажности происходит нечто похожее. Как ни странно, в мороз мы тоже потеем (намного меньше, но все-таки это происходит). Если влажность на улице низкая, то пот испарится из-под куртки и нам будет комфортно. А при высокой влажности — он там задержится и будет проводить тепло наружу, забирая у нас драгоценные Джоули тепла. Поэтому зимой в Петербурге холоднее, чем в Москве.
У животных этот механизм работает схожим образом. Но, например, собакам испарения с кожи недостаточно, поэтому они часто открывают пасть, высовывают язык и дышат порой ну очень смешно 🐶
Именно гортань и язык собаки идеально подходят для испарения влаги и охлаждения тела животного.
Испарение у растений
Удивительно, но у растений механизм испарения тоже работает схожим образом. Растения очень любят воду, поэтому домашние растения мы поливаем, а в пустынях их просто нет.
Ту воду, которую цветы поглотили, они могут испарять, чтобы не перегреться под жарким солнцем. Да, вода нужна, чтобы растения питались, но в жаркие дни еще и для температурной саморегуляции. Поэтому не забывайте поливать цветы, а в очень жаркие дни делайте это еще интенсивнее.
Испарение в природе и окружающей среде
Процесс испарения напрямую связан с круговоротом воды в природе. Именно круговоротом воды в природе обеспечивается жизнь на Земле — так как влага разносится по всему миру, растения в дикой природе способны жить без наших попыток полить большую пальму из леечки.
Испарение воды с поверхности рек, озер, морей и океанов создает дождевые тучи, которые затем, проливаясь дождем, поливают растения и деревья. Многие дождь не любят, мол, он мокрый, мерзкий и затекает в ботинки, но он очень нужен засушливым регионам — Северной Африке или Центральной Индии, которые часто страдают от засухи.
Испарение в промышленности и быту
С бытом совсем все просто: мы сушим вещи, готовим еду, покупаем увлажнители воздуха или размазываем разлитую лужу по полу.
В случае с промышленностью для нас все не так очевидно. Промышленная техника, работающая на основе испарения, разрабатывается по схожей схеме: в ней всегда максимально увеличена площадь поверхности жидкости, чтобы испарение шло интенсивно.
Например, испаритель, изображенный на схеме, состоит из совокупности соединенных между собой испарителей. В основе его действия — пар, полученный в одной ступени, который используют в качестве источника тепла для следующей ступени. По мере того, как температура уменьшается от одной ступени к другой, вакуум увеличивается, так что температура кипения становится ниже и испарение поддерживается. Он предназначен для того, чтобы очистить воду от отходов.
Источник