Тепловой аккумулятор на основе сульфата натрия
Экология потребления.Наука и техника: Теплоаккумулятор с использованием раствора сульфата натрия обеспечивает значительно в 8-10 раз большее количество запасаемого аккумулятором тепла, по сравнению с простой водой
Проблемы накопления и сохранения тепла по прежнему актуальны и весьма заманчиво решить их с помощью на простого нагрева какого либо теплоемкого тела, а с использованием физических особенностей перехода вещества из одного агрегатного состояния в другое. Известно, что количество тепла, необходимое для, например, плавления льда в воду эквивалентно количеству тепла необходимому для нагрева этой же воды на 80 (!) градусов.
К сожалению, число веществ, изменяющих свое агрегатное состояние в диапазоне температур солнечного коллектора (40-70 гр.С) не так велико. Да и те — достаточно дороги. Это прежде всего — парафины. Можно составить смесь парафинов плавящихся в этом диапазоне температур. Но парафины достаточно дороги (>1$US за килограмм). К счастью, есть и другое вещество — сульфат натрия или глауберова соль.
Поскольку в строящемся мною доме предполагается активно использовать тепловой аккумулятор (совместно с солнечным коллектором и отопительными приборами), то есть смысл рассмотреть возможную реализацию его на основе глауберовой соли или сульфата натрия.
Подробнее, что такое сульфат натрия вы можете узнать, набрав в любом поисковике запрос «сульфат натрия» или «глауберова соль», я лишь упомяну об одном замечательном свойстве этого минерала, вернее одной его разновидности – т.н. десятиводном сульфате. Десятиводный он потому, что каждая его молекула «связывает» вокруг себя 10 молекул воды. В результате чего сульфат начинает растворяться в собственной воде с ростом температуры с огромным поглощением тепла. При температуре +32 градуса он становится густой жидкостью. А при охлаждении ниже этой температуры может начать кристаллизоваться и отдавать тепло назад. Количество тепла достаточно велико — 78,5 кДж/моль. Что эквивалентно количеству тепла, запасаемого водой, например (4,2 кДж/кг*град) в диапазоне либо несколько десятков градусов (!) одним литром, либо десятками литров воды!

«Может» — потому, что если насыщенный раствор сульфата натрия находится а абсолютном покое, то кристаллов не образуется. Но если его переохлажденный раствор сотрясти или как то побеспокоить, то начинается лавинообразная кристаллизация с сильным разогревом. Раствор быстро нагревается до +32 и поддерживает эту температуру, пока весь не кристаллизуется. Т.е. в зависимости от обстоятельств и желания, можно получить запасенное тепло либо сразу, по мере остывания. А можно – по желанию, вызвал кристаллизацию переохлажденного раствора.
Эти замечательные свойства, разумеется, открыл не я, они давным-давно известны и используются исследователями альтернативных источников энергии. Вот и я решил провести кое-какие эксперименты. Для чего было закуплено некоторое количество глауберовой соли.
Глауберова соль продается в обезвоженном виде (иначе ее было бы очень трудно хранить). Поэтому я взял примерно 2 литра горячей воды и начал растворять в ней сульфат натрия до состояния насыщенного раствора (т.е. до тех пор, пока соль не перестанет растворяться). В 2-х литрах растворилось примерно 600-650 мл соли. (мне удобно пользоваться объемными мерами, ввиду отсутствия точных весов). Плотность сульфата — примерно 1,5 Кг/литр, т.е. в литре растворилось примерно 450-480 грамм (что близко к справочным показателям — максимальная его растворимость в воде при 32,4° С, которая составляет 49,8 г в 100 г воды (в расчете на безводную соль). После тщательного двойного процеживания раствора через фильтровальную бумагу (фильтры для кофеварки), я приступил к опытам.
Важно было максимально точно воспроизвести условия, в которых будет «работать» раствор сульфата натрия в условиях теплового аккумулятора. Как то: абсолютная неподвижность ( в подвале канистры с раствором никто беспокоить не будет); достаточно медленные процессы нагрева и охлаждения, поэтому охлаждение осуществляется естественным образом, а нагрев — очень маломощной электрической грелкой, которой я оборачивал бутылку с раствором.
Контроль температуры производился с помощью лабораторного ртутного термометра (к сожалению, электронного в выносным датчиком под рукой не оказалось). Что бы измерять температуру раствора, и при этом не вмешиваться в раствор, пришлось сбоку бутылки приделать специальную П-образную «капсулу» из пенополистирола, в которую вставлялся термометр так, что бы своей колбой с ртутью касаться стенки бутылки. Для улучшения теплопередачи от бутылки к термометру я туда натолкал алюминиевой фольги. Впрочем, важно было отследить динамику температур в различных условиях, а не ее абсолютные значения.
Нагрев с помощью электрической грелки раствор до 45 градусов (примерно до такой температуры я рассчитываю заряжать свой теплоаккумулятор в эко-доме) я установил ее место, где она на подвергалась вибрациям, дополнительному нагреву или охлаждению и достаточно прохладное место. Т.е. в погребе (фактически — подвал дома и будет погребом, так что условия схожи). Температура окружающего воздуха +10 градусов.
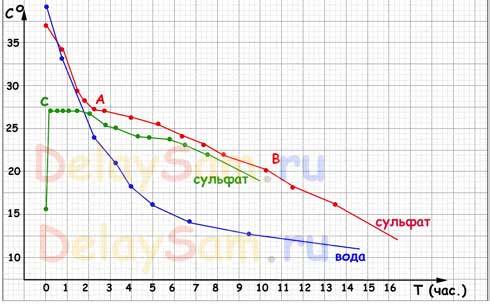
Результаты проведенных испытаний вы видите на графике:
Пояснения:
Синий график – график остывания воды. Как видите, тут никаких «приключений». Вода остывает по обратной экспоненте, стремясь к температуре окружающего ее воздуха. И чем меньше разница температуры между водой и воздухом, тем медленнее идет остывание.
График остывания раствора соли БЕЗ инициализации кристаллизации совершенно повторяет график остывания воды. Поэтому я даже не стал его рисовать.
Красный график — график остывания насыщенного раствора с внесенной затравкой. Дело в том, что для того, что бы началась естественная кристаллизация в растворе, необходимо наличие какой-либо неоднородности. Обычно ею служит некоторое количество нерастворенной соли на дне сосуда. Т.е. раствор немного пересыщен. По мере остывания раствора, в точке «А» началась кристаллизация соли в бутылке и процесс остывания резко замедлился. Тепло, выделяющееся при кристаллизации нагревало сам раствор и компенсировало теплопотери. Так продолжалось до точки «В».
Следует учитывать, что я фактически измерял не температуру раствора, а температуру поверхности бутылки. Но именно это и важно, поскольку воздух в теплоакккумуляторе будет контактировать не с раствором, а именно с поверхностью канистр, в которых будет находится теплоаккумулирующее вещество, вода или раствор сульфата натрия.
В точке «В» кристаллы заняли примерно 4/5 объема бутылки и выделение тепла замедлилось, хотя ее верхняя часть все еще была на ощупь ощутимо теплее той зоны, в которой находился термометр. Очевидно, что просто передача тепла внутри самой бутылки замедлилась и термометр перестал фиксировать ее.
Зеленый график — график поведения переохлажденного раствора. Раствор без затравки был просто охлажден до +15, а на следующие сутки в нем была вызвана кристаллизация (фактически – прикосновением к бутылке). Сразу начали расти кристаллы по всему объему бутылки, а бутылка фактически мгновенно разогрелась до 27 градусов (наружная температура поверхности). После разогрева часть кристаллов снова «расплавилась» и раствор перешёл в равновесное состояние. Т.е. кристаллизовалась только та часть раствора, необходимая на поддержание температуры равновесия.
Выводы.
Как видим из графиков, теплоаккумулятор с использованием раствора сульфата натрия обеспечивает значительно большее количество запасаемого аккумулятором тепла, практически в 8-10 раз, по сравнению с простой водой. Причем температура раствора находится в самой комфортной температурной зоне для человека — + 20-27 градусов!
Формально можно сказать, что 100 литров раствора могут заменить примерно 1 тонну воды по теплоемкости.
Но наряду с этим достоинством проявляются и его определенные особенности. Не хочу писать «недостатки» потому что они могут обернутся и дополнительными достоинствами, смотря как ими распорядиться.
В частности, достаточно трудно вызвать «монотонную» кристаллизацию раствора, т.е. естественную, в процессе остывания. Это можно сделать затравкой, но тогда процесс становится неуправляемым. Поэтому, очевидно придется придумать какой то прибор с термодатчиком, который бы срабатывал и вызывал кристаллизацию раствора при его охлаждении, например до 20-24 градусов. С другой стороны, следует предусмотреть возможность управления этим прибором вручную. Тогда в ситуации, когда тепловой аккумулятор разряжен до 20 градусов и хотелось бы поднять его температуру за счет кристаллизации раствора сульфата, НО прогноз погоды в ближайшее день-два обещает потепление или просто солнечные дни, которые позволят подзарядить теплоаккумулятор, можно будет лучше немного «потерпеть», но сохранить потенциал ТА полностью. И в конце-концов, ТА — это не один большой бассейн, а набор емкостей с водой или раствором сульфата. И кто мешает организовать достаточно гибкое управление им, что бы начинать кристаллизацию раствора по частям.
Так же следует провести и небольшой экономический анализ целесообразности применения сульфата натрия. Он хотя и недорог, но не бесплатен. Стоимость его – 7-8 рублей за килограмм. А 1 килограмм соли (сухой) дает нам 2,5 литра насыщенного раствора.
Допустим, мы купили 1 тонну соли, что даст нам 2500 литров раствора. И обошлось нам это примерно в 8000 рублей. Теперь давайте сравним.
8000 рублей — это примерно 5000 чистых кВт электроэнергии, или 18.000 МДж тепла. КПД электронагревателей близко к 100%.
8000 рублей — это примерно 5 кубометров дров (3000 кг). Это, с учетом КПД печи даст нам примерно 20.000-25.000 МДж тепла
Просто бесплатная вода (2500 литров) остывая с 40 градусов до 20 (когда еще есть смысл отнимать у нее тепло для обдува помещения воздухом такой температуры) Не отдает 200 МДж
А 2500 литров сульфата натрия дадут нам тепла соответственно в 6 раз (берем по минимуму) больше. Т.е. 200 х 6 = 1200 МДж.
Получается, что прежде чем затраты на сульфатный теплоаккумулятор окупятся, он должен будет совершить как минимум полных «оборотов» 15 по сравнению с электричеством, и 20 по сравнению с дровами.
С одной стороны, затраты на теплоаккумулятор являются разовыми и будут «отбиваться» достаточно долго, очевидно 2-3 года. А за электричество можно платить малыми дозами, и дрова можно использовать «случайные» — валежник вдоль дорог, всякое деревянное старье и отходы. А с другой стороны, и дрова, и электричество можно сжечь только 1 раз. И потом придется вновь тратить очередные «8000 тысяч» на них. А теплоаккумулятор будет служить долгие годы, возможно – десятилетия…
Поэтому тут уж каждый решает сам — стоит ли тратиться на сульфат натрия, или просто увеличить объем обычного водяного теплоаккумулятора в 6-10 раз, и строить ли его вообще… Очевидно, что использование сульфата — выход для тех, кто не может себе позволить достаточно объемный теплоаккумулятор на обычной воде или гравийно-каменнный.опубликовано econet.ru
Понравилась статья? Напишите свое мнение в комментариях.
Подпишитесь на наш ФБ:
Источник
Расчет водяного теплового аккумулятора систем отопления
Запись дневника создана пользователем Андрей-АА, 14.11.14
Просмотров: 106.876, Комментариев: 31
Исходная «формула» для расчета накопленной энергии:
Для нагрева 1 тонны воды на 1*С необходимо 1,16кВт*часа энергии. Значит для нагрева на 40*С — 46,4кВтчаса.
Надо учитывать, что дельта в 40*С это наиболее близкая к максимально- реальной дельте температур в тепловом аккумуляторе. Лучше конечно больше, но заметно больше получается редко, а меньше — не выгодно. Хотя, стремиться повысить эту дельту — надо.
Сначала — про единицы измерения теплопотерь.
Это — Ватты и киловатты.
Теплопотери это — потери энергии в единицу времени.
Т.е., кВт*часы в час (кВт* час / час ). Часы сокращаются, остаются киловатты.
Для этого расчета надо знать теплопотери дома в формате «кВт при дельте температур улица-дом». К примеру, по последнему СНиПу теплопотери должны быть не больше, чем 50 Вт/кв.метр отапливаемой площади дома при максимально холодной неделе (для Москвы — минус 28*С)). Т.е., если дом — 100кв.м., то по этому СНиПу его теплопотери при -28*С будут 5кВт. Это — без учета потерь на ГВС и вентиляцию!
Если Вы хотите отапливать такой дом, то при -28*С на улице Вам надо иметь в сутки 120кВтчасов энергии (5кВт*24часа).
Предположим, что накопление энергии в тепловом аккумуляторе будет идти 7 часов (это — обычно длительность ночного электротарифа). Тогда суммарная мощность нагревателей должна быть 17кВт (120кВтчасов/7часов). А накоплено в тепловом аккумуляторе за ночь будет 85кВтчасов (120кВтчасов минус 5кВт*7часов, которые потрачены на отопление ночью).
Т.е., Вам надо к утру иметь в тепловом аккумуляторе 85кВтчасов при дельте температур в тепловом аккумуляторе (нагрето-остыло) 40*С.
Примечание:
Вообще-то, дом должен быть теплым не в среднем за неделю, а в любую микросекунду
В тонне воды (см. «формулу» выше) при дельте 40*С содержится 46кВтчасов тепла. Это значит, что для накопления 85кВтчасов надо 1,8 тонны воды (85/46).
Все необходимые для Вас перерасчеты под свои условия здесь должны быть линейны, т.е. пропорциональны изменениям площади дома, дельтам температур и теплопотерям.
Для снижения объема теплового аккумулятора можно еще постараться максимизировать дельту температур в нём, сделав её выше 40*С. При отапливаемых полах это вполне реально.
4. Что делать если немного не хватает мощности сети?
1. Дополнительно утеплить дом.
2. В самые морозы закрыть и не отапливать некоторые комнаты.
3. Увеличить подводимую мощность сети (через поставщика э/энергии) и внутреннюю, при необходимости.
4. Включать нагрев теплового аккумулятора не только в ночное время, но (в самые морозы) и днем. А т. к. самые морозы бывают не часто, то и финансовые потери на дневной тариф будут небольшими.
5. Добавить в систему твердотопливный котел — как резервное отопление и как добавка в морозы. Считаю, что при электро-отоплении резервное отопление очень желательно в любом случае. Я для себя в этом вопросе разобрался: Стратегия твердотопливного круглогодичного отопления.
Ну, или заключить с энергетиками жестокий для них договор, чтобы почти никогда (надолго) не отключали э/э. Впрочем, тому кто это сможет сделать надо будет вручить орден «За заслуги перед Отечеством» (и это — не шутка, хоть и забавно звучит).
6. При работе на пределе электро-мощностей можно использовать реле приоритета (реле разгрузки), которые, при необходимости, на короткое время будут отключать мощные нагреватели (а лучше — только часть из них) для возможности использования других потребителей без превышения предельной мощности сети. Если эти «другие потребители» находятся внутри дома, то вся электроэнергия потраченная на них всё равно перейдет в тепло.
Источник