- Общеклинические исследования
- 1. Вода — универсальный биологический растворитель
- Вода-растворитель
- Вода – растворитель
- Что такое раствор
- Образование пещер
- Почвенные растворы
- Нерастворимые вещества
- Что мы узнали?
- Вода как растворитель — свойства, значение и примеры
- Свойства воды как растворителя
- Какие вещества растворяются в воде
- Что не растворяется в воде
- Значение воды как растворителя
Общеклинические исследования
1. Вода — универсальный биологический растворитель
Растворителем, в котором работают почти все известные живые системы, служит окись водорода, или вода (H 2O). В молекуле воды атом кислорода соединен с двумя атомами водорода одинарными ковалентными связями. Чтобы понять, почему это важно и на что это влияет, нам придется ввести несколько дополнительных понятий из общей химии.
Электроотрицательность — сила, с которой атом в составе молекулы оттягивает на себя общие с другим атомом электроны, образующие ковалентную связь. Это понятие ввел Лайнус Полинг (Linus Carl Pauling). Самый электроотрицательный элемент — фтор, за ним на шкале электроотрицательности следует кислород. Иными словами, кислород превосходит по электроотрицательности все другие атомы, за исключением фтора (который в биологической химии практически не встречается). Запомним этот факт.
Электроотрицательность одинаковых атомов по определению равна. Если между двумя одинаковыми атомами есть ковалентная связь, то образующие ее электроны никуда не смещены (в рамках старинной планетарной модели атома можно сказать, что они находятся точно посредине между атомами, как на картинке). Такая ковалентная связь называется неполярной.
Если ковалентную связь образуют два разных атома, то общие электроны смещаются к тому из них, у которого выше электроотрицательность. Такая связь называется полярной. При очень большой разнице в электроотрицательности она может даже стать ионной — это случится, если один атом полностью “отберет” у другого общую пару электронов.
Связь между водородом и кислородом в молекуле воды — типичный пример ковалентной полярной связи. Электроотрицательность кислорода намного выше, поэтому общие электроны смещены к нему. В результате на кислороде возникает маленький отрицательный заряд, а на водороде маленький положительный; эти заряды принято обозначать буквой δ (“дельта”).
Связи кислорода с водородом или углеродом (H-O или C-O) — всегда полярные. Молекулы, в которых много таких связей, несут многочисленные частичные заряды, отрицательные на кислороде и положительные на водороде или углероде. В то же время связь между углеродом и водородом (C-H) считается неполярной: разница в электроотрицательности между этими элементами так мала, что смещение электронов незаметно. Например, молекулы углеводородов в силу этого полностью неполярны, они не несут никаких частичных зарядов ни на каких атомах.
При наличии полярных связей между водородом и кислородом частичные заряды на этих атомах (отрицательные на кислороде и положительные на водороде) притягиваются друг к другу, образуя водородные связи. Эти связи гораздо слабее ковалентных, но могут давать сильный эффект, если их много. Например, именно из-за колоссального количества водородных связей у воды очень высокая теплоемкость — ее трудно нагреть и трудно остудить. Строго говоря, водородная связь может образоваться не только с кислородом, но и с другими электроотрицательными атомами (например, с азотом или фтором).
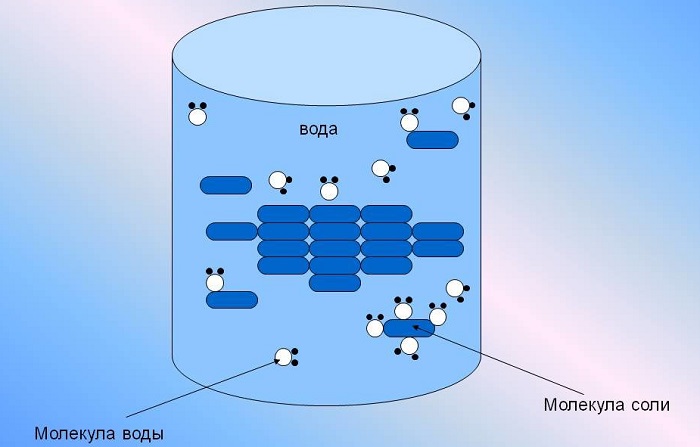
Любые заряженные частицы в водном растворе гидратируются, то есть окружаются молекулами воды — конечно, по-разному ориентированными в зависимости от того, положительная это частица или отрицательная. Любые ионы, растворенные в воде, на самом деле присутствуют там в гидратированном состоянии, то есть с водной оболочкой. На картинке для примера показана растворенная поваренная соль (NaCl) — образец чисто ионного вещества.
Полярные молекулы (а тем более ионы) хорошо взаимодействуют с водой, образуя с ней водородные связи и (или) подвергаясь гидратации. Такие вещества хорошо растворяются в воде и называются гидрофильными. Неполярные молекулы взаимодействуют с водой гораздо слабее, чем друг с другом. Такие вещества плохо растворяются в воде и называются гидрофобными. Типичные гидрофобные вещества — углеводороды. Типичные гидрофильные вещества — спирты, такие как этанол или показанный на картинке глицерин. Вообще кислородсодержащие соединения углерода, как правило, гидрофильны, если только в них нет совсем уж огромных углеводородных радикалов.
Могут ли подойти для жизни другие растворители, кроме воды? Ответ — да. Например, двуокись углерода (CO 2) при более высоких давлениях, чем наше атмосферное, становится жидкостью и представляет собой хороший гидрофильный растворитель, в котором успешно идут многие биохимические реакции. В этом растворителе могут жить даже земные микроорганизмы: например, на дне Окинавского желоба в Восточно-Китайском море обнаружено целое озеро жидкой углекислоты, в котором постоянно живут довольно разнообразные бактерии (Inagaki et al., 2006).
Некоторые исследователи предполагают, что океаны жидкой двуокиси углерода могут существовать на планетах-“суперземлях” с массой, в несколько раз превосходящей массу Земли (Budisa, Schulze-Makuch, 2014). На картинке — художественное изображение планеты GJ1214b в созвездии Змееносца.
На крупнейшем спутнике Сатурна — Титане — есть углеводородные озера и даже моря, состоящие из метана (CH 4), этана (C 2H 6) и пропана (C 3H 8). Это гидрофобный растворитель, в котором тоже иногда предполагают существование жизни, хотя прямых подтверждений тому пока нет. На картине — пейзаж Титана. Жидкой воды на поверхности Титана нет, там слишком холодно.
Аммиак (NH 3) — гидрофильный растворитель, образующий много водородных связей, в данном случае между водородом и азотом, и напоминающий воду по физико-химическим свойствам. На более холодных планетах, чем Земля, аммиак находится в жидком состоянии и вполне может быть средой для жизни.
Теоретически возможно существование холодных землеподобных планет с аммиачными океанами (на картинке художественное изображение такой планеты). Есть ли там жизнь, никто не знает. Но почему бы и нет? Если насчет альтернатив углеродной жизни есть сомнения, то углеродную жизнь в неводном растворителе представить гораздо легче.
Можно придумать и другие экзотические варианты — например, океан из плавиковой кислоты (HF) на планете, описанной в фантастической повести Ивана Ефремова “Сердце Змеи”. “Люди Земли увидели лиловые волны океана из фтористого водорода, омывавшие берега черных песков, красных утесов и склонов иззубренных гор, светящихся голубым лунным сиянием…” Возвращаясь к земной биохимии, будем помнить, что она — не единственная теоретически возможная.
Источник
Вода-растворитель
Краткий доклад по окружающему миру для начальных классов.
Вода — самый сильный природный растворитель. В ней растворяются почти все вещества – какие-то больше и быстрее, какие-то – меньше и дольше. Даже металл при длительном контакте с водой начинает в ней растворяться. А когда мы пьем из стакана горячий чай, то вместе с ним в наш организм попадает около 0,1 миллиграмма растворенного в этом чае стекла.
Вода, как и другие вещества, состоит из особых мельчайших частичек — молекул. Молекулы воды электронейтральны, т.е. они «дружат» со всеми веществами. К некоторым веществам они испытывают особое притяжение. Это позволяет водным молекулам легко соединяться с молекулами других веществ, несущих заряд. При их встрече притяжение усиливается, в результате вещество смешивается с водой, полностью в ней растворяясь. Если же притяжения нет, то соответственно, всё остается неизменным. Вещество останется лежать на дне стакана.
Твердые вещества, постепенно растворяясь в воде, становятся важнейшей составляющей круговорота живой природы. Вода с растворенными компонентами твердых веществ — это среда питания и поставщик микроэлементов, необходимых для жизни растений, животных и человека.
В природе не существует абсолютно чистой воды. Почти все жидкости, которые мы видим в повседневной жизни, являются растворами. Вода из-под крана является раствором воды с примесями железа от труб, по которым она течет. Натуральными растворами являются напитки — чай, сок и компоты, которые содержат полезные для организма человека компоненты. Вода может растворять не только твердые, но и жидкие, и газообразные вещества.
Как мы видим, абсолютно чистой воды в окружающей нас среде не бывает, в ней всегда что-либо растворено. В дождевой, водопроводной, речной, морской – в каждой воде содержатся какие-либо примеси. Вода с растворёнными в ней компонентами приобретает новые качества. Например, раствор серебра убивает микробы. Таким образом, вода, в зависимости от своего состава, может быть как полезной, так и вредной для человека.
В среднем, за свою жизнь человек потребляет 75 тонн воды. И вместе с ней – огромное количество растворенных веществ.
Источник
Вода – растворитель

Средняя оценка: 4.5
Всего получено оценок: 27.
Средняя оценка: 4.5
Всего получено оценок: 27.
Вода окружает человека, является составной частью животных и растений, без воды невозможна жизнь на Земле. Вода не имеет запаха, цвета, вкуса. Вода легко испаряется, течёт, на морозе превращается в лёд. В воздухе присутствуют пары воды, это даёт возможность дышать всем существам. Ещё одно свойство воды — способность растворять многие вещества.
Что такое раствор
Раствором называют однородную смесь из нескольких веществ, где компоненты неотделимы друг от друга. Обычно растворы представляют собой жидкость.
На обеденном столе множество растворов. Это подсоленный суп, соус к макаронам, сладкий чай и кофе, минеральная вода. Основой большинства растворов является вода.
В природе также много растворов. Самый известный — солёные озёра, где вода растворяет ископаемую соль.
Одно из самых солёных озер — Мёртвое море, где в 1 литре воды содержится 310–350 грамм соли. В растворе присутствуют соли магния, кальция, натрия и калия.
Образование пещер
В горах, сложенных известняком, часто образуются пещеры. В известняке множество микротрещин, по которым с дневной поверхности просачивается вода. Вода — растворитель известняка, поэтому постепенно твёрдое вещество растворяется, на его месте образуется маленькая пустота. Пустота расширяется, формируется пещера.
При растворении известняка вода превращается в раствор, стекающий по стенкам пещеры и капающий с потолка. Из раствора откладывается известняк, очень медленно растут сталактиты, похожие на сосульки.

Почвенные растворы
Вода впитывается в почву, проникает в нижние горизонты. В воде растворяются минеральные вещества, органические соединения. Так образуются почвенные растворы, из которых корневая система растений усваивает питательные вещества. Если почвенные растворы содержат недостаточное количество питательных веществ, применяют различные удобрения.
Нерастворимые вещества
Некоторые вещества не растворяются в воде, их называют нерастворимыми. Это металлы, большинство горных пород, масла, нефть, бензин, воск и другие.
Вещества, более тяжёлые, чем вода, оседают на дно сосуда или водоёма. Дно реки или озера покрыто песком и окатанными камешками-галькой.
Нефть и нефтепродукты легче воды, поэтому при загрязнении реки растекаются по водной поверхности. При этом прекращается доступ воздуха в воду, что приводит к гибели водных организмов.
Что мы узнали?
Вода — природный растворитель. В докладе для урока по окружающем миру в 3 классе можно кратко описать описать это свойство воды на примере растворов природных (солёные озёра, почвенные растворы) и созданных человеком — жидкие блюда (супы, соусы) и напитки (чай, кофе).
Источник
Вода как растворитель — свойства, значение и примеры
Вода как растворитель играет предельно важную роль далеко не только в плане нашего быта. Исследователи давно говорят, что данное волшебное соединение является основой для образования жизни вообще. И именно поэтому его наличие выступает обязательным условием для существования чего-то более сложного, нежели неживая природа.
Растворимость тех или иных химических элементов напрямую связана с существованием воды, так как она чаще всего выступает той средой, которая преобразует все вокруг себя и создает новые формы органической и неорганической материи.
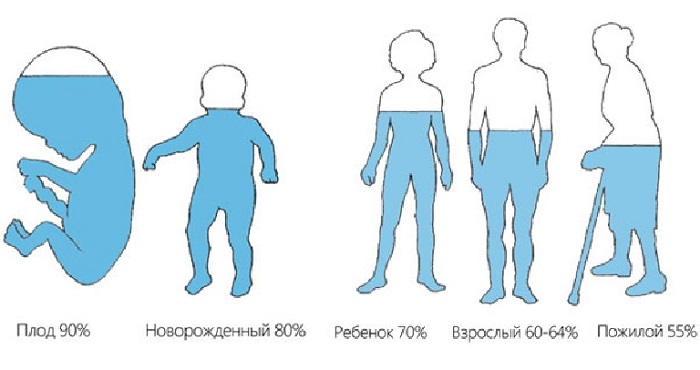
Человек примерно на 70% состоит из воды (имеется ввиду кровь, межклеточная жидкость, плазма крови и прочие вещества), у большинства других существ этот показатель колеблется от 50 до 95%. Очевидно, что свойства данного соединения оказывают решающую роль на происходящие вокруг нас и внутри нас процессы синтеза, регенерации и многие другие.
Это универсальный растворитель, который буквально формирует окружающий мир, постоянно преображает и обновляет его!
Свойства воды как растворителя
Вода – сложное вещество, отличающееся многими уникальными характеристиками, которые нельзя встретить больше нигде.
Она способна растворить большую часть существующих в природе комплексных соединений, содержащих в своей структуре молекулы как с положительными, так и отрицательными ионами одновременно.
При проведении так называемых кинетических исследований все растворы также изготавливаются на основе H2O.
Яркий пример особенности воды – при схожести по своей структуре с метаном CH4, она имеет температуру кипения выше на целых 250 0 С!
Важную роль играет также ее способность выступать одновременно либо донором, либо акцептором частиц водорода, благодаря чему проходят многие химические процессы. Химия говорит нам еще и о том, что вода выступает идеальным растворителем для диссоциирующих соединений.
Интересно отметить, что по причине высокого уровня диэлектрической проницаемости, вода отлично экранирует электрические поля ионов друг от друга. Благодаря этому притяжение противоположно заряженных частиц в воде снижается примерно в 80 раз.
Какие вещества растворяются в воде
Даже если школьник ходит только в 3 класс, он наверняка может привести примеры материалов, которые боятся контакта с водой, или, другими словами, растворяются в ней и теряют свои свойства.
Вот перечень только некоторых веществ такого типа:
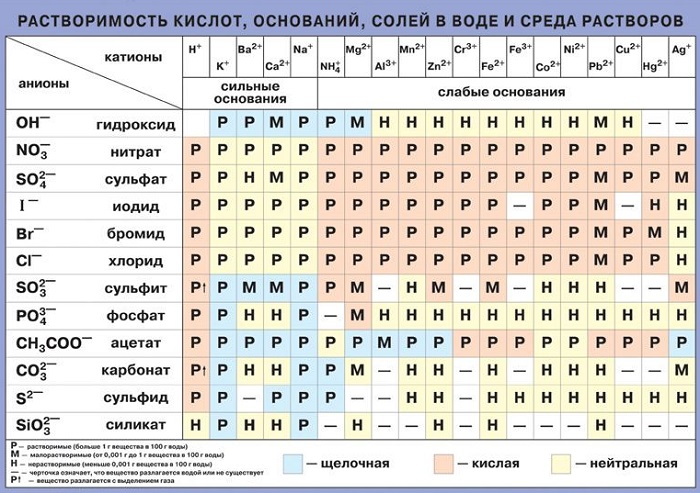
К хорошо растворимым относятся: соль, сахар, сода, хлориды, щелочные металлы и нитраты, а также бромиды. Воздух также претерпевает изменения при контакте с жидкой средой. Крахмал полностью растворим, спирт тоже.
К средней степени взаимодействия относятся: бертолетова соль, метан, гипс, кислород, азот, другие химические элементы, например, сульфаты, некоторые газообразные вещества.
Есть и такие материалы, которые являются нерастворимыми: сульфид меди, стекло, золото, керосин, серебро, растительный жир и многие другие. Правда, при некоторых условиях даже они не способны устоять от такого мощного воздействия.
В организме человека есть целая группа витаминов (С, В1, 2, 3(РР), В12 и другие), которые способны оказывать свое положительное воздействие на здоровье только в контакте с H2O. Это касается также и фолиевой кислоты, биотина и т. д.
Что не растворяется в воде
Существуют такие химические образования, которые не воспринимают воздействия воды в качестве растворителя совсем.
Хороший пример: углерод С, который находится в простом карандаше, многие металлы и сплавы, типа алюминия, а также золото, серебро, медь.
Такая ситуация складывается благодаря тому, что между молекулами и атомами нерастворимых веществ действуют сильные связи, которые водород разрушить не в состоянии. Полярное состояние молекулы также способствует большей прочности материала, который состоит из таких частиц.
Многие вещи, которые мы видим вокруг себя в быту, также являются нерастворимыми. Очень популярный пример – пластик.
В мировом океане плавает огромное пятно из пластикового мусора, которое ежегодно растет, и количество пластмассы там совершенно не желает уменьшаться естественным путем. Его не могут никак переработать, что очень плохо для всей экосистемы.
Именно поэтому экологи бьют тревогу и в ЕС уже сейчас планируется отказ от целлофановых пакетов, пластиковых стаканчиков и трубочек и тому подобные меры.
Значение воды как растворителя
Как уже упоминалось в начале статьи, рассматриваемые свойства воды являются ключевыми для всей живой и неживой природы нашей планеты.
Если бы она не обладала этими характеристиками, то большинство химических процессов на Земле, в живых организмах, в органической природе бы просто остановилось. Картинка такого мира была бы очень неутешительна – темная пустыня без признаков жизни.
Роль воды настолько огромна, что именно ее определение в далеких планетах и галактиках является для астрономов основным занятием в надежде когда-то отыскать там если не разумное существование, то хотя бы зачатки жизни.
Источник